El objetivo fue evaluar el riesgo de hepatotoxicidad asociado a los antagonistas de los receptores de la endotelina como clase terapéutica.
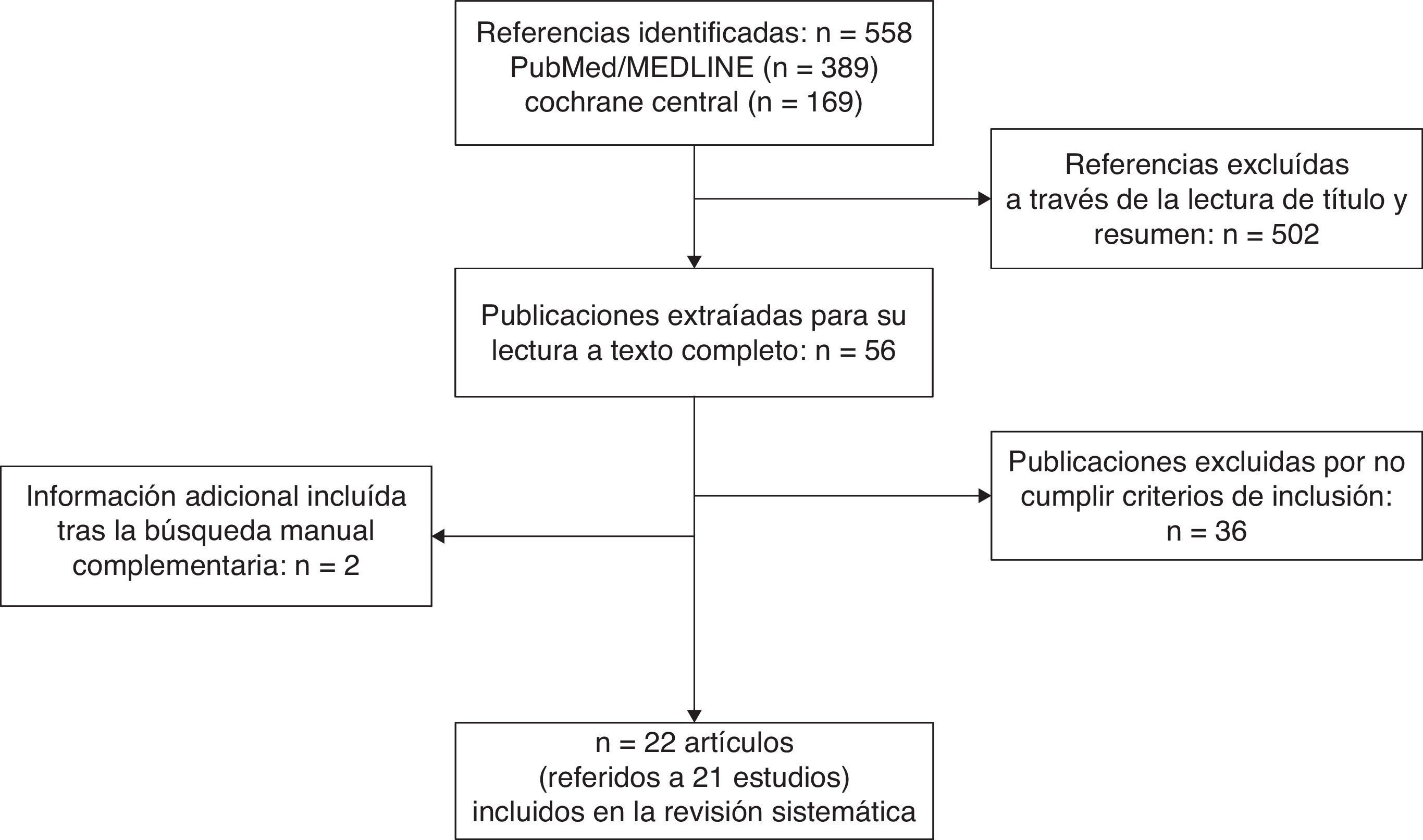
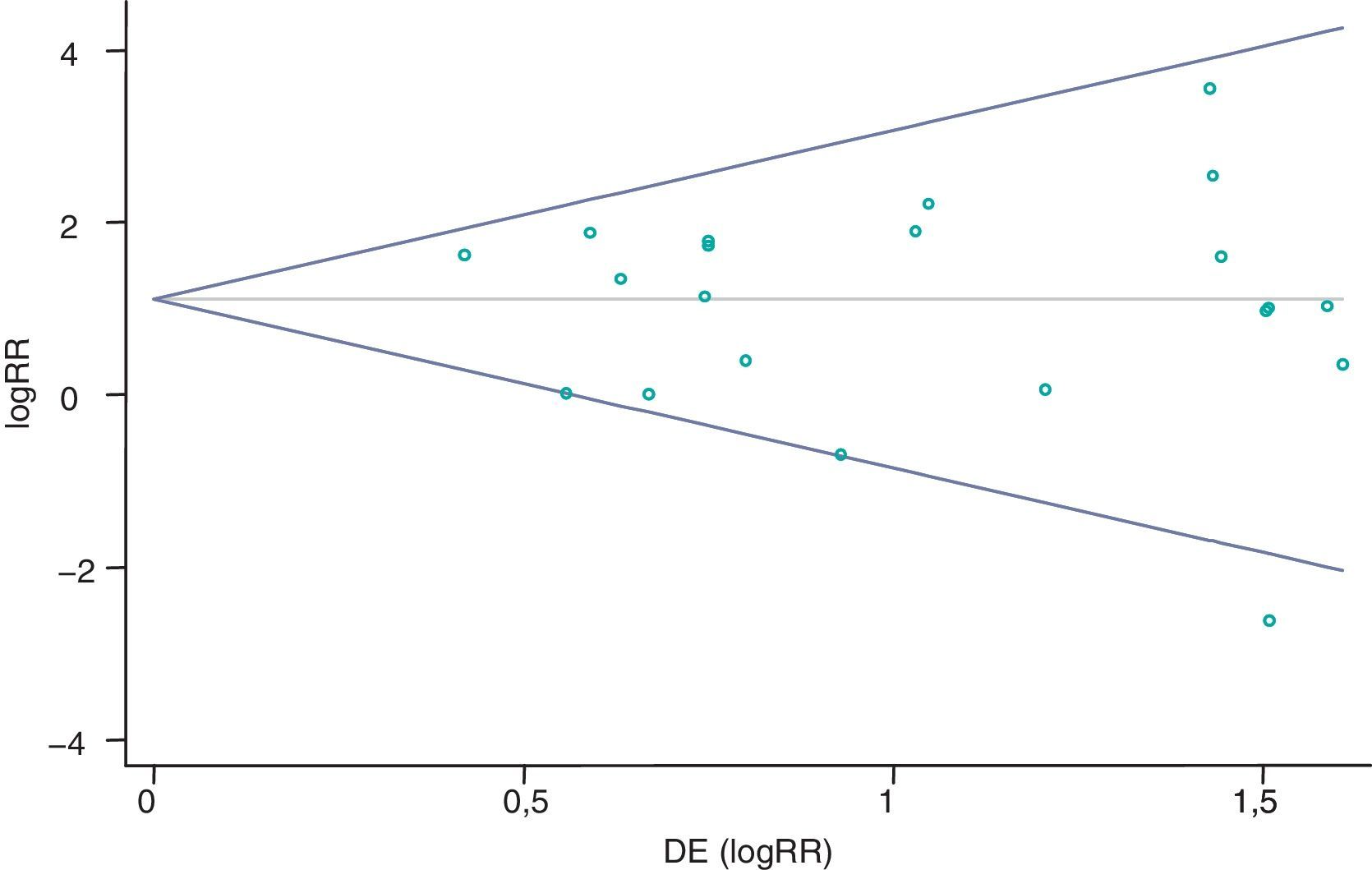
Pacientes y métodoSe realizaron búsquedas sistemáticas en PubMed/MEDLINE, Cochrane Library y en las páginas web de las agencias reguladoras. Se incluyeron ensayos clínicos aleatorizados y controlados en pacientes tratados con antagonistas de los receptores de la endotelina (bosentán, sitaxentán o ambrisentán) en al menos uno de los grupos de intervención. Se calculó el efecto de los tratamientos junto con los intervalos de confianza del 95% (IC 95%) utilizando modelos de efectos aleatorios. La heterogeneidad se analizó mediante la Q de Cochran y la prueba I2. El sesgo de publicación se evaluó mediante gráficos en embudo y el método de Egger.
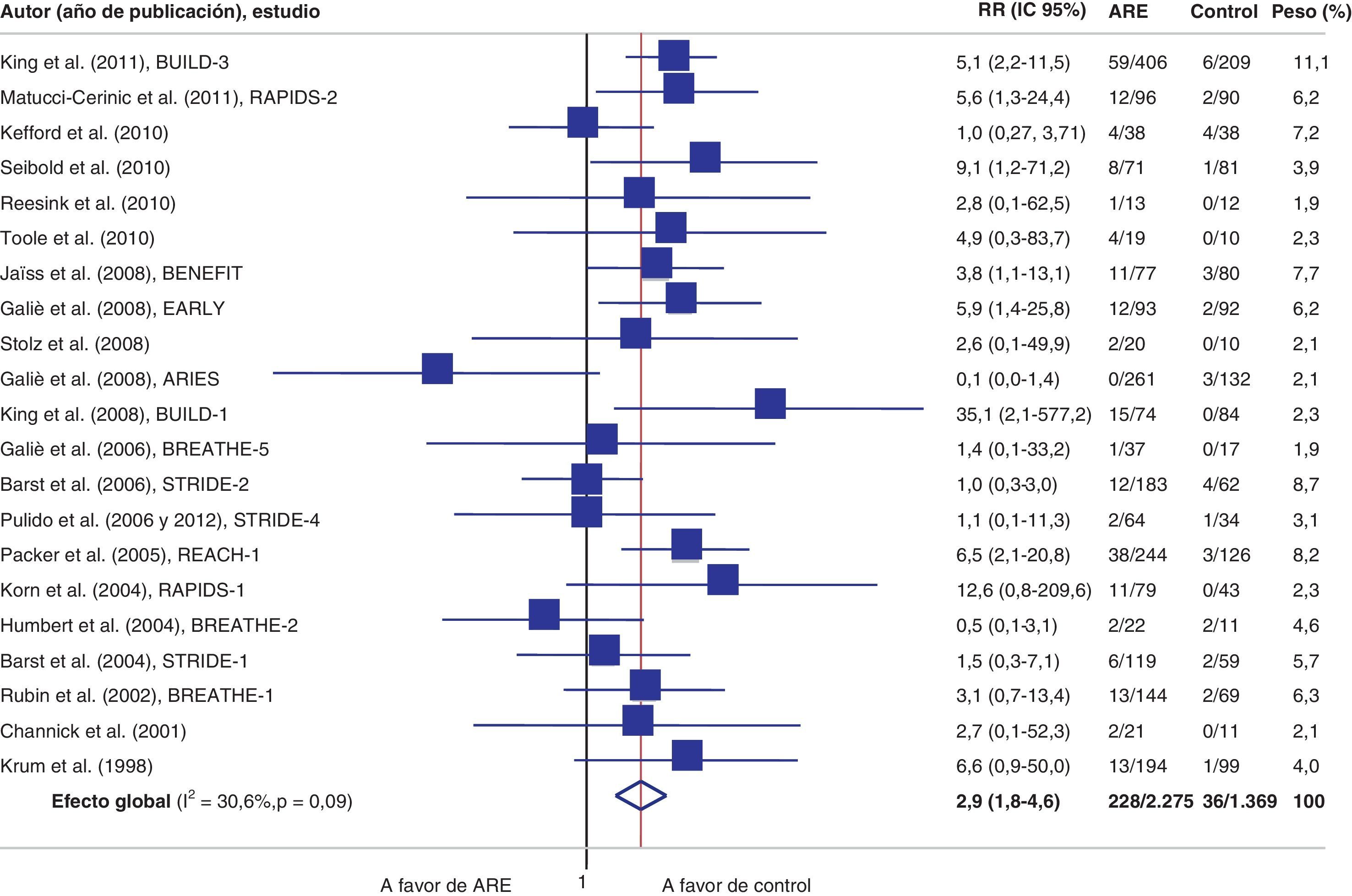
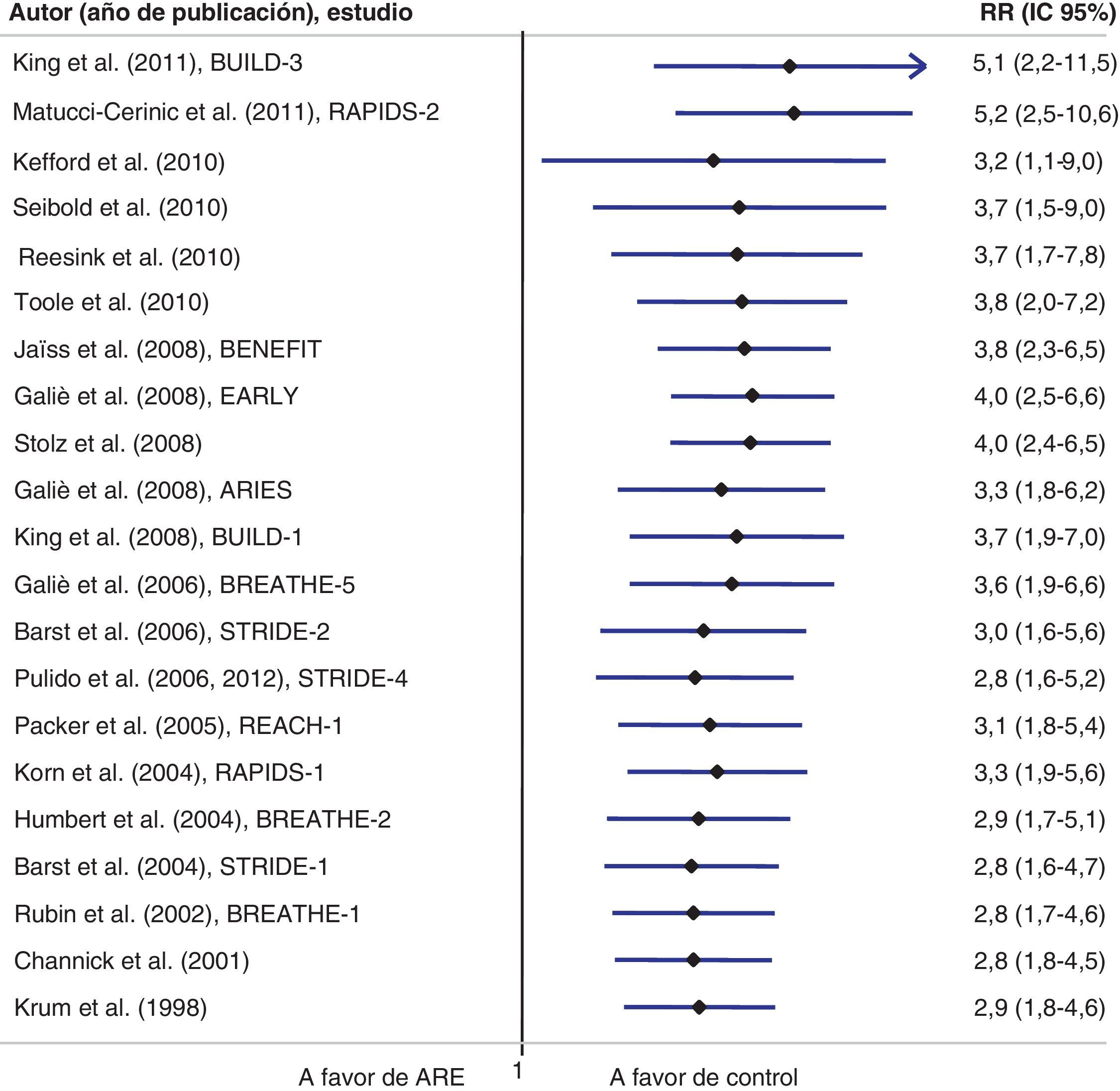
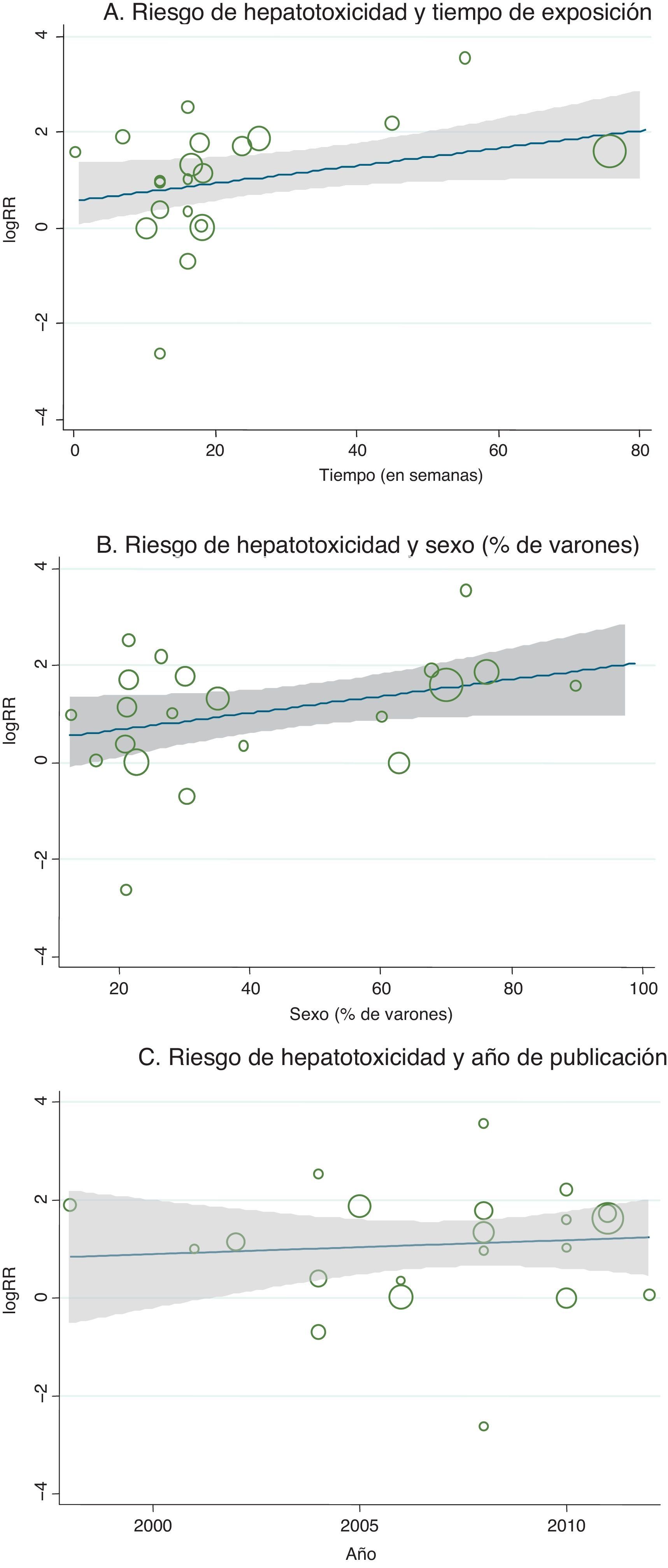
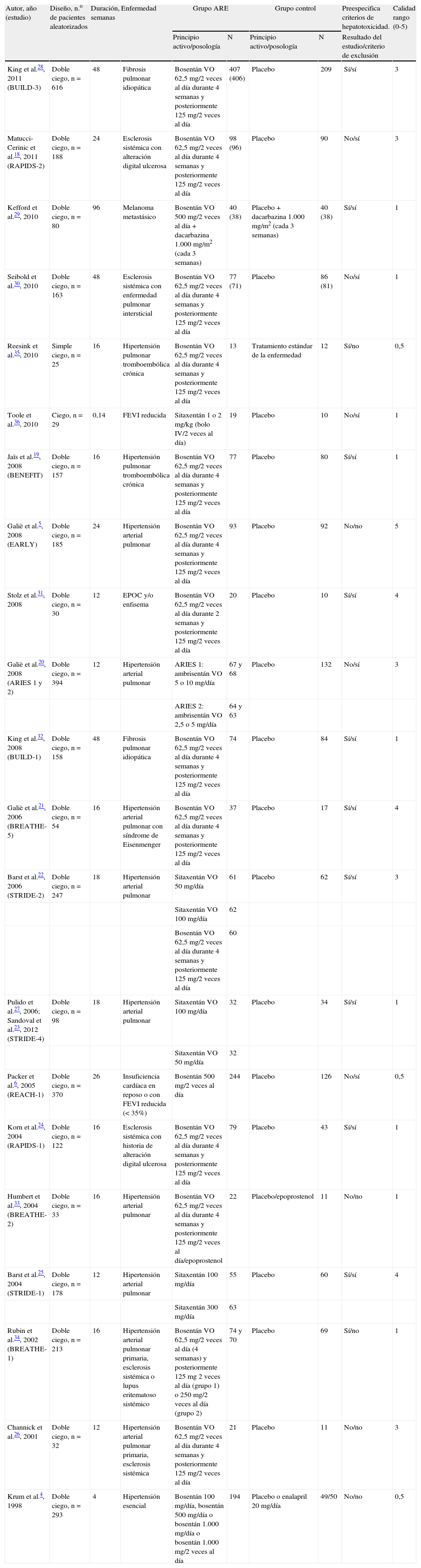
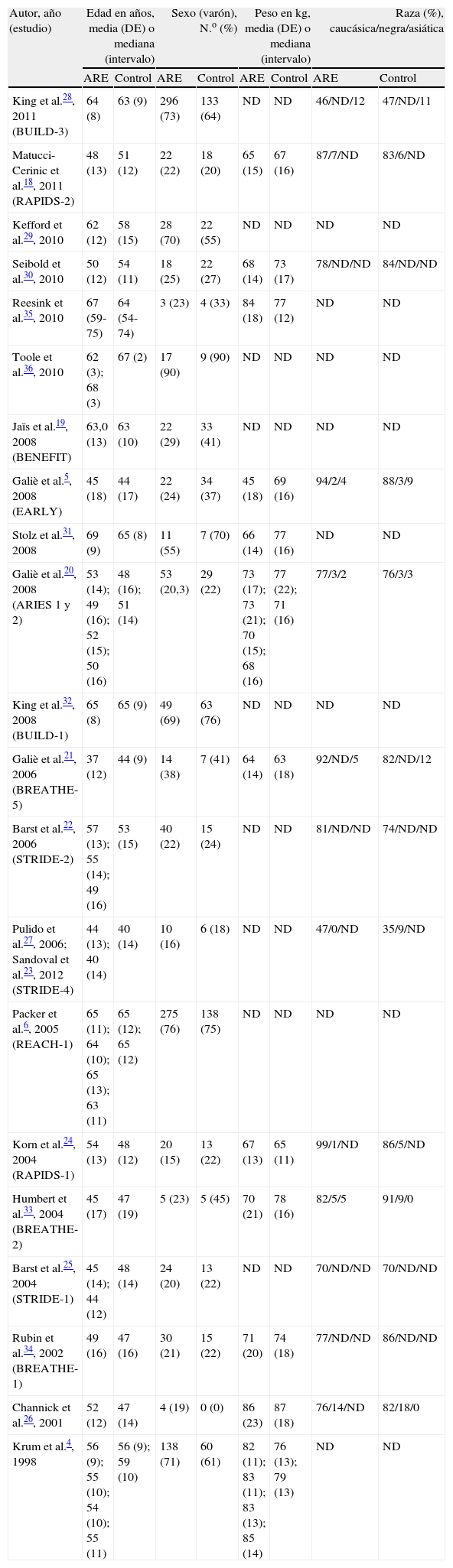
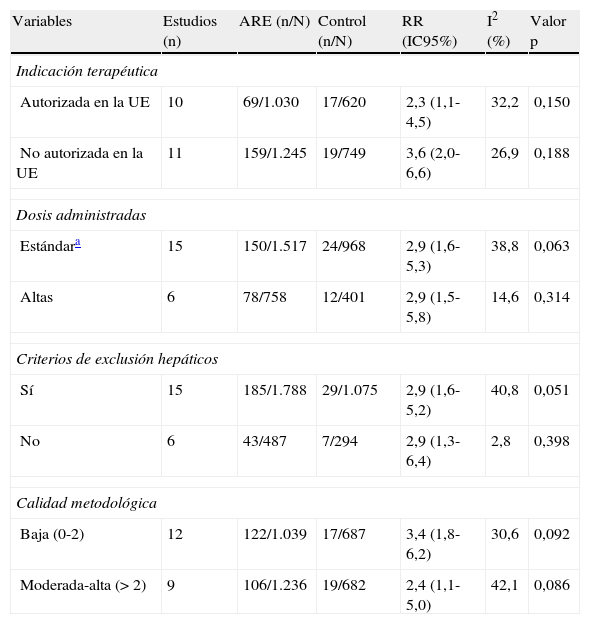
ResultadosSe encontraron 21 estudios que cumplieron los criterios de inclusión (3.644 pacientes). Bosentán fue el fármaco evaluado en 1.689 (74%) pacientes. El riesgo relativo de cualquier reacción adversa hepática respecto a los controles fue de 2,92 (IC 95% 1,85-4,62; I2=30,6%). Cuando la hepatotoxicidad se definió como elevaciones en alanina o aspartato aminotransferasa≥3 veces el límite superior de lo normal, el riesgo relativo fue de 2,98 (IC 95% 1,69-5,25; I2=40,9%). No hay evidencia de un posible sesgo de publicación (Egger: p=0,68).
ConclusionesLos resultados sugieren que los antagonistas de los receptores de la endotelina se asocian a un mayor riesgo de hepatotoxicidad. No hay suficientes datos de hepatotoxicidad de antagonistas de la endotelina diferentes al bosentán para establecer sus riesgos individuales.
We evaluated the risk of hepatotoxicity associated to endothelin receptor antagonists.
Patients and methodSystematic searches in PubMed/MEDLINE, the Cochrane Library as well as regulatory agencies websites were performed. Randomized controlled trials in patients receiving endothelin receptor antagonists (bosentan, sitaxentan or ambrisentan) in at least one treatment group were included. Prior to data extraction, definitions of hepatotoxicity were established. Effect sizes with 95% confidence intervals were calculated using random effects models. Heterogeneity was analysed using Cochran's Q and I2 tests. Publication bias was assessed using Egger's method and funnel plots were generated.
ResultsTwenty-one trials met the inclusion criteria (3,644 patients). Bosentan was the evaluated drug in 1,689 (74%) patients who received endothelin receptor antagonists. Compared with controls, relative risk for any hepatic adverse reaction was 2.92 (1.85-4.62; I2=30.6%). When hepatotoxicity was defined as elevations of liver alanine or aspartate aminotransferases equal or greater than 3 times the upper limit of normal, relative risk was 2.98 (1.69-5.25; I2=40.9%). No evidence of publication bias was found (Egger's method: p=0.68).
ConclusionsOur results suggest an increased risk of hepatotoxicity in patients receiving endothelin receptor antagonists. Given the limited data available for endothelin receptor antagonists other than bosentan, it is not possible to draw firm conclusions about the individual risk associated for the remaining endothelin receptor antagonists.