Los sistemas automáticos de administración de insulina (AID) mejoran el control glucémico y la calidad de vida en las personas con diabetes tipo 1 (DT1). Nuestro objetivo fue evaluar la viabilidad, la efectividad y la seguridad de un recambio masivo de sistema bomba/sensor (SAP) a AID en sujetos con DT1 y alto riesgo de hipoglucemia.
Material y métodosSe realizó un programa grupal e híbrido de 3 sesiones a cargo del fabricante. En 3 días, todos los pacientes realizaron presencialmente la primera sesión en grupos de 6-12 personas para entrenar el uso del dispositivo. De forma virtual, se activó el modo automático (sesión 2) y la descarga de datos online (sesión 3). Se evaluaron resultados glucométricos tras un mes, así como eventos adversos graves (EAG), incidencias técnicas y satisfacción percibida.
ResultadosEl cambio de dispositivo se efectuó en 125 pacientes, 56,8% mujeres y edad media 44,1±14,9 años. El 99,2% (n=124) iniciaron modo automático. Se observó un aumento del tiempo en rango 70-180mg/dl (64,3±11,3 vs. 74,7±11,2; p<0,001) y una reducción del tiempo <70mg/dl (4,1±3,9 vs. 2,0±1,8; p<0,001) (N=97). Recibimos 41 llamadas relacionadas, de las cuales 10 requirieron visita presencial. El servicio técnico de Medtronic atendió 92 incidencias relacionadas con el recambio (0,74 por paciente), provenientes de 47 usuarios (37,6%). Como EAG se registró una hipoglucemia grave. La seguridad y la satisfacción percibidas con el proceso de cambio fue alta en el 91 y 92% de los pacientes.
ConclusionesEl recambio masivo de un sistema SAP a AID en los pacientes con DT1 y alto riesgo de hipoglucemia es factible y seguro mediante un programa híbrido y en colaboración con el fabricante.
Automatic insulin delivery (AID) systems improve glycemic control and quality of life in individuals with type 1 diabetes (T1D). Our aim was to assess the feasibility, effectiveness, and safety of switching from a sensor-augmented pump (SAP) to AID in T1D subjects at high risk of hypoglycemia.
Materials and methodsA manufacturer-led program consisting of three sessions was implemented. Over three days, all patients completed the first session in-person, in groups of 6-12 people, to receive device training. Subsequently, the automatic mode was activated virtually (session 2), followed by online data download (session 3). Glucometric outcomes were evaluated after one month, along with serious adverse events (SAEs), technical incidents, and perceived satisfaction.
ResultsThe switch was performed in 125 patients, 56.8% of whom were women, with a mean age of 44.1±14.9 years. 99.2% (n=124) initialized auto-mode. There was an increase in time in range 70-180mg/dl (64.3±11.3 vs. 74.7±11.2; P<.001) and a decrease in time below 70mg/dl (4.1±3.9 vs. 2.0±1.8; p<0.001) (N=97). Forty-one related calls were received, with 10 requiring in-person visits. Medtronic technical service handled 92 related calls (0.74 per patient), from 47 different users (37.6%). One event of severe hypoglycemia was recorded as an SAE. Perceived security and satisfaction with the switch process were high in 91% and 92% of patients, respectively.
ConclusionsMassive switch from SAP to AID in T1D patients at high risk of hypoglycemia is feasible and safe through a hybrid program conducted in collaboration with the manufacturer.
Los sistemas automáticos de administración de insulina (AID, del inglés Automated Insulin Delivery) han supuesto un cambio de paradigma en el tratamiento de la diabetes tipo 1 (DT1)1. Estos sistemas incorporan un algoritmo de control capaz de automatizar la infusión de una bomba de insulina a partir de la integración de datos de monitorización continua de la glucosa (MCG) para mantener las cifras de glucemia en los objetivos prefijados, minimizando la intervención del usuario.
En ensayos clínicos aleatorizados comparativos con la terapia bomba/sensor (SAP, del inglés sensor-augmented pump), el uso de los sistemas AID ha demostrado disminuir la HbA1c un 0,15-0,33% y aumentar el tiempo en rango 70-180mg/dl (TIR) un 9-12%, logrando un TIR promedio cercano al 70% (65,0-71,2%)2–6. Estos resultados se han obtenido sin aumentar el tiempo en hipoglucemia o incluso disminuyéndolo. Además, han demostrado una franca superioridad frente al tratamiento estándar de la DT1 en nuestro medio (múltiples dosis de insulina y MCG), reduciendo la HbA1c un 1,4% en los pacientes con control glucémico subóptimo previo7.
El inicio de la implantación de estos dispositivos en nuestro entorno también se ha asociado en vida real con aumentos rápidos8 y mantenidos del TIR, con independencia del tratamiento previo9–12, así como a descensos del tiempo en hipoglucemia9,11–13 y una mejoría de la percepción de la hipoglucemia14. Asimismo, su inicio se ha asociado a una disminución de la carga neuropsicológica asociada a la DT113 y a un aumento de la satisfacción con el tratamiento15. Dichos resultados se han observado con los distintos sistemas AID disponibles en la actualidad, sin observar diferencias significativas entre ellos en los escasos estudios comparativos a día de hoy16.
Ante la abundante evidencia científica disponible, las guías de práctica clínica más recientes recomiendan considerar el inicio de este tratamiento en prácticamente cualquier paciente con DT1 capacitado para su uso17–19. Asimismo, alguna guía proveniente de un sistema público de salud, como el inglés, ya recomienda el uso de estos dispositivos en todos aquellos sujetos con control glucémico subóptimo (HbA1c≥7,5%) o con hipoglucemias recurrente20, aunque la evidencia específica en población con alto riesgo de hipoglucemia ha sido escasamente evaluada14,21,22.
En España aproximadamente el 20% de las personas con DT1 son usuarias de infusores subcutáneos continuos de insulina (ISCI)23, pero los múltiples beneficios observados con los sistemas AID pueden propiciar un aumento exponencial de su uso en los próximos años. En la Unidad de Diabetes del Hospital Clínic de Barcelona, especializada en este tipo de terapia y que sigue activamente a 2.000-2.500 personas con DT1, el número de usuarios de ISCI supera los 500 pacientes. En el momento de realización de este estudio, aproximadamente una cuarta parte de estos contaban con un sistema integrado SAP, mientras que el uso de sistemas AID era residual (<5%). En un contexto como el nuestro, se necesita evidencia de la viabilidad, efectividad y seguridad de programas de recambio masivo a sistemas AID, pudiendo ser de especial interés precisamente en subpoblaciones con hipoglucemias recurrentes.
El objetivo de este estudio fue evaluar la efectividad de un programa de recambio masivo de terapia SAP con prestaciones avanzadas a sistemas AID en sujetos con DT1 y alto riesgo de hipoglucemia en una unidad de diabetes de referencia. Asimismo, como objetivos secundarios, se evaluó la satisfacción referida por los pacientes y la seguridad durante el proceso.
Material y métodosDiseño del estudio y participantesEstudio observacional y ambispectivo, realizado en la Unidad de Diabetes del Hospital Clínic de Barcelona. Se incluyeron adultos con DT1 usuarios de terapia SAP con parada en predicción de hipoglucemia (Medtronic MiniMed® 640G [Medtronic-Minimed, Northridge, CA, EE. UU.] con sensor Guardian 3®), iniciada bajo financiación pública por hipoglucemias de repetición: >4 eventos de hipoglucemia leve-moderada a la semana y/o ≥2 hipoglucemias graves (necesidad de ayuda de terceros para su resolución) en los últimos 2 años, pese al uso de una bomba de insulina. Asimismo, en todos ellos se minimizó el riesgo de hipoglucemia durante el seguimiento mediante educación terapéutica específica. En contexto de una licitación y concurso público en nuestro centro, el tratamiento con SAP en todos estos pacientes fue cambiado masivamente a un sistema AID (MiniMed® 780G con sensor Guardian 4®) en un plazo de 3 días (13-15 de marzo de 2023). Previo al cambio, los pacientes fueron sistemáticamente incluidos en el estudio.
El proceso de recambio masivo de terapia incluyó un programa híbrido (presencial y virtual) de 3 sesiones grupales a cargo del fabricante. El programa educativo fue aprobado y supervisado por el equipo de educación terapéutica de nuestro centro y parte de dicho equipo había participado en la elaboración del mismo a nivel nacional. La primera sesión fue presencial en grupos de 6-12 personas, de 2-3h de duración y se entrenó en el uso del ISCI y el MCG, haciendo hincapié en las escasas diferencias técnicas respecto a los dispositivos previos. En la segunda sesión, de 1h de duración y realizada telemáticamente por videoconferencia al cabo de 1 semana y en grupos de 10-15 personas, se explicó detenidamente y se inicializó la función de modo automático. Dado que se trataba de una población con antecedente de hipoglucemias de repetición, se programó de forma conservadora y generalizada un objetivo de glucosa de 110mg/dl y un tiempo de insulina activa de 3h, hasta la valoración y el ajuste por el equipo médico habitual. Finalmente, en la tercera sesión, de 1h de duración y realizada de modo virtual en grupos de 10-20 personas y una semana después de la segunda, se abordó cómo activar la descarga automática de datos online al sistema CareLink™ cada 24h mediante dispositivo móvil y, alternativamente, cómo realizarlo manualmente en el ordenador personal mediante conexión del ISCI.
El protocolo del estudio fue aprobado por el Comité Ético de nuestro centro (HCB/2022/0473) y se llevó a cabo según los principios de la Declaración de Helsinki. Los pacientes fueron incluidos después de dar su consentimiento informado.
ProcedimientosLas características iniciales de los pacientes se recogieron en el momento de la inclusión (sexo, edad, duración de la diabetes, HbA1c). En el momento del recambio de ISCI se realizó una descarga de datos glucométricos y del uso de insulina de los últimos 14 días. Se incluyó el uso del sensor, unidades totales de insulina administrada, glucosa media, coeficiente de variación (CV), glucose management indicator (GMI) y proporción (%) de TIR, tiempo en hipoglucemia (<54mg/dl [TBR<54] y <70mg/dl [TBR<70]) y en hiperglucemia (>180mg/dl [TAR>180] y >250mg/dl [TAR>250]). De igual manera, estas variables, así como el porcentaje de tiempo en modo automático, se recogieron para cada paciente tras >30 días de la activación del modo automático. En este caso los datos se obtuvieron directamente de las descargas automáticas en la plataforma CareLink™.
Asimismo, al finalizar el proceso de recambio se analizó mediante cuestionarios la satisfacción y la seguridad de los pacientes con el programa de recambio realizado (Tabla suplementaria 1). Tras un mes de uso del sistema AID, también se evaluó mediante cuestionarios la satisfacción con el nuevo dispositivo (Tabla suplementaria 2). En ambos casos se utilizaron cuestionarios no validados, por ausencia de alternativas en el caso del proceso de recambio y por interés en la valoración de parámetros vinculados a la tecnología de diabetes que no se evalúan con los cuestionarios validados en la actualidad en el caso del tratamiento. Finalmente, se recogieron prospectivamente los eventos adversos graves (EAG) (cetoacidosis diabética o hipoglucemia grave) durante los 2 meses de proceso de recambio, así como el número de incidencias atendidas por el fabricante, las llamadas hospitalarias relacionadas y las posteriores visitas educativas asociadas durante este periodo.
ObjetivosEl objetivo primario fue evaluar la efectividad en términos de control glucémico medido por TIR, incluyendo como objetivos secundarios predefinidos la efectividad en reducción del tiempo en hipoglucemia (TBR<70 y TBR<54) y la seguridad en el proceso medida con la presencia de EAG durante el proceso de recambio. Además, se evaluó la viabilidad medida por el porcentaje de recambios realizados con éxito, así como por la cifra de incidencias técnicas (atendidas por el fabricante) y clínicas (atendidas en nuestro centro). Finalmente, se evaluó el grado de satisfacción de los pacientes con el programa de recambio y con el sistema AID.
Análisis estadísticoLos datos se presentan como media ± desviación estándar o como porcentajes. Las comparaciones de variables continuas se realizaron mediante la prueba t de Student para muestras relacionadas. El análisis estadístico se realizó mediante el software R, versión 4.3.1, (R Foundation for Statistical Computing, Viena, Austria). Todas las pruebas estadísticas fueron bilaterales y un valor de p<0,05 se consideró estadísticamente significativo.
ResultadosSe incluyeron un total de 125 sujetos, 71 de los cuales eran mujeres (56,8%), y presentaban una edad media de 44,5±12,3 años. La duración media de la DT1 fue de 27,9±11,4 años y la HbA1c media de los participantes fue de 7,4±0,8%. Los participantes eran usuarios de terapia SAP desde hacía 3,9±1.9 años. La media de hipoglucemias graves en el último año fue de 0,14±0,55, con una prevalencia de ≥1 evento del 8% (n=10). Respecto a la asistencia a las 3 sesiones, esta fue del 96,0, 97,6 y 83,9%, respectivamente. El cambio de dispositivo se realizó efectivamente en todos los sujetos, pero el modo AID fue inicializado en 124 personas (99,2%). Solo una persona decidió no iniciar modo automático y mantenerse en modo manual por preferencia.
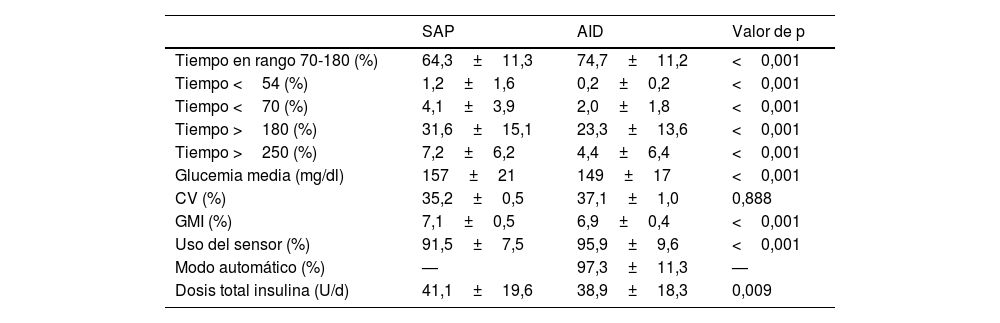
Se obtuvieron datos glucométricos previos y tras un mes del recambio en 97 sujetos (77,6%) (tabla 1), sin poder obtener datos en el resto por problemas con la aplicación móvil o de conectividad. El TIR medio aumentó del 64,3±11,3% al 74,7±11,2% (p<0,001), observándose también un descenso del TBR<70 (4,1±3,9 vs. 2,0±1,8; p<0,001) y del TBR<54 (1,2±1,6 vs. 0,2±0,2; p<0,001). El GMI también disminuyó del 7,1±0,5% al 6,9±0,4% (p<0,001). Dichos cambios se obtuvieron con una menor dosis de insulina total diaria (41,1±19,6 vs. 38,9±18,3; p=0,009). Tras el cambio a terapia AID, los pacientes se mantuvieron el 97,3% del tiempo en modo automático y se observó un aumento significativo del uso del sensor (91,5±7,5% vs. 95,9±9,6%; p<0,001). Como efecto adverso grave se registró únicamente una hipoglucemia grave, atribuida a un mal recuento de los hidratos de carbono en la ingesta previa y a consumo de alcohol. No se reportó ninguna cetoacidosis.
Datos glucométricos tras un mes de uso del sistema automático de administración de insulina, comparado con los datos basales con el uso de la terapia bomba/sensor (n=97)
| SAP | AID | Valor de p | |
|---|---|---|---|
| Tiempo en rango 70-180 (%) | 64,3±11,3 | 74,7±11,2 | <0,001 |
| Tiempo <54 (%) | 1,2±1,6 | 0,2±0,2 | <0,001 |
| Tiempo <70 (%) | 4,1±3,9 | 2,0±1,8 | <0,001 |
| Tiempo >180 (%) | 31,6±15,1 | 23,3±13,6 | <0,001 |
| Tiempo >250 (%) | 7,2±6,2 | 4,4±6,4 | <0,001 |
| Glucemia media (mg/dl) | 157±21 | 149±17 | <0,001 |
| CV (%) | 35,2±0,5 | 37,1±1,0 | 0,888 |
| GMI (%) | 7,1±0,5 | 6,9±0,4 | <0,001 |
| Uso del sensor (%) | 91,5±7,5 | 95,9±9,6 | <0,001 |
| Modo automático (%) | — | 97,3±11,3 | — |
| Dosis total insulina (U/d) | 41,1±19,6 | 38,9±18,3 | 0,009 |
Los datos se expresan en media±desviación estándar.
AID: automated insulin delivery o sistemas automáticos de administración de insulina; CV: coeficiente de variación; GMI: glucose management indicator; SAP: sensor-augmented pump o terapia bomba/sensor.
Durante el proceso de recambio se recogieron sistemática y prospectivamente todas las incidencias técnicas y clínicas (tabla 2). Se recibieron a nivel hospitalario 41 llamadas relacionadas por parte de los pacientes, de las cuales 10 requirieron la programación de una visita presencial posterior para completar educación terapéutica. El servicio técnico de Medtronic atendió de forma telefónica 220 incidencias de pacientes en seguimiento en nuestro centro entre los meses de marzo-abril, representado un incremento del 142% respecto al mismo periodo del año previo. De estas, 92 incidencias estaban relacionadas con el proceso de recambio (media de 0,74 incidencias por paciente), provenientes de 47 personas (37,6%). Las incidencias fueron mayoritariamente por problemas relacionados con el MCG (51 incidencias; 55,4%), seguido de problemas con la aplicación móvil o la descarga de datos (17 incidencias; 18,5%), con el ISCI (14 incidencias; 15,2%) o con el material fungible o el insertador (10 incidencias; 10,9%).
Incidencias clínicas y técnicas durante el proceso de recambio
| N.° | |
|---|---|
| Incidencias atendidas por el fabricante | |
| Totales durante el periodo (porcentaje respecto mismo periodo del año previo) | 220 (+142%) |
| Relacionadas con el proceso de recambio | 92 |
| Llamadas hospitalarias relacionadas | 41 |
| Visitas educativas asociadas | 10 |
| Eventos adversos graves | |
| Hipoglucemia grave | 1 |
| Cetoacidosis diabética | 0 |
Respecto a los datos de satisfacción (tabla 3), todos los pacientes respondieron la encuesta al finalizar el programa y manifestaron una satisfacción global con el proceso de recambio de 8,6±1,3 (puntuación: 0-10), valorando con un 8,4±1,6 (puntuación: 0-10) la duración del entrenamiento y con un 8,2±1,9 el formato híbrido (presencial/virtual) utilizado. Preguntados sobre la probabilidad de recomendar el programa de recambio realizado (del 0 al 10), el Net Promoter Score (NPS; porcentaje de puntuaciones 9-10 menos porcentaje de puntuaciones 0-6) fue del 73%. Tras un mes de uso del sistema AID, los pacientes (N=84) mostraron una satisfacción del 8,9±0,8 y de 8,6±0,8 (puntuación: 0-10) en términos de calidad de vida y control glucémico, respectivamente. La peor puntuación con el nuevo sistema fue respecto a la conectividad con dispositivos móviles (7,4±1,1; puntuación: 0-10).
| Puntuación (0-10) | |
|---|---|
| Satisfacción global con el proceso de cambio de dispositivo | 8,6±1,3 |
| Satisfacción con la duración del entrenamiento con el nuevo dispositivo | 8,4±1,6 |
| Satisfacción con el formato híbrido de recambio utilizado | 8,2±1,9 |
| Satisfacción con el sistema AID tras un mes de su inicio | |
| Calidad de vida | 8,9±0,8 |
| Control global de la glucemia | 8,6±0,7 |
| Manejo situaciones de hiper e hipoglucemia | 8,1±0,9 |
| Control posprandial | 7,9±0,9 |
| Conectividad de las aplicaciones | 7,4±1,1 |
AID: automated insulin delivery o sistemas automáticos de administración de insulina.
En nuestra cohorte de pacientes con DT1 y alto riesgo de hipoglucemias en tratamiento con SAP, el recambio masivo a un sistema AID mediante un programa híbrido (presencial y virtual) fue factible, efectivo y seguro. Además, los pacientes se mostraron satisfechos no solo con el cambio del dispositivo, sino también con el formato de programa realizado.
La terapia SAP con predictive low glucose suspend (PLGS, parada en predicción de hipoglucemia) ha demostrado ser eficaz en reducir el tiempo en hipoglucemia sin empeoramiento de la HbA1c, tanto en ensayos clínicos24 como en estudios en vida real25. Además, también se ha mostrado eficaz y segura en la reducción de hipoglucemias e HG en población de alto riesgo con percepción alterada de las hipoglucemias26. Pese a eso, la hipoglucemia clínicamente significativa sigue siendo un riesgo no despreciable27, y el desarrollo de nuevas tecnologías resulta necesario para minimizarlo y poder alcanzar los objetivos de control recomendados28. En este sentido, la irrupción de los sistemas AID representa una estrategia prometedora, aunque la evidencia específica para este subgrupo de pacientes es escasa21,29. En nuestro trabajo con una cohorte de pacientes con hipoglucemias graves de repetición, el recambio de un sistema SAP a AID fue efectivo, reduciendo rápidamente el tiempo en hipoglucemia a la mitad y minimizando el tiempo <54mg/dl. Además, dichos cambios se asociaron a un aumento significativo del TIR medio y a una alta satisfacción por parte de los pacientes con el nuevo dispositivo.
Considerando los múltiples beneficios observados hasta la fecha tanto en control glucémico como en calidad de vida con el inicio de los sistemas AID, estos dispositivos ya están recomendados en prácticamente todos los pacientes con DT118 y se prevé un aumento exponencial de su uso en los próximos años, incluso en el contexto de sistemas públicos de salud30. Sin embargo, en nuestro entorno el uso de ISCI se sitúa actualmente en torno al 20% de los individuos con DT123 y no contamos con experiencias previas publicadas de la efectividad y seguridad en vida real de programas de implantación masiva de sistemas AID. En este sentido, sí contamos con experiencias previas exitosas de programas específicos para la rápida implementación de tecnología en el tratamiento de la diabetes, como es el caso de la MCG tras su financiación por el sistema público de salud31–33. Nuestro trabajo añade nueva información al respecto y demuestra que la implantación masiva de los sistemas AID, en sujetos previamente usuarios de SAP, también puede ser viable, segura y efectiva. Mediante un programa grupal híbrido de 3 sesiones realizadas a lo largo de 3 semanas con la colaboración del fabricante, se pudo realizar el cambio simultáneo de terapia con una excelente efectividad. Asimismo, la seguridad y satisfacción percibidas con el proceso de cambio fue alta (>7/10) en el 91 y 92% de los pacientes. Pese al esperable aumento de las incidencias técnicas durante ese periodo, la mayoría de estas fueron resueltas por el servicio técnico del fabricante y no tuvo un impacto significativo a nivel hospitalario. En un entorno donde los recursos necesarios adicionales no siempre están a plena disposición de los equipos asistenciales, la colaboración desde el Sistema Público de Salud con el fabricante en la preparación y realización de un programa de recambio se plantea como una alternativa factible y segura.
Nuestro estudio tiene algunas limitaciones. Primero, se trata de un estudio observacional y, por lo tanto, no se puede establecer causalidad. Asimismo, los datos glucométricos se obtuvieron de 2 períodos cortos y desconocemos si los hallazgos positivos pueden extenderse durante un período más largo. Además, cabe señalar que no se pudieron obtener datos glucométricos antes y después del recambio en todos los sujetos, en probable relación con una menor asistencia a la tercera sesión del programa y a la incompatibilidad de algunos dispositivos móviles para realizar la descarga automática de datos online. Desafortunadamente tampoco contamos con información del tiempo entre la realización del recambio y la primera visita con el equipo médico. Finalmente, la inclusión de una muestra homogénea de un solo centro terciario puede no ser representativa de otros subgrupos, áreas geográficas o centros médicos, lo que impide la generalización a poblaciones más amplias. Asimismo, dado el diseño del estudio, no es posible establecer la factibilidad y la seguridad de un proceso de recambio masivo sin la colaboración del fabricante.
Nuestro trabajo también tiene fortalezas. La primera de ellas es que la mayoría de los datos se recogieron de forma prospectiva, contando con un registro de incidencias tanto del fabricante como a nivel hospitalario. Además, la robustez de los resultados se sustenta en la estandarización de un programa realizado para su posterior implantación en la práctica clínica. Asimismo, este es el primer estudio que evalúa un programa masivo de recambio de sistemas SAP a AID, así como el primero en estudiar la efectividad y seguridad del inicio de un sistema AID específicamente en una cohorte de sujetos con hipoglucemias de repetición.
En resumen, el recambio masivo de un sistema SAP a AID en pacientes con DT1 y alto riesgo de hipoglucemia es factible, efectivo y seguro mediante un programa híbrido (presencial y virtual) y en colaboración con el fabricante.
Conflicto de interesesO.M. y J.C. son empleadas de Medtronic. Los demás autores no manifiestan ningún conflicto de intereses en relación con la redacción de este artículo.
Agradecemos a Medtronic su ayuda en la obtención y análisis estadístico de los datos que han contribuido a la redacción de este artículo.