Green Chemistry entails a philosophy which is summarized in the twelve principles enunciated by Anastas and Warner, and whose aim is an industrial chemical process based on clean and safe reactions. This philosophy applies as well to other industries and activities which are based on chemical conversions, or on use of chemicals. Study of the industrial chemical process allows the visualization of convenient strategies for its greening, which are to be accomplished by related research or development fields, such as use of renewable source materials, substitution of traditional organic solvents, use of catalytic and biocatalytic procedures, or selective activation of reacting molecules. Previous to the industrial process, although with much later effects on the environment, new chemicals must be designed to fulfill conveniently their function and to be easily recycled o degraded at the end of their use.
Se puede afirmar sin temor a la exageración que la vida contemporánea, y cualquiera de los aspectos que la caracterizan, resultan imposibles sin los conocimientos que proporciona la química como ciencia, y sin la aplicación que de ellos hace la industria. Pero resultan innegables, así mismo, los efectos nocivos asociados a la actividad química industrial de los dos últimos siglos. La química verde nació en la Environmental Protection Agency (EPA) de Estados Unidos de América en los inicios de los 1990 como un enfoque y una herramienta conceptual para la protección del medio ambiente ante la contaminación originada por la industria química, y fue expresada de manera sucinta y atractiva por medio de los 12 principios de Paul Anastas y John Warner (1998). Resultaba evidente desde sus orígenes que no resultaría eficaz este instrumento a menos que la industria lo hiciera suyo. La experiencia en América, Europa y Japón demuestra que su mensaje ha penetrado ya la mente del químico industrial por consideraciones no sólo éticas, sino también económicas. En efecto, su aplicación conduce a modificaciones económicamente rentables en los procesos industriales, en parte al reducir sustancialmente los costes de las químicas e ingenierías paliativas, imprescindibles cuando se generan y manejan sustancias peligrosas.
Se puede resumir el pensamiento de Anastas y Warner que llevó a la formulación de sus principios en tres apartados fundamentales y distintivos: a) Prevención de la causa de riesgo; b) Metodologías químicas, y c) Acción de acuerdo con un diseño.
La prevención de la causa de peligro es el mensaje del primer principio de Anastas y Warner. Resulta evidente que la mejor opción cuando se trata de cuestiones de sustancias y materiales peligrosos es evitarlas en su misma fuente (v. Principio 1).
Por “metodologías químicas” se pretende significar que la contaminación y los peligros que tienen su origen en las sustancias químicas deben tener también solución química: la química y la ingeniería química del propio proceso. El énfasis en la metodología química es compatible con el trabajo conjunto de la química y la ingeniería con la biología y otras áreas científicas y tecnológicas; pero es radicalmente distinto de la química y la ingeniería que trata de evitar la dispersión y efectos de las sustancias y residuos contaminantes y peligrosos generados o empleados en la planta industrial.
El término “diseño” se encuentra en casi todos los escritos y conferencias de Paul Anastas (2007) y pone de relieve que, para que se pueda hablar propiamente de química verde, el reverdecimiento de la actividad debe ser fruto, no de la casualidad, sino de un propósito definido y de una planificación orientada precisamente a la consecución de un proceso más eficiente, inherentemente limpio y seguro.
2Química sostenibleEl término “Green Chemistry” fue acuñado y definido por primera vez por Anastas y es hoy umversalmente aceptado. Química Sostenible es una traducción preferida cuando el término “verde” no parece adecuado en el contexto social del país, aunque los dos términos no son totalmente equivalentes. En efecto, “sostenible”, en el contexto de la química, responde a la obligación ética de contribuir al desarrollo y bienestar de todas las naciones del planeta, sin afectar a la naturaleza ni a las generaciones futuras. Esta contribución tiene lugar de manera primordial por la sostenibilidad de la propia actividad química industrial, que ve amenazada la viabilidad de su producción por el previsible agotamiento irreversible de las fuentes de las materias de partida, y por las normativas legales, formuladas en defensa de la sociedad y de la naturaleza, cada vez más estrictas y económicamente onerosas.
Química Sostenible designa más claramente una finalidad general: la reducción de la contaminación por las sustancias nocivas para la salud y para el medio ambiente, sin merma de las ventajas sociales que aporta la actividad química. La Química Verde, en el sentido que Anastas y Warner dan a Green Chemistry, contiene los principios de actuación para conseguir la sostenibilidad en la producción de las sustancias químicas (Warner, Cannon & Dye, 2004). Los principios de Anastas y Warner constituyen así el instrumento eficaz y el fundamento del modo de pensar propio de la química sostenible.
De alguna manera podría presentarse la Química Sostenible como la química del siglo xxi. Sería una pretensión excesiva, ya que existen otros temas sustanciales para el progreso de la química que quedan fuera de su ámbito. Sin embargo, sí puede reclamarse que todas las aplicaciones de la química sean sostenibles.
3Ámbito de la Química SostenibleLos “12 principios” están dirigidos primordialmente a la química preparativa, y los mayores éxitos de su aplicación se han dado en las industrias de química fina y farmacéutica. Sin embargo, a la química del siglo xxi se le presenta un reto de ámbito mucho más amplio: cortar en su mismo origen cualquier tipo de contaminación y riesgo debido a las sustancias y conversiones químicas.
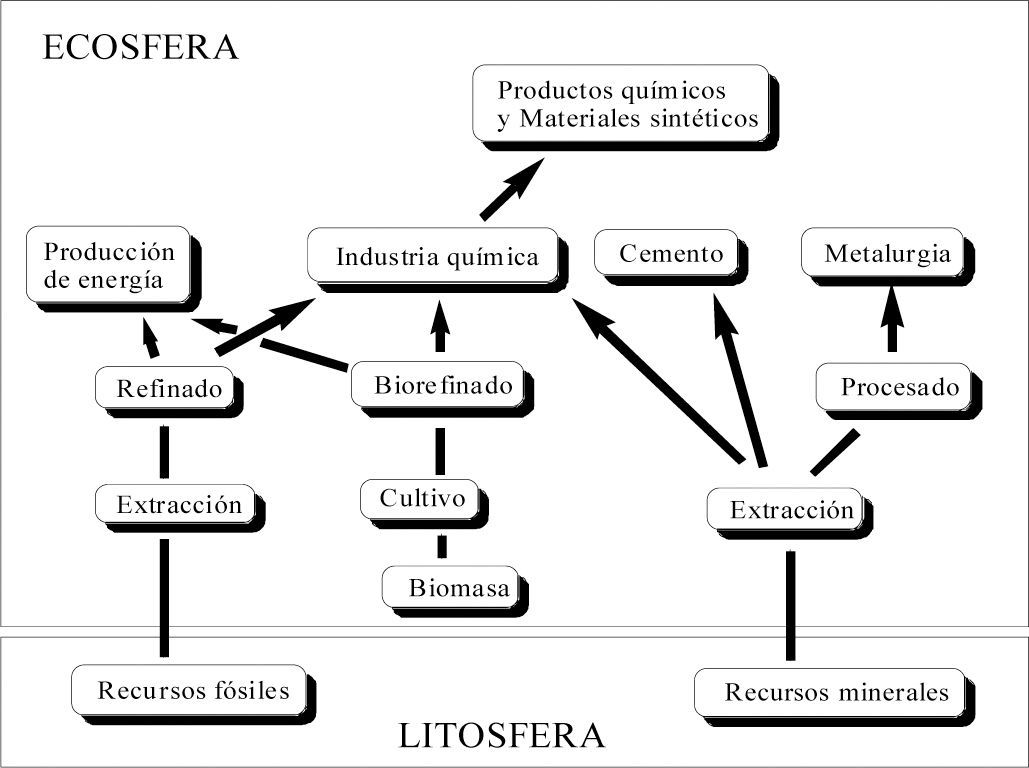
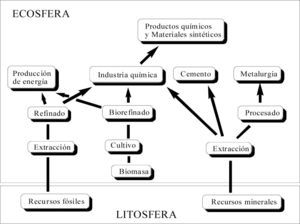
La demanda social de bienes materiales es satisfecha por diversos tipos de industrias y sectores, que se pueden presentar en cuatro grupos: producción de energía (incluido el transporte), industria química, cemento (y otros materiales de construcción) y metalurgia (figura 1). Existe un quinto grupo importante que comprende el amplio espectro de sectores y actividades que usan productos y materiales derivados de la industria química: farmacia, agricultura, fibras y colorantes textiles, materiales plásticos, pigmentos, disolventes, papel, etc. Todos estos sectores sin excepción: a) contribuyen directamente a la generación y emisión de contaminantes químicos, y b) se nutren fundamentalmente de materiales extraídos del subsuelo. Así, por ejemplo, la producción de energía eléctrica por combustión de carbón es uno de los orígenes principales del dióxido de carbono, de los óxidos de azufre y nitrógeno, del mercurio y de otros metales tóxicos, emitidos a la atmósfera. La utilización de sustancias químicas en la agricultura ha conducido a la diseminación por todo el planeta de los insecticidas policlorados, mientras que una multitud de aplicaciones tecnológicas ha justificado el amplio uso de los policlorobifenilos (PCB), también presentes en todo el planeta. Los plásticos son particularmente persistentes en el medio ambiente y aparecen diseminados en multitud de lugares. Algo parecido ocurre con el cemento y otros materiales de construcción.
Por otra parte, la extracción de petróleo y gas del subsuelo, la minería del carbón y los imprescindibles procesos de limpieza y refinado son orígenes muy importantes de contaminación. Lo mismo es válido para la minería, metálica y no metálica, el procesado inmediato de los minerales y la metalurgia del hierro, del acero y de otros metales, causantes de contaminación fuerte y persistente por metales tóxicos, polvo y ácidos de roca (Bridge, 2004).
En este contexto resulta conveniente añadir tres consideraciones. En primer lugar, la simple introducción en la ecosfera de materiales hasta ahora mantenidos en el subsuelo supone un incremento del potencial global de contaminación. En segundo lugar, la condición limitada de las fuentes de materiales fósiles disponibles en el planeta para la producción de energía y para la industria química orgánica, obliga a la búsqueda de fuentes alternativas. El agotamiento irreversible de las fuentes es válido, así mismo, para los metales escasos, y no se puede olvidar que el agua es localmente escasa en algunos países en desarrollo, y puede serlo de manera general en un próximo futuro.
Como tercera consideración, el incremento antropogénico de la concentración de los gases invernadero en la atmósfera es una forma de contaminación. Este incremento provoca un desajuste en el estado estacionario del efecto invernadero y puede contribuir de manera sustancial al calentamiento global. Excepto los compuestos halocarbona-dos, cuya sustitución por otras sustancias inocuas es un tema de alta prioridad en la industria química, los gases invernadero estaban ya presentes en la atmósfera antes de la era industrial; las emisiones asociadas a la actividad humana contribuyen simplemente a la elevación de su concentración. Se trata de una situación de contaminación debida al incremento de concentración de un componente natural (Doménech, 1999).
Debe esperarse de la química una contribución relevante al reverdecimiento de todos los sectores productivos mostrados arriba. Esto supone la minimización de la introducción en la ecosfera, y de la generación, de materiales susceptibles de contribuir a la contaminación y de ocasionar otros efectos nocivos. Las estrategias sostenibles, los campos de investigación y los progresos alcanzados son notables en industrias como la química fina y la farmacéutica, pero la definición de rutas para la contribución química al reverdecimiento de la metalurgia, la producción de cementos o la reducción del recurso a los carburantes de origen fósil, queda muy por detrás. Bajo la orientación de estas estrategias se abren unos campos en los que la química debe aportar soluciones efectivas (Mestres, 2008ab).
4Reducción de la utilización y generación de materiales químicos contaminantes o peligrosos en los procesos de producciónLos procesos de producción de cemento, hierro, acero y otros metales se basan en conversiones químicas que parten de mezclas de materiales de origen mineral. La mejora de estos procesos con el fin de reducir su consumo energético, la generación de dióxido de carbono en el propio proceso y la emisión de metales tóxicos a la atmósfera constituye un gran desafío para la química. Algunos estudios ya muestran que es posible la manufactura del cemento con menor consumo energético y mejor calidad del producto y rentabilidad económica, a partir de productos reciclados o de desechos del tratamiento de minerales (Phair, 2006).
La química ha prestado desde la mitad del siglo xix una especial atención al proceso químico industrial, que se reorienta ahora bajo la óptica de la Química Verde y Sostenible, con su reverdecimiento como objetivo.
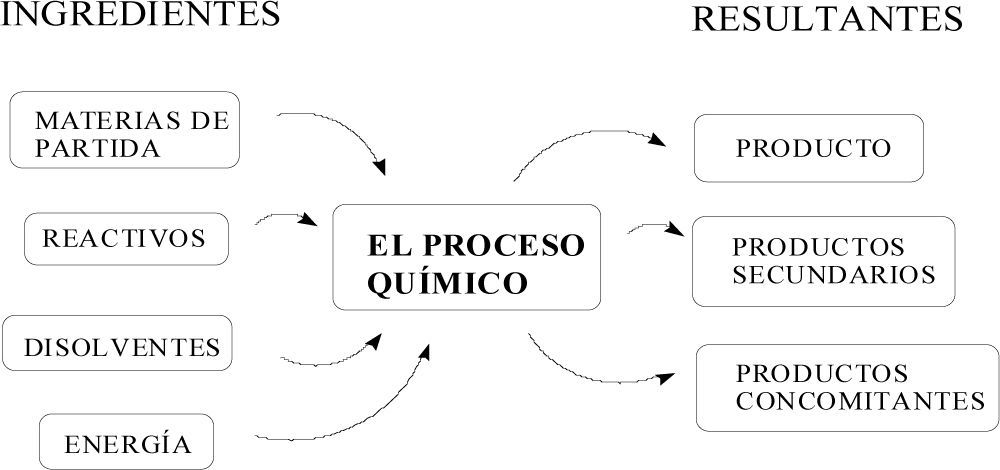
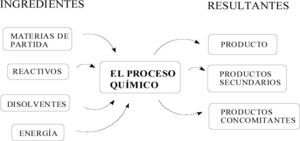
En el proceso químico unas materias de partida sufren conversión en el reactor bajo la acción de unos reactivos, con frecuencia en presencia de catalizadores. Los disolventes facilitan la mezcla de los reactivos y participan después en los procedimientos de aislamiento y purificación (figura 2). Se emplea energía en la calefacción, la refrigeración y la agitación en las fases previas, en la conversión química como tal, en la separación y purificación del producto, y en la recuperación de disolventes y de los otros materiales auxiliares usados. El producto de la reacción puede ser un intermedio de síntesis o bien un producto para ser suministrado a otro sector industrial, pero viene casi siempre acompañado de unos productos secundarios, resultantes de las rutas de conversión que compiten con la principal, y de unos productos concomitantes, aquellos que aparecen formulados en la ecuación química completa. Los productos secundarios y concomitantes, junto con los disolventes, constituyen la masa principal de los residuos del proceso.
4.1Reverdecimiento de los materiales ingredientesResulta evidente que una industria química sostenible no puede basar su producción en materias de partida escasas, con fuentes susceptibles de agotamiento irreversible, tal como es el caso de los materiales fósiles, de algunos metales y del agua (v. Principio 7).
Sin duda la reducción del uso de materiales fósiles en la producción industrial ha de venir de la mano del empleo eficiente de la biomasa. Además de una fuente importante de carburantes, la biomasa puede proporcionar materias primas para la industria química orgánica. Todos los esfuerzos y logros en la preparación de combustibles, como el etanol, el gas de síntesis o el glicerol, a partir de la biomasa, son válidos en relación a materias primas industriales (Corma, Iborra & Velty 2007; Díaz-Álvarez et al., 2011). Existe una variedad de sustancias oxigenadas obtenibles mediante procesos fermentativos a partir de los carbohidratos del material lignocelulósico, que pueden constituir bloques útiles para la síntesis, y que resultan difícilmente asequibles a partir de los materiales de origen fósil. Para mayor interés, algunas de ellas son obtenidas en forma homoquiral, especialmente conveniente para la preparación de sustancias con actividad farmacológica. Por otro lado, además de los productos naturales tradicionales, la manipulación de grandes cantidades de materia vegetal, exigida por la producción de combustibles, puede hacer rentable la obtención de sustancias tales como hormonas vegetales, vitaminas, aminoácidos, o azúcares, que se encuentran en cantidades pequeñas en la planta y que hasta hace poco tiempo resultaba impensable separar o modificar de manera sostenible (Martín-Luengo et al., 2011).
La producción directa de plásticos por procesos fermentativos a partir de la glucosa o de otros azúcares presenta también un interés especial. Los polihidroxialcanoatos y el ácido poliláctico han demostrado poseer propiedades excelentes para competir con plásticos del tipo del polietileno o poliestireno, con el atractivo adicional de ser biodegradables (Krochta & De Mulder, 1996).
Cabe añadir aquí que el reciclado químico de los plásticos puede convertirse en un medio de recuperación de los productos derivados de las fuentes fósiles, y que por lo tanto constituye una especie de fuente de materia prima renovable (Aguado & Serrano, 1999).
Otra clase de materiales susceptibles de agotamiento irreversible son algunos de los metales empleados como catalizadores en la síntesis orgánica. Algunos de ellos, como paladio, rutenio, rodio e iridio han estado confinados en sus yacimientos durante millones de años, por lo que resultan totalmente extraños al ambiente. Su uso hace imprescindible evitar su difusión ambiental, con un impacto absolutamente desconocido, que puede resultar persistente e irreversible (Poliakoff & Licence, 2007; Cano, Ramón & Yus, 2011). De ahí el extraordinario interés del desarrollo de catalizadores basados en metales de transición asequibles y ordinariamente empleados por los seres vivos, tales como hierro, zinc, cobalto, molibdeno (Enthaler, Junge & Beller, 2008), a los que se pueden añadir oro, plata, níquel, cobre (Stephen & Hashmi, 2007; Alonso, Riente & Yus, 2011), metales que, aunque no inocuos, han sido empleados durante muchos siglos, sin mostrar especial peligrosidad ambiental. Dentro de la misma línea de pensamiento, presenta extraordinario interés el desarrollo, muy activo en la actualidad, de la llamada organocatálisis (Alcaide & Almendros, 2008; Dondoni & Massi, 2008; Hernández & Juaristi, 2012), y por supuesto, de la biocatálisis (Faber, 2000; Mestres, 2010; Alcántara, Hernaiz & Sinisterra, 2011).
Cabe también considerar aquí que el agua es o puede ser un componente escaso, especialmente en algunos países. Uno de los Green Chemistry Presidential Awards fue concedido el año 2003 por el desarrollo de un proceso de preparación de óxidos metálicos en el que se evitaba el empleo de agua, requerida en gran cantidad en un procedimiento anterior (Ritter, 2003).
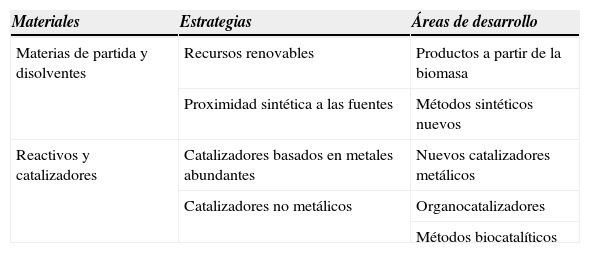
Para la mejora de la sostenibilidad del proceso resulta significativo también el llamado impacto de base de los materiales ingredientes; es decir, el impacto ambiental que ha generado la manufactura de estos materiales a partir de las fuentes. Una estrategia general para la reducción del impacto de base es sin duda el recurso a las fuentes renovables en sustitución de las fósiles, pero debe serlo también la proximidad sintética a las fuentes (tabla 1). A menos que se disponga de valores concretos, se puede asumir que en cada paso sintético empleado en la manufactura del material de partida, catalizador, reactivo, o disolvente del proceso, se generan residuos y se consume energía. Se puede entonces inferir, como aproximación, que cuanto menor sea el número de etapas sintéticas para la manufactura de estos materiales, menor será el impacto acumulado.
Reverdecimiento de los materiales ingredientes.
| Materiales | Estrategias | Áreas de desarrollo |
|---|---|---|
| Materias de partida y disolventes | Recursos renovables | Productos a partir de la biomasa |
| Proximidad sintética a las fuentes | Métodos sintéticos nuevos | |
| Reactivos y catalizadores | Catalizadores basados en metales abundantes | Nuevos catalizadores metálicos |
| Catalizadores no metálicos | Organocatalizadores | |
| Métodos biocatalíticos |
La reducción del número de pasos sintéticos para la manufactura de los ingredientes requiere nuevos métodos que permitan la conversión directa de las mezclas de las fuentes en compuestos definidos. Por ejemplo, nuevas estrategias para la activación del enlace CH pueden evitar la necesidad de productos intermedios halogenados en la introducción selectiva de grupos funcionales del oxígeno (alcoholes, éteres, aldehidos) y del nitrógeno (aminas, amidas) a partir de los hidrocarburos. Hace falta conseguir métodos simples y eficaces que utilicen alcoholes como agentes alquilantes directos, sin la generación de residuos (Alonso, Riente & Yus, 2011).
4.2Reverdecimiento de la conversión químicaLas ideas y avances de la química verde giran de manera primordial alrededor de la reducción de la generación de residuos en el proceso químico y de los riesgos de incendio, explosión e intoxicación en la planta. En este apartado y en los siguientes se presentan las estrategias y áreas con las que se espera conseguir la reducción importante de la generación de residuos por un lado, y de los riesgos en la conversión química por otro (Mestres, 2005).
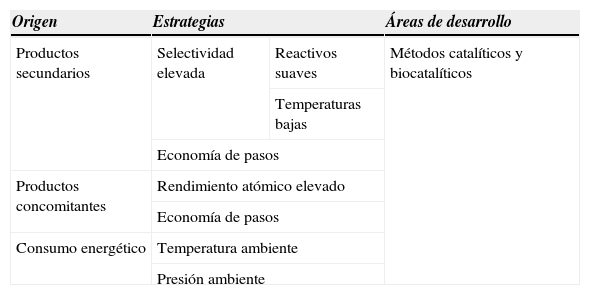
Cualquier estudiante de química es consciente de la importancia de evitar la generación de productos secundarios en una reacción de síntesis. Significan bajos rendimientos y gravan el coste de producción. La novedad estriba ahora en que la formación de los productos secundarios supone la generación de residuos y una separación y purificación del producto más laboriosa y costosa, con cristalizaciones, extracciones, destilaciones o cromatografías que incrementan notablemente la cantidad de residuos y que exigen un consumo adicional de energía (tabla 2).
Reducción de la generación de residuos en la conversión química.
| Origen | Estrategias | Áreas de desarrollo | |
|---|---|---|---|
| Productos secundarios | Selectividad elevada | Reactivos suaves | Métodos catalíticos y biocatalíticos |
| Temperaturas bajas | |||
| Economía de pasos | |||
| Productos concomitantes | Rendimiento atómico elevado | ||
| Economía de pasos | |||
| Consumo energético | Temperatura ambiente | ||
| Presión ambiente | |||
Las estrategias para la reducción de productos secundarios están vinculadas al concepto de selectividad, tan familiar para el químico de síntesis. A una selectividad elevada corresponde la formación de cantidades mínimas de productos secundarios o también la reducción del número de pasos de síntesis (v. Principio 8) (Mestres, 2010). En el contexto de las estrategias para los procesos limpios se puede suponer que un número reducido de etapas de síntesis dé también menores cantidades de productos secundarios y concomitantes, de acuerdo con un argumento totalmente similar al dado arriba para el impacto de base. La economía de pasos, un término acuñado por Paul Wender para la reducción del número de etapas de síntesis, no es nuevo en síntesis orgánica, pero la química verde reconoce que la multiplicación de pasos es ordinariamente causa de multiplicación de residuos y de menores rendimientos globales. El diseño de los procesos “dominó” y “en cascada” es una de las formas de economía de pasos (Wender, Croatt & Witulski, 2006).
Desde el punto de vista mecanístico, la selectividad depende, por lo general, de las diferencias entre las energías de activación de los pasos determinantes de velocidad de reacción de las conversiones que compiten en la mezcla reaccionante. Estas diferencias son mayores cuanto más baja es la temperatura y más suaves los reactivos, de acuerdo con principios bien conocidos de la reactividad. Estas dos condiciones abren entonces un conflicto práctico entre la selectividad y los tiempos adecuados de residencia en el reactor, ya que las bajas temperaturas y los reactivos suaves pueden significar velocidades de reacción demasiado lentas. Los sistemas biológicos superan este conflicto gracias a la disponibilidad de la catálisis enzimática, que conduce a reacciones rápidas y extraordinariamente selectivas con reactivos suaves y a temperatura ambiente. De manera similar, el uso de sistemas catalíticos y biocatalíticos puede llevar a nuevos métodos de síntesis basados en conversiones que transcurren en condiciones suaves (v. Principio 9) (Faber, 2000; Mestres, 2010; Sheldon & van Bekkum, 2001; Sánchez-Montero & Sinisterra, 2007; Climent, Corma & Iborra, 2011; Hudlicky 2011).
En la práctica, la selectividad en el reactor industrial viene afectada por el hecho de que la reacción puede transcurrir exclusivamente bajo control cinético, o bien con equilibración parcial o total. La equilibración se ve favorecida por altas concentraciones de los reactivos, temperaturas elevadas y tiempos prolongados de contacto de los reactantes, y en algunas ocasiones este estado es el que se pretende. Pero el control general y local de la temperatura, la homogeneidad de las concentraciones de los reactivos, así como la brevedad de contacto en el reactor, son cruciales para alcanzar la mejor selectividad posible en una conversión controlada cinéticamente. Son aquí fundamentales las técnicas de análisis a tiempo real para el control de la mezcla reaccionante en el reactor (v. Principio 11), así como el diseño de reactores convenientes, en los que esté asegurada la homogeneidad de las concentraciones y de las temperaturas (Jachuk, 2002; Jachuck, Selvaraj & Varma, 2006; Mason et al., 2007).
Por lo que se refiere a los productos concomitantes, el concepto de economía atómica puede constituir una buena guía en el diseño o la elección de las reacciones químicas más convenientes para reducir su cantidad (v. Principio 2). Una economía atómica óptima supone que todos los átomos de las sustancias reactivas se encuentran en el producto después de la reacción (Trost, 1991). En gran número de reacciones el porcentaje de incorporación es inferior al 100% porque parte de los átomos de los reactantes no aparecen en el producto, sino en los concomitantes, sustancias ajenas al producto, que con cierta frecuencia resultan ambientalmente tóxicas, aunque también pueden ser irrelevantes, como agua, nitrógeno o soluciones diluidas de NaCl o etanol.
La generación de concomitantes viene determinada por la clase de conversión química. Las reacciones de sustitución y de eliminación dan lugar necesariamente a otras sustancias además del producto, contrariamente a lo que ocurre en adiciones y cicloadiciones. Así, la mejora de la economía atómica puede requerir un cambio de clase de reacción. Por otra parte, la economía atómica de una síntesis depende del número de pasos de síntesis, bajo el supuesto de que en cada paso se producen productos concomitantes (v. Principio 8). Los procedimientos catalíticos y biocatalíticos son de nuevo fundamentales, ya que pueden ofrecer la oportunidad de un cambio de clase de reacción, la generación de concomitantes ambientalmente irrelevantes, así como la reducción del número de etapas sintéticas.
La visión de que la generación de energía supone la introducción de materiales fósiles en la ecosfera y la emisión de dióxido de carbono a la atmósfera, justifica que el consumo energético en el proceso pueda ser considerado una forma de contaminación. La minimización del consumo energético es uno de los objetivos tradicionales de la ingeniería química; ordinariamente por razones económicas, pero con nueva motivación ahora. Dado que el mayor consumo energético se produce en la calefacción y en la refrigeración del reactor, o en la presurización en procesos a presión elevada, una estrategia para el ahorro de energía consiste en la realización de los procesos a temperaturas y presiones próximas a las ambientes (v. Principio 6). Es especialmente interesante aquí la circunstancia ya citada, de que las reacciones en los seres vivos tienen lugar ordinariamente a temperaturas próximas a la ambiente.
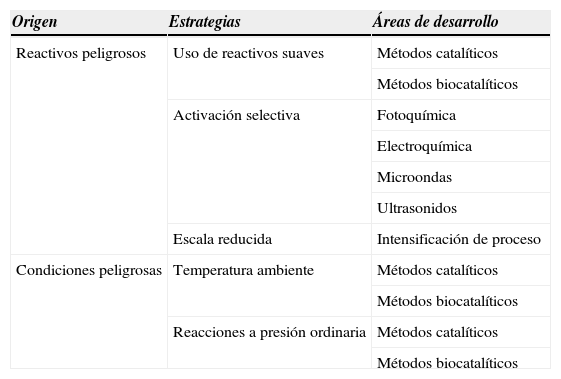
4.3Reducción del uso de reactivos peligrososUna de las posibles estrategias para reducir el peligro de explosión, incendio o fugas de materiales tóxicos puede ser el uso de reactivos más suaves, pero no siempre es la mejor (v. Principio 3). Un reactivo suave puede ser ciertamente más selectivo y menos peligroso, pero por lo general exige mayores tiempos de residencia o temperaturas superiores; y cada una de estas condiciones se opone a la selectividad de la conversión. La sustitución de reactivos peligrosos por otros más suaves resulta factible cuando se puede diseñar una conversión equivalente en la que se emplean catalizadores o biocatalizadores apropiados, con energías de activación más bajas, o en la que se acude a la activación selectiva de algunos de los reactivos (tabla 3). Una activación por irradiación con luz ultravioleta, como se emplea en la reacciones fotoquímicas, puede excitar alguna de las moléculas reaccionantes, de manera que las conversiones consiguientes pueden entonces transcurrir adecuadamente con reactivos suaves y a temperatura ambiente. La activación selectiva tiene lugar también en reacciones electroquímicas, o en otras formas de activación, tales como las microondas o los ultrasonidos (de la Hoz, Diaz-Ortis & Moreno, 2005; Mestres, 2010; Cravotto & Cintas, 2012; Montilla et al., 2012). Las reacciones fotoquímicas y las otras formas de activación selectiva pueden ciertamente evitar el uso de algunos reactivos peligrosos, pero de manera más importante, aportan al arsenal de la síntesis química nuevas conversiones inalcanzables de otro modo (Fagnoni et al., 2007; Mestres, 2010). La aplicación de las formas de activación selectiva o las combinaciones de varias de ellas es un campo que puede dar lugar a nuevos métodos sostenibles, siempre y cuando resulten viables y eficientes en la planta industrial.
Reducción de riesgos por reactivos y condiciones.
| Origen | Estrategias | Áreas de desarrollo |
|---|---|---|
| Reactivos peligrosos | Uso de reactivos suaves | Métodos catalíticos |
| Métodos biocatalíticos | ||
| Activación selectiva | Fotoquímica | |
| Electroquímica | ||
| Microondas | ||
| Ultrasonidos | ||
| Escala reducida | Intensificación de proceso | |
| Condiciones peligrosas | Temperatura ambiente | Métodos catalíticos |
| Métodos biocatalíticos | ||
| Reacciones a presión ordinaria | Métodos catalíticos | |
| Métodos biocatalíticos |
Una estrategia complementaria para la reducción del peligro en el proceso químico consiste en la reducción de las cantidades de materia en el reactor (v. Principio 12). Éste es en parte el fin de las técnicas de intensificación de proceso (Jachuk, 2002, Mason et al., 2007). Cuando se alcanza muy rápidamente la mezcla íntima y eficiente de los reaccionantes a nivel molecular en pequeños canales u otros tipos de dispositivos, que actúan como un reactor en continuo, las cantidades en contacto son muy pequeñas, puede haber un control excelente de la temperatura, y queda reducida al mínimo la ocasión de descontrol o de explosión. El control cinético de la reacción y la aplicación más fácil de las formas de activación selectiva son otras de las ventajas que se aducen a favor de los microrreactores y de las técnicas de intensificación de proceso (Jachuck, Selvaraj & Varma, 2006).
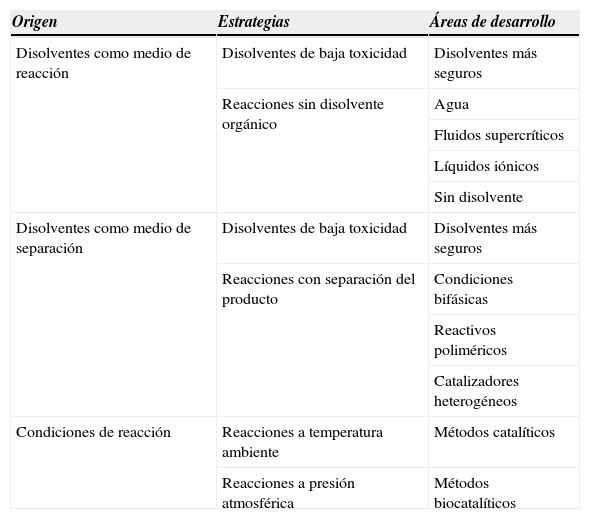
4.4DisolventesFormando parte de los ingredientes y constituyendo un origen sustancial de los residuos, los disolventes merecen un comentario especial (tabla 4). Son necesarios ordinariamente tanto como medio de reacción, como en la separación y purificación del producto. Son empleados en cantidades que están en uno o más órdenes de magnitud respecto a las materias de partida, reactivos y catalizadores. El hecho de ser fluidos los hace propensos a fugas en forma de vertidos y, si son volátiles, de pérdidas por evaporación. Para mayor complicación, la mayoría de disolventes orgánicos son ambientalmente nocivos, o fácilmente inflamables. Por esta razón existe actualmente una actividad muy intensa dirigida a la sustitución de los disolventes orgánicos convencionales como medio de reacción por otros sistemas, tales como agua, fluidos supercríticos, líquidos iónicos o disolventes orgánicos más seguros y de origen renovable (v. Principio 5). La última opción es la ruta más usual para el reverdecimiento inmediato de los procesos actualmente en planta en las industrias de química fina y farmacéutica (Horváth et al., 2008).
Reducción de contaminación y riesgos por los disolventes.
| Origen | Estrategias | Áreas de desarrollo |
|---|---|---|
| Disolventes como medio de reacción | Disolventes de baja toxicidad | Disolventes más seguros |
| Reacciones sin disolvente orgánico | Agua | |
| Fluidos supercríticos | ||
| Líquidos iónicos | ||
| Sin disolvente | ||
| Disolventes como medio de separación | Disolventes de baja toxicidad | Disolventes más seguros |
| Reacciones con separación del producto | Condiciones bifásicas | |
| Reactivos poliméricos | ||
| Catalizadores heterogéneos | ||
| Condiciones de reacción | Reacciones a temperatura ambiente | Métodos catalíticos |
| Reacciones a presión atmosférica | Métodos biocatalíticos |
Se ensayan también estrategias para la reducción de la necesidad de disolventes en las fases de separación y purificación. Por ejemplo, sistemas bifásicos, reactivos poliméri-cos, otras formas de reactivos soportados, catalizadores heterogéneos. Las reacciones “sobre agua”, en la interfase agua-aceite, puede convertirse en una línea significativa para reducir la necesidad de disolventes orgánicos como medio de separación de productos (Jung & Marcus, 2007; Cozzi & Zoli, 2008). Especial interés presentan las técnicas de expansión de líquidos por gases a presión (CO2 o dimetil éter), que permiten modificar la solubilidad de los productos o los catalizadores, y facilitar así la separación de los componentes de la mezcla de reacción (Akien & Poliakoff, 2009; Eckert et al., 2004).
5Diseño de productos químicos funcionales e inocuos para la salud y el medio ambienteEl resultado final de la cadena sintética es el producto químico que la industria química proporciona a otros sectores y en último término de forma indirecta, al ciudadano. El motivo de la demanda del producto o material es la función concreta que debe cumplir como adhesivo, fibra textil, plaguicida, antibiótico, etc. Para un número importante de sustancias sintéticas, los efectos nocivos no resultan patentes inmediatamente. Para algunas, una escasa toxicidad aguda, y la experiencia del manejo habitual sin incidentes en el laboratorio, puede ocultar una toxicidad crónica, o sus efectos letales en organismos del medio ambiente, tal como ocurrió con los disolventes clorados. El conocimiento de la toxicidad y de la ecotoxicidad de los productos químicos ha progresado, pero aun así no hay actualmente un nivel de conocimiento global satisfactorio de todos los efectos dañinos que pueden ocasionar. Es más, la falta de reactividad, originariamente una propiedad altamente valorada en los compuestos halocarbonados, los PCB, o los materiales plásticos, se reveló posteriormente como un grave inconveniente. Nada puede asegurar que no vayan a darse situaciones similares en el futuro.
Resulta evidente que algunos de los productos químicos comerciales actuales deben ser reemplazados por otros. El enfoque de la química sostenible ante esta cuestión es que las nuevas sustancias deben ser diseñadas para presentar las propiedades químicas y físicas idóneas para cubrir perfectamente la función para la que van a ser comercializadas, y presentar al mismo tiempo toxicidad e impacto ambiental bajos o nulos (v. Principio 4). Estas propiedades deberían ser conocidas, al menos con una buena aproximación, de manera previa a su primera síntesis en el laboratorio. Un mejor conocimiento de la bioquímica, fisiología, microbiología y toxicología facilita ciertamente este proceso de diseño, por lo que el diseño de sustancias intrínsecamente inocuas debe ser llevado a cabo de la mano de científicos pertenecientes al área toxicológica de la medicina y la farmacia. Existen ya métodos predictivos que establecen relaciones entre la estructura de la sustancia y sus efectos de tipo biológico (Quantitative Structure-Activity Relationship, QSAR) o basados en la topología molecular, pero queda todavía un gran camino por recorrer (García-Doménech et al., 2008; Voutchkova, Osimitz & Anastas, 2010; Verma & Hansch, 2011; Pla-Franco et al., 2011).
A fín de evitar efectos imprevistos por las nuevas sustancias, se hace preciso comprender mejor la química del medio ambiente, los equilibrios y las cinéticas de la difusión de las sustancias, así como los procesos químicos y biológicos de su degradación ambiental. Los efectos de un producto químico en el ambiente están estrechamente relacionados con sus propiedades físico-químicas (Schwarzenbach, Gschwend & Imboden, 1993; Doménech; 1999; Figueruelo & Marino-Dávila, 2004;Mestres, 2010). Así, la movilidad ambiental y la bioacumulabilidad de una sustancia química es fácilmente predecible a partir del conocimiento de algunos parámetros, a saber, la presión de vapor, la constante de Henry y el coeficiente de reparto octanol/agua. También es predecible la inercia de las sustancias a los agentes químicos ambientales oxidantes, reductores e hidrolíticos. Sin embargo, la predicción de la toxicidad resulta mucho más difícil. Esto es cierto incluso cuando se ha establecido la modalidad (aguda o crónica), y la vía (ingestión, pulmonar, cutánea) de la exposición. Con todo, son innegables los avances logrados en el diseño para evitar efectos tóxicos específicos (Roncaglioni & Benfenati, 2008).
En el diseño de nuevos productos debe ser fuertemente subrayada la conveniencia de la inspiración en la naturaleza. Como ejemplo, el control eficiente y específico de las plagas de insectos en los cultivos mediante el uso adecuado de las mismas moléculas que controlan el comportamiento natural de las especies causantes de la plaga. Las feromonas y otros semioquímicos naturales son aplicadas con indudable éxito desde hace ya muchos años en la agricultura (Cuñat, 1984; Bellés, 1988). Los métodos naturales o inspirados por la naturaleza son sin duda menos agresivos, más específicos y más respetuosos con el ambiente que los basados en productos sintéticos, pero su uso no siempre resulta tan simple.
Los nuevos productos han de ser además fácilmente reutilizados, reciclados o degradados tras su utilización (v. Principio 10). Así, el diseño de los plásticos debe tener en cuenta no sólo su función, sino también su reciclado o degradación final. Una dificultad muy usual en el reciclado de los plásticos consiste en la presencia de aditivos incorporados en el material con el objeto de proporcionarle algunas de las propiedades requeridas para su función: plastificantes, colorantes, rellenos, antioxidantes, ignífugos, que convierten los plásticos en mezclas complejas. Como consecuencia su reciclado resulta ineficiente y económicamente insostenible (Aguado & Serrano, 1999). El diseño de nuevos plásticos debe ir dirigido a sus monómeros de partida y procedimientos de polimerización de tal modo que las macromoléculas presenten directamente las propiedades funcionales requeridas, sin necesidad de aditivos. La biodegradación de los plásticos puede ser diseñada, por ejemplo, mediante la inclusión en la macromolécula de sitios susceptibles de hidrólisis o de oxidación. Por supuesto, una opción muy importante para los plásticos degrada-bles se encuentra en los recursos renovables, en los materiales de origen vegetal (Krochta & De Mulder-Johnson, 1996; Meyer, Metzger & Schubert, 2007).
La exigencia de diseño para el reciclado o degradación tras uso es aplicable no sólo a los plásticos, sino también a los productos constituidos por moléculas pequeñas (Boehtling, Sommer & Di Fiore, 2007). En este contexto, una preocupación fundamental se centra en los productos farmacéuticos y otras sustancias relacionadas con la salud humana o animal. Existen fármacos en el mercado (protectores estomacales, anticolesterolémicos, anticonceptivos) que son empleados por muchos miles de personas, y son excretados inalterados o en forma de sus metabolitos, para terminar en el medio ambiente. Se realizan estudios predictivos y ensayos exhaustivos para prevenir efectos tóxicos posibles, pero no siempre alcanzan la ecotoxicidad (Kümmerer, 2007). La enorme variedad de aplicación de productos químicos en la actividad humana ofrece múltiples posibilidades para el diseño de productos sostenibles para la limpieza en seco, detergentes, superabsorbentes o material pirotécnico (Herrmann et al., 2008; Steinhauser & Klapötke, 2008).
Cuando se considera la mejora de la funcionalidad y el ciclo de vida del producto es posible descubrir un amplio conjunto de objetivos que deben añadirse en el diseño. Así, la mejora en la función puede incluir aspectos, tales como la reducción y simplificación de las condiciones de envasado, embalaje y transporte; más fácil aplicación; menores cantidades requeridas para el mismo efecto o evitar la necesidad de aditivos.
6SostenibilidadQueda pendiente una cuestión realmente ardua: el establecimiento de la sostenibilidad en la comparación entre dos o más procesos, o productos. Sin resolver esta cuestión, un supuesto reverdecimiento puede conducir a una situación menos ventajosa que la de partida. Con todas sus dificultades, se han establecido criterios y parámetros cuando sólo se consideran cantidades y el ciclo de vida de ingredientes y emergentes, pero la tarea resulta todavía más difícil cuando la estimación trata de incluir las diversas formas y grados de toxicidad, ecotoxicidad, persistencia y bioacumulabilidad ambiental, inflamabilidad o el riesgo de reacciones violentas. Se trata de un aspecto de la química sostenible que es objeto de amplia y viva discusión por su indudable interés y dificultad (Azapagic, 2002; García, 2009; Mestres, 2010).
7PerspectivaEn conclusión, se ha presentado aquí una visión somera de los objetivos, estrategias, conceptos y cuestiones relacionadas con la química sostenible. Su objetivo último es minimizar el flujo de productos químicos que se vierten en el medio ambiente, incluidos los gases invernadero, en todo tipo de actividad industrial basada en conversiones químicas. El reverdecimiento debe darse primordialmente en la industria química, con el diseño de procesos y de productos bajo la guía de los principios de Anastas y Warner, con el empleo de productos químicos procedentes de las fuentes renovables, sin generación de residuos peligrosos, para producir nuevos materiales eficientes e inocuos. Cabe esperar del ingenio e inventiva de los químicos que, como resultado de modificaciones espectaculares o, más probablemente, de aproximaciones sucesivas, se consigan procesos y productos notoriamente más satisfactorios que los que están actualmente en operación.
Red Española de Química Sostenible, Álvarez de Castro 63, 08100 Mollet, Barcelona, España http://es-es.facebook.com/pages/RED-ESPA%C3%910LA-DEQU%C3%8DMICA-SOSTENIBLE-REDQS/162669047153030