La endometriosis es una patología hormonodependiente causada por la presencia de tejido endometrial fuera de la cavidad uterina, que induce una reacción inflamatoria crónica. Tiene una prevalencia del 10% en mujeres en edad reproductiva, pudiendo alcanzar hasta el 50% entre mujeres con infertilidad. Es una enfermedad de interés creciente debido a su prevalencia y a los avances científicos ocurridos que han permitido conocer sus diferentes fenotipos, derivando en un diagnóstico más preciso y un tratamiento con un enfoque multidisciplinar. En los últimos años han cambiado muchos paradigmas en torno a esta patología, tanto en su etiopatogenia como en su diagnóstico y tratamiento. Además, han tomado interés creciente aspectos olvidados anteriormente, como su relación con las complicaciones obstétricas y sus comorbilidades asociadas. Tratamos su impacto a lo largo de la vida de las pacientes, haciendo énfasis en nuevas perspectivas que están revolucionado la manera de entender la endometriosis.
Endometriosis is a hormone-dependent disease caused by the presence of endometrial tissue outside the uterine cavity, which induces a chronic inflammatory reaction. It has a prevalence of 10% in women of reproductive age and can reach up to 50% among women with infertility. It is a disease of growing interest due to its prevalence and to the scientific advances regarding its different phenotypes, leading to a more precise diagnosis and treatment with a multidisciplinary approach. In recent years, many paradigms around this pathology have changed, both in its aetiopathogenesis and in its diagnosis and treatment. In addition, previously forgotten aspects such as the relationship with obstetric complications and the associated comorbidities have taken on increasing interest. We discuss its impact throughout the patient's life, emphasizing new perspectives that are revolutionizing the way we understand endometriosis.
La endometriosis es una enfermedad crónica, dependiente de la presencia de estrógenos pero no provocada por dichas hormonas, en la que tejido con características histológicas y funcionales muy parecido al endometrial aparece y crece fuera de la cavidad uterina y presenta cambios cíclicos similares a los del endometrio eutópico, produciendo una reacción inflamatoria que es la responsable última de los síntomas que presenta la paciente; tiene tendencia a la recidiva después de su tratamiento médico o quirúrgico1.
Aunque su frecuencia exacta no es conocida, se ha calculado que afecta a aproximadamente el 10% de las mujeres en edad reproductiva, siendo bien conocido que su prevalencia varía en función de la muestra de población estudiada o el método diagnóstico utilizado2. Así, entre mujeres infértiles la prevalencia alcanza el 30-50%, y entre el 5-21% de las mujeres ingresadas por dolor pélvico crónico. Todo ello representa que la enfermedad afecta a más de 175 millones de mujeres en el mundo3, lo que supone unos dos millones en el estado español.
La endometriosis es una enfermedad heterogénea con tres fenotipos bien reconocidos: endometriosis peritoneal superficial (SUP), endometriomas ováricos (OMA) y endometriosis profunda (DIE). En la SUP, la forma menos grave, las lesiones endometriales superficiales aparecen en el peritoneo, mientras que los OMA son masas quísticas que surgen del crecimiento de tejido endometrial ectópico dentro del ovario. En el fenotipo DIE, el más grave, el tejido endometrial infiltra más de 5mm la superficie peritoneal o infiltra la muscularis propia de los órganos pélvicos como vejiga, intestino y uréteres1. Además, la endometriosis puede ocurrir también en localizaciones extragenitales, como pleural, diafragmática o umbilical4. En el 30% de los casos la endometriosis se asocia a adenomiosis, que se define como la infiltración del miometrio por glándulas y estroma endometrial. Por sí misma, la adenomiosis contribuye al dolor y la infertilidad que se observan comúnmente en la endometriosis, y además produce en muchas pacientes sangrado menstrual abundante5.
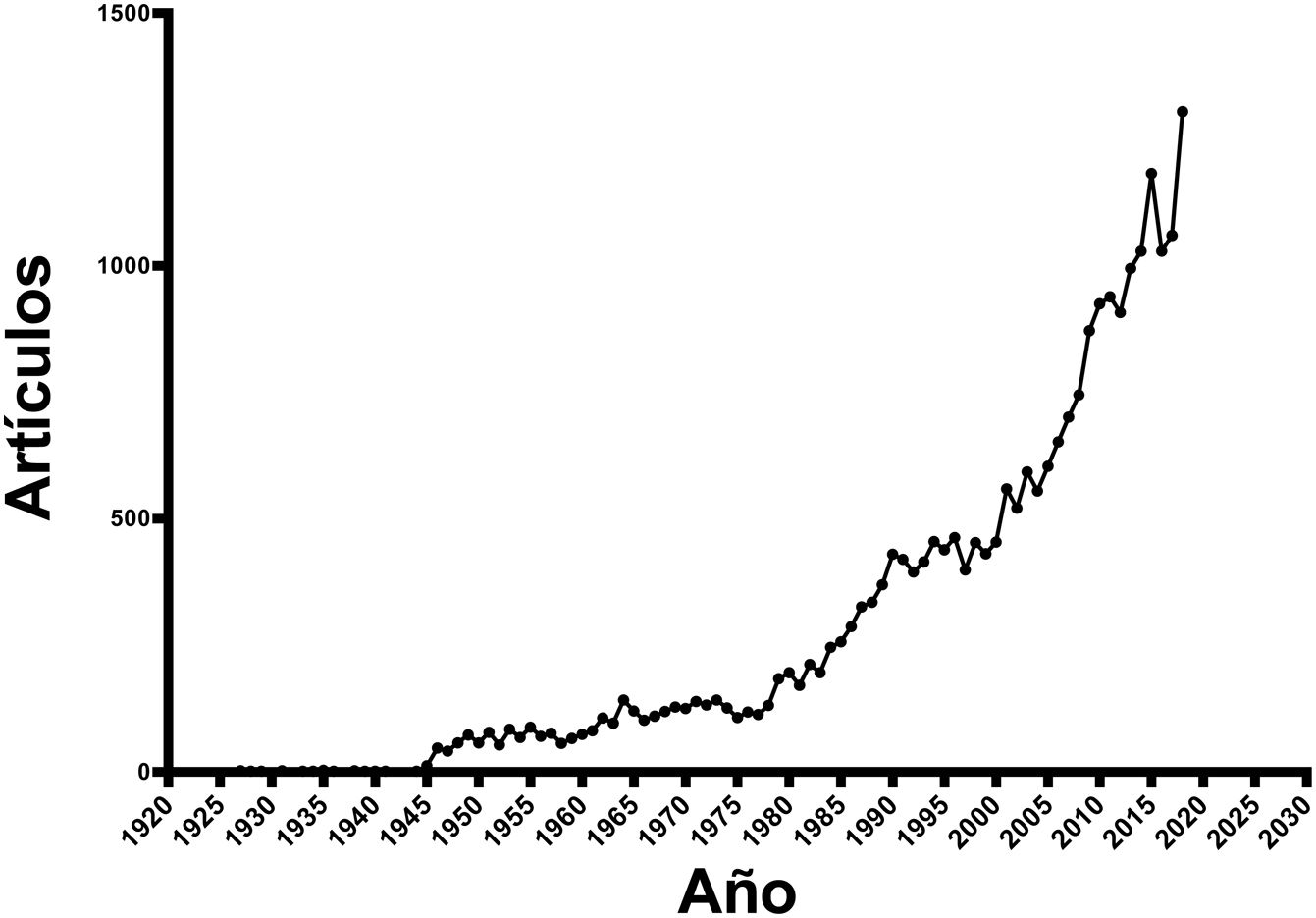
Aunque ya en el Corpus Hipocraticum se hace referencia a síntomas presentados por algunas mujeres y que son totalmente compatibles con el diagnóstico de endometriosis, lo cierto es que la investigación científica sobre la endometriosis ha sido muy escasa hasta épocas muy recientes (fig. 1). De hecho, el cambio de tendencia en el número de artículos publicados anualmente se produjo a finales del siglo pasado, y solo durante los primeros años de este siglo se superó la cifra de 100 artículos anuales publicados. Como consecuencia de este incremento marcado en la investigación y la producción científica relacionada con la endometriosis, durante los últimos años hemos cambiado conceptos que han sido paradigma durante décadas. Así, hemos modificado conceptos bien establecidos hasta ahora en áreas como la definición de la enfermedad6, su epidemiología7 las diferentes clasificaciones de la endometriosis que tenemos hoy en día y la necesidad de desarrollar una nueva que tenga una mejor correlación con la sintomatología y el pronóstico de cada paciente8, la patogénesis9,10, el diagnóstico1 y el tratamiento de la endometriosis1. Sin embargo, probablemente el mayor cambio de paradigma que hemos presenciado en esta enfermedad ha sido el cambio de concepto de que la endometriosis es una enfermedad exclusiva de la vida reproductiva de la mujer para pensar que en realidad se trata de una enfermedad que puede afectar a la mujer a lo largo de toda su vida.
No hay consenso sobre el origen histológico de la endometriosis. Sin embargo, existen diversas teorías (tabla 1) que intentan explicar su origen. Estas pueden dividirse en aquellas que proponen que el origen de los implantes endometriósicos provendría del endometrio uterino, y otras que proponen que los implantes surgirían de tejidos extrauterinos. Las diferentes teorías tienen en común el sostener que debe haber factores inductores y susceptibilidades genéticas que pueden ser diferentes en cada paciente y actuar en diferentes tiempos11.
Etiopatogenia de la endometriosis
| Teorías sobre el origen de la endometriosis | Mecanismos moleculares en la etiopatogenia de la endometriosis |
|---|---|
| • Teoría de la menstruación retrógrada o de la implantación• Teoría de la metaplasia celómica• Teoría de la inducción• Teoría de los restos embriónicos mülerianos o mülerianosis• Teoría de las células progenitoras que se originan en la médula ósea• Teoría de las metástasis benignas | • Supervivencia de las células endometriales• Ambiente hormonal alterado: dependencia estrogénica y resistencia a la progesterona• Escape del sistema de limpieza celular• Adhesión e invasión de las células endometriales• Neuroangiogénesis, vasculogénesis y crecimiento• Inflamación• Progresión lesional |
Así, se puede decir que existe una predisposición genética a padecer la enfermedad al existir gran número de polimorfismos genéticos que se han asociado a un mayor riesgo de desarrollar la enfermedad12. Es también bien sabido que existe un riesgo aumentado de presentar endometriosis en las mujeres que presentan una historia familiar de endometriosis, y que este riesgo es mayor cuanto más cercano sea el parentesco con el familiar afecto13.
El concepto de los llamados 1.000 primeros días de vida (que incluyen la etapa fetal y los primeros dos años de vida neonatal) nace a partir de un artículo en Lancet de 200814 sobre desnutrición materno-infantil. Desde entonces se ha evidenciado la importancia de este periodo en el crecimiento y el desarrollo humano y se le ve como una ventana de oportunidad para realizar intervenciones que pueden modificar el resultado en la vida adulta15. En relación con la endometriosis, diferentes evidencias apoyan también la importancia de estos primeros 1.000 días de vida. Así, un estudio caso-control publicado en 201616 demostró que las madres de mujeres con endometriosis habían fumado más durante el embarazo de la paciente que las madres de mujeres control sin endometriosis, probablemente a través de un mecanismo relacionado con la hipoxemia antenatal. Por otra parte, las mujeres con endometriosis reportan con más frecuencia ser producto de gestaciones que han presentado complicaciones perinatales como prematuridad, bajo peso al nacer o preeclampsia16,17. Recientemente también, se ha demostrado que una mayor exposición a los andrógenos durante la vida fetal (evaluado de manera indirecta mediante la medición de la distancia ano-genital en la edad adulta) se relaciona con una menor probabilidad de desarrollar endometriosis durante la edad reproductiva18.
Los acontecimientos neonatales de esos primeros 1.000 días también parecen estar relacionados con la probabilidad de desarrollar endometriosis durante la vida adulta. Así, se sabe que las niñas que presentan sangrado uterino por deprivación al nacer tienen más posibilidades de presentar endometriosis tras la menarquia y durante la adolescencia19. De manera parecida, se ha demostrado que las pacientes con endometriosis tienen más probabilidades de haber sido alimentadas con biberón que las mujeres de un grupo control sin la enfermedad que con más frecuencia recibieron lactancia materna durante sus primeros días de vida20.
Pero no solo los acontecimientos perinatales tienen relación con el desarrollo ulterior de endometriosis, ya que también ciertas características y eventos de la infancia y la adolescencia están relacionados con un mayor riesgo de presentar endometriosis en la vida adulta. Se sabe que un menor índice de masa corporal durante la infancia y la adolescencia se asocia con mayor riesgo de endometriosis en la vida adulta21, sugiriendo de nuevo que los indicadores de la presencia de endometriosis están presentes en etapas más tempranas de la vida. Pero también factores exógenos acontecidos en estas etapas tienen relación con el desarrollo de endometriosis. Hace poco se ha publicado que existe una relación entre los abusos sexuales y el maltrato físico en la infancia y la adolescencia y el desarrollo de endometriosis en la vida adulta22,23. Por todo ello, es fácil comprender que la antigua aseveración de que la endometriosis es rara en adolescentes es rotundamente falsa. En algunas series de pacientes con endometriosis las adolescentes representan hasta el 20% de las afectadas24, y que algunos síntomas en adolescentes como la dismenorrea severa, sobre todo si esta es resistente a los antiinflamatorios no esteroides o si causa absentismo escolar durante la regla o se acompaña de síntomas gastrointestinales, hacen muy probable el diagnóstico de endometriosis25.
La edad reproductiva es la etapa en que la endometriosis produce más síntomas, y es también en la que hemos asistido a más cambios de paradigmas. Estos cambios se han producido en todos los aspectos de la enfermedad: diagnóstico, tratamiento del dolor y la fertilidad y aparición de comorbilidades y tratamiento de estas.
El síntoma cardinal de la endometriosis es el dolor pélvico, predominantemente premenstrual o perimenstrual (dismenorrea), es decir, que se inicia al comienzo de la menstruación o unos 2días antes, y persiste o incluso se intensifica durante y después de la menstruación. Pueden existir otros síntomas asociados, a menudo condicionados por la localización de los focos de endometriosis, como dispareunia, disuria, tenesmo vesical, tenesmo rectal, colon irritable, cistitis intersticial, seudoobstrucción intestinal y crisis renoureterales y asociarse o no a esterilidad26. Diagnosticar la endometriosis en base solo a los síntomas y a la exploración física es difícil, porque la presentación es muy variable y existe un solapamiento con otras condiciones como el síndrome del intestino irritable o la enfermedad pélvica inflamatoria, u otras enfermedades digestivas o ginecológicas, lo que puede conllevar a un retraso de varios años en el diagnóstico definitivo.
La evolución extraordinaria en las técnicas de imagen ha permitido que hoy en día sea la ecografía transvaginal la herramienta diagnóstica de primera elección cuando hay sospecha de endometriosis27, habiéndose descrito con precisión los signos ecográficos de existencia de endometriomas, endometriosis profunda y adenomiosis28,29. En las pacientes que se sospeche endometriosis profunda por la severidad de los síntomas o por la presencia de síntomas guía de afectación de otros órganos pélvicos, o por la presencia de endometriomas ováricos bilaterales adheridos entre sí y a la cara posterior uterina («kissing ovaries»), debe valorarse la realización de esta ecografía transvaginal con preparación intestinal para aumentar la detección de nódulos de endometriosis y mejorar la valoración de infiltración intestinal30.
De tal manera, hoy en día se considera que la laparoscopia exploradora, que había sido el gold standard, ya no ha de jugar ningún papel en el diagnóstico de la endometriosis1.
En cuanto al tratamiento, también se han producido importantes cambios de paradigma, siendo el más importante de ellos el considerar que la endometriosis no es una enfermedad quirúrgica «por definición»31, remarcándose la necesidad de tratamiento médico universal en todas las pacientes con endometriosis, con la única excepción de las mujeres que están buscando un embarazo. El tratamiento médico se basa en el uso de diferentes pautas terapéuticas que incluyen antiinflamatorios no esteroideos (AINE), analgésicos y terapias hormonales. El tratamiento médico más eficaz es el hormonal (contraceptivos hormonales combinados [vía oral, transcutánea o vaginal], danazol, gestrinona, desogestrel, acetato de medroxiprogesterona, acetato de noretisterona, dienogest, análogos del GnRH), habiéndose demostrado que la supresión de la función ovárica durante 6meses reduce de manera significativa el dolor asociado a la endometriosis, aunque la recurrencia de los síntomas es habitual después de la suspensión del tratamiento32.
Así pues, el tratamiento médico está indicado siempre, antes (para tratar el dolor) y después de la cirugía (para reducir la aparición de recidivas), y el tratamiento quirúrgico se reserva para los casos en que no hay respuesta al tratamiento médico, cuando hay afectación severa de órganos como el intestino o el uréter, con riesgo de obstrucción intestinal o de hidronefrosis, o cuando la mujer se está planteando la gestación, para abrir así una ventana de oportunidad que incremente sus posibilidades de quedarse embarazada2.
En el caso de la paciente estéril existe una gran controversia sobre el papel que tiene la cirugía de la endometriosis profunda en incrementar las tasas tanto de gestación espontánea como de gestación por fecundación in vitro (FIV); así, mientras que para algunos autores no existe indicación quirúrgica en este contexto33, otros sugieren que los resultados de la FIV mejoran si este procedimiento se realiza después de la extirpación quirúrgica de los focos de endometriosis. Asimismo, existe consenso general en el efecto deletéreo que la cirugía exerética del endometrioma tiene sobre la reserva ovárica34, por lo que se ha sugerido que este procedimiento debe reservarse para casos muy concretos y bien seleccionados, sobre todo en mujeres afectas de esterilidad35.
Otro cambio muy importante es el referente al paradigma sobre la relación embarazo y endometriosis. Mientras clásicamente se aceptaba que el embarazo ejercía un efecto beneficioso sobre la endometriosis y no se reconocían complicaciones de esta en el transcurso de la gestación, hoy en día se conoce bien que, como se resume en la tabla 2, existen tanto complicaciones de la endometriosis a consecuencia del embarazo como que los embarazos de mujeres con endometriosis profunda pueden presentar más complicaciones que los de mujeres sin la enfermedad36. Por lo tanto, las gestaciones de pacientes con endometriosis deben ser consideradas de alto riesgo y tratadas como tales.
Relaciones entre el embarazo y la endometriosis
| Complicaciones de la endometriosis | Complicaciones obstétricas |
|---|---|
| Hemoperitoneo espontáneoPerforación intestinalRotura uterina | Retraso de crecimiento intrauterinoBajo peso al nacerParto prematuroRotura prematura de membranasAnomalías de la placentaciónTrastornos hipertensivosHemorragia obstétrica |
Asimismo, hoy en día se conoce bien el importante impacto que tiene la endometriosis sobre la calidad de vida de las pacientes no solo por sus consecuencias directas en forma de dolor, esterilidad, cirugías o efectos secundarios del tratamiento médico37, sino por el marcado incremento de comorbilidades (tabla 3) asociadas a la enfermedad que pueden incrementar los riesgos de esta38.
Comorbilidades asociadas a endometriosis
| Fibromialgia |
| Fatiga crónica |
| Síndrome del intestino irritable |
| Migraña |
| Síndrome de las piernas inquietas |
| Síndrome de sensibilidad química múltiple |
| Esclerosis múltiple |
| Enfermedades autoinmunes |
| LES, artritis reumatoide, síndrome de Sjögren |
| Alteraciones tiroideas |
| Riesgo cardiovascular aumentado |
| Síndrome miofascial |
| Sensibilización central y/o periférica |
El último gran paradigma sobre endometriosis que se ha modificado durante los últimos años ha sido el referente a la desaparición de la enfermedad tras la menopausia. Hoy en día se conoce que la enfermedad puede persistir, o incluso debutar, en pacientes posmenopáusicas39, lo que tiene implicaciones no solo en el manejo de la enfermedad sino en el tratamiento de la sintomatología posmenopáusica en pacientes con endometriosis. Asimismo, esta asociación plantea numerosos interrogantes sobre la posibilidad de transformación maligna de la endometriosis40.
Por lo tanto, la endometriosis constituye una entidad con todavía incógnitas que resolver y terreno por explorar. Hoy es una patología de interés creciente a nivel científico y social, lo que contribuirá sin duda al avance del conocimiento en los próximos años.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
FinanciaciónLos autores declaran la ausencia de financiación para la realización de esta revisión.
Conflicto de interesesLos autores declaran la ausencia de conflicto de intereses.