La rehabilitación multimodal precoz (RMP) ha demostrado en la cirugía colorrectal una reducción de la morbilidad y de la hospitalización sin comprometer la seguridad de los pacientes. La experiencia de la RMP en la duodenopancreatectomía cefálica (DPC) es más limitada. Los objetivos de este estudio fueron analizar la aplicabilidad de un programa RMP en los pacientes intervenidos mediante una DPC en nuestro medio y evaluar los resultados postoperatorios.
MétodosEstudio retrospectivo utilizando una base de datos prospectiva de 41 pacientes a los que se realizó DPC y fueron incluidos en un programa de RMP. Se evaluaron 3 elementos clave: retirada precoz de sondas y drenajes, ingesta oral y movilización precoz. Las variables analizadas fueron la mortalidad, morbilidad, datos perioperatorios, estancia hospitalaria, reintervenciones y reingresos. Este grupo de pacientes fue comparado con un grupo control de 44 pacientes consecutivos, en los que se realizó una DPC con manejo postoperatorio estándar.
ResultadosSe estudió a 85 pacientes intervenidos con DPC (41 pacientes en el grupo RMP y 44 pacientes en el grupo control). La mortalidad global fue del 2,4%: 2 pacientes pertenecientes al grupo control. No encontramos diferencias significativas en la mortalidad, ingreso en Reanimación, reintervenciones ni reingresos. El grupo RMP presentó una morbilidad menor que el grupo control (32 vs. 48%; p = 0,072), y una estancia hospitalaria menor (14,2 vs. 18,7 días; p=0,014). Todos los elementos clave propuestos fueron conseguidos.
ConclusionesLa RMP en la DPC puede implantarse con seguridad en nuestro medio. Permite unificar los cuidados perioperatorios, disminuir la variabilidad clínica y la estancia media y como consecuencia, el coste hospitalario.
Enhanced recovery after surgery (ERAS) has demonstrated in colorectal surgery a reduction in morbidity and length of stay without compromising security. Experience with ERAS programs in pancreatoduodenectomy (PD) is still limited. The aims of this study were first to evaluate the applicability of an ERAS program for PD patients in our hospital, and second to analyze the postoperative results.
MethodsA retrospective study using a prospectively maintained database identified 41 consecutive PD included in an ERAS program. Key elements studied were early removal of tubes and drainages, early oral feeding and early mobilization. Variables studied were mortality, morbidity, perioperative data, length of stay, re-interventions and inpatient readmission. This group of patients was compared with an historic control group of 44 PD patients with a standard postoperative management.
ResultsA total of 85 pancreatoduodenectomies were analyzed (41 patients in the ERAS group, and 44 patients in the control group. General mortality was 2.4% (2 patients) belonging to the control group. There were no statistical differences in mortality, length of stay in intensive care, reoperationss, and readmissions. ERAS group had a lower morbidity rate than the control group (32 vs. 48%; P=.072), as well as a lower length of stay (14.2 vs. 18.7 days). All the key ERAS proposed elements were achieved.
ConclusionsERAS programs may be implemented safely in pancreaticoduodenectomy. They may reduce the length of stay, unifying perioperative care and diminishing clinical variability and hospital costs.
La aplicación de protocolos de rehabilitación multimodal en el área de la cirugía colorrectal ha conseguido disminuir la morbilidad, reducir la estancia hospitalaria, mejorar la satisfacción del paciente y reducir los costes hospitalarios1–3. La implantación de estos protocolos en la duodenopancreatectomía (DPC) resulta difícil dada su complejidad y alta morbilidad4. En los últimos años la mortalidad de la DPC ha disminuido a niveles inferiores al 5% gracias a la evolución de la técnica quirúrgica, a la mejora de los cuidados perioperatorios y a la concentración de pacientes en centros de alto volumen3,5,6. Dada la reacción inflamatoria y catabólica que se produce tras la DPC, la aplicación de un protocolo estructurado y multimodal dirigido a reducir el estrés perioperatorio puede ser una herramienta muy útil para lograr objetivos similares a los conseguidos en la cirugía colorrectal. Los objetivos de este estudio fueron: 1) Determinar la aplicabilidad de un programa de rehabilitación multimodal precoz (RMP) para la DPC en nuestro medio. 2) Evaluar la posibilidad de mejorar los resultados en términos de reducción de la morbilidad, mortalidad y estancia hospitalaria.
MétodosEn enero de 2011 elaboramos un protocolo de RMP para la DPC (tabla 1). Entre enero de 2011 y enero de 2014 se realizaron 41 DPC consecutivas que fueron incluidas en el programa de RMP. Se evaluaron los siguientes elementos clave: 1) retirada precoz de sondas y drenajes; 2) ingesta oral precoz y 3) movilización precoz. Los resultados de este grupo de pacientes fueron comparados con un grupo control histórico constituido por 44 pacientes intervenidos de forma consecutiva entre enero de 2005 y diciembre de 2010, en los que se realizó una DPC con manejo postoperatorio estándar. Todos los datos se recogieron a partir de una base de datos prospectiva que incluye las resecciones pancreáticas que se realizan de forma consecutiva en nuestro centro.
Protocolo de rehabilitación multimodal precoz en la DPC
| Día 0 Cirugía |
| • Ingreso el mismo día de la intervención• Ayunas: líquidos 2 h; sólidos: 6 h antes de la IQ• No preparación de colon• Profilaxis antibiótica (amoxicilina-clavulánico)• Medias de compresión intermitente• C. epidural torácico: perfusión de levobupivacaína 0,25% intraoperatoria• Normotermia con manta de convección• Monitorización: PVC; P. arterial invasiva; temperatura esofágica; relajación muscular; profundidad anestésica; SNG• Fluidoterapia iv estándar en función de PVC y diuresis• Criterios de transfusión: Hg 7,5 g/dl, ajustando a morbilidad del paciente• Analgesia preventiva: Paracetamol+dexketoprofeno+tramadol• Profilaxis para naúseas/vómitos: dexametasona+ondansetrón• Drenajes (2)• Extubación en quirófano• Estancia en U. de Reanimación Posquirúrgica: 24 h, salvo complicación |
| Día 1 |
| • Fisioterapia respiratoria; medias de compresión• PCA epidural: levobupivacaín 0,125%+fentanilo (2μg/ml): 5ml/hora• AINE+paracetamol+morfina de rescate• Retirada de SNG (si débito<400ml en 24 h)• Nutrición parenteral total (NPT)• Iniciar sorbos de agua fría |
| Día 2 |
| • Dieta líquida (agua–infusiones)• Sedestación una hora mañana y tarde• Higiene personal en cama |
| Día 3 |
| • Dieta líquida (caldos)• Determinación de amilasa en drenajes• Retirar sonda vesical• PCA epidural: disminución a 3ml/hora• Sedestación 2 h mañana y tarde• Higiene personal en el baño |
| Día 4 |
| • Dieta triturada sin grasas (si tolerancia)• Retirada de catéter epidural• AINE+paracetamol+morfina de rescate• Retirar drenajes (si apropiado)• Iniciar deambulación |
| Días 5-6 |
| • Dieta de fácil masticación sin grasas• Disminuir nutrición parenteral (si buena tolerancia oral)• Retirar drenajes (si apropiado)• Deambulación |
| Día 7 |
| • Retirar vía central y nutrición parenteral (si buena tolerancia oral)• Dieta blanda sin grasas• Valoración de criterios de alta |
Las variables analizadas fueron el American Society of Anesthesiology (ASA), retirada de sondas y drenajes, tránsito intestinal, ingesta oral, sedestación/ambulación, estancia en Reanimación, estancia hospitalaria, porcentaje de reintervenciones y porcentaje de reingresos. La mortalidad y las complicaciones fueron seguidas hasta el alta hospitalaria o fallecimiento del paciente. Los reingresos se registraron hasta los 30 días siguientes al alta. Las complicaciones postoperatorias fueron registradas según la clasificación de Clavien-Dindo7.
Técnica quirúrgicaTodas las intervenciones fueron realizadas por los 2 mismos cirujanos. La resección incluyó una antrectomía, linfadenectomía del ligamento hepatoduodenal, tronco celíaco y cara lateral derecha de la arteria mesentérica superior. La reconstrucción fue en ambos grupos con doble asa en Y de Roux y anastomosis pancreático-yeyunal término-lateral en 2 planos con tutor de silicona y hepático-yeyunostomía término-lateral. La anastomosis gastroyeyunal latero-lateral fue retrocólica en el grupo control y antecólica en el grupo de RMP según la descripción de Hartel8. Todas las resecciones vasculares fueron venosas y se realizaron sobre el eje venoso mesentérico-portal (VMS/P). Se realizaron 3 tipos de reconstrucciones vasculares según el grado de infiltración vascular: 1) sutura lateral de VMS/P en casos de infiltración igual o menor del 25% de la circunferencia de la vena; 2) resección segmentaria con anastomosis término-terminal autóloga en los casos con infiltración superior al 50% de la circunferencia y 3) sustitución con prótesis de politetrafluoroetileno (PTFE) en un caso con infiltración de la vena porta de 3cm de longitud.
Todos los pacientes permanecieron en la Unidad de Reanimación Posquirúrgica al menos 24 h. La administración de octreótido se empleó únicamente en los pacientes con alto riesgo de fístula pancreática (ducto pancreático ≤ 1mm, o páncreas blando). Se dejaron 2 drenajes, uno subhepático y otro próximo a la anastomosis pancreática. Se realizó un doppler portal a las 24 h en todos los pacientes con resección vascular. Los drenajes en el grupo de RMP se retiraron según la determinación de amilasa medida en el líquido de drenaje a partir del tercer día postoperatorio. Solo se administraron fármacos procinéticos en los casos de vaciamiento gástrico lento (VGL) establecido. Se determinó el valor de los niveles de amilasa en los drenajes a partir del tercer día postoperatorio.
DefinicionesFístula pancreática. Persistencia en el drenaje de líquido con amilasa superior a 3 veces su valor mayor en plasma después del tercer día postoperatorio. Se clasificó el tipo de fístula pancreática según el grado A, B o C de acuerdo con los criterios del International Study Group on Pancreatic Surgery (ISGPS)9.
Vaciamiento gástrico lento (VGL). Necesidad de sonda nasogástrica (SNG) durante más de 3 días, o su colocación después del tercer día postoperatorio, así como la ausencia de tolerancia oral después de la primera semana de la intervención10.
Fístula biliar. Persistencia de líquido en el drenaje con bilirrubina superior a 3 veces el valor mayor en plasma después del quinto día postoperatorio5.
Análisis estadísticoLos datos se presentan como la media±SE (IC 95%), o como número (%). Las comparaciones entre grupos se analizaron mediante muestras independientes, como t-test o prueba de Mann Whitney para las variables continuas y chi cuadrado o la prueba exacta de Fisher para las variables categóricas. Un valor de p<0,05 fue considerado estadísticamente significativo. Los análisis estadísticos se realizaron con el paquete informático SPSS® 16.0 (SPSS® Inc., Chicago, IL, EE. UU.).
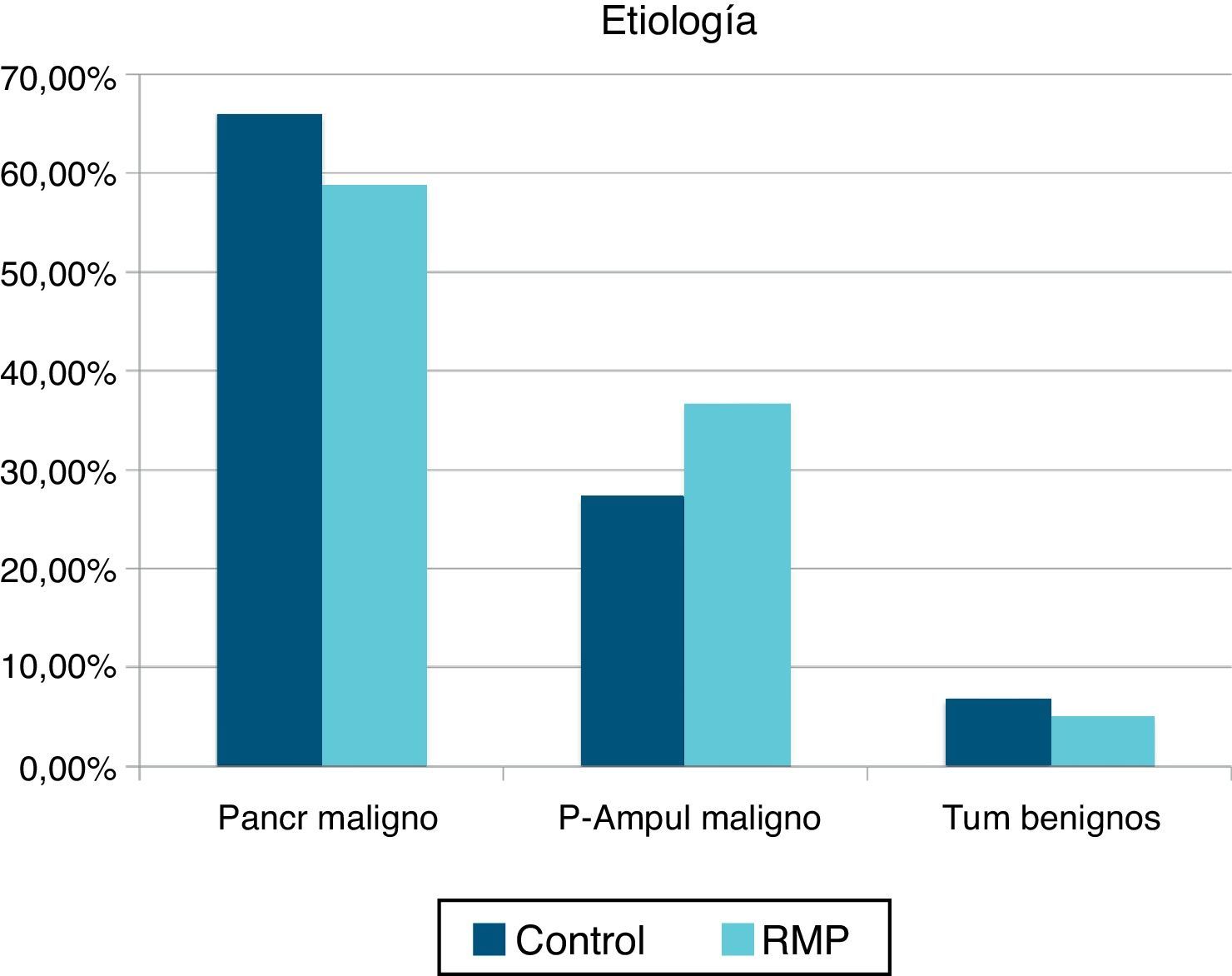
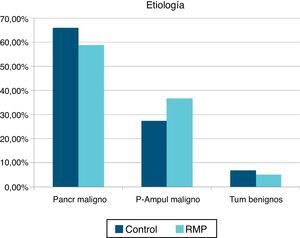
ResultadosSe estudió a un total de 85 pacientes intervenidos con DPC (41 pacientes en el grupo de RMP y 44 pacientes en el grupo control). La edad media fue de 66,7 (41-84) años en el grupo control y 61,3 años (44-80) en el grupo de RMP. La proporción mujer/hombre fue del 39/61% en el grupo control y del 41/59% en el grupo de RMP. No se registraron diferencias estadísticamente significativas en el ASA entre ambos grupos (ASA I: 52,9% en el grupo control y 47,1% en el grupo RMP). Para el ASA II-III la distribución fue de 51,4 y 48,6% respectivamente. Tampoco apreciamos diferencias en la clasificación por histología (fig. 1). En el grupo control se registró una menor incidencia de drenaje biliar preoperatorio (68,2 vs. 73,1%), aunque sin diferencias significativas.
En el 98% de los pacientes se empleó analgesia epidural torácica intra- y postoperatoria. La duración de la intervención fue significativamente menor en el grupo RMP (5,9 h) frente al grupo control (6,4 h) (p = 0,001). No hubo diferencias en la transfusión media intraoperatoria entre ambos grupos. Sin embargo, el grupo control precisó en el postoperatorio un mayor número de concentrados de hematíes que el grupo RMP (1,45 vs. 0,44; p = 0,001). Tampoco se registraron diferencias en cuanto al tipo de resección vascular. En ambos grupos se realizaron 3 resecciones venosas laterales y una resección segmentaria con anastomosis término-terminal. La reconstrucción venosa del grupo control se hizo mediante prótesis de PTFE. La estancia media en reanimación fue de 2,8 días en el grupo control y de 1,8 días en el grupo RMP (p = 0,95).
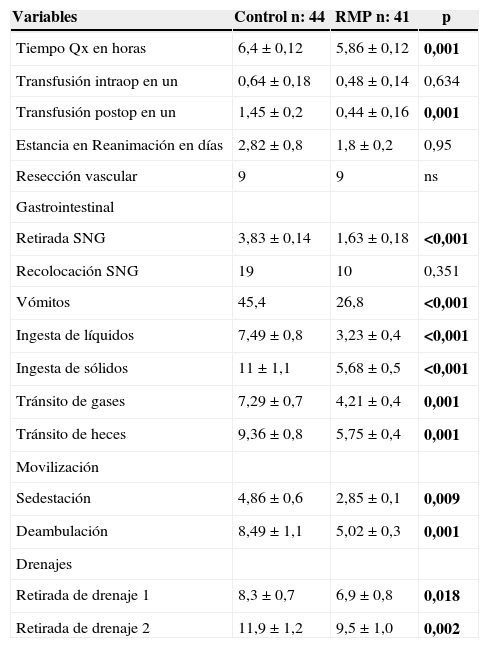
Desde el punto de vista digestivo destaca una permanencia de la SNG menor en el grupo RMP (1,6 vs. 3,8 días; p < 0,001), sin una mayor necesidad de recolocación y con un índice de vómitos tras su retirada menor en el grupo RMP (26,8 vs. 45,4%; p = 0,029). Tanto la ingesta de líquidos y de sólidos como el tránsito intestinal para gases y heces fue significativamente más precoz en el grupo RMP (p<0,001) (tabla 2).
Variables perioperatorias
| Variables | Control n: 44 | RMP n: 41 | p |
|---|---|---|---|
| Tiempo Qx en horas | 6,4±0,12 | 5,86±0,12 | 0,001 |
| Transfusión intraop en un | 0,64±0,18 | 0,48±0,14 | 0,634 |
| Transfusión postop en un | 1,45±0,2 | 0,44±0,16 | 0,001 |
| Estancia en Reanimación en días | 2,82±0,8 | 1,8±0,2 | 0,95 |
| Resección vascular | 9 | 9 | ns |
| Gastrointestinal | |||
| Retirada SNG | 3,83±0,14 | 1,63±0,18 | <0,001 |
| Recolocación SNG | 19 | 10 | 0,351 |
| Vómitos | 45,4 | 26,8 | <0,001 |
| Ingesta de líquidos | 7,49±0,8 | 3,23±0,4 | <0,001 |
| Ingesta de sólidos | 11±1,1 | 5,68±0,5 | <0,001 |
| Tránsito de gases | 7,29±0,7 | 4,21±0,4 | 0,001 |
| Tránsito de heces | 9,36±0,8 | 5,75±0,4 | 0,001 |
| Movilización | |||
| Sedestación | 4,86±0,6 | 2,85±0,1 | 0,009 |
| Deambulación | 8,49±1,1 | 5,02±0,3 | 0,001 |
| Drenajes | |||
| Retirada de drenaje 1 | 8,3±0,7 | 6,9±0,8 | 0,018 |
| Retirada de drenaje 2 | 11,9±1,2 | 9,5±1,0 | 0,002 |
En negrita, las variables intraoperatorias y postoperatorias.
Tras la aplicación del protocolo de RMP se consiguió una movilización postoperatoria más rápida. El inicio de la sedestación pasó de 4,8 días en el grupo control a 2,85 días en el grupo RMP (p = 0,018). Igualmente, la deambulación disminuyó de 8,4 días de media en el grupo control a 5 días en el grupo RMP (p = 0,001). Con relación a la retirada de drenajes las diferencias también fueron significativas. En el grupo control los 2 drenajes permanecieron de media 8,3 y 11,9 días respectivamente, frente a los 6,9 y 9,5 días en el grupo RMP (p = 0,018 y 0,002).
La mortalidad global de la serie fue del 2,4%, que corresponde a 2 pacientes del grupo control. Un caso por trombosis aguda del injerto de PTFE expandido tras una resección de vena porta y un segundo paciente fallecido por neumonía nosocomial. No hubo fallecimientos en el grupo RMP.
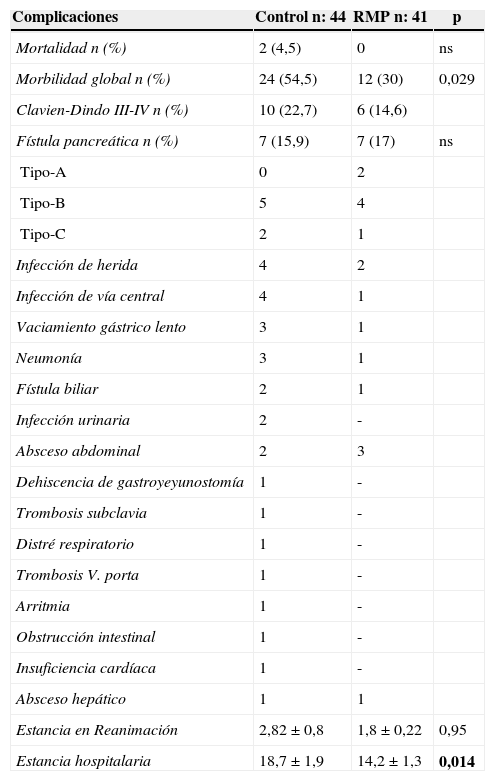
La morbilidad global fue del 42,3% (54,5% en el grupo control y 30% en el grupo RMP) (p = 0,029). Las complicaciones más frecuentes en el grupo control fueron la fístula pancreática (15,9%), el VGL (6,6%) y la infección de herida (8,8%). Las complicaciones más frecuentes del grupo RMP fueron la fístula pancreática (17%), absceso intraabdominal (7,3%) e infección de herida (4,9%). Las complicaciones grado III-IV de la clasificación de Clavien-Dindo fueron un 22,2% en el grupo control y un 14,6% en el grupo RMP (tabla 3). El índice de reintervenciones fue similar en ambos grupos (11,3 vs. 12,1%), al igual que la tasa de reingresos (9 vs. 9,7%). La estancia hospitalaria fue significativamente menor en el grupo de RMP (14,2 días), frente a 18,7 días en el grupo control (p=0,014).
Morbimortalidad
| Complicaciones | Control n: 44 | RMP n: 41 | p |
|---|---|---|---|
| Mortalidad n (%) | 2 (4,5) | 0 | ns |
| Morbilidad global n (%) | 24 (54,5) | 12 (30) | 0,029 |
| Clavien-Dindo III-IV n (%) | 10 (22,7) | 6 (14,6) | |
| Fístula pancreática n (%) | 7 (15,9) | 7 (17) | ns |
| Tipo-A | 0 | 2 | |
| Tipo-B | 5 | 4 | |
| Tipo-C | 2 | 1 | |
| Infección de herida | 4 | 2 | |
| Infección de vía central | 4 | 1 | |
| Vaciamiento gástrico lento | 3 | 1 | |
| Neumonía | 3 | 1 | |
| Fístula biliar | 2 | 1 | |
| Infección urinaria | 2 | - | |
| Absceso abdominal | 2 | 3 | |
| Dehiscencia de gastroyeyunostomía | 1 | - | |
| Trombosis subclavia | 1 | - | |
| Distré respiratorio | 1 | - | |
| Trombosis V. porta | 1 | - | |
| Arritmia | 1 | - | |
| Obstrucción intestinal | 1 | - | |
| Insuficiencia cardíaca | 1 | - | |
| Absceso hepático | 1 | 1 | |
| Estancia en Reanimación | 2,82±0,8 | 1,8±0,22 | 0,95 |
| Estancia hospitalaria | 18,7±1,9 | 14,2±1,3 | 0,014 |
En negrita, la mortalidad intrahospitalaria y las complicaciones postoperatorias.
En los últimos años se ha producido una disminución de la mortalidad en la DPC con cifras por debajo del 5% que se atribuye a la evolución de la técnica quirúrgica, a la mejora de los cuidados perioperatorios y a la concentración de pacientes en centros de alto volumen3,5,11–13. Sin embargo, la morbilidad de este procedimiento es todavía elevada, con tasas de alrededor del 40-50%, y estancia hospitalaria entre 14 y 28 días5,14,15. La aplicación de los programas de RMP en la cirugía colorrectal ha demostrado no solo su seguridad, sino, además, una mejora de los resultados con disminución de la morbilidad y de la estancia hospitalaria, mejora del bienestar de los pacientes y disminución de la variabilidad clínica, sin aumentar la morbilidad ni la mortalidad1,2,16,17. Si bien son numerosas las publicaciones de RMP en cirugía colorrectal, su aplicación en la cirugía pancreática ha sido hasta ahora más limitada, probablemente por su mayor complejidad y morbilidad. Dada la reacción inflamatoria y catabólica que provoca la DPC, la aplicación de un protocolo estructurado dirigido a reducir el estrés perioperatorio resulta especialmente interesante. Por ello, en los últimos años se han publicado varios estudios retrospectivos con resultados prometedores en esta área3,14,15,18. En nuestro país el grupo de Montiel et al.19 publicó un estudio descriptivo de 82 pacientes sin comparar con grupo control.
En 2011 decidimos aplicar un protocolo de RMP en la DPC en el Hospital Son Espases para evaluar su aplicabilidad y la posibilidad de mejorar los resultados. Todos los elementos clave propuestos en el programa de RMP fueron conseguidos. Se observaron diferencias significativas en la retirada de sondas y drenajes, la ingesta de líquidos y sólidos, así como en la movilización de los pacientes. La retirada precoz de la SNG en el grupo de RMP se acompañó de una disminución significativa de los vómitos postoperatorios (45,4 vs. 26,8%) y de una menor necesidad de recolocación de la sonda (19 vs. 10%), si bien no alcanzó diferencias significativas. La ingesta precoz de líquidos no aumentó la incidencia de náuseas/vómitos. Gracias a la retirada precoz de las sondas y drenajes, y al protocolo de analgesia epidural, se consiguió una movilización precoz con sedestación al segundo día y deambulación completa a los 5 días.
El abordaje multimodal del dolor agudo postoperatorio es uno de los factores clave en los programas de RMP20, ya que permite disminuir la dosis de opioides y sus efectos secundarios. Un reciente metaanálisis21 demuestra que el uso de la epidural junto a la anestesia general en la cirugía abdominal mayor disminuye la mortalidad, las complicaciones cardiovasculares y las respiratorias. Además, acelera el tránsito intestinal, disminuye el íleo postoperatorio y la incidencia de náuseas/vómitos. Los estudios en DPC han demostrado un mejor control del dolor agudo postoperatorio y menos complicaciones con el uso de la analgesia epidural22. Por otra parte, el uso de la epidural se asocia a una menor estancia media23.
El uso de drenajes en la cirugía pancreática es una práctica rutinaria. La incidencia de fístulas es mayor que en la cirugía de colon, por lo que su trascendencia es distinta. A pesar de que algunos autores se plantean no usarlos en los casos de bajo riesgo de fístula24, la mayoría de los grupos los utilizan, recomendando su retirada de forma precoz, para lo que es útil realizar determinaciones de amilasa en el líquido de drenaje25–27.
Se registró un menor índice de transfusión y duración de la intervención en el grupo RMP, que podría ser atribuido a una mayor experiencia del equipo quirúrgico. La mayoría de los estudios describen una menor tasa de complicaciones en el grupo de RMP6,28. En nuestra serie, la morbilidad global fue significativamente menor en el grupo RMP, aunque es preciso analizar este dato con prudencia ya que puede verse influido por el tamaño muestral. La incidencia de fístula pancreática, al igual que en otras series15, se mantuvo en cifras similares en el grupo de RMP a pesar de la ingesta oral precoz. El VGL se presenta tras la DPC en el 15-35% de los casos10,29–31. La causa más frecuente es la presencia de una fístula pancreática, aunque también se han propuesto otras causas como la disminución de la motilina plasmática tras la resección duodenal y una posible denervación vagal por la disección y la linfadenectomías del ligamento hepatoduodenal y tronco celíaco5. La incidencia de VGL en nuestro estudio fue menor en el grupo de RMP (6,6 vs. 2,4%), en consonancia con los trabajos en los que se aplica este protocolo5,15,32. Las únicas medidas específicas que asociamos para disminuir la incidencia de VGL fueron la ingesta oral precoz y la realización de la gastroyeyunostomía de forma antecólica, descrita previamente por el grupo de Heidelberg5. La eficacia de los fármacos procinéticos en la cirugía pancreática es discutida, y en nuestro centro solo los empleamos en caso de VGL establecido.
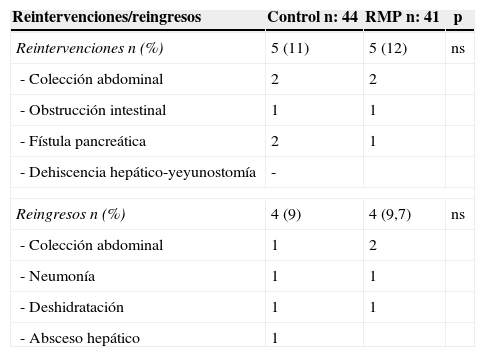
La disminución de la estancia hospitalaria es uno de los indicadores más importantes de los programas de RMP14,15,19,32. En el presente estudio, la aplicación de este programa permitió disminuir la estancia hospitalaria de manera significativa (18,7 vs. 14 días). Los índices de reintervenciones y de reingresos fueron similares en ambos grupos (tabla 4).
Reintervenciones y reingresos
| Reintervenciones/reingresos | Control n: 44 | RMP n: 41 | p |
|---|---|---|---|
| Reintervenciones n (%) | 5 (11) | 5 (12) | ns |
| - Colección abdominal | 2 | 2 | |
| - Obstrucción intestinal | 1 | 1 | |
| - Fístula pancreática | 2 | 1 | |
| - Dehiscencia hepático-yeyunostomía | - | ||
| Reingresos n (%) | 4 (9) | 4 (9,7) | ns |
| - Colección abdominal | 1 | 2 | |
| - Neumonía | 1 | 1 | |
| - Deshidratación | 1 | 1 | |
| - Absceso hepático | 1 | ||
Como limitaciones del presente estudio planteamos su carácter retrospectivo, la ausencia de aleatoriedad y la comparación con un grupo histórico, lo que podría suponer una mayor experiencia y mejora de la práctica clínica en el segundo período. Otro factor a tener en cuenta es que la implantación progresiva de los programas de RMP en la DPC con buenos resultados va a dificultar la realización de estudios aleatorizados con un grupo control por razones éticas.
Se ha producido una evolución de los programas de RMP desde los años 90 hasta ahora. De los 20 elementos planteados inicialmente por Kehlet, las estrategias actuales se dirigen a definir los factores clave para lograr los objetivos. El estudio de Feroci señala en un análisis multivariante 5 factores relevantes para lograr buenos resultados: laparoscopia, retirada precoz de sondas, retirada precoz de drenajes, movilidad precoz y nutrición oral33. Una de las dificultades en la interpretación de los resultados de la RMP es la heterogeneidad de los estudios. Una revisión de 5.747 pacientes con cáncer colorrectal muestra una gran variabilidad en la adherencia a los programas de RMP. La estancia media y los reingresos son 2 de los elementos con mayor variabilidad34.
El futuro de los programas de RMP plantea diversos retos35,36: diferenciar el alta clínica del tiempo de alta real, influida por factores organizativos y sociosanitarios; separar las complicaciones médicas de las quirúrgicas; homogenizar las definiciones para poder definir y comparar mejor los resultados; y señalar los factores clave que se deben incluir en los programas para garantizar los objetivos. Finalmente, si bien los resultados de estos programas son más evidentes en los pacientes sin complicaciones, algunos autores plantean aplicar también la RMP en los pacientes que desarrollan complicaciones postoperatorias y que probablemente también podrían beneficiarse de los principios de la rehabilitación precoz31,37.
En conclusión, los programas de RMP en la DPC pueden ser implantados con seguridad en nuestro medio. Permiten disminuir la estancia hospitalaria y, como consecuencia, el coste hospitalario, contribuyendo a unificar los cuidados perioperatorios y disminuir la variabilidad clínica. A pesar de la heterogeneidad de los estudios, los resultados son prometedores. La implantación progresiva de estos programas va a dificultar la realización de estudios aleatorizados con un grupo control por razones éticas.
Conflicto de interesesTodos los autores declaran haber leído el artículo, estar de acuerdo con sus conclusiones y no tener ningún conflicto de intereses.
Queremos mostrar nuestro agradecimiento al Dr. José Manuel Ramírez por su trabajo incansable en la difusión e implantación de los conceptos de la rehabilitación multimodal precoz en nuestro país.