El trasplante cardiopulmonar (TCP) ha presentado una disminución progresiva en el número de procedimientos. En nuestro país existe poca información al respecto, siendo el objetivo de este estudio analizar la experiencia de un hospital de referencia.
MétodosEstudio observacional unicéntrico de una cohorte histórica en el periodo entre 1990 y 2021. Las asociaciones entre categorías se evaluaron mediante la prueba de X2 o la f de Fisher. La supervivencia se analizó a través del método de Kaplan-Meier. Las diferencias se evaluaron con el estudio de log-rank y el análisis multivariante con el método de Cox.
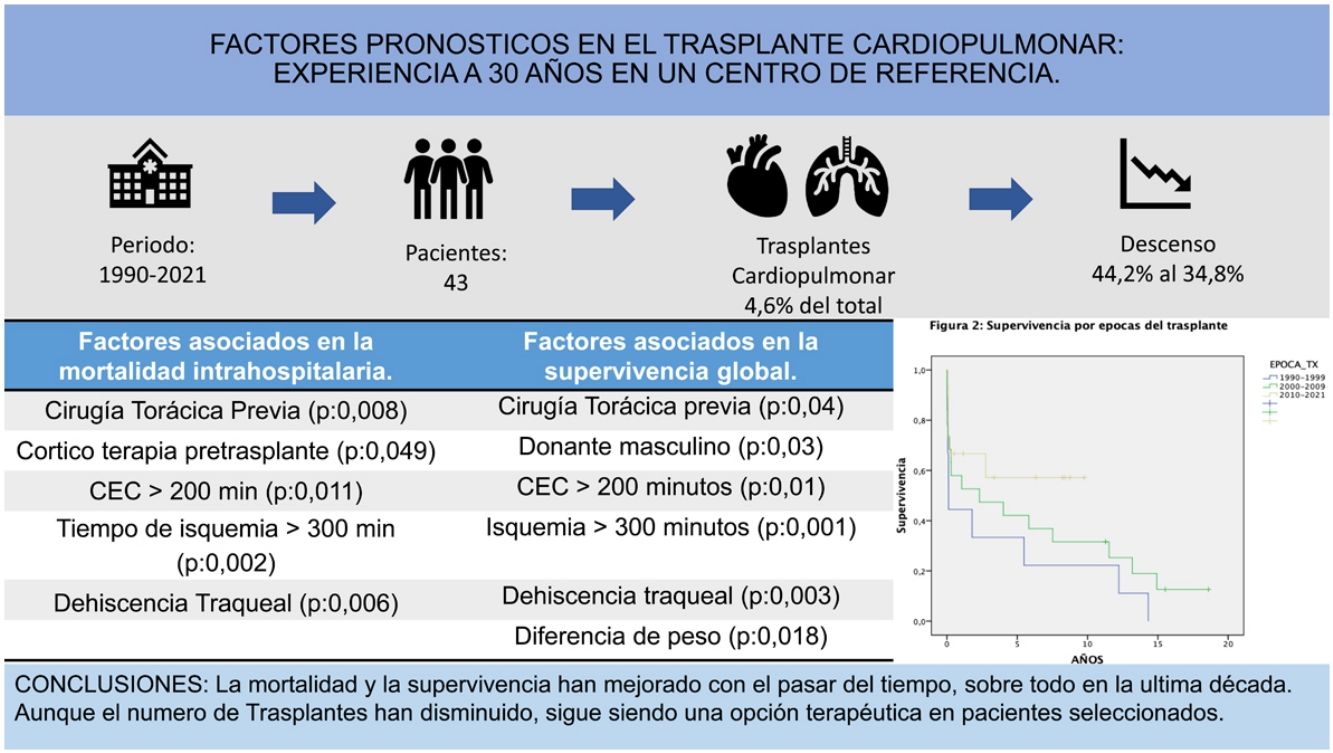
ResultadosSe observó una reducción del número de procedimientos realizados en el último decenio (2000-2009: 19 [44,2%]; 2010-2021: 15 [34,8%]). La mortalidad posoperatoria precoz fue de 23,3%, reduciéndose a 13,3% a partir del 2010. La intrahospitalaria fue de 41%, disminuyendo a 33% en 2010. Los factores asociados a la mortalidad fueron cirugía torácica previa, corticoterapia, circulación extracorpórea (CEC) mayor a 200 min, tiempo de isquemia mayor a 300 min y dehiscencia traqueal (p < 0,005). La supervivencia global a uno, cinco y 10 años fue de 58, 44,7 y 36,1%, respectivamente. Los factores asociados a menores tasas de supervivencia fueron cirugía torácica previa, donante masculino, CEC mayor 200 min, tiempo de isquemia mayor a 300 min, dehiscencia traqueal y diferencia de pesos (p < 0,005).
ConclusionesExiste una disminución en el número de procedimientos, siendo más evidente en la última década, pero evidenciando una mejora tanto de la mortalidad posoperatoria y supervivencia.
Heart–lung transplantation has shown a progressive decrease in the number of procedures. There is a lack of information about this field in Spain. The main goal of this study is to analyze the experience of a national reference hospital.
MethodsWe performed a retrospective study of a historical cohort of heart–lung transplanted patients in a single center, during a 30 years period (from 1990 to 2021). The associations between variables were evaluated using the χ2 test or Fisher's exact test. Survival was analyzed using the Kaplan–Meier method. Differences were evaluated using the log-rank test and multivariate analysis with the Cox method.
ResultsA decrease in the number of procedures performed in the last decade was observed [2000–2009: 19 procedures (44.2%); 2010–2021: 15 procedures (34.8%)]. Early postoperative mortality was 23.3%, falling to 13.3% from 2010. In-hospital mortality was 41%, falling to 33% from 2010.
Main factors related to higher mortality: previous thoracic surgery, corticosteroid therapy, extracorporeal circulation (ECLS) greater than 200 min, ischemia time greater than 300 min, and tracheal dehiscence (p < 0.005).
Overall survival at one, five, and ten years was 58%, 44.7%, and 36.1%, respectively. Factors associated with lower survival rates: previous thoracic surgery, male donor, extracorporeal circulation greater than 200 min, ischemia time greater than 300 min, tracheal dehiscence and weight difference (p < 0.005).
ConclusionsThere has been a progressive decrease in the number of heart–lung transplantations, being more evident in the last decade, but showing an improvement in both mortality and survival.
El trasplante cardiopulmonar (TCP) es una opción terapéutica en pacientes con enfermedad cardiaca y pulmonar en etapa terminal, desde su inicio en Stanford en 1982, demostrando buenas supervivencias a largo plazo1.
El informe de la International Society for Heart and Lung Transplantation (ISHLT) de 2019, recoge un total de 4.884 TCP desde 1988 hasta el 30 de junio de 2018, de los cuales 4.128 fueron en adultos y 733 en edad pediátrica2,3.
El número de TCP alcanzó su punto máximo en 1989 con un promedio de 200 trasplantes al año, habiendo disminuido progresivamente a un promedio de 50 anuales en la última década3.
La principal razón para esta disminución progresiva ha sido la demostración de similares supervivencias tras realizar trasplante bipulmonar (TBP)4–8 en pacientes con hipertensión pulmonar (HP), dada la mejoría de la función del ventrículo derecho después de disminuir las presiones pulmonares4,6,9.
De igual manera, en pacientes con cardiopatía y síndrome de Eisenmenger (EE), las nuevas terapias para la HP y la insuficiencia cardiaca pueden prolongar la supervivencia sin necesidad de TCP10–12. Esta reducción de las indicaciones del TCP también se evidencia en España según datos de la Organización Nacional de Trasplantes de 2021, siendo nuestro hospital el que más volumen presenta en nuestro país13.
A lo largo de los años, las indicaciones para el TCP se han modificado. La hipertensión pulmonar idiopática (HPI) fue la indicación más común en los primeros años del trasplante, seguida de la cardiopatía congénita (CC) y la fibrosis quística (FQ). Actualmente, la CC complicada por EE se ha convertido en la indicación más común seguida de la HPI3,14. También está indicado en pacientes que tienen enfermedad pulmonar en etapa terminal e insuficiencia ventricular izquierda refractaria a tratamiento, fibrosis o infarto del ventrículo derecho con insuficiencia ventricular11,15–18, así como en aquellos con EE con cardiopatía coronaria severa, reparación fallida o incorregible de cardiopatía coronaria e insuficiencia ventricular izquierda grave10,14. Finalmente, se debe considerar en los que cuentan con HP grave refractaria al tratamiento clínico17–19. El último documento de consenso para la selección de candidatos a trasplante pulmonar de la ISHLT describe las indicaciones en aquellos con enfermedades cardiacas y pulmonares avanzadas que no sean susceptibles de trasplantes aislados de corazón o pulmón15.
Los resultados del TCP han mejorado progresivamente, con una mediana de supervivencia de 3,7 años en la década de los 90 y de 6,5 en la última época (p = 0,025)3.
El objetivo de este estudio es analizar la experiencia del TCP en un centro de tercer nivel desde sus inicios hasta la actualidad, así como identificar aquellas variables pronosticas que condicionan la morbimortalidad posoperatoria y la supervivencia.
MétodosDiseñoEstudio observacional unicéntrico de una cohorte histórica de los pacientes sometidos a TCP en un hospital de referencia nacional en trasplante pulmonar y cardiopulmonar.
PacientesSe incluyeron en el estudio a 43 pacientes a los que se realizó un TCP en el periodo comprendido entre 1990 y 2021. Se incluyeron tanto adultos como pediátricos. Todas las indicaciones se decidieron en un comité multidisciplinar. Este estudio fue aprobado por el comité de ética del Hospital.
VariablesLas variables a estudio incluyeron datos demográficos como edad (media y rango), sexo, peso, talla, índice de masa corporal (IMC kg/m2), grupo sanguíneo, antecedente de cirugía torácica previa, tratamiento con corticoides, diagnóstico primario e indicación para TCP clasificado según el último consenso sobre HP20, estado basal del paciente pretrasplante (escala New York Heart Association [NYHA]), pruebas de función respiratoria (capacidad vital forzada [CVF] y volumen espiratorio forzado en el primer segundo [FEV1]), capacidad de transferencia de monóxido de carbono [DLCO)], pruebas de función cardiaca medidas mediante ecocardiograma y cateterismo cardiaco, y variables del donante (edad, sexo, talla, peso y presión arterial de oxígeno).
Las variables del procedimiento quirúrgico incluyeron tiempo de isquemia y de circulación extracorpórea (CEC).
Los resultados posoperatorios analizados fueron complicaciones posoperatorias quirúrgicas y clínicas: disfunción primaria del injerto pulmonar (DPIP)21, duración de estancia en reanimación y estancia hospitalaria (días), mortalidad perioperatoria a los 30 días, mortalidad intrahospitalaria y supervivencia.
Análisis estadísticoPara la recogida de datos se utilizó el programa de Filemaker® (Filemaker pro v.18, Claris International Inc. CA, USA) y SPSS® (SPSS v.20, IBM) para el análisis estadístico.
Las variables continuas se presentan como media ± desviación estándar (DE) si se distribuyen normalmente o como mediana en caso contrario. Las categóricas como frecuencias y porcentajes. Las asociaciones entre categorías se evaluaron mediante la prueba de X2 o la f de Fisher, cuando fue necesario. Se utilizó la t de Student o la U de Mann-Whitney para las variables continuas. La supervivencia se analizó a través el método de Kaplan-Meier y sus diferencias se evaluaron mediante el estudio de log-rank, realizándose un estudio multivariante con el método de Cox. Se consideró significativa una p < 0,05.
ResultadosCaracterísticas de los receptores y donantesSe realizaron un total de 43 TCP que representan 4,6% del total de trasplantes pulmonares y TCP realizados en el periodo de 1990 a 2021 (n = 917).
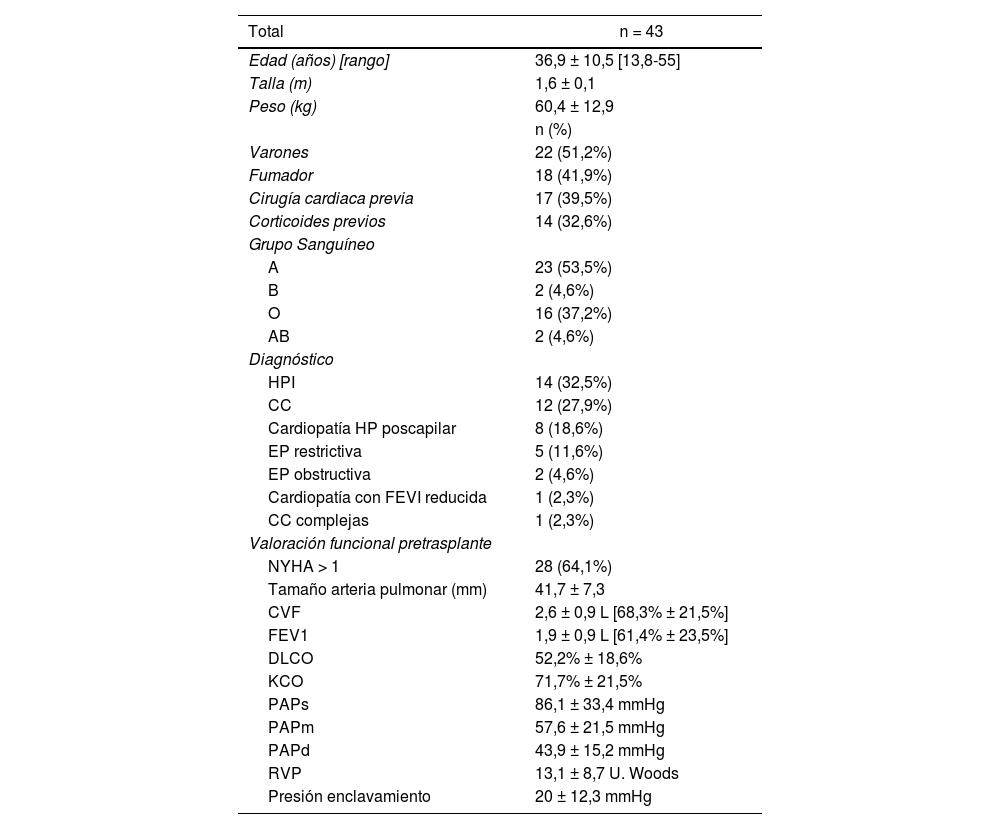
Las características demográficas, basales del receptor y valoración funcional preoperatoria se describen en la tabla 1, mientras que las de los donantes se exponen en la tabla 2.
Características demográficas y preoperatorias
| Total | n = 43 |
|---|---|
| Edad (años) [rango] | 36,9 ± 10,5 [13,8-55] |
| Talla (m) | 1,6 ± 0,1 |
| Peso (kg) | 60,4 ± 12,9 |
| n (%) | |
| Varones | 22 (51,2%) |
| Fumador | 18 (41,9%) |
| Cirugía cardiaca previa | 17 (39,5%) |
| Corticoides previos | 14 (32,6%) |
| Grupo Sanguíneo | |
| A | 23 (53,5%) |
| B | 2 (4,6%) |
| O | 16 (37,2%) |
| AB | 2 (4,6%) |
| Diagnóstico | |
| HPI | 14 (32,5%) |
| CC | 12 (27,9%) |
| Cardiopatía HP poscapilar | 8 (18,6%) |
| EP restrictiva | 5 (11,6%) |
| EP obstructiva | 2 (4,6%) |
| Cardiopatía con FEVI reducida | 1 (2,3%) |
| CC complejas | 1 (2,3%) |
| Valoración funcional pretrasplante | |
| NYHA > 1 | 28 (64,1%) |
| Tamaño arteria pulmonar (mm) | 41,7 ± 7,3 |
| CVF | 2,6 ± 0,9 L [68,3% ± 21,5%] |
| FEV1 | 1,9 ± 0,9 L [61,4% ± 23,5%] |
| DLCO | 52,2% ± 18,6% |
| KCO | 71,7% ± 21,5% |
| PAPs | 86,1 ± 33,4 mmHg |
| PAPm | 57,6 ± 21,5 mmHg |
| PAPd | 43,9 ± 15,2 mmHg |
| RVP | 13,1 ± 8,7 U. Woods |
| Presión enclavamiento | 20 ± 12,3 mmHg |
CC: cardiopatía congénita; EP: enfermedad pulmonar; HPI: hipertensión pulmonar idiopática. CVF: capacidad vital forzada; DLCO: capacidad de transferencia de monóxido de carbono; FEV1: volumen espiratorio forzado en el primer segundo; FEVD: fracción eyección ventrículo derecho; FEVI: fracción eyección ventrículo izquierdo; KCO: factor de transferencia para monóxido de carbono; NYHA: escala New York Heart Association; PAPd: presión arterial pulmonar diastólica; PAPm: presión arterial pulmonar media; PAPs: presión arterial pulmonar sistólica; RVP: resistencias venosas periféricas.
Las variables cuantitativas se expresan en media y rango.
Las indicaciones y los diagnósticos pretrasplante se describen en la tabla 1.
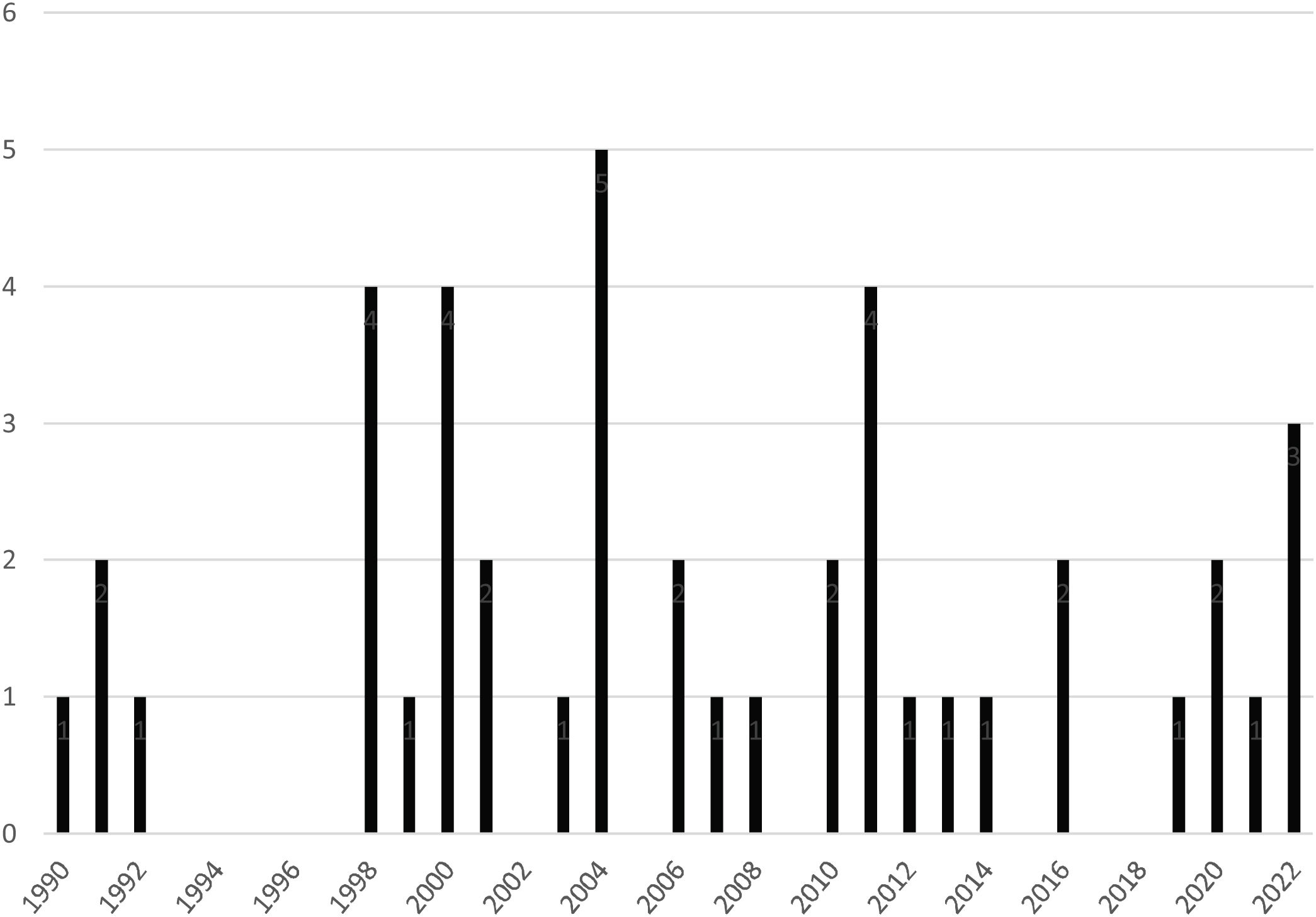
Se observó una reducción del número de TCP realizados en el último decenio de estudio (fig. 1).
Procedimiento y curso posoperatorioSe realizaron cinco (11,6%) trasplantes en situación de urgencia. El tiempo de isquemia medio fue de 223 ± 69,7 min, con un tiempo medio de CEC de 199,9 ± 71,3 min.
La estancia media hospitalaria tras el trasplante fue de 46,8 ± 34,7 días y en reanimación de 17,1 ±18,6, con un tiempo medio de intubación de 6,6 ± 8,4. Siete (16,2%) pacientes requirieron reingreso en reanimación.
Las complicaciones posoperatorias más frecuentes fueron el derrame pleural (32,5%), el hemotórax (30,2%) y el edema pulmonar cardiogénico (30,2%). Se presentaron 12 casos de disfunción primaria de injerto de los cuales seis (13,9%) fueron grado 3. De los pacientes, 10 requirieron reintervención (23,2%); siete (16,2%) por hemorragia y tres (7%) por dehiscencia de herida quirúrgica.
Factores asociados a mortalidad precozLa mortalidad perioperatoria global de la serie fue de 23,3% (n = 10) reduciéndose a 13,3% a partir de 2010. La mortalidad intrahospitalaria fue de 41,9%, disminuyendo a 33% en 2010.
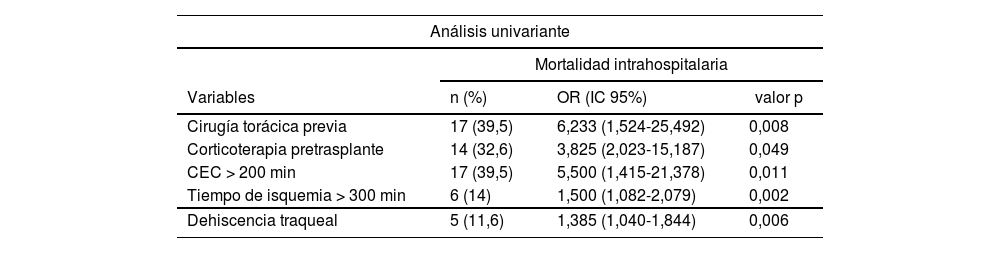
Los factores asociados a mortalidad intrahospitalaria (análisis univariante) se describen en la tabla 3. En el análisis multivariante se evidencia que la corticoterapia pretrasplante (odds ratio [OR]: 7,750; intervalo de confianza [IC] 95%: 1,621-37,064; p = 0,021) y la CEC > 200 min (OR: 5,060; IC 95%: 1,019-25,117; p = 0,47) estuvieron asociados a la mortalidad (tabla 3). Las causas de muerte más frecuentes fueron la infección respiratoria (18%) y las complicaciones quirúrgicas (hemorragia y dehiscencia traqueal, 9%).
Factores asociados a la mortalidad intrahospitalaria
| Análisis univariante | |||
|---|---|---|---|
| Mortalidad intrahospitalaria | |||
| Variables | n (%) | OR (IC 95%) | valor p |
| Cirugía torácica previa | 17 (39,5) | 6,233 (1,524-25,492) | 0,008 |
| Corticoterapia pretrasplante | 14 (32,6) | 3,825 (2,023-15,187) | 0,049 |
| CEC > 200 min | 17 (39,5) | 5,500 (1,415-21,378) | 0,011 |
| Tiempo de isquemia > 300 min | 6 (14) | 1,500 (1,082-2,079) | 0,002 |
| Dehiscencia traqueal | 5 (11,6) | 1,385 (1,040-1,844) | 0,006 |
| Análisis multivariante | OR (IC 95%) | valor p |
| Corticoterapia pretrasplante | 7,750 (1,621-37,064) | 0,021 |
| CEC > 200 min | 5,060 (1,019-25,117) | 0,047 |
CEC: circulación extracorpórea; IC: intervalo de confianza; OR: odds ratio.
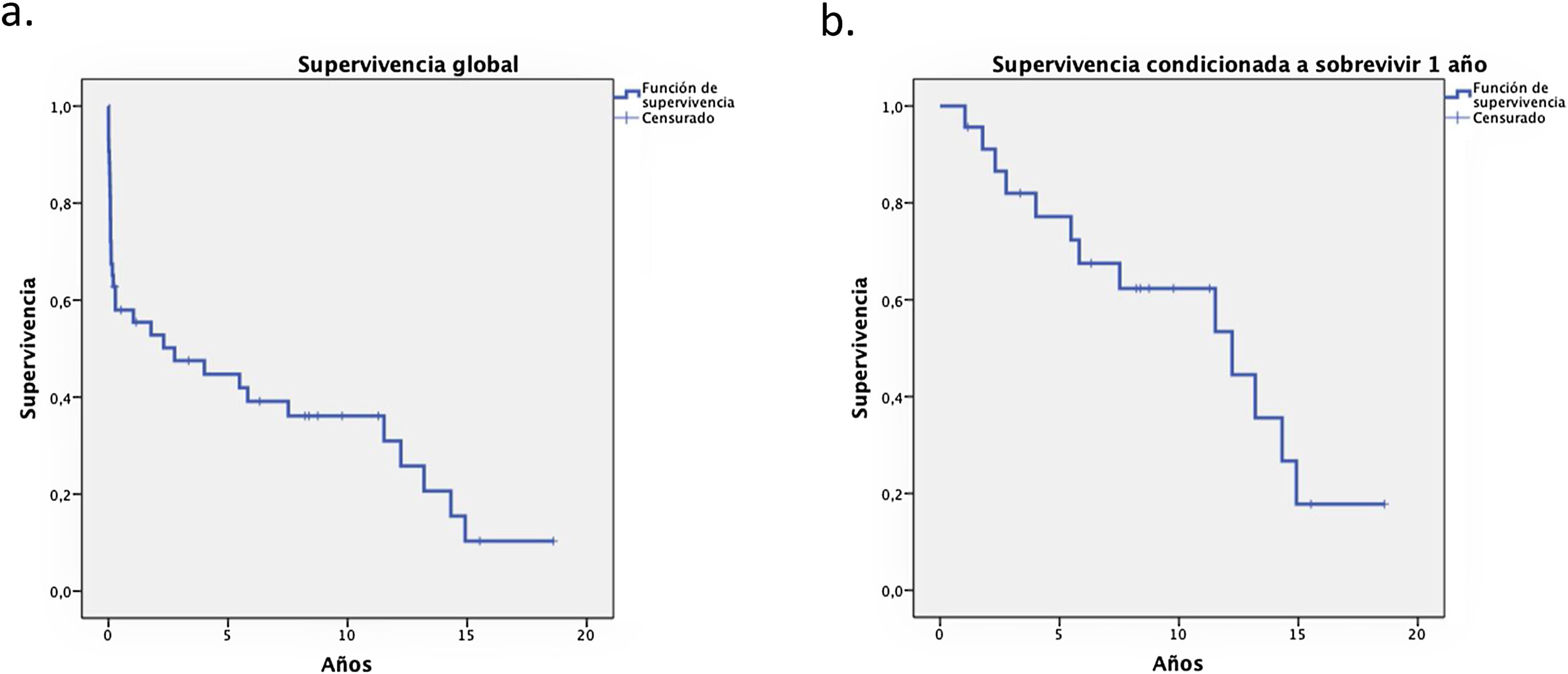
La supervivencia global a uno, cinco y 10 años fue de 58, 44,7 y 36,1%, respectivamente. Cuando se analizó la condicionada a sobrevivir el primer año, la de cinco y 10 años mejoró a 77,2 y 62,3%, respectivamente, haciendo evidente el impacto del primer año en la supervivencia a largo plazo (fig. 2).
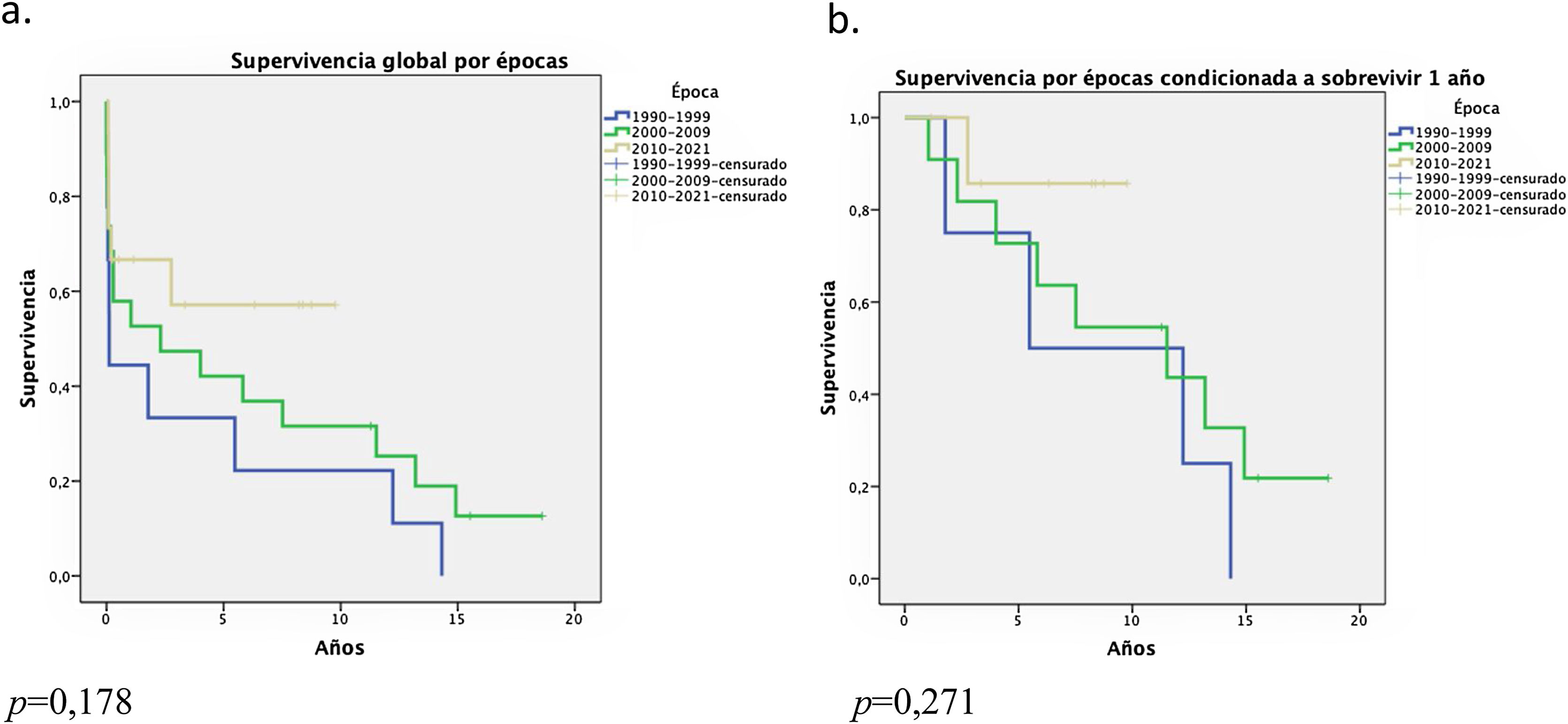
La supervivencia por épocas a uno y cinco años pasó de 44,4 y 33,3%, en 1990-1999 a 66,7 y 57,1%, en 2010-2020, (p = 0,178). Cuando se analizó la supervivencia por épocas condicionada a sobrevivir el primer año, se observó la misma tendencia (p = 0,231) (fig. 3).
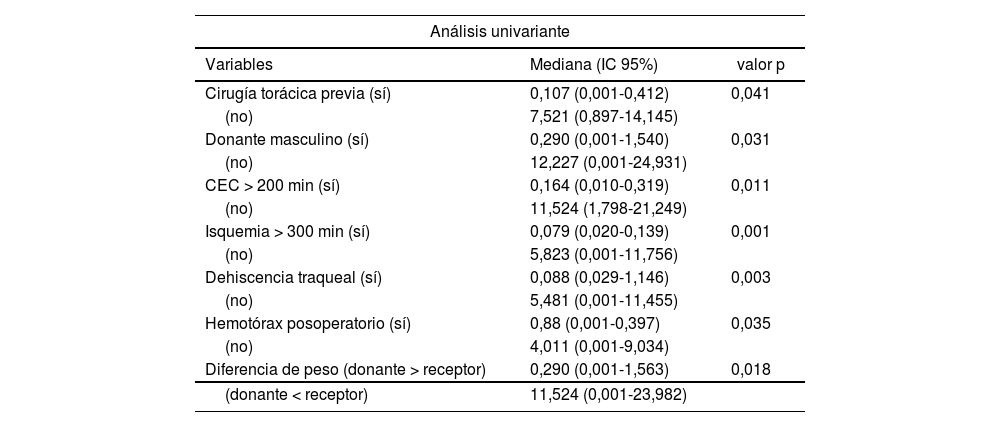
Los factores asociados a la supervivencia a largo plazo se describen en la tabla 4 (análisis univariante). En el multivariante se evidenció que la isquemia mayor a 300 min (OR: 4,6; IC 95%: 1,5-14; p = 0,007) y el peso del donante mayor al del receptor (OR: 2,7; IC 95%: 1,01-7,1; p = 0,04) afectaron negativamente a la supervivencia a largo plazo.
Factores asociados a la supervivencia
| Análisis univariante | ||
|---|---|---|
| Variables | Mediana (IC 95%) | valor p |
| Cirugía torácica previa (sí) | 0,107 (0,001-0,412) | 0,041 |
| (no) | 7,521 (0,897-14,145) | |
| Donante masculino (sí) | 0,290 (0,001-1,540) | 0,031 |
| (no) | 12,227 (0,001-24,931) | |
| CEC > 200 min (sí) | 0,164 (0,010-0,319) | 0,011 |
| (no) | 11,524 (1,798-21,249) | |
| Isquemia > 300 min (sí) | 0,079 (0,020-0,139) | 0,001 |
| (no) | 5,823 (0,001-11,756) | |
| Dehiscencia traqueal (sí) | 0,088 (0,029-1,146) | 0,003 |
| (no) | 5,481 (0,001-11,455) | |
| Hemotórax posoperatorio (sí) | 0,88 (0,001-0,397) | 0,035 |
| (no) | 4,011 (0,001-9,034) | |
| Diferencia de peso (donante > receptor) | 0,290 (0,001-1,563) | 0,018 |
| (donante < receptor) | 11,524 (0,001-23,982) | |
| Análisis multivariante | OR (IC 95%) | |
| Isquemia > 300 min | 4,6 (1,5-14) | 0,007 |
| Peso donante > receptor | 2,7 (1,01-7,1) | 0,04 |
CEC: circulación extracorpórea; IC: intervalo de confianza; OR: odds ratio.
El número de TCP realizados a nivel mundial ha presentado una reducción progresiva. Según el último informe de la ISHLT, el pico de incidencia se dio en el año 1989 con 229 trasplantes, reduciéndose a tan solo 36 en 20153. Dimopoulos et al.10 evidenciaron una disminución de la tasa de TCP en su serie global de 34,9 antes de 2005 a 6,7% a partir del año 2006 (p = 0,0001).
En nuestra experiencia, esta reducción progresiva del número de TCP también ha sido evidente, siendo actualmente de un procedimiento/año, con una disminución progresiva de las tasas de TCP con respecto al número total de trasplantes realizados.
Esta tendencia a la reducción de la indicación de TCP se debe principalmente al cambio en los procedimientos realizados en los pacientes afectos de HP no secundaria a CC, donde se ha comprobado una mejoría en la función ventricular al disminuir las resistencias pulmonares tras la realización de un TBP22,23, presentado los mismos resultados tanto en mortalidad como en supervivencia que el TCP4,6,24. Sin embargo, esta mejoría no se evidencia con la realización de trasplante unipulmonar (TUP) en estos casos25,26.
Las indicaciones del TCP también han experimentado un cambio a lo largo del tiempo. Actualmente, la principal indicación de TCP es la HP no idiopática con 37,7%, seguida de la HPI con 28,4% y, en tercer lugar, la FQ con 14,9%3. Esta última se ha convertido en una indicación poco común en la actualidad comparado con la década de los 90 donde se realizaron 230 TCP por dicha patología3,27.
De igual manera, en nuestro trabajo pudimos evidenciar la misma tendencia en relación con las indicaciones, presentando en la última década 36,8% de trasplantes con CC y 28,6 con HPI.
Una de las mayores complicaciones iniciales del trasplante pulmonar es la DPIP que ocurre hasta en 50% de receptores pulmonares, siendo en la mayoría de los casos leve y transitoria, pero hasta en 30% puede resultar en hipoxemia grave28. Varios estudios describen la DPIP como una de las principales causas de morbimortalidad precoz, requiriendo de soporte ventilatorio y medidas como ventilación mecánica, traqueotomía o reintubación para su tratamiento6,14,17. La DPIP en nuestro estudio se produjo en 27,9%, inferior a lo descrito por otros autores, que describen un porcentaje mayor a 50%14,17.
Otra de las grandes complicaciones son las infecciones pulmonares11, siendo una causa importante de mortalidad12–14. En nuestra serie, se produjeron complicaciones infecciosas en 19 pacientes (44,2%), siendo la causa de muerte intrahospitalaria en ocho de ellos.
En relación con las complicaciones quirúrgicas destacan las relacionadas con patología pleural, siendo de gran importancia el hemotórax posoperatorio, que frecuentemente requiere de reintervención. Se ha descrito una incidencia aumentada de complicaciones hemorrágicas con respecto a la anticoagulación y el tiempo de CEC durante la cirugía. Hjortshøj et al.12 comunican la necesidad de reintervención en 20 pacientes (31,7%), siendo 95% por hemorragia posoperatoria. De igual manera, Brouckaert et al.17 reintervienen a 11 (28,9%) por la misma condición, datos similares a los presentados en nuestro estudio.
La mortalidad intrahospitalaria y durante el primer año tras el TCP sigue siendo elevada, si bien se ha ido observando una mejora progresiva con el paso del tiempo y la experiencia acumulada3,8,10. En nuestros resultados hemos observado la misma tendencia, con una reducción progresiva en torno a 10% de la mortalidad en dicho periodo con el desarrollo del programa.
Fadel et al.6 comparan los resultados del TCP y TBP en HP y describen una tasa de mortalidad hospitalaria global de 19,6% y para el TCP de 21,7%. De igual manera, Brouckaert et al.17 mencionan una tasa global de mortalidad intrahospitalaria de 19,1% y del TCP de 23,7%, Yun et al.14 de 20% y Dawkins et al.29 de 26%.
Estos resultados ponen de relevancia la importancia del periodo perioperatorio, ya que durante este se produce el principal número de muertes, ya sea por DPIP, complicaciones quirúrgicas o infecciones no citomegalovirus3,11.
La ISHLT describe como factores de riesgo independientes para mortalidad la era de realización del TP, la dependencia de ventilación mecánica del receptor, la edad avanzada del paciente y la discordancia de serología de citomegalovirus3. Dimopoulos et al.10 comparan el TCP y el trasplante cardiaco en usuarios con cardiopatías congénitas y describe como predictores de mortalidad la edad avanzada, el TCP y el trasplante antes de 2006. En nuestra serie observamos que la cirugía torácica previa, el tiempo de CEC mayor de 240 min, el tiempo de isquemia de los órganos mayor a 300 min, la corticoterapia y la dehiscencia traqueal influyeron en la mortalidad intrahospitalaria.
La supervivencia global de nuestra serie fue de 58, 44,7 y 36,1% a uno, cinco y 10 años, respectivamente, ligeramente inferior a lo comunicado por la ISHLT27. Cuando se analizó la supervivencia condicionada a sobrevivir el primer año, los resultados mejoraron a 77,2 y 62,3% a los cinco y 10 años, respectivamente, evidenciando el impacto que tiene el primer año en la supervivencia a largo plazo.
Tal y como se describe en otros trabajos17,23,30, el impacto de las épocas en las que se realizaron los TCP también estuvo presente en nuestra serie. En los últimos 10 años, la supervivencia mejoró a 66,7 y 57,1% a uno y cinco años, respectivamente. Brouckaert et al.17 describen una supervivencia significativamente mejor para los pacientes trasplantados en 2011 a 2014 en comparación con los años 90 (p = 0,03). Toyoda et al.5 encontraron una supervivencia actuarial significativamente mejor en el grupo trasplantado entre 1994-2006 con respecto al de 1982-1993 (p = 0,004). Esta mejora en la supervivencia de los sometidos a TCP probablemente se pueda atribuir a las mejoras en las técnicas quirúrgicas, en el desarrollo de las soluciones de preservación de órganos, mejor selección de pacientes, un mejor desarrollo en la inmunosupresión y profilaxis antibiótica, además de los cuidados perioperatorios y un manejo multidisciplinar11,17,19.
Se han descrito otros factores que afectan a la supervivencia a largo plazo, como el diagnóstico de HPI y la diferencia de peso donante-receptor3. Fadel et al.6, en uno de los estudios más grandes sobre TCP, definen la cirugía previa, la presencia de disfunción renal preoperatoria, la DPIP y el síndrome de bronquiolitis obliterante como factores pronósticos para la supervivencia. En nuestra serie, el donante de sexo masculino, el tiempo de CEC y de isquemia prolongada, el hemotórax, la dehiscencia traqueal y la diferencia de peso del receptor menor que el donante influyeron negativamente en la supervivencia, manteniéndose en el análisis multivariante el tiempo de isquemia prolongado y la diferencia de peso entre receptor y donante como factores pronósticos.
Las principales limitaciones de este estudio fueron debidas a la naturaleza de su diseño, ya que, al ser un estudio retrospectivo con un número relativamente pequeño de pacientes, se reduce la potencia del análisis.
A modo de conclusión, observamos que existe una disminución progresiva en el número de procedimientos, secundario a cambios en las indicaciones y una mejora importante de la mortalidad precoz y de la supervivencia del TCP en la última década. Los factores del receptor como los antecedentes de cirugía previa y uso de corticoides, del procedimiento, como la excesiva prolongación de los tiempos de isquemia y CEC, como la presencia de complicaciones graves (hemotórax y dehiscencia traqueal) afectaron negativamente a la mortalidad precoz y la supervivencia a largo plazo. Algunas variables relacionadas con el donante (sexo masculino y mayor tamaño) impactaron de forma negativa en la supervivencia a largo plazo. El TCP sigue siendo una opción de tratamiento eficaz en pacientes altamente seleccionados.
FinanciaciónEste trabajo no ha recibido ningún tipo de financiación.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.