La duodenopancreatectomía cefálica (DPC) es la única posibilidad de cura y supervivencia a largo plazo para los pacientes con carcinoma de cabeza pancreática y tumores del área periampular1-3. A pesar de ello, el índice de resecabilidad y la supervivencia a los 5 años siguen siendo bajos, comparados con los de otros tumores digestivos4. Las intervenciones más agresivas que incluyen la pancreatectomía total o la linfadenectomía extensa retroperitoneal no han demostrado disminuir la recidiva o aumentar la supervivencia5. Los tratamientos adyuvantes preoperatorios y postoperatorios tampoco han conseguido mejorar sensiblemente el pronóstico6. Entre los avances recientes más importantes, se ha podido observar que la regionalización de los procedimientos en centros de gran volumen y equipos que acumulen importante experiencia se asocia a una disminución de la mortalidad por debajo del 5% y de las complicaciones por debajo del 40%3,7-9. Las complicaciones más frecuentes de esta intervención son la fístula pancreática, el absceso intraabdominal, la sepsis y el vaciamiento gástrico retardado.
Algunas modificaciones de la técnica quirúrgica, inicialmente descrita por Whipple10, tampoco han demostrado diferencias significativas en la morbilidad en manos de grupos quirúrgicos con experiencia. Un reciente metaanálisis ha evidenciado que la DPC con preservación pilórica no disminuye la mortalidad ni la morbilidad y que la incidencia de retraso de vaciamiento gástrico es la misma11. Varios estudios aleatorizados, que comparan las anastomosis pancreatoyeyunal y pancreatogástrica, han evidenciado que en manos expertas la proporción de fístulas pancreáticas permanece inalterada con ambas técnicas12.
Existen innumerables modificaciones en la técnica quirúrgica de la DPC. Durante la fase de resección de la DPC, habitualmente se prioriza la ligadura de las venas pancreáticas entre la cabeza pancreática y la vena mesentérica. El último paso, antes de la exéresis completa de la pieza, suele ser la liberación de la arteria mesentérica superior (AMS), la ligadura de las arterias pancreatoduodenales y la sección del meso uncinado. La priorización de la disección de la AMS a nivel de la aorta y la inframesocólica es una innovación reciente. Entre las ventajas de esta técnica estaría el diagnóstico precoz de la invasión arterial y una exéresis menos hemorrágica, debido a la ligadura previa de las arterias pancreatoduodenales, y evitar la congestión venosa de la cabeza pancreática13.
Con respecto a la fase de reconstrucción, el grupo de Heidelberg, en un estudio retrospectivo que comparaba series históricas de dos centros distintos, ha preconizado que la reconstrucción del tránsito gástrico en situación antecólica se asociaría a una disminución en la incidencia de la complicación más frecuente de la DPC, que es el vaciamiento gástrico retardado14.
No obstante, las ventajas de estas modificaciones técnicas no han sido demostradas. El objetivo de este estudio es analizar el impacto de dos modificaciones recientes en la técnica quirúrgica de la DPC, introducidas en nuestro grupo (disección primaria de la AMS y de la gastroenterostomía antecólica), en los parámetros perioperatorios (transfusión, duración de la intervención), mortalidad y morbilidad postoperatorias, estancia hospitalaria y reingresos.
Pacientes y métodoEntre junio de 2000 y octubre de 2007 se han realizado en nuestra unidad 56 DPC por tumores malignos periampulares. A partir de marzo de 2005 se ha priorizado la disección precoz de la AMS previamente a cualquier gesto exerético irreversible. A partir de mayo de 2006 se ha realizado la reconstrucción gástrica o duodenal mediante anastomosis terminolateral con el yeyuno en posición antecólica. El tipo de resección gástrica, Whipple o preservación pilórica, se dejó a elección del cirujano, si bien en los tumores de la ampolla y el colédoco distal se prefirió esta última.
Diagnóstico y estadificaciónLa técnica utilizada preferentemente para el diagnóstico y la estadificación de los tumores periampulares es la tomografía computarizada multicorte (TCMC) con técnica multifásica.
Los parámetros habituales son: colimación fina (0,75-1 mm), reconstrucción de imágenes de 1-2,5 mm, inyección de un bolo rápido de contraste yodado intravenoso (150 ml a 3,5-4 ml/s), adquisición de los datos en un solo barrido por fase durante una apnea.
Nuestro protocolo de estudio incluye la realización de 3 fases: arte-rial-pancreática, que se inicia a los 40 s de la inyección del contraste; fase venosa portal, a los 70 s, y fase tardía de equilibrio, a los 3 min. La fase arterial tiene por objeto la detección de las lesiones periampulares y el análisis de la vascularización arterial regional (tronco celíaco y sus ramas, arteria mesentérica superior); la fase portal permite la valoración de las estructuras venosas del eje portal-mesentérico y la detección de lesiones en el parénquima hepático; la fase tardía muestra el realce progresivo de algunas lesiones, como el colangiocarcinoma, y completa la caracterización de las lesiones hepáticas.
Para el diagnóstico y la estadificación de estas lesiones es muy importante realizar la TCMC antes de cualquier maniobra de drenaje biliar, como la colocación de endoprótesis. Por un lado, la dilatación del colédoco actúa como una guía insustituible para la localización y detección del tumor; por el otro, la endoprótesis no está exenta de producir artefactos que dificultan la interpretación de las imágenes radiológicas.
De acuerdo con los criterios expuestos por Lu et al15, se considera altamente probable la invasión de una estructura vascular cuando hay contacto con la lesión tumoral mayor del 50% de su circunferencia (valor predictivo positivo, 95%). Otros signos fiables de invasión vascular son la estenosis y la irregularidad de los contornos de la imagen vascular.
Los principales criterios de afectación ganglionar son morfológicos, fundamentalmente un diámetro mayor que 1 cm en su eje corto, aunque dado el bajo rendimiento de la TCMC la presencia de adenopatías significativas no contraindica la cirugía.
La TCMD en fase arterial también tiene un papel importante a la hora de diagnosticar anomalías vasculares, principalmente de la arteria hepática derecha, que serán de mucha ayuda para el cirujano.
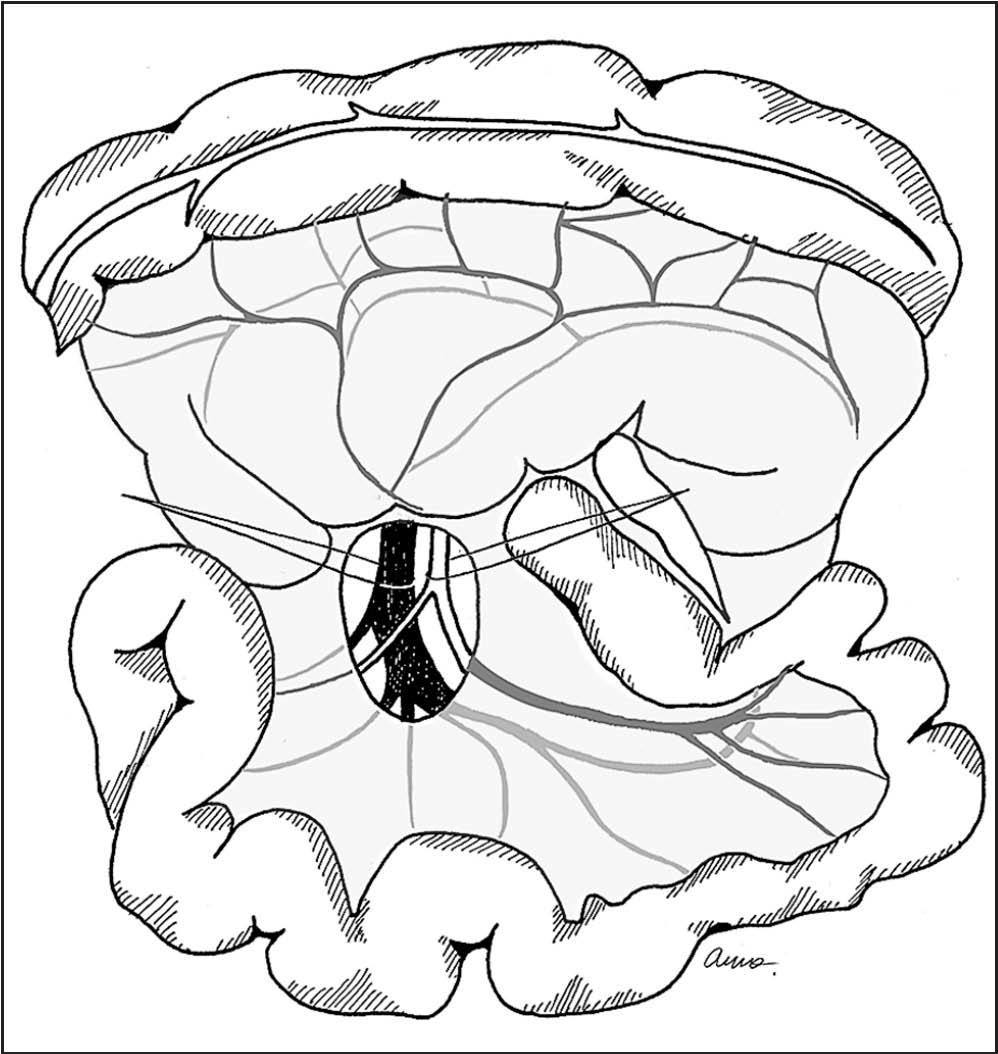
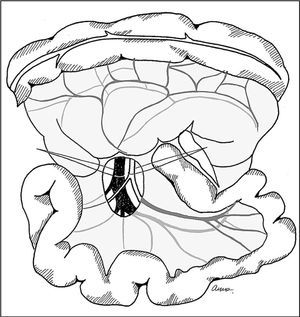
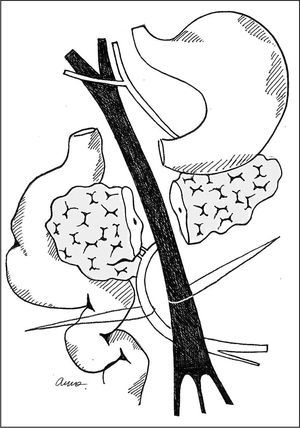
Técnica quirúrgicaLos detalles de la técnica han sido descritos anteriormente16. Brevemente se realiza una laparotomía subcostal bilateral. Después de descartar enfermedad a distancia y efectuar citología peritoneal, se expone la cabeza pancreática mediante descenso del ángulo del colon y maniobra de Kotcher. Se realiza exéresis de los ganglios interaortocava desde el tronco celíaco hasta la arteria mesentérica inferior para estudio intraoperatorio. Si el estudio histológico fuese positivo para tumor, se abandona la exéresis por considerar que no beneficiaría al paciente17. Seguidamente, se diseca y localiza con una cinta la AMS en su nacimiento en la aorta. A continuación, a nivel inframesocólico se localiza la vena mesentérica superior (VMS) y la AMS que se identifican con dos cintas (fig. 1). Estas maniobras permiten una identificación fácil de variaciones vasculares de la arteria hepática derecha y de la arteria pancreatoduodenal inferior, así como de la invasión tumoral, suponiendo que exista13.
Fig.1.Identificación de la vena y la arteria mesentérica superior a nivel del inframesocólico.
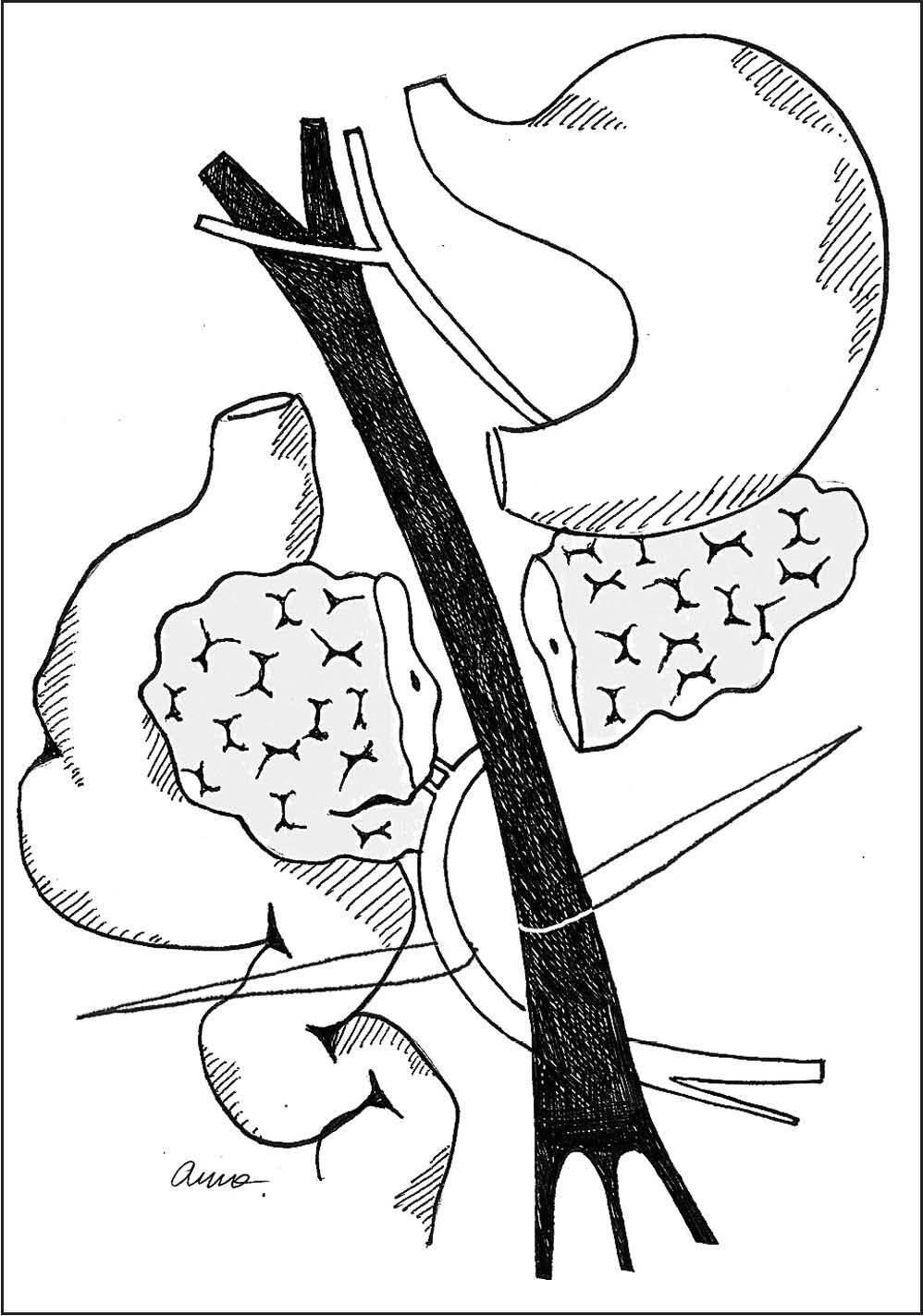
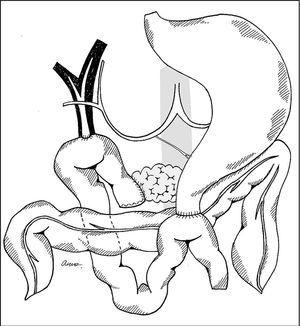
Una vez confirmada la resecabilidad, se procede a la exéresis pancreática. La estrategia y el orden de las maniobras pueden variar, pero se basa en los siguientes pasos:a)linfadenectomía de la arteria hepática y del pedículo hepático con ligadura de la arteria gastroduodenal18 y de la arteria cística; b) colecistectomía y sección de la vía biliar supracística, con muestra de bilis para estudio bacteriológico; c) sección del antro gástrico o del duodeno si se hace una preservación pilórica, en este caso se debe conservar la arteria gástrica derecha; d) sección inframesocólica de la tercera porción duodenal y de su mesenterio para proceder al descruzamiento; e) sección del cuello pancreático, sección del meso uncinado con esqueletización de la AMS y ligadura de las arterias pancreatoduodenales si no se ha realizado anteriormente, y f)en este momento se debe evaluar la invasión tumoral de la VMS y proceder a la resección venosa, suponiendo que exista19 (fig. 2).
Fig.2.Sección y ligadura de las arterias pancreatoduodenales inferiores antes de la sección de las venas pancreatoduodenales.
Después de la exéresis tumoral, con o sin resección venosa, se procede a la reconstrucción por el siguiente orden:a)pancreatoyeyunosto-mía terminolateral ductomucosa en dos planos con puntos sueltos de monofilamento reabsorbible3,20; b) hepatoyeyunostomía terminolateral con puntos sueltos de monofilamento reabsorbible, y c) reconstrucción de la continuidad gástrica o duodenal mediante sutura continua de material irreabsorbible. Todas las anastomosis se realizaron con la misma asa.
En casos de páncreas de textura muy blanda y Wirsung muy fino, una alternativa que se ha utilizado para la anastomosis pancreática es la intususpección yeyunal (en un caso) o la pancreatogastrostomía (en cuatro casos).
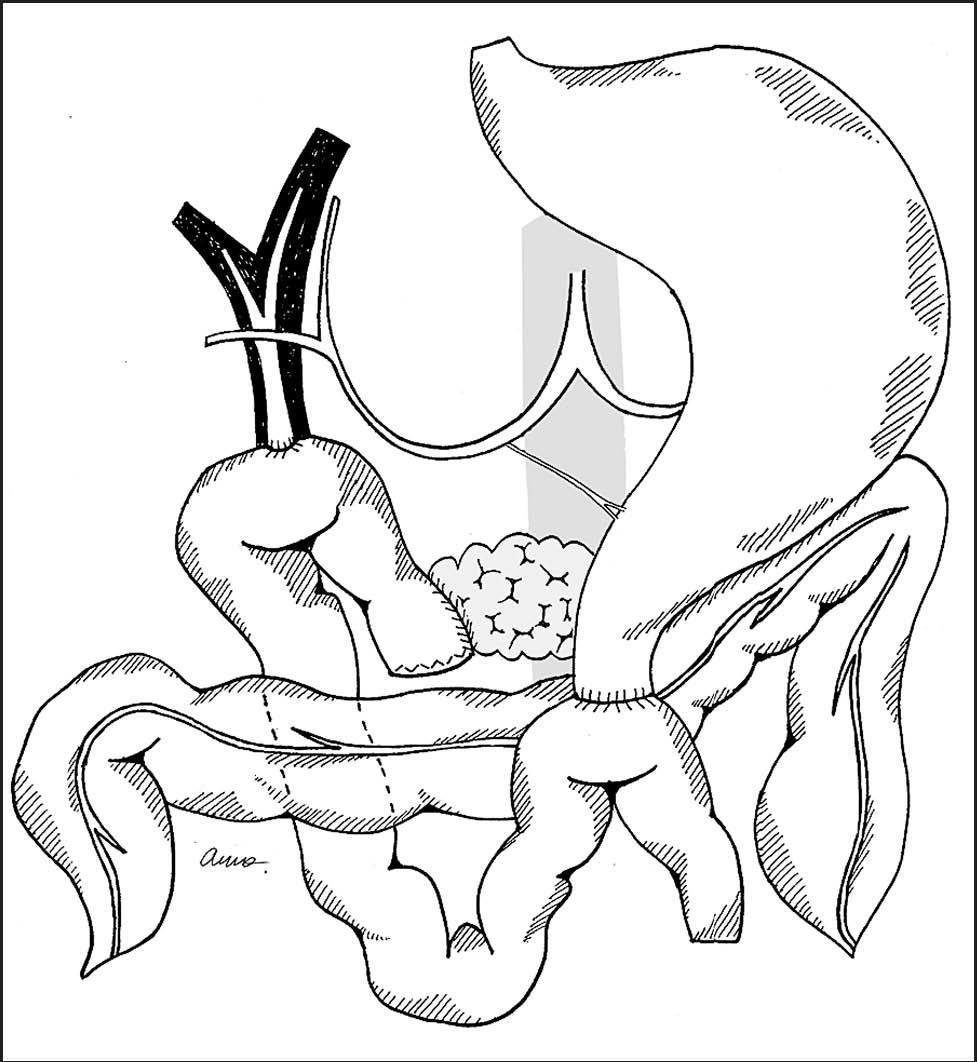
Durante el período comprendido entre mayo de 2006 y abril de 2007, se reintrodujo el yeyuno en el espacio inframesocólico y se realizó la reconstrucción gástrica o duodenal colocando el asa yeyunal en posición antecólica14 (fig. 3).
Fig.3.Reconstrucción duodenoyeyunal antecólica.
Cuidados perioperatoriosA los pacientes con concentraciones de bilirrubina mayores de 15 mg/dl se les practicó una colangiografía retrógrada endoscópica (CREP) y colocación de endoprótesis de plástico, para disminuir la bilirrubina con biopsia o citología si era posible. Durante los últimos 6 meses también se practicó ecoendoscopia con citología por punción si se visualizaba el tumor.
La cirugía de resección pancreática requiere de un cuidadoso manejo anestésico. La valoración preoperatoria debe ser exhaustiva, con especial énfasis en el estado nutricional del paciente. La técnica anestésica de elección consiste en anestesia general combinada con la colocación de un catéter epidural torácico21. La anestesia locorregional continúa en el postoperatorio, además de controlar el dolor, reduce la incidencia de complicaciones pulmonares, cardíacas e íleo paralítico y atenúa la respuesta neuroendocrina al estrés22.
La manipulación pancreática y la disección de los grandes vasos asociados suponen importantes cambios hemodinámicos intraoperatorios, por lo que la monitorización invasiva de estos parámetros resulta fundamental. Como toda cirugía abdominal mayor, la restricción hídrica debe ser la norma para minimizar complicaciones tanto en el intraoperatorio (menor sangrado) como en el postoperatorio. La reposición hídrica durante el acto quirúrgico debe estar guiada por valores de diuresis y parámetros hemodinámicos, intentando mantener en lo posible presión venosa central (PVC) < 4 mmHg23. Debe tenerse especial cuidado al mantenimiento de la normotermia.
El despertar debe ser precoz, a ser posible con extubación en el quirófano, por ello los fármacos anestésicos de elección para el mantenimiento son los de vida media corta con mínima acumulación, e iniciar la perfusión de anestésicos locales y/u opioides vía epidural antes de finalizar la intervención.
El modelo fast-track (o recuperación rápida) en cirugía pancreática es el ideal a conseguir; es necesario, dada la complejidad y la duración de la cirugía y la anestesia, un manejo perioperatorio agresivo y especializado en centros con equipos expertos y gran volumen de pacientes.
Actualmente, se usa sistemáticamente quimioterapia y radioterapia adyuvante con el esquema 5 FU intravenoso y 45 Gy sobre el lecho quirúrgico.
DefinicionesPara la fístula pancreática se adoptó la definición de la ISGP, que la define como cualquier cantidad mesurable de líquido procedente de un drenaje colocado durante la operación o percutáneamente, con un contenido de amilasas superior a tres veces el valor plasmático, después del tercer día24.
Vaciamiento gástrico retardado se definió como la necesidad de sonda gástrica durante más de 10 días, la imposibilidad de ingesta durante más de 10 días o vómitos durante más de 3 días después del quinto día postoperatorio en ausencia de estenosis anastomótica orgánica14.
La mortalidad operatoria se definió como el fallecimiento antes de los 30 días o durante el ingreso hospitalario si era mayor de 30 días.
Análisis estadísticoLos datos categóricos fueron analizados mediante el test exacto de Fisher. Los datos continuos se expresan como media ± desviación estándar (DE) y se analizaron con el test de la t de Student. La supervivencia general se estimó con el método de Kaplan-Meier y se comparó con la prueba de los rangos logarítmicos. La significación estadística se definió como p < 0,05. Los datos fueron analizados mediante un software SPSS (SPSS Inc, Chicago, ILL).
ResultadosEn el período enero de 2000-marzo de 2005, se intervino a 18 (41%) pacientes, sin disección precoz de la AMS, y constituyen el grupo control. Entre abril de 2005 y junio de 2007 se han realizado 38 DPC con disección inicial de la AMS (DIAMS) y constituyen el grupo de estudio. Todos los pacientes eran consecutivos y presentaban algún tipo de tumor maligno en la cabeza pancreática o área periampular.
Datos epidemiológicos operatorios y de técnica quirúrgica
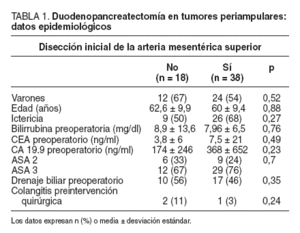
Los datos demográficos eran comparables y se hallan resumidos en la tabla 1. No se observaron diferencias significativas de sexo, edad, presencia de ictericia, concentración de bilirrubina, valores de marcadores tumorales CEA y CA 19.9, clasificación del riesgo según la American Society of Anesthesiologists (ASA), presencia de colangitis y utilización de drenaje biliar preoperatorio.
TABLA 1.Duodenopancreatectomía en tumores periampulares: datos epidemiológicos
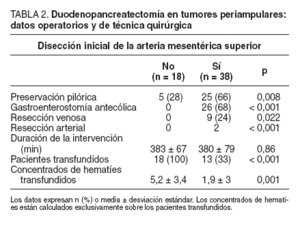
Los datos operatorios se hallan resumidos en la tabla 2. La preservación pilórica fue más frecuente en el grupo DIMS (p = 0,008). El 68% del grupo DIAMS recibió reconstrucción antecólica frente a ninguno en el grupo control. En el grupo DIAMS se realizaron reconstrucciones venosas y ninguna en el grupo control. Hubo significativamente más pacientes que precisaron transfusión perioperatoria y el volumen transfundido fue mayor en los pacientes sin DIAMS (p < 0,001).
TABLA 2.Duodenopancreatectomía en tumores periampulares: datos operatorios y de técnica quirúrgica
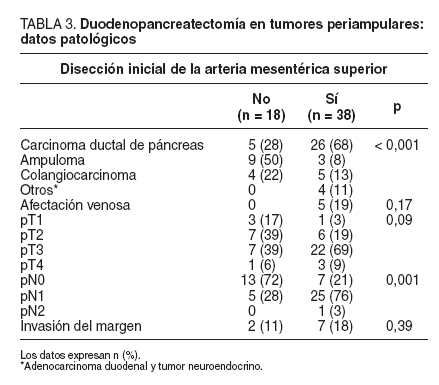
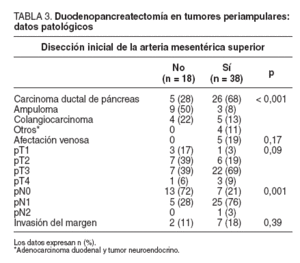
Datos patológicosLos datos histopatológicos se hallan resumidos en la tabla 3. El carcinoma ductal de páncreas fue el tumor más frecuente en el grupo con DIAMS (68%) (p = 0,001). A la inversa, el ampuloma se observó con mayor frecuencia en el grupo control, aunque sin alcanzar significación. La presencia de colangiocarcinoma fue similar en ambos grupos. Se observó afectación venosa en 5 (19%) del grupo DIAMS y ningún caso en el grupo control, porque en esa época la infiltración venosa era una contraindicación para la resección.
TABLA 3.Duodenopancreatectomía en tumores periampulares: datos patológicos
Respecto a la estadificación: la afectación ganglionar (pN1) fue significativamente más frecuente entre los pacientes del segundo grupo DIAMS (p = 0,001). No hubo variaciones en la técnica de linfadenectomía aunque sí en la selección preoperatoria.
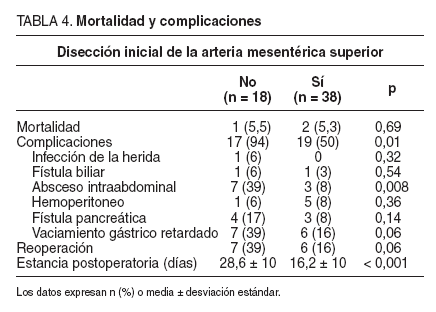
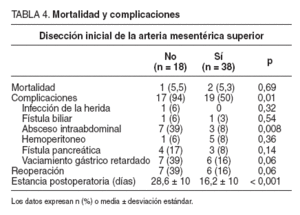
Los datos de mortalidad y morbilidad se hallan resumidos en la tabla 4. La mortalidad perioperatoria general fue del 5%, sin diferencias entre ambos grupos. Consideradas globalmente, las complicaciones fueron significativamente menores en el grupo DIAMS que en el control: 19 (50%) frente a 17 (94%), respectivamente, p = 0,01. Estas diferencias en morbilidad se debieron básicamente a una menor frecuencia de abscesos intraabdominales (p = 0,008) y una menor tasa de retardo en el vaciamiento gástrico, aunque en este último caso sin alcanzar significación estadística. La estancia postoperatoria fue significativamente menor en DIAMS (mediana, 12 frente a 26 días; p < 0,001).
TABLA 4.Mortalidad y complicaciones
Las tasas de recidiva fueron las mismas en ambos grupos. Aunque al segundo grupo se trató mayoritariamente con quimioterapia y radioterapia adyuvante (p = 0,0001) (tabla 5).
TABLA 5.Recidiva y tratamiento adyuvante
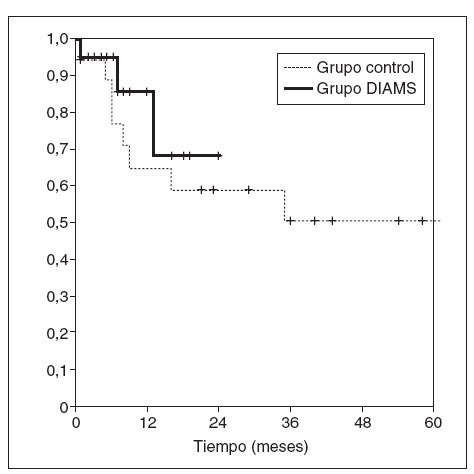
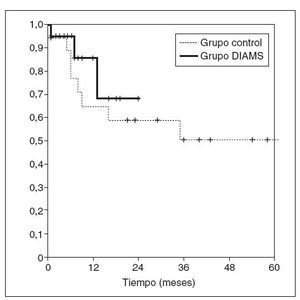
No hubo diferencias en la supervivencia calculada mediante el sistema actuarial (fig. 4).
ig.4.Supervivencia actuarial de ambos grupos.DIAMS:disec-ción inicial de la arteria mesentérica superior.
Impacto de la reconstrucción gástrica con anastomosis antecólica
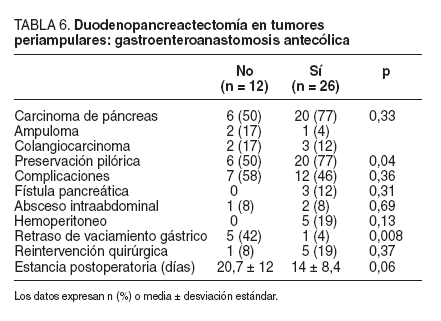
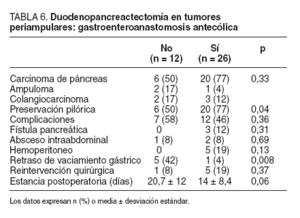
En el grupo de estudio con DIAMS (n = 38), la reconstrucción antecólica (bien sea gastroyeyunostomía o duodenoyeyunostomía) se utilizó en 26 pacientes y los datos más llamativos fueron comparados con los de 12 pacientes con reconstrucción retrocólica, también con DIAMS (tabla 6). El tipo histopatológico del tumor periampular fue similar entre ambos grupos. Hubo mayor tasa de preservación pilórica entre los pacientes con reconstrucción antecólica (20 [77%]) que retrocólica (6 [505%]) (p = 0,04). Consideradas en general, las complicaciones no fueron significativamente diferentes. El retraso en el vaciamiento gástrico se observó en 5 (42%) pacientes con reconstrucción retrocólica frente a uno en el grupo antecólico (p = 0,008). La estancia postoperatoria fue significativamente menor en el grupo antecólico (mediana, 13 días) que en el retrocólico (mediana,15 días), aunque sin alcanzar significación debido, probablemente, al escaso número de pacientes.
TABLA 6.Duodenopancreactectomía en tumoresperiampulares: gastroenteroanastomosis antecólica
No tenemos datos sobre el índice de resecabilidad porque las laparotomías de la primera época no están recogidas.
La cirugía de resección de los tumores pancreáticos benignos y malignos han experimentado notables avances recientemente25-27. No obstante, la técnica quirúrgica de la DPC y sus resultados a largo plazo siguen muy similares desde hace decenios. El dato más llamativo de nuestra experiencia es la disminución de complicaciones y estancia hospitalaria en el grupo de estudio o segundo período, cuando se ha realizado la disección inicial de la AMS (tabla 4). Estos resultados se han asociados a una menor tasa de transfusión, abscesos intraabdominales y reintervenciones (tabla 3). Durante el segundo período las indicaciones quirúrgicas fueron más agresivas (mayor tasa de carcinoma de páncreas e invasión ganglionar) y los gestos quirúrgicos (resección venosa) fueron también más agresivos (tabla 2). A pesar de ello, los resultados generales en conjunto son significativamente mejores.
Según se ha descrito, la técnica de ligadura precoz de las arterias pancreatoduodenales es útil para reducir las pérdidas de sangre debidas a congestión de la cabeza pancreática13,16,18. Además, la disección precoz de la AMS asegura una linfadenectomía total18,28, y permite una identificación, dentro del marco de seguridad, de variaciones anatómicas, como una arteria hepática originada en la AMS13. La arteria hepática derecha que nace de la AMS ocurre en aproximadamente el 15% de los casos. En estas circunstancias el riesgo de lesión de la arteria hepática derecha es alto en el curso de una DPC convencional29. La preservación de la totalidad del aporte sanguíneo al hígado y al árbol biliar es importante para prevenir las fístulas biliares después de la operación de Whipple, y en algunos casos, la isquemia hepática30. La lesión suele ocurrir durante la disección del proceso uncinado del páncreas, cuando se está tratando de separarlo de los vasos mesentéricos19. Este problema se puede obviar mediante el abordaje inicial de la AMS13,16. No obstante, se debe ser cuidadoso en respetar los nervios procedentes del plexo celíaco que se encuentran en el lado izquierdo de la AMS, porque de otra manera son más frecuentes las diarreas31.
Cuando se realiza la técnica clásica, el abordaje de los vasos mesentéricos superiores constituye el final de la técnica de resección, cuando el cuello pancreático ya se halla seccionado. Si en este momento se identifica una invasión de la AMS, la DPC debe continuar pues el páncreas ya se halla seccionado. La resultante es una gran cirugía con todo su coste en términos de morbilidad y mortalidad y sin ningún tipo de beneficio. La técnica del abordaje inicial de la AMS no tiene ese inconveniente, pues en el momento de la disección inframesocólica de la AMS, si se sospecha su invasión, la operación se da por terminada28 (fig. 1).
Es evidente que el factor curva de aprendizaje y la casuística también deben tener un papel importante en la mejora de nuestros resultados. Durante el período inicial la casuística fue de 3 pacientes/año, mientras que en el segundo período ésta fue de 12 pacientes/año. Según se ha descrito, la regionalización, el volumen y la experiencia del equipo y el centro son factores fundamentales en los resultados1-4,7-9.
Otro de los factores clásicamente considerado determinante de no resecar los tumores periampulares es la afectación de la vena porta. En los últimos años, sin embargo, varias publicaciones muestran que la resección de tumores con afectación venosa portal o mesentérica obtiene resultados similares que la de tumores en el mismo estadio sin invasión venosa. La DPC con resección portal es facilitada en gran manera por el abordaje inicial de la AMS, puesto que la anastomosis venosa puede realizarse en un campo exangüe32,33.
El cáncer periampular metastatiza frecuentemente en los ganglios linfáticos localizados alrededor de la AMS. La disección simultánea del plexo nervioso alrededor de la AMS, sin embargo, a veces resulta en el desarrollo de una diarrea intratable. La disección de los ganglios linfáticos mesentéricos superiores, preservando el plexo nervioso, es teóricamente posible y su abordaje se facilita por esta técnica31.
En nuestra serie, la reconstrucción gástrica antecólica se asoció a una incidencia significativamente menor de retraso de vaciamiento gástrico (p = 0,008). Asimismo, los pacientes con reconstrucción antecólica tuvieron una menor estancia hospitalaria postoperatoria, probablemente favorecida por la menor tasa de retardo de vaciamiento gástrico, aunque sin alcanzar la significación, debido, probablemente, al escaso número de pacientes. La fisiopatología del retraso de vaciamiento gástrico es motivo de controversia. Se han propuesto varios mecanismos: lesión de los nervios de Latarjet, daño isquémico del antro y el píloro, cambios en la concentración plasmática de motilina. Todos estos factores deberían afectar por igual tanto a la reconstrucción antecólica como retrocólica. Durante años se ha sostenido que la DPC con preservación pilórica se asociaba a una mayor incidencia de retardo en el vaciamiento gástrico que la DPC clásica. Estudios más recientes, sin embargo, muestran que no hay diferen-cias5,11. Nuestros resultados en esta serie son coincidentes, ya que se observó una tendencia a la disminución del retardo de vaciamiento gástrico en el grupo con reconstrucción antecólica, aunque la DPC con preservación pilórica se use preferentemente (tabla 6). Algunos autores han propuesto que el retraso de vaciamiento gástrico que sigue a la DPC podría tener un componente mecánico. La torsión o angulación de la duodenoyeyunostomía podría afectar negativamente al vaciamiento gástrico. La angulación podría ser la consecuencia de la gastroparesia postoperatoria o de la dilatación del colon transverso. Con la reconstrucción antecólica, el asa yeyunal descendente sería más móvil que con la reconstrucción retrocólica. Una explicación muy atractiva es aquella que nos dice que, aun en las mejores manos, la anastomosis pancreaticoyeyunal a menudo presenta microfugas y grados leves de pancreatitis postoperatoria. Esta inflamación alrededor de la pancreatoyeyunostomía podría afectar por vecindad a la duodenoyeyunostomía, que queda colocada encima, provocando retardo de vaciamiento. Nuestros resultados indican que esta última podría ser la explicación fisiopatológica del retraso de vaciamiento gástrico. La reconstrucción antecólica establecería una barrera protectora constituida por el mesocolon transverso que protegería a la duodenoyeyunostomía14. Un estudio aleatorizado reciente ha confirmado también que la duodenoyeyunostomía antecólica disminuye drásticamente el vaciamiento gástrico retardado durante el postoperatorio34.
En nuestra experiencia, la DPC con abordaje inicial de la AMS es una técnica segura, con una menor tasa de transfusión y complicaciones, y una menor estancia intrahospitalaria. Cuando se asocia a reconstrucción gastroyeyunal antecólica, los retrasos de vaciamiento gástrico son menos frecuentes.
Correspondencia: Dr. J. Figueras. Sección de Cirugía Hepatobiliar y Pancreática. Departamento de Cirugía. Hospital Dr. Josep Trueta. Ctra. de França, s/n. 17007 Girona. España. Correo electrónico: info@jfigueras.net
Manuscrito recibido el 10-9-2007 y aceptado el 17-12-2007.