Introducción. Presentamos 20 años de experiencia con nuestra técnica personal de amputación reconstrucción simultánea más mastectomía subcutánea contralateral profiláctica en el cáncer de mama.
Pacientes y métodos. De 943 pacientes tratadas por carcinoma de mama, 642 lo han sido con la técnica quirúrgica original, que se desglosa en tres tiempos, siendo el primero el de carácter puramente oncológico, el segundo para la obtención del colgajo miocutáneo, que permitirá en el tercer tiempo la reconstrucción de la mama amputada y la mastectomía subcutánea contralateral, en el mismo acto quirúrgico.
Resultados. Desde el punto de vista oncológico, los resultados son superponibles a los de otros autores que realizan cirugía radical, siendo la supervivencia global a los 10 años del 70% y no detectándose recidivas locales en los estadios I y II a los 5 años frente a las altas tasas que se describen en la cirugía conservadora (8-25%). Hemos podido detectar en nuestras pacientes un 12% de multicentricidad en la mama afectada y un 6,4% de bilateralidad.
Desde el punto de vista estético, nuestras pacientes refieren un alto nivel de satisfacción (96%).
La tasa de complicaciones se sitúa en torno al 4%.
Conclusión. Consideramos que el tratamiento quirúrgico del cáncer de mama debe ser oncológico radical y reconstructor en un mismo tiempo, condiciones que reúne la técnica que se describe, siendo de elección en el tratamiento quirúrgico del cáncer de mama.
Introduction. We present 20 years of experience using our own technique for simultaneous amputation and reconstruction plus prophylactic contralateral subcutaneous mastectomy in breast cancer.
Patients and methods. Of the 943 patients we have treated for breast cancer, 642 have undergone this original surgical technique, which can be broken down into three stages: the first of purely oncologic nature, the second to obtain the myocutaneous flap with which the amputated breast is reconstructed in the third stage, during which contralateral subcutaneous mastectomy is also performed.
Results. From the oncologic point of view, our results are similar to those of other authors using radical surgery, with an overall 10-year survival rate of 70% and no evidence of local recurrence in stages I and II at 5 years, in comparison with the high rates associated with conservative surgery (8% to 25%). We have observed a rate of multicentricity of 12% in the affected breast and bilaterality in 6.4% of cases.
From the cosmetic point of view, 96% of our patients are highly satisfied.
We have recorded a rate of complications of approximately 4%.
Conclusion. We consider that breast cancer should be treated with radical and reconstructive surgery at the same time, conditions which the technique described here fulfills. Therefore, we consider it the treatment of choice in breast cancer patients.
I ntroducción
Consideramos nuestra técnica personal de amputación reconstrucción simultánea más mastectomía subcutánea contralateral profiláctica en el cáncer de mama, como técnica de elección ideal en el tratamiento de esta enfermedad1,2. Nuestra experiencia de 20 años y los resultados obtenidos, tanto estéticos como oncológicos, apoyan nuestra afirmación.
Nuestra técnica se fundamenta en la reconstrucción inmediata de la mama tras mastectomía radical con criterio oncológico con colgajo miocutáneo de gran dorsal y mastectomía subcutánea contralateral profiláctica, con objeto de disminuir el traumatismo psicológico que crea la amputación, evitar una segunda intervención para la reconstrucción secundaria, eliminar el carcinoma contralateral sincrónico o metacrónico.
Las pacientes, que saben de la reconstrucción, acuden antes al médico, lo que favorece un diagnóstico más temprano.
La reconstrucción inmediata no interfiere ni retrasa los tratamientos complementarios con quimioterapia, radioterapia y hormonoterapia, ni el diagnóstico de una posible recidiva locorregional.
Pacientes y métodos
Hemos tratado a 943 pacientes afectadas de carcinoma de mama. De éstas, 243 han sido mastectomías radicales sin reconstrucción, 27 mastectomías subcutáneas bilaterales por carcinoma in situ no infiltrante y 29 mastectomías subcutáneas bilaterales y limpieza axilar homolateral en carcinoma in situ infiltrante. Nuestra técnica personal de amputación-reconstrucción simultánea con colgajo miocutáneo más mastectomía subcutánea contralateral profiláctica en el cáncer de mama la hemos realizado en 644 pacientes afectadas de carcinoma de mama palpable. De las 644, en 2 casos la reconstrucción se realizó con colgajo miocutáneo de recto anterior del abdomen y en las 642 restantes con colgajo miocutáneo de gran dorsal, técnica que describimos a continuación.
Técnica quirúrgica
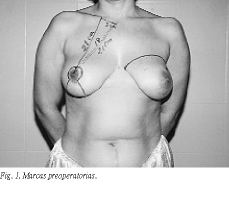
Marcaje preoperatorio: Se realiza incisión de Stewart3 en la mama afectada y de mastopexia en la contralateral con el patrón de Wise4 (fig. 1) y en la espalda marcaje de la isla cutánea sobre el gran dorsal de 15 * 8 cm aproximadamente.
Distinguimos 3 tiempos quirúrgicos:
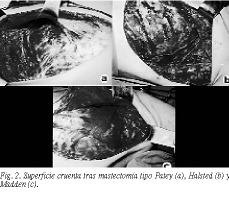
1. En el primer tiempo o tiempo de resección, habitualmente realizamos mastectomía radical modificada tipo Patey5 (fig. 2a), aunque excepcionalmente se han tratado con Halsted6 (fig. 2b), o Madden7 (fig. 2c). Previamente a la mastectomía procedemos a la extracción del complejo areola-pezón y extirpamos la base del mismo para su estudio anatomopatológico intraoperatorio; si el resultado del estudio de dicha base fuera de no invasión, guardaremos el complejo areola-pezón para reinjertarlo posteriormente.
En la linfadenectomía axilar (de los 3 niveles) es obligado anatomizar la salida de los vasos escapulares inferiores siguiendo caudalmente hasta su bifurcación en escapular inferior propiamente dicha y vasos toracodorsales, que disecamos hasta su entrada en el músculo gran dorsal. Estos vasos van acompañados en este territorio del nervio del gran dorsal, formando todos ellos el pedículo neurovascular que va a ser el nutriente del colgajo miocutáneo a emplear en la reconstrucción. Terminada la mastectomía, este tiempo finaliza con la desinserción distal del pectoral mayor hasta su línea esternal.
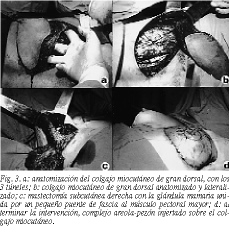
2. Segundo tiempo o de extracción del colgajo. Colocamos a la paciente en decúbito lateral e incindimos sobre las marcas del colgajo miocutáneo de gran dorsal8-12, hasta alcanzar el plano muscular del gran dorsal, que disecamos ampliamente. Para una correcta disección del colgajo hemos descrito 3 túneles13 (fig. 3a), partiendo del borde superior del gran dorsal; una vez anatomizado en su totalidad (fig. 3b) lo transponemos al defecto de la mastectomía y cerramos la superficie cruenta de la espalda por aproximación directa o mediante injerto de piel total.
3. Tercer tiempo o de reconstrucción y mastectomía subcutánea contralateral. Colocamos a la paciente en decúbito supino y con los brazos en aducción, procedemos a la readaptación del colgajo miocutáneo de gran dorsal sobre el defecto de la mastectomía radical y practicamos la mastectomía subcutánea contralateral.
En la mastectomía subcutánea nos situamos por encima de los ligamentos de Cooper, dejando unos colgajos cutáneos finos, e incluimos en la pieza la fascia del pectoral mayor, cola de Spencer y las adenopatías más bajas del nivel I de la axila14 (fig. 3c), dejando únicamente los conductos distales del pezón, que no suponen ni el 1% del tejido glandular. Tras la readaptación de los colgajos cutáneos introducimos una prótesis de gel de silicona para dar volumen, que queda ubicada retropectoralmente en su porción superior.
En la mama reconstruida, tras la readaptación del colgajo miocutáneo introducimos una prótesis de gel de silicona por un pequeño ojal, dejado a tal efecto.
Para la reconstrucción del complejo areola-pezón, marcamos el área que se va a desepidermizar para injertar la areola, cuando ésta puede ser utilizada (fig. 3d). En el caso contrario, cuando hay afectación de la base o la desechamos por la proximidad del tumor, la reconstruimos con un injerto de piel total de la cara interna de muslo y el pezón del contralateral o con 4 colgajos dérmicos.
Colocamos drenajes aspirativos de Redón y vendaje ligeramente compresivo.
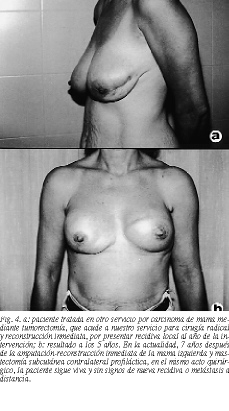
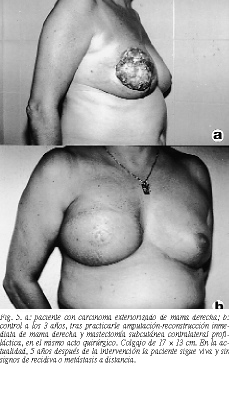
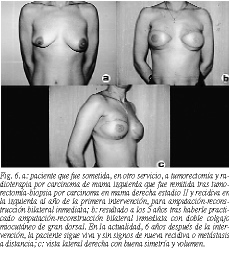
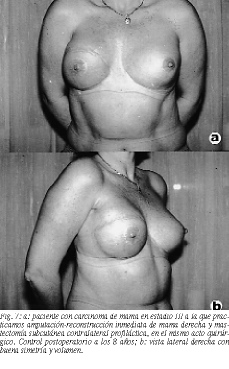
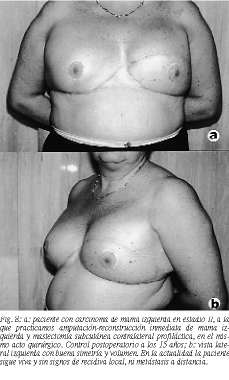
Resultados (figs. 4-8)
La duración de esta intervención es de 3 a 3 horas y media.
Nuestros resultados, desde el punto de vista oncológico, son superponibles a los de otros autores que realizan cirugía radical sin reconstrucción. A los 10 años, el resultado global era de un 70% de supervivencia. De las 8 pacientes con carcinoma bilateral encontrado a los 5 años, en la actualidad, 15 años después (20 años de postoperatorio) siguen vivas 2 pacientes (un 25%) y libres de enfermedad.
Nunca se ha detectado enfermedad neoplásica a posteriori en la mama que hemos practicado la mastectomía subcutánea, y tampoco nunca hemos evidenciado una recidiva local cuando hemos reinjertado el complejo areola-pezón.
No tenemos recidivas locales en estadios I y II a los 5 años de control postoperatorio y un 4% en estadio III.
Encontramos un 12% de multicentricidad y un 6,4% de bilateralidad.
El 96% de las pacientes refieren estar satisfechas o muy satisfechas.
Hemos detectado un 4% de complicaciones.
Complicaciones inmediatas
En la mama reconstruida, en 6 casos se ha producido un desplazamiento de la prótesis a la axila. En 6 ocasiones se produjo linforragia que coincidió con los 6 casos de desplazamiento de la prótesis a la axila. En 22 pacientes se produjo una dehiscencia parcial de la sutura de la espalda y en tres un hematoma de esta zona. En 5 casos se produjo una necrosis parcial del colgajo (en el tercio distal), que afectó sólo a la parte cutánea y que no obligó a retirar la prótesis. En 10 pacientes se apreció una necrosis parcial del complejo areola-pezón. Presentaron lin forragias el 1,2% de las pacientes.
En la mama contralateral, en 21 pacientes se apreció necrosis parcial de la areola, en 20 se produjo una dehiscencia de la rama vertical y en 6 una extrusión de prótesis.
Complicaciones a distancia
En la mama reconstruida hemos apreciado una despigmentación del complejo areola-pezón, más acusada en las pacientes sometidas a radioterapia, en torno al 20%, aplanamiento del pezón en el 20% de los reinjertados y en un 40% de los reconstruidos, extrusión de prótesis en 6 casos, contractura en un 20% de los casos, apreciándose una mayor incidencia en las pacientes sometidas a radioterapia (40%), linfedema en el 20%, plexopatía braquial en 2 casos posradioterapia.
En la mama contralateral hemos tenido 3 extrusiones de prótesis y contracturas en el 10% de las pacientes. En 15 casos se ha producido rotura espontánea cuando utilizábamos prótesis hinchables salinas. Asimetría en un 30%.
Se produjo un fallecimiento atribuible a un embolismo pulmonar en el noveno día de postoperatorio.
Discusión
Como cirujanos generales, hasta finales de los años setenta nos satisfacía el resultado obtenido con una mastectomía radical, plenamente indicada entonces ante todo cáncer de mama, pero como cirujanos plásticos nos preocupaba e intranquilizaba, como a las pacientes tratadas, el trauma psicológico que les provocaba esta mutilación.
Muchas pacientes evitaban ir al cirujano por el temor a que las amputasen, aun a pesar de haberse palpado una masa, por el pánico que les ocasionaba que el médico les diagnosticase un cáncer y les propusiese como tratamiento la mastectomía, con la consiguiente minusvalía desde el punto de vista orgánico, psíquico y sexual que acarrea una pérdida tan importante para una mujer, símbolo de la maternidad y la sexualidad. Ante esta situación el diagnóstico era tardío, de mal pronóstico y abocado a la pérdida de la mama.
Esta problemática nos sirvió de estímulo para intentar realizar la cirugía oncológica y reconstruir en un mismo acto quirúrgico. En enero de 1979 logramos realizar, en el mismo acto quirúrgico, la primera mastectomía radical tipo Halsted y reconstrucción inmediata con colgajo miocutáneo de gran dorsal y biopsia reducción de los 4 cuadrantes de la mama contrala teral15,17.
Presentamos las primeras pacientes amputadas y reconstruidas en el mismo acto quirúrgico en la Mesa redonda de Reconstrucción mamaria, en la Clínica Planas en septiembre de 197916.
Fueron años de intensos ataques dialécticos por gran parte de los cirujanos plásticos, no así de los oncólogos ni cirujanos generales. En febrero de 1980 presentamos la técnica en el Congreso Nacional de Oncología en Zaragoza y el mismo año, en el Congreso Nacional de Cirugía en Barcelona, sin sufrir ninguna crítica desde el punto de vista oncológico ni quirúrgico; en octubre de 1980 tras la lectura de la tesis doctoral: Contribución a la radiobiología de las prótesis mamarias17, se asentaron las conclusiones que son plenamente vigentes en la actualidad.
En 1981 se presentó el trabajo en el II Congreso Internacional de Senología en Barcelona, no sufriendo crítica alguna porque la técnica quirúrgica cumplía escrupulosamente los requisitos de cirugía radical oncológica y reconstrucción inmediata, no interfiriendo ni retrasando los tratamientos complementarios de radioterapia y quimioterapia.
Algunos cirujanos plásticos, tal vez por la incomprensión del tratamiento del cáncer de mama, como su evolución y resultados, se empecinaban en que las prótesis podían interferir el tratamiento radiante postoperatorio, en que había que esperar 5 años para descartar una radionecrosis, en que las pacientes no valoraban la reconstrucción inmediata y era mejor que se vieran mutiladas y, entonces, aunque el resultado no fuese bueno, siempre apreciaban más la reconstrucción. Eran críticas sin bases en argumentos científicos, tal vez por el natural rechazo a lo nuevo que siempre se acoge con escepticismo y precaución, y más cuando se trata de un compatriota. Si el innovador hubiera tenido otra procedencia, posiblemente la aceptación hubiese sido más rápida y menos suspicaz.
Fueron años de fuerte rechazo en los congresos de cirugía plástica, pero que fueron reafirmando nuestro criterio, porque era de total aceptación por parte de los oncólogos y cirujanos generales y porque estaba avalado por nuestros trabajos de investigación, que motivaron una tesis doctoral17, en los que demostramos que nuestra técnica de reconstrucción inmediata era perfectamente oncológica, cumplía los requisitos de cumplimentar los tratamientos adyuvantes, evitaba o disminuía el trauma de la amputación e indirectamente intentaba un diagnóstico precoz, porque las pacientes acudían antes al cirujano, ya que perdían el miedo a la amputación.
Durante el inicio de nuestra técnica se empezaban a implantar las técnicas de la cirugía conservadora (en nuestro criterio insuficiente), basándose en teorías de que las células cancerosas no seguían la teoría halstediana de una colonización ganglionar escalonada, sino que había saltos de las células por vía hematógena, y que ya no era preciso hacer una cirugía tan ablativa; y en estos momentos vuelve a tomar fuerza la teoría halstediana basándose en el ganglio centinela, que tampoco compartimos.
Creemos que la propagación del cáncer de mama puede seguir las teorías descritas por Halsted y Fisher18, y tenemos pacientes que corroboran ambas. Puesto que ignoramos qué casos van a evolucionar según una u otra, nuestra actitud quirúrgica es la de ser más agresivos desde el punto de vista locorregional y no realizamos nunca cirugía conservadora.
Los defensores de la cirugía conservadora iban aumentando, unos por convicción y otros porque su formación quirúrgica, coincidiendo con Tejerina19, no muy familiarizada con la cirugía oncológica radical, les inducía más acogerse a este criterio y actitud quirúrgica.
Toda la cirugía del cáncer en cualquier territorio orgánico, sigue la teoría halstediana de la mama, según la cual se extirpan el órgano y las vías de drenaje linfático (estómago, útero, etc.) porque en estos territorios los pacientes no ven que es lo que se les ha hecho; pero en la mama, como es una parte anatómica visible y de gran calado psíquico, se han creado nuevas teorías para justificar nuevas cirugías menos agresivas. Hoy por hoy, a pesar de todos los tratamientos sistémicos, coincidimos con Broder, director del National Cancer Institute, que demostró que las estadísticas nacionales de oncología respecto a tasas de mortalidad por cáncer mamario apenas han cambiado en los últimos 15 años, a pesar de las actitudes triunfalistas de los oncólogos estadounidenses. Se acepta que los tratamientos sistémicos coadyuvantes perturban la evolución natural del cáncer mamario, prolongando el tiempo hasta la recaída, pero no han provocado una disminución global de las tasas de mortalidad20.
Todos conocemos los índices de supervivencia, complicaciones y pautas de la cirugía radical o de nuestra técnica; hay intentos de demostrar con nuevas teorías y series que la cirugía conservadora obtiene los mismos resultados21: pero la realidad demuestra que no se están cumpliendo los objetivos de disminuir la mortalidad. Así pues, creemos que habrá que reconsiderar la técnica de la cirugía conservadora por varias razones de peso:
1. No se ha disminuido la mortalidad, aun a pesar de realizar las intervenciones en estadios favorables (I y II).
2. Si se practica una cuadrantectomía, sumada a los 5.000 + 2.000 rads de refuerzo en la zona quirúrgica con iridio o electrones (no en todos los servicios disponen de estos medios terapéuticos)22 y la mama se reduce a un cuarto menos que la contralateral, con cicatriz, discromía de la radioterapia, riesgo de recidiva local, controles exhaustivos, aumento ostensible de biopsias, ¿qué mama se está conservando? Es una seudomama antiestética y de alto riesgo.
3. Si se practican tumorectomías para no deformar la mama y conseguir un resultado perfecto, la cirugía oncológica brilla por su ausencia, pero los controles exhaustivos y el riesgo de recidivas son más altos que en el caso anterior.
4. Precisamente en los estadios que indican la cirugía conservadora, con cirugía radical y reconstrucción mamaria se obtienen los mejores resultados, sin tener que someter a las pacientes al estrés de los controles, la radioterapia postoperatoria y el riesgo de recidiva, mejorando la calidad de vida, con lo que coinciden Ganz23 y Lizón24.
5. Al no actuar sobre la mama contralateral no se evita el 8% de bilateralidad, que evidenciamos en las 100 primeras pacientes, cuando practicábamos biopsia de los 4 cuadrantes y pexia en la mama contralateral; este 8% de bilateralidad fue el que nos indujo a practicar desde entonces (1984) mastectomía contralateral profiláctica25-27.
El análisis de estos datos permite extraer las siguientes conclusiones:
Si hoy día se están operado más casos en estadios I y II que en épocas anteriores, con el consiguiente buen pronóstico y resultado de supervivencia óptimo, se está haciendo en estos casos cirugía conservadora, acompañada de dosis altas de radioterapia (70 Gray) y quimioterapia coadyuvante que, sin embargo, no han disminuido las tasas de mortalidad con respecto a casuísticas anteriores en que se hacía cirugía radical, con o sin radioterapia, con o sin poliquimioterapia en los mismos estadios clínicos. Para nosotros está claro que si las pautas radiológicas son más altas que antes, la quimioterapia más contrastada y de aplicación a todas las pacientes y, a pesar de esas mejoras técnicas en diagnóstico y tratamiento, la mortalidad por cáncer de mama crece lentamente, según Donado et al28, esto se debe a que la cirugía conservadora, única terapia que se ha modificado, no es lo suficientemente resolutiva para que con los tratamientos coadyuvantes mejore la supervivencia o, como dice Broder, disminuya la mortalidad20.
Hemos objetivado en el seguimiento postoperatorio a los 5 años la ausencia de recidivas locales en los estadios I y II, y una tasa inferior al 4% en estadios III (12 casos), carcinomas agudos (3 casos) y en 4 casos que ya habían sido tratados en otros centros con cirugía conservadora, que acudieron a nuestra consulta con recidiva local, para cirugía radical y reconstrucción.
Al realizar localmente una cirugía más amplia, el porcentaje de las recidivas locales es menor, lo que se suma a la menor tensión de los colgajos cutáneos por la interposición del colgajo miocutáneo de gran dorsal y el aumento de la vascularización que aporta el mismo. El bajo índice de recidiva local lo ha ratificado.
El mayor porcentaje de recidivas locorregionales (80-90%) aparecen en el intervalo de los primeros 2 años. Shimkin29, Devitt30, Spratt31, Kaae32, Millard33, etc., llaman la atención sobre el alto índice de recidivas locales que se comunican en los trabajos sobre cirugía conservadora: Pérez Manga34 publica un estudio sobre 3.156 pacientes de varios autores sometidas a tratamiento conservador y la recidiva local es de un 10,9% global, Rissanen35 comunica un 20% y Mustakallio un 25%36.
En las pacientes con estadios III, carcinomas agudos y cánceres exteriorizados la indicación quirúrgica es de mastectomía radical, dejando a las pacientes mutiladas. Lógicamente, también en estos casos la indicación quirúrgica para nosotros es de mastectomía radical y reconstrucción inmediata, que en nuestra casuística es del 50,6% de las pacientes.
Las pacientes en estadios I y II suponen en nuestro medio el 17,8% de estadios I y el 31,6% de estadios II; si de estos casos excluimos las pacientes en las que no está indicado realizar la cirugía conservadora (en tumores mayores de 3 cm, los de localización retroareolar ni en cuadrantes internos, ni los próximos al surco submamario, en carcinomas intraductales, en tumores multicéntricos, cuando hay microcalcificaciones difusas, mamas muy ptósicas o hipertrofias marcadas, mamas hipoplásicas y tumores de aumento rápido)37, según nuestra casuística en teoría las tributarias de cirugía conservadora se reducirían a un 10% aproximadamente.
Si a este dato añadimos el alto índice de recidiva local hallado de un 8 a un 25%, según las series, practicando cirugía conservadora y la ausencia de la misma en nuestra serie en estadios I y II, con cirugía radical y reconstrucción inmediata, nos inclinamos por nuestra técnica cualquiera que sea el estadio, evitando a la vez la angustia de la paciente y del médico ante la posible recidiva y el aumento de citologías y biopsias.
Desde 1984 somos partidarios de realizar mastectomía subcutánea contralateral profiláctica, debido al 8% de carcinomas metacrónicos encontrados, siendo todos de estadio clínico avanzado25-27,38, aunque sea inferior a la bilateralidad encontrada por Urban (14%)39 y Leis (17%)40. Desde entonces hemos bajado la bilateralidad global al 6,4%, siendo todos ellos carcinomas in situ, sin afectación ganglionar, desapareciendo el carcinoma metacrónico y sin que se evidenciara en las 531 mastectomías contralaterales profilácticas realizadas hasta la actualidad, la presencia clínica ni radiológica de un carcinoma. Por este motivo creemos que hemos mejorado el pronóstico en un 8%.
En los estadios II (tumores mayores de 3 cm), estadios III, carcinomas agudos, etc., evitamos el trauma psicológico de verse mutiladas, con lo que coinciden con nosotros Stevens41 y Noguchi42, con lo que se adaptan psicológicamente mejor a su situación.
Ni la obesidad ni la edad (mayores de 60 años) son contraindicación para la reconstrucción inmediata. En nuestra casuística, la paciente de mayor edad amputada y reconstruida tenía 74 años.
Siempre que hay indicación de amputación la hay de reconstrucción inmediata con colgajo miocutáneo de gran dorsal, como ya demostramos en 1979. En la actualidad son muchos los autores, Corral y Mustoe43, Hughes44, Martínez-Villoria45, etc., que llegan a las mismas conclusiones que publicamos en 1980.
Todas las reconstrucciones inmediatas que hemos realizado han sido efectuadas con colgajo miocutáneo de gran dorsal y en dos pacientes con colgajo miocutáneo de recto anterior del abdomen46,47, con islas cutáneas amplias.
La reconstrucción inmediata con implantación de prótesis no provoca alteraciones del colágeno, coincidiendo con nosotros Schusterman48, como comprobamos en 125 pacientes a las que se les practicó sistemáticamente controles de inmunoglobulinas C-3, C-4, ANA y factor reumatoide.
La reconstrucción inmediata no retrasa ni interfiere el tratamiento radioterápico49, ni quimioterápico, en lo que coinciden Johnson50 y Elliott51.
Algunos autores creen que hay riesgo de trasplantar un carcinoma al injertar el complejo areola-pezón52. Ésta es una complicación que nunca hemos observado y siempre realizamos anatomía patológica peroperatoria de la base del pezón; es más, si es intraductal difuso y/o próximo a la base del pezón, lo desechamos aunque la anatomía patológica sea negativa.
La reconstrucción no aumenta el riesgo de recidiva local, ni regional, no retrasa el diagnóstico, ni su tratamiento, así como tampoco la supervivencia, coincidiendo con nosotros Georgiade53, Johnson50, Slavin54, Frazier55, Feller56, Kroll57, Grotting58 y Martínez-Villoria45.
La reconstrucción inmediata no sólo no aumenta el riesgo de recidiva local ni regional, sino que lo hemos disminuido notablemente por:
1. La resección cutánea es mucho más amplia, ya que cerramos el defecto del tórax, si es grande, sin ninguna dificultad porque siempre podremos hacer el colgajo miocutáneo de gran dorsal mucho mayor.
2. Al aportar el colgajo miocutáneo de gran dorsal aportamos vascularización a la zona donde se va a irradiar, mejorándola desde el punto de vista radiobiológico.
3. La aparición de una recidiva no ha supuesto ningún retraso en el diagnóstico clínico, porque siempre han sido las pacientes las que se lo han descubierto y nosotros lo hemos confirmado clínica y radiológicamente, no retrasando ni interfiriendo su tratamiento.
Si analizamos, finalmente, costes, gastos, controles, etc., tanto a las pacientes como al Ministerio de Sanidad les es mucho más rentable la reconstrucción inmediata que la cirugía conservadora porque: en estadio I y II (tumores menores de 3 cm) con la amputación-reconstrucción se evita la radioterapia postoperatoria, la angustia generada por los controles continuados, biopsias, etc., sin garantizar la aparición de recidivas, cuyo porcentaje en una paciente joven es elevado, y aumenta la posibilidad cada año que transcurre así como la posibilidad de la bilateralidad. La reconstrucción inmediata no aumenta las complicaciones postoperatorias (4%), con lo que coinciden Jarrett59 y Taylor60, disminuyendo considerablemente el número de linforragias al 1,2%. Disminuimos el número de intervenciones y el gasto, también de acuerdo con Elkowitz61, el número de ingresos hospitalarios y, como consecuencia, los períodos de recuperación, lo que conlleva menos bajas laborales.
Nos achacaron en un tiempo que nos preocupaba sobre todo la estética: no era sencilla la defensa, porque nunca lo es cuando se llega al punto de tener que demostrar obviedades. Como, por ejemplo, la de que en todo momento practicábamos, como primer recurso, una cirugía oncológica de base, con reconstrucción. Ahora, el reproche es el de que la intervención quirúrgica es excesiva. ¿Cómo explicar más claramente a quien no desea oír (o leer) que son estos críticos poco objetivos quienes debieran preocuparse seriamente por las consecuencias de lo que hacen, al dejar una mama operada con riesgo de recidiva locorregional y posibilidad de metástasis, más el adicional de la mama contralateral que en un 8% de los casos se traduce en carcinoma bilateral?
Cierto que hay casuísticas para todos los gustos, susceptibles de ser utilizadas en apoyo de cualquier tipo de intervención quirúrgica (más o menos agresiva), pero supeditar la supervivencia de la paciente a la conservación de un órgano como es la mama, que hoy día tras las operaciones de reconstrucción inmediata o secundaria, sin riesgo recidiva, obtiene óptimos resultados, nos parece una postura en la que la paciente resulta sometida de forma innecesaria a un serio riesgo, tal vez por la plena convicción en que el facultativo está actuando correctamente, tal vez para enmascarar su falta de familiaridad con la técnica de la cirugía radical, o de cirugía radical con reconstrucción inmediata. Son profesionales que no explican a sus pacientes, sea por la causa que fuere, las posibles complicaciones y riesgos de la cirugía conservadora ni las ventajas de la cirugía radical con reconstrucción.
Creemos firmemente que el tratamiento quirúrgico del cáncer de mama debe ser mutilante y reconstructor en el mismo acto, por lo que nuestra técnica de amputación-reconstrucción inmediata y mastectomía subcutánea contralateral profiláctica y prótesis, que cumple ambos objetivos, es la técnica de elección en el tratamiento quirúrgico del cáncer de mama1,2.
Conclusiones
1. La técnica descrita de la reconstrucción de la mama, la poscirugía radical en un solo tiempo, es perfectamente realizable, bien tolerada y no prolonga el postoperatorio.
2. La intervención que describimos no crea problemas técnicos, permitiendo realizar normalmente el tratamiento radioterápico, quimioterápico y hormonoterápico postoperatorio.
3. La intervención quirúrgica descrita mejora la vascularización y, por tanto, la oxigenación de los tejidos de la zona que posteriormente se va a irradiar. Este hecho tiene una gran importancia radiobiológica cuando se utilizan radiaciones de baja energía lineal transferida (fotones y electrones), como sucede habitualmente en nuestro medio.
4. La prótesis utilizada no sufre alteraciones ni se polimeriza con dosis de radiaciones muy superiores a las habituales de radioterapia clínica.
5. No se han detectado, desde el punto de vista físico, efectos de incremento positivo ni negativo en la interfase prótesis-tejido.
6. No hemos objetivado ninguna alteración de las inmunoglobulinas (C-3, C-4, ANA ni del factor reumatoide), en 125 pacientes estudiadas, y ninguna enfermedad del colágeno en las pacientes de nuestra casuística (640 pacientes).
7. Desde el punto de vista estético, morfológico y subjetivo ha sido beneficioso en todos los casos.
8. Pese a la mejoría observada en los últimos 250 casos, consideramos que el diagnóstico del cáncer de mama sigue siendo tardío (estadio I, 26%; estadio II, 36%; estadio III, 38%) en contraposición con los 100 primeros casos, cuya estadificación fue estadio I, 4%; estadio II, 22%; estadio III, 74%; y con el global de los 500 casos: estadio I, 17,8%; estadio II, 31,6% y estadio III, 50,6%.
9. El 12% de multicentricidad nos reafirma en nuestro criterio de mastectomía radical modificada (tipo Patey).
10. La baja incidencia de recidivas locorregionales (< 4%) y ninguna en estadios I y II nos reafirma en nuestro criterio de amputación-reconstrucción inmediata.
11. El 6,4% de bilateralidad nos reafirma en nuestro criterio de mastectomía subcutánea profiláctica de la mama contrala teral.
12. Siempre que hay indicación de amputación la hay de reconstrucción inmediata y mastectomía subcutánea contralateral profiláctica con inclusión de prótesis, salvo contraindicación de orden general o negativa expresa de la paciente.