La gastrectomía vertical laparoscópica es una intervención quirúrgica para el tratamiento de la obesidad mórbida. Existen controversias respecto a su eficiencia en términos de reducción de peso e incidencia de complicaciones. En este estudio prospectivo, presentamos la experiencia en un centro de referencia en el tratamiento de la obesidad mórbida con gastrectomía vertical laparoscópica.
Material y métodosEstudio prospectivo con 73 pacientes tratados mediante gastrectomía vertical laparoscópica, desde febrero de 2009 hasta septiembre de 2013. Los pacientes fueron seguidos durante un periodo de 12 meses. Se evaluaron: el desarrollo de complicaciones, la reducción del volumen gástrico, y la pérdida ponderal asociada a la intervención; así como su impacto en la mejora de las comorbilidades presentes al inicio del estudio.
ResultadosSe observó una significativa reducción entre el índice de masa corporal (IMC) preoperatorio y el IMC a los 12 meses tras la gastrectomía vertical laparoscópica (± DE p<0.001); ello pese a que los pacientes experimentaron un incremento en el volumen de la cavidad gástrica, medido al mes y a los 12 meses tras la intervención (± DE p <0.001). Cinco pacientes (6.85%) presentaron complicaciones, ninguna de ellas graves. No hubo muertes en la totalidad de la serie.
ConclusionesLa gastrectomía vertical laparoscópica es una técnica segura y eficaz para el tratamiento de la obesidad mórbida, su uso se asocia a una importante reducción en la presencia de comorbilidades asociadas a la obesidad. Son necesarios estudios multicéntricos, con un mayor periodo de seguimiento, que confirmen la eficacia y seguridad de esta técnica quirúrgica.
Laparoscopic sleeve gastrectomy is a surgical procedure for the treatment of morbid obesity. However, there are still controversies regarding its efficiency in terms of weight reduction and incidence of complications. In this prospective study, the experience is presented of a referral centre for the treatment of morbid obesity with laparoscopic sleeve gastrectomy.
Material and methodsA prospective study on 73 patients subjected to laparoscopic sleeve gastrectomy from February 2009 to September 2013. Patients were followed-up for a period of 12 months, evaluating the development of complications, reduction of gastric volume, and the weight loss associated with the surgery, as well as their impact on the improvement of comorbidities present at beginning of the study.
ResultsThere was a statistically a significantly reduction between the preoperative body mass index (BMI) and the BMI at 12 months after laparoscopic sleeve gastrectomy (p < 0.001), despite there being an increase in the gastric volume during follow-up, measured at one month and 12 months after surgery (p < 0.001). Five patients (6.85%) had complications, with none of them serious and with no deaths in the whole series.
ConclusionsLaparoscopic sleeve gastrectomy is a safe and effective technique for the treatment of morbid obesity. Its use is associated with a significant reduction in the presence of comorbidities associated with obesity. Multicentre studies with a longer period of monitoring are required to confirm the efficacy and safety of this surgical technique.
La gastrectomía vertical laparoscópica es una herramienta quirúrgica cuyo uso se ha incrementado a nivel mundial como tratamiento de la obesidad mórbida. Se trata de una técnica restrictiva cuya eficacia, al parecer, no solo es como consecuencia de la reducción del volumen gástrico que conlleva una saciedad precoz, sino que también podrían existir mecanismos neurohumorales, al observarse una disminución en los niveles de ghrelina, la hormona estimulante del apetito1,2.
Esta técnica aparece como la parte restrictiva complementaria a otros procedimientos, conocidos como técnicas mixtas, nos referimos al cruce duodenal, en el que, además, se realiza una derivación biliopancreática. Hess y Hess realizaron el primer cruce duodenal en 19883. Almogy et al.4 desde 1993 realizaban la gastrectomía tubular por vía abierta con el fin de disminuir el riesgo a los pacientes superobesos (más de 55 de IMC), mayores de 55 años y hombres. En 1999, Gagner y Patterson5 llevaron a cabo la primera gastrectomía vertical laparoscópica en el Hospital Mount Sinai de Nueva York, como parte de un cruce duodenal; unos años después, Regan et al.6 proponen la gastrectomía vertical laparoscópica como un primer paso del bypass gástrico, como una alternativa de tratamiento en pacientes obesos de alto riesgo, en los que se pretende disminuir así la morbimortalidad.
Desde entonces, muchos equipos quirúrgicos han adoptado esta técnica, con buenos resultados, aunque sus indicaciones permanecen inciertas. Algunas instituciones defienden la gastrectomía vertical laparoscópica como un primer paso en pacientes de alto riesgo y en pacientes con alto índice de masa corporal (IMC), con la idea de realizar una segunda intervención definitiva tras una pérdida de peso aceptable que disminuya el riesgo quirúrgico. Otros equipos, en cambio, la consideran una alternativa a la banda gástrica ajustable, al bypass gástrico o a la derivación biliopancreática con cruce duodenal7,8.
El hecho de que esta técnica se haya considerado erróneamente como sencilla y fácilmente reproducible ha llevado a un gran número de cirujanos a practicarla. Podría parecer que, en comparación con el bypass gástrico y las derivaciones biliopancreáticas, es una cirugía más asumible desde el punto de vista laparoscópico, pero debemos saber que sus complicaciones, como la aparición de fístulas gástricas, pueden ser muy serias y la mayoría de los autores coinciden en que es necesaria una larga curva de aprendizaje9–12. Se trata de complicaciones que, aunque aparecen en un bajo porcentaje, aumentan la morbilidad, la estancia hospitalaria y ponen en peligro la vida del paciente.
En vista de lo anterior, evaluamos prospectivamente una serie de pacientes intervenidos mediante gastrectomía vertical laparoscópica, como tratamiento de la obesidad mórbida en nuestro centro.
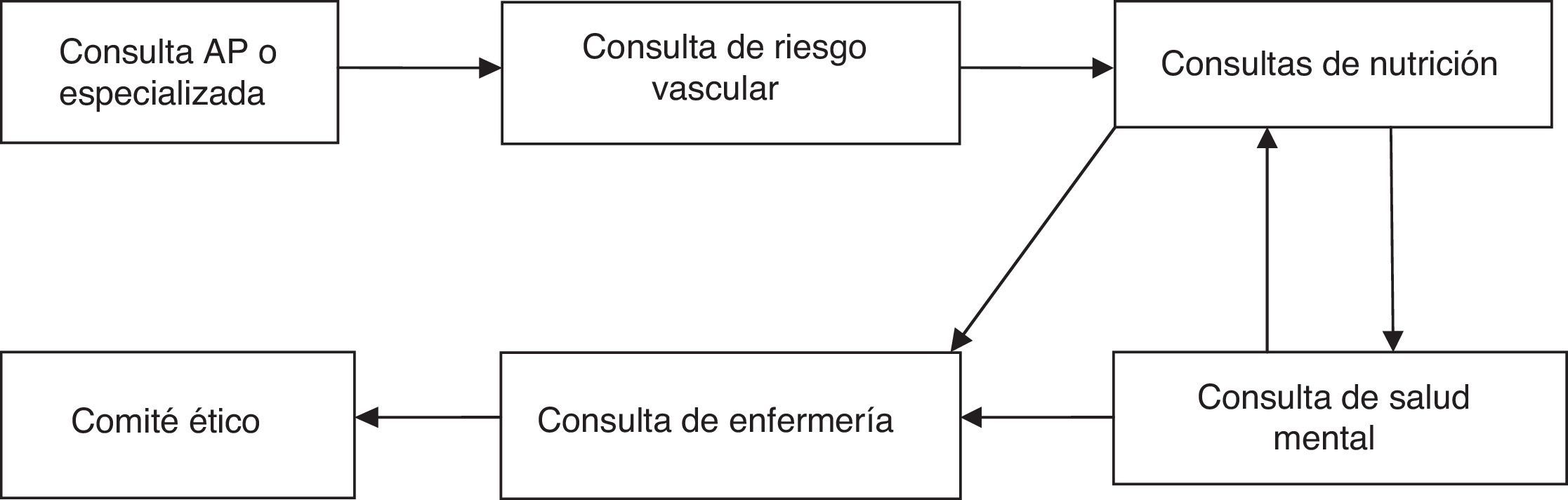
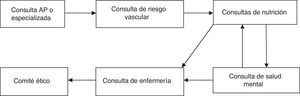
Material y métodosSe trata de un estudio prospectivo observacional en el que se incluyó a pacientes intervenidos de forma consecutiva entre el 2 de febrero de 2009 y el 26 de septiembre de 2013. Todos los pacientes fueron intervenidos por el equipo de cirugía bariátrica del Complejo Hospitalario Torrecárdenas de Almería (España), compuesto por 3 cirujanos y un equipo multidisciplinar formado por endocrinólogos, nutricionistas y psicólogos. Los pacientes candidatos a cirugía son aquellos con IMC ≥ 40 kg/m2, o IMC ≥ 35 kg/m2 y, además, al menos una de las siguientes comorbilidades: diabetes mellitus, hipertensión arterial, dislipidemia, osteoartritis severa, síndrome de apnea obstructiva del sueño y síndrome de hipoventilación-obesidad. Además del IMC los pacientes candidatos a cirugía debían cumplir con los siguientes criterios: a) edad comprendida entre los 18 y 60 años; b) obesidad mantenida durante más de 5 años; c) fracaso de otros tratamientos, d) aceptable riesgo quirúrgico; e) seguridad en la cooperación del paciente durante el seguimiento, y f) firma del consentimiento informado. Los pacientes que cumplen estos criterios son valorados por un equipo multidisciplinar como se muestra en la (fig. 1). Una vez indicada la cirugía, son valorados por el comité bariátrico donde se les asigna un baremo para ingresar a la lista de espera quirúrgica. Los pacientes son ingresados el día previo a la cirugía para realizarles una evaluación completa de los parámetros físicos, psíquicos y de laboratorio, que son consignados como datos preoperatorios.
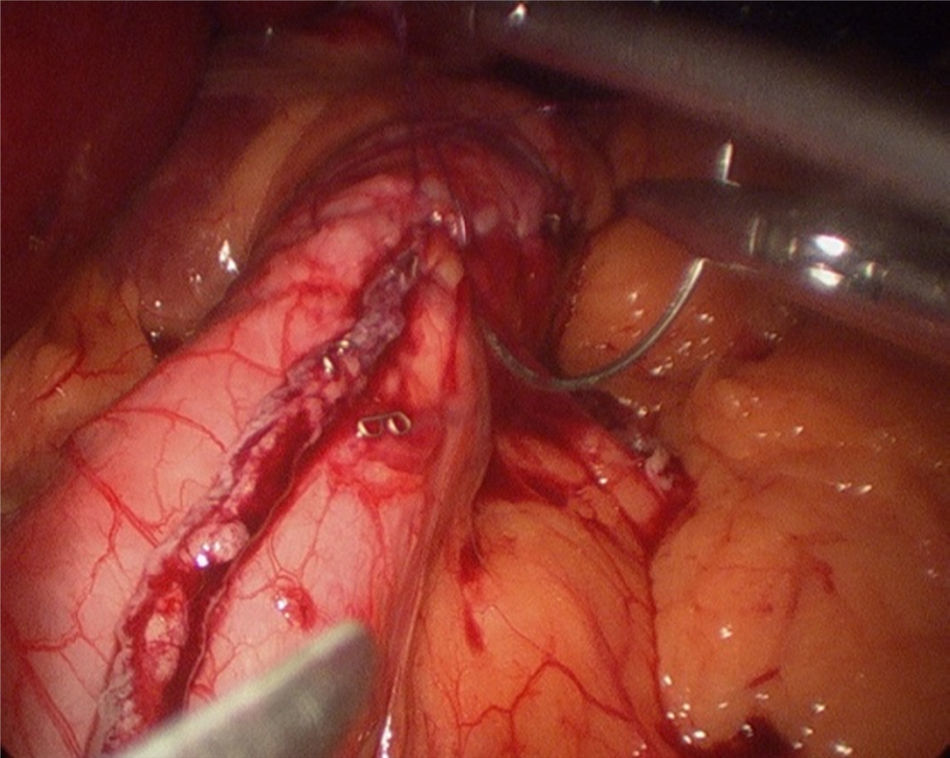
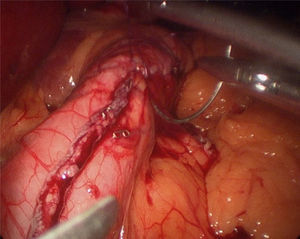
Comienza la intervención con la entrada del trocar óptico supraumbilical y se colocan 4 trocares accesorios (12 mm). Se realiza la disección de la curvatura mayor gástrica mediante Ligasure, comenzando a unos 4 cm del píloro, hasta el ángulo de Hiss. Se liberan las adherencias existentes de la cara posterior gástrica. Se introduce sonda de Faucher de 34 F previamente a la realización de la sección gástrica. Se realiza la sección mediante endocortadora y, posteriormente, se refuerza con sutura invaginante con monofilamento 2-0 reabsorbible (fig. 2). Se realiza test de estanqueidad con azul de metileno y se extrae la pieza quirúrgica, dejándose un drenaje aspirativo. En la cirugía no se utiliza sonda nasogástrica ni vesical. Durante el postoperatorio se moviliza al paciente la misma noche y al día siguiente. A las 48 h se realiza test con azul de metileno y, si es negativo, se comienza la tolerancia a líquidos. El paciente es dado de alta de cirugía del hospital a las 72 h de la intervención si no hay incidencias.
SeguimientoTodos los pacientes mantienen una dieta semilíquida durante las 4 semanas siguientes a la intervención quirúrgica y luego son valorados en consultas externas durante los meses 1, 3, 6 y 12 tras la intervención; además todos los pacientes mantuvieron un seguimiento cercano por parte de Nutrición.
Las comorbilidades mencionadas en los criterios de inclusión preoperatorios fueron evaluadas a los 12 meses de la intervención y se definieron como presente o en remisión según: remisión de diabetes mellitus como suspensión de la medicación antidiabética por parte del endocrinólogo, HBA1c ≤ 6.5% y glucemia por debajo de 126 mg/dl; remisión de hipertensión arterial como tensión arterial ≤ 140/90 mmHg con retiro de la medicación antihipertensiva; la remisión de hiperlipidemia fue considerada para un nivel de colesterol LDL por debajo de 160 mg/dl, y triglicéridos < 200 mg/dl; la remisión de osteoartritis severa se consideró como respuesta a la eliminación de la medicación para controlar el dolor y a la ausencia de la sintomatología asociada; la remisión del síndrome de apnea obstructiva del sueño es la interrupción del uso de la mascarilla de presión continua positiva de la vía aérea, y la remisión del síndrome
de hipoventilación-obesidad como la ausencia de hipersomnia diurna y de los síntomas cardiorrespiratorios. La remisión de los 2 últimos trastornos fue confirmada mediante polisomnografía.
Al mes y a los 12 meses de la intervención se realizó un estudio de tránsito esofagogastroduodenal con bario, en todos los pacientes, exceptuando los pacientes que presentaron fístulas, en quienes se empleó gastrografin para valorar las medidas y características del cilindro gástrico. En este caso, el volumen general del cilindro gástrico (V) equivale a V=πr2h (en cm3), donde h=altura y r=el radio en cm.
Análisis estadísticoLas variables continuas son expresadas como medias±desviaciones estándar o rango. Las comparaciones entre 2 variables continuas se realizaron mediante t de Student o test de Wilcoxon para variables normalizadas o no normalizadas, respectivamente. Del mismo modo, la comparación entre más de 2 variables continuas se realizó mediante test de Anova o Kruskal-Wallis, según si tuvieron una distribución normal o no. La comparación entre variables ordinales preoperatorias y después de la intervención se evaluó mediante el test de McNemar o prueba de χ2 y test exacto de Fisher en los casos que lo requerían. Los análisis fueron realizados mediante SPSS versión 22.0 para Windows.
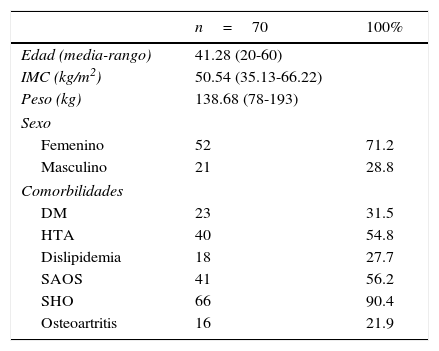
ResultadosEntre febrero de 2009 y agosto de 2013 se ha intervenido a un total de 73 pacientes. Las características preoperatorias de estos pacientes son presentadas en la (tabla 1).
Características de los pacientes (datos preoperatorios)
| n=70 | 100% | |
|---|---|---|
| Edad (media-rango) | 41.28 (20-60) | |
| IMC (kg/m2) | 50.54 (35.13-66.22) | |
| Peso (kg) | 138.68 (78-193) | |
| Sexo | ||
| Femenino | 52 | 71.2 |
| Masculino | 21 | 28.8 |
| Comorbilidades | ||
| DM | 23 | 31.5 |
| HTA | 40 | 54.8 |
| Dislipidemia | 18 | 27.7 |
| SAOS | 41 | 56.2 |
| SHO | 66 | 90.4 |
| Osteoartritis | 16 | 21.9 |
DM: diabetes mellitus; HTA: hipertensión arterial; SAOS: síndrome de apnea obstructiva del sueño; SHO: síndrome de hipoventilación-obesidad.
La mayoría fueron mujeres con una de edad de 41.28 (20-60) años (media [rango]), un peso medio de 138.68 (78-193) kg y un IMC medio de 50.54 (35.13-66.22) kg/m2. Como comorbilidades, la mayoría presentaban trastornos del sueño (90.4% síndrome de hipoventilación-obesidad y 56.2% apnea obstructiva del sueño), el 54.8% eran hipertensos, el 31.5% eran diabéticos tipo 2, el 24.7% tenían dislipidemia y el 21.9%, osteoartritis. Ninguno de los pacientes había sido intervenido previamente mediante cirugía bariátrica.
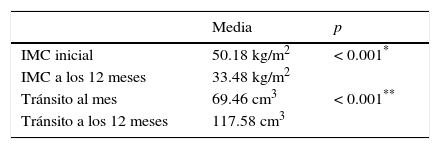
Todos los pacientes experimentaron una reducción del IMC medio significativa tras la gastrectomía vertical laparoscópica a los 12 meses, comparada con la medición preoperatoria (33.5±6.2 kg/m2 y 50.2±6.9 kg/m2 respectivamente; p < 0.001) (tabla 2).
Por otro lado, la reducción en el IMC tras la intervención quirúrgica no se vio afectada por la curva de aprendizaje, ya que al dividir la serie en 3 grupos según el momento de la intervención, los primeros 25 pacientes operados durante el primer año desde el inicio de la técnica experimentaron una reducción en el IMC similar a los siguientes 25 operados durante el segundo año y también similar a los últimos 23 pacientes de la serie intervenidos durante el tercer y cuarto años (15.9±5.5; 16.8±6.5 y 17.5±5.8 respectivamente; p=0.7). El porcentaje de sobrepeso perdido ha sido del 61.19%, y el porcentaje de exceso de IMC perdido del 67.92%; y tampoco se vieron afectadas por la curva de aprendizaje. El efecto en la reducción de peso asociado a la gastrectomía vertical laparoscópica se mantuvo durante el seguimiento, pese a que los pacientes experimentaron un aumento significativo en el volumen de la cavidad gástrica, determinado mediante estudio gastroduodenal, en el que se observa un incremento desde 69.46 (18.8-196.3) cm3 al mes de la cirugía, hasta los 117.58 (25.13-274.88) cm3 a los 12 meses (p<0.001) (tabla 2).
La remisión de la diabetes mellitus ocurrió en el 83% de los casos preexistentes, la hipertensión en un 70%, la osteoartritis y la dislipidemia en un 86 y 94%, respectivamente, mientras que el síndrome de apnea obstructiva del sueño y del síndrome de hipoventilación-obesidad remitió en la totalidad de los pacientes. Estas diferencias entre los datos preoperatorios y a los 12 meses resultaron significativas (tabla 3).
Comparación de las enfermedades asociadas a la obesidad tras 12 meses de intervención
| Preintervención | Postintervención | ||||||
|---|---|---|---|---|---|---|---|
| Comorbilidades | Presentan enfermedad tras intervención | No presentan enfermedad tras intervención | |||||
| n | % | n | % | n | % | p | |
| DM | 23 | 31.5 | 4 | 5.5 | 69 | 94.5 | < 0.001 |
| HTA | 40 | 54.8 | 12 | 16.4 | 61 | 83.6 | < 0.001 |
| Dislipidemia | 18 | 27.7 | 1 | 1.4 | 72 | 98.6 | < 0.001 |
| SAOS | 41 | 56.2 | 0 | 0 | 73 | 100 | |
| SHO | 66 | 90.4 | 0 | 0 | 73 | 100 | |
| Osteoartritis | 16 | 21.9 | 2 | 2.7 | 71 | 97.3 | < 0.001 |
DM: diabetes mellitus; HTA: hipertensión arterial; SAOS: síndrome de apnea obstructiva del sueño; SHO: síndrome de hipoventilación-obesidad.
Valor de p obtenido por el test de McNemar y test de Fisher.
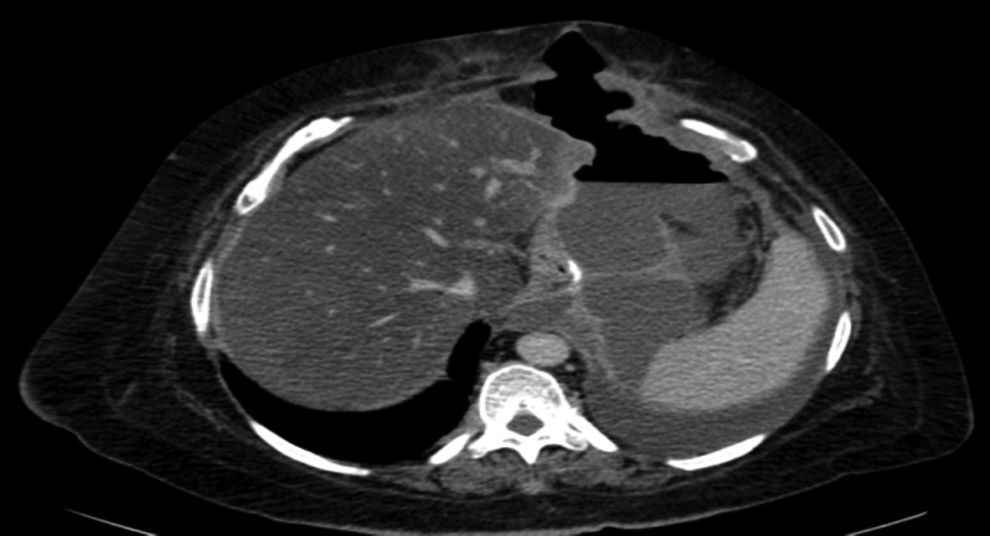
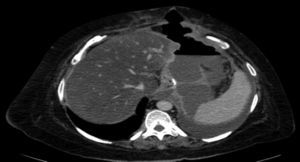
Como complicaciones hemos presentado 3 fístulas en el postoperatorio (4.1%), una estenosis completa (1.4%) y un sangrado postoperatorio (1.4%) sin signos de repercusión hemodinámica. Las 3 fístulas se diagnosticaron durante el seguimiento ambulatorio por el cuadro clínico y prueba de imagen (tomografía computada) (fig. 3). Todas fueron resueltas satisfactoriamente, una con tratamiento conservador y colocación de endoprótesis y las otras 2 con tratamiento quirúrgico tras intentos fallidos de colocación de endoprótesis; en una se realizó un cierre simple laparoscópico y la otra se reconvirtió a bypass gástrico. La estenosis requirió conversión de la cirugía a bypass gástrico. El sangrado se solventó mediante revisión quirúrgica y hemostasia de vaso corto. Todas las complicaciones se presentaron durante las primeras 25 intervenciones de la curva de aprendizaje. Los 73 pacientes completaron los 12 meses de seguimiento y ningún paciente falleció durante todo este periodo.
DiscusiónDurante los últimos años la cirugía laparoscópica ha supuesto un avance quirúrgico hasta el punto que hoy difícilmente se concibe esta cirugía si no se realiza mediante técnicas mínimamente invasivas. La primera gastrectomía vertical laparoscópica fue realizada por Gagner y Patterson5 como parte de un cruce duodenal; sin embargo, en los últimos años esta cirugía se ha consolidado como un procedimiento único para el tratamiento de la obesidad mórbida, debido a sus buenos resultados y a la baja incidencia de complicaciones en comparación con otras técnicas quirúrgicas7,8.
La formación de los cirujanos bariátricos requiere un entrenamiento importante en cirugía laparoscópica avanzada9. A pesar de que la gastrectomía vertical laparoscópica es considerada por algunos autores como una técnica sencilla, debemos tener en cuenta que sus complicaciones pueden comprometer la vida del paciente, y generalmente son más difíciles de solucionar que aquellas complicaciones que aparecen tras la realización de técnicas mixtas. Hay autores que consideran que existe una curva de aprendizaje larga (superior a los 100 casos) durante la cual la morbilidad intra- y postoperatoria es más elevada10–12. Por las condiciones inherentes del paciente y la dificultad de la técnica quirúrgica, hay 2 campos de aprendizaje atribuibles a la cirugía laparoscópica: en primer lugar, es necesario tener experiencia en el tratamiento de pacientes obesos, y en segundo lugar, es imprescindible tener experiencia en técnicas avanzadas de cirugía laparoscópica reconstructiva13.
Una de las complicaciones más temidas por los cirujanos bariátricos tras la realización de la gastrectomía vertical laparoscópica es la aparición de una fístula en el tercio proximal, tanto por la morbilidad que conlleva como por la dificultad de su resolución. La incidencia de la fístula tras dicha cirugía varía entre el 0 y el 7%14–16. Baker et al.17 defienden que las causas de las fístulas en la línea de grapas son muchas, pero estas pueden incluirse en 2 categorías: causas mecánico-tisulares y causas isquémicas. En ambas, la presión intraluminal excede la resistencia del tejido y la línea de sutura, dando lugar a la fístula. Las fístulas isquémicas clásicas suelen aparecer entre el 5.° y el 6.° día del postoperatorio, cuando el proceso de cicatrización de la pared se encuentra entre la fase de inflamación y fibrosis. Cuando la causa es mecánico-tisular, suelen descubrirse antes, en los primeros 2 días tras la cirugía. Esto apoya el uso de materiales de refuerzo que, aunque no actúen sobre la causa isquémica de las fístulas, teóricamente podrían disminuir el riesgo de fallo mecánico18. Baltasar et al.19, al igual que nuestro grupo, protegen la línea de sección con una sutura continua sero-serosa que invierte las grapas, controla la hemorragia e intenta disminuir el número de fugas, sin aumentar el costo de la intervención (fig. 2). Recientemente, describen su técnica utilizando un parche de epiplón junto a la invaginación con la idea de disminuir el número de fugas y mejorar la estabilidad y vaciado al disminuir la torsión parcial que sufren algunos tubos residuales20.
Las 3 fístulas que presentaron los pacientes de nuestro estudio fueron, en todos los casos, tras el alta hospitalaria (pasadas 72 h) por lo que podría descartarse el fallo mecánico como causa. La clínica presentada en los 3 casos fue de fiebre y disnea, y en ningún caso presentaron dolor abdominal. Por tanto, debemos tener en cuenta que, aquellos pacientes que acuden tras el alta por fiebre o disnea en el postoperatorio de una gastrectomía vertical laparoscópica, pueden presentar una fístula y se debería realizar tomografía computada abdominal urgente. Con la aparición de las nuevas máquinas endocortadoras «tri staple», el porcentaje de fístulas parece haber disminuido; de hecho, desde su uso en nuestro grupo (últimos 48 pacientes) no se ha vuelto a presentar.
A lo largo de nuestra serie, el índice total de complicaciones fue de 6.85%, inferior al 17% reportado en otras series21, sin embargo, fue similar al de una larga cohorte española multicéntrica que incluyó a 540 pacientes y al aceptado en un documento de consenso de la sociedad americana de cirugía bariátrica7,22. Estas complicaciones aparecieron durante las 25 primeras intervenciones de la curva de aprendizaje, todas en mujeres, y solo una de las fístulas y el sangrado postoperatorio se presentaron en pacientes superobesos.
Deitel y Greeinstein23 proponen el uso del porcentaje de exceso de IMC perdido para valorar los resultados, de manera que se considera un resultado excelente si supera el 65%; bueno, si se encuentra entre el 50 y el 65%, y fracaso cuando es menor de 50%. En nuestra serie, la media de porcentaje de exceso de IMC perdido es de 67.92%, acorde con los datos que ofrece la literatura7,24,25. Por otro lado, es importante señalar que la reducción en el IMC, en el porcentaje de exceso de IMC perdido y en el porcentaje de sobrepeso perdido no fueron dependientes del tiempo en la curva de aprendizaje de nuestra serie.
Existen todavía muchos puntos controvertidos en la gastrectomía vertical laparoscópica que la convierten en un abanico de posibilidades sin consensuar26, como a) el tamaño de la bujía utilizada como calibrador, b) la distancia desde el píloro hasta la primera línea de sección, c) el refuerzo de la línea de grapado, y d) el uso rutinario de test intraoperatorios de estanqueidad, todas ellas cuestiones que se debaten constantemente por parte de los autores de otras series y que deben ser evaluadas en estudios prospectivos aleatorizados.
La comorbilidad estaba presente en un porcentaje importante de pacientes de la serie. La diabetes mellitus, la hipertensión arterial, la dislipidemia, el síndrome de apnea obstructiva del sueño, el síndrome de hipoventilación-obesidad y la osteoartritis muestran remisiones de al menos un 70% y en el caso del síndrome de apnea obstructiva del sueño y del síndrome de hipoventilación-obesidad desaparecieron en su totalidad. Esto demuestra que la gastrectomía vertical laparoscópica es una técnica que no solo influye en la pérdida de peso sino también en la mejora de las complicaciones27–29. Los mecanismos responsables de esta asociación están fuera del alcance del presente estudio.
En lo que se refiere a los volúmenes medios de los tránsitos realizados tras el primer mes y los 12 meses de la intervención, 69.46 y 117.58 cm3 respectivamente, se observan diferencias estadísticamente significativas, tanto a nivel general de los pacientes como por sexos. En el artículo de Vidal et al.30 se exponen medias de volúmenes tanto al mes como a los 12 meses, similares a las presentadas en nuestro estudio. Es cierto que, a pesar de aumentar el volumen de la manga gástrica, los pacientes han seguido manteniendo la pérdida de peso en su revisión al año. Sería conveniente realizar un seguimiento a largo plazo para valorar tanto la pérdida de peso de los pacientes como el aumento proporcional del volumen gástrico, y confirmar si sigue manteniéndose esta ecuación o si, por el contrario, estas cifras se frenarían o, incluso, podrían facilitar una nueva ganancia de peso.
Como conclusión, la gastrectomía vertical laparoscópica es una técnica eficaz y segura para el tratamiento de la obesidad mórbida en centros de referencia con experiencia en cirugía bariátrica. Se asocia también a una significativa remisión en las comorbilidades asociadas a la obesidad mórbida, aunque el mecanismo fisiopatológico no es del todo comprendido.
El hecho de que se haya considerado erróneamente una técnica sencilla ha llevado a un gran número de cirujanos a practicarla; sin embargo, no está exenta de complicaciones que se presentan en un bajo porcentaje y son dependientes de la curva de aprendizaje.
Si estos hallazgos se confirman en series más largas de pacientes, la gastrectomía vertical laparoscópica sería el tratamiento de elección para la obesidad mórbida y debería practicarse preferentemente en centros de referencia.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.