Durante los últimos años el número de pacientes de avanzada edad que presentan insuficiencia cardíaca congestiva se ha incrementado de manera dramática. En el contexto del estancamiento global del trasplante cardíaco nace la necesidad de una terapia definitiva alternativa para estos pacientes. Recientemente, los dispositivos de asistencia ventricular izquierda (DAVI) han experimentado un auge, sobrepasando incluso el número de pacientes trasplantados mundialmente. El desarrollo tecnológico de los nuevos dispositivos y el surgimiento de nuevas técnicas quirúrgicas derivados de la cirugía cardíaca mínimamente invasiva han formado parte de este desarrollo. El propósito del presente estudio fue revisar la primera serie de implantes de DAVI mínimamente invasivo en pacientes septuagenarios.
MétodosEl diseño del ensayo clínico es monocéntrico prospectivo. Se incluyó a todos los pacientes mayores o iguales a 70 años que requirieron un implante de DAVI (HVAD, HeartWare Inc.) como terapia de destino durante los años 2013 y 2015 en la Medizinische Hochschule Hannover. El seguimiento concluyó luego de 2 años. Todos los pacientes fueron operados por una técnica mínimamente invasiva compuesta por una miniesternotomía en «J» y una toracotomía lateral izquierda.
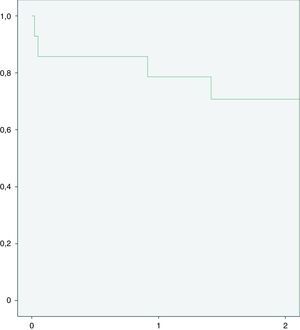
ResultadosUn total de 14 pacientes fueron incluidos (edad 71,8±1,5 años, 100% hombres, miocardiopatía isquémica 64,3%). El 50% de los casos correspondía a una reoperación, un 7,1% recibió soporte mecánico circulatorio previo. Todos los pacientes fueron operados utilizando circulación extracorpórea (CEC) (tiempo medio de CEC 51±8min). El tiempo promedio de permanencia en la Unidad de Cuidados Intensivos fue de 6,4±5,2 días. Eventos adversos en el transcurso postoperatorio temprano fueron: reintervención quirúrgica por sangrado 7,1%, falla ventricular derecha 14,3% y diálisis 14,3%. Los niveles de supervivencia fueron: 30 días: 85,7%, un año: 78,6%, y 2 años: 70,7%.
ConclusionesNuestros resultados iniciales demuestran que el implante mínimamente invasivo de DAVI puede ser realizado de manera eficaz, segura y con buenos resultados en pacientes septuagenarios terapia de destino. Los bajos niveles de eventos adversos durante el seguimiento por 2 años demuestran que la terapia de destino puede ser realizada incluso en pacientes septuagenarios.
The number of elderly patients suffering from congestive heart failure has increased dramatically in recent years. In the context of global stagnation of heart transplantation, comes the need for an alternative definitive therapy for these patients. Recently left ventricular assist devices (LVAD) have increased significantly, surpassing even the number of transplants worldwide. The technological development of new devices and the emergence of new surgical techniques arising from minimally invasive cardiac surgery have been part of this development. The purpose of this study was to review the first series of minimally invasive LVAD implants in septuagenarian patients.
MethodsA prospective single-centre clinical trial was conducted on all patients greater than or equal to 70 years that required an LVAD implant (HVAD, HeartWare Inc.) as destination therapy for the years 2013 to 2015 in the Medizinische Hochschule Clinic in Hannover. The monitoring ended after two years. All patients were operated by a minimally invasive technique consisting of a “J” mini-sternotomy and a left lateral thoracotomy.
ResultsA total of 14 patients were included (age 71.8 ± 1.5 years, all (100%) males, and 64.3% with ischaemic heart disease). It was a second operation for 50% of the cases, and 7.1% received a prior mechanical circulatory assist device (MCAD). All patients were operated on using extracorporeal circulation (ECC) for a mean time of 51 ± 8 min). The mean length of stay in ICU was 6.4 ± 5.2 days. Adverse events during the early post-operative period included, surgical re-intervention due to bleeding (7.1%), right ventricular failure (14.3%), and dialysis (14.3%). Survival rates were: 30 days: 85.7% 1 year: 78.6% 2 years: 70.7%.
ConclusionsThe initial results show that minimally invasive implantation of LVAD can be performed effectively, safely, and with good results in septuagenarian patients as destination therapy. There were low levels of adverse events during a two year follow-up, showing that destination therapy can be performed even in patients in their seventies.
Las enfermedades cardiovasculares exhiben un aumento progresivo en el mundo y las proyecciones estiman que hasta el año 2020 el número de pacientes muertos por este grupo de enfermedades ascenderá a más de 7 millones en todo el mundo1. La insuficiencia cardíaca es la fase final de muchas enfermedades cardiovasculares, entre las que destaca la cardiopatía isquémica2. En España, un estudio prospectivo realizado en Cádiz demostró que entre el año 2000 y el 2007, la incidencia de insuficiencia cardíaca aumentó en esa comunidad en un 30%, alcanzando 390 por 100.000 años/persona3. Paradójicamente, parte de este fenómeno se explica por la mejora en el tratamiento médico de las enfermedades cardiovasculares en sí, mientras que antiguamente muchos pacientes fallecían debido a un infarto agudo de miocardio, hoy en día el nivel de sobrevida es mayor que antes, a cuestas de un creciente número el número de pacientes que desarrollan una insuficiencia cardíaca crónica progresiva. Estudios recientes demuestran que la mortalidad de la insuficiencia cardíaca avanzada es incluso superior a la de otras enfermedades catastróficas como el virus de la inmunodeficiencia humana o distintos tipos de leucemia y se compara con la mortalidad del cáncer pulmonar o el cáncer pancreático4. Históricamente, la terapia patrón oro para la insuficiencia cardíaca terminal ha sido el trasplante cardíaco. Tradicionalmente, España ha sido uno de los países europeos más exitosos en la aplicación de esta terapia, reuniendo entre otros factores, una muy buena infraestructura médica con una tasa elevada de donantes por millón de habitantes. Sin embargo, esto ha cambiado: no solo ha bajado el promedio de trasplantes realizados durante los últimos 10 años, sino también ha cambiado el perfil de los receptores. Hoy en día la fracción de pacientes de alta urgencia ha aumentado hasta un 40% del total, incluyendo un creciente número (1 de cada 5) de pacientes con soporte mecánico circulatorio previo al trasplante5. Por el lado de los donantes, se suma una fracción cada vez mayor de donantes subóptimos. Hay que rescatar que a pesar de estos factores negativos, el trasplante cardíaco en España sigue manteniendo excelentes resultados. Sin embargo, desde un punto de vista global, nos estamos enfrentando a un escenario que claramente desfavorece al trasplante cardíaco. Mientras que el número de pacientes en lista de espera aumenta cada año, los números de trasplantes anuales se mantienen estables, produciendo un vacío entre la constante oferta y creciente demanda de órganos. Para estos pacientes, el surgimiento de los dispositivos de asistencia ventricular izquierda (DAVI) (left ventricular assist device [LVAD]) como soporte mecánico circulatorio representa una excelente alternativa para franquear y prolongar el tiempo entre implante y trasplante6-8. De hecho, según el registro actual de la International Society of Heart and Lung Transplantation (ISHLT), aproximadamente el 40% de los pacientes trasplantados fueron tratados previamente con DAVI, con tendencia creciente. Aunque esta estrategia posibilitará una reducción en mortalidad en la lista de espera, por las razones anteriormente mencionadas, será difícil garantizar un trasplante cardíaco para cada paciente. A esto se suma el grupo de pacientes que debido a una edad avanzada y comorbilidades como la diabetes, hipertensión pulmonar, historia reciente de cáncer, obesidad mórbida o insuficiencia renal, no cumplen los criterios para el trasplante cardíaco9. Considerando los cambios demográficos que afectarán a los países europeos durante las próximas décadas, es de esperar que aumente el número de pacientes candidatos a DAVI como terapia de destino que no son candidatos a trasplante. El desarrollo de dispositivos de asistencia ventricular de última generación con mayor fiabilidad y de menor tamaño ha hecho posible esta alternativa terapeutica8. Es más, especialmente en Europa nuevas técnicas quirúrgicas consideradas menos invasivas se están aplicando de manera cada vez más amplia prometiendo reducir el riesgo perioperativo10,11. Sobre todo en pacientes terapia de destino, que representan un colectivo complejo y de alto riesgo estas nuevas técnicas pueden contribuir a mejorar los resultados9.
En los Estados Unidos (EE. UU.), la terapia de destino ha visto un incremento importante desde su aprobación en 2010. Actualmente, el 45% de todos los implantes del año 2014 del registro INTERMACS fueron para terapia de destino12. En su artículo precursor, Slaughter et al. demostraron que pacientes terapia de destino tratados con DAVI de flujo continuo tenían una supervivencia de 58% 2 años postimplante7. Con respecto al REMATCH trial, que mostraba una supervivencia de un 23% en pacientes con un DAVI pulsatil6, esto constituía una mejora significativa y fue la base para aprobar el uso del HeartMate II (Thoratec-SJM) como terapia de destino en EE. UU. El análisis de mayor envergadura acerca de pacientes con terapia de destino se realizó en EE. UU. postaprobación del HeartMate II (Thoratec-SJM) y siguió a 247 pacientes por 2 años consecutivos13. Incluyendo una población de distintas edades (solo el 53% del total fueron mayores de 60 años), los resultados mostraron niveles de supervivencia del 74 y el 61% tras uno y 2 años. Mientras que en Europa nuevos dispositivos como el HVAD (HeartWare) o el HeartMate 3 (SJM) ya cuentan con aprobación para la aplicación en pacientes terapia de destino, en EE. UU. se están realizando estudios como el ENDURANCE trial para ampliar la indicación de los nuevos dispositivos. Todavía el número de publicaciones sobre la terapia de destino es bastante limitado, especialmente en los pacientes de edad avanzada (mayores de 70 años). El propósito de este trabajo es analizar la primera serie de pacientes septuagenarios destino que recibieron un implante de DAVI como terapia de destino mediante cirugía mínimamente invasiva (HVAD, HeartWare).
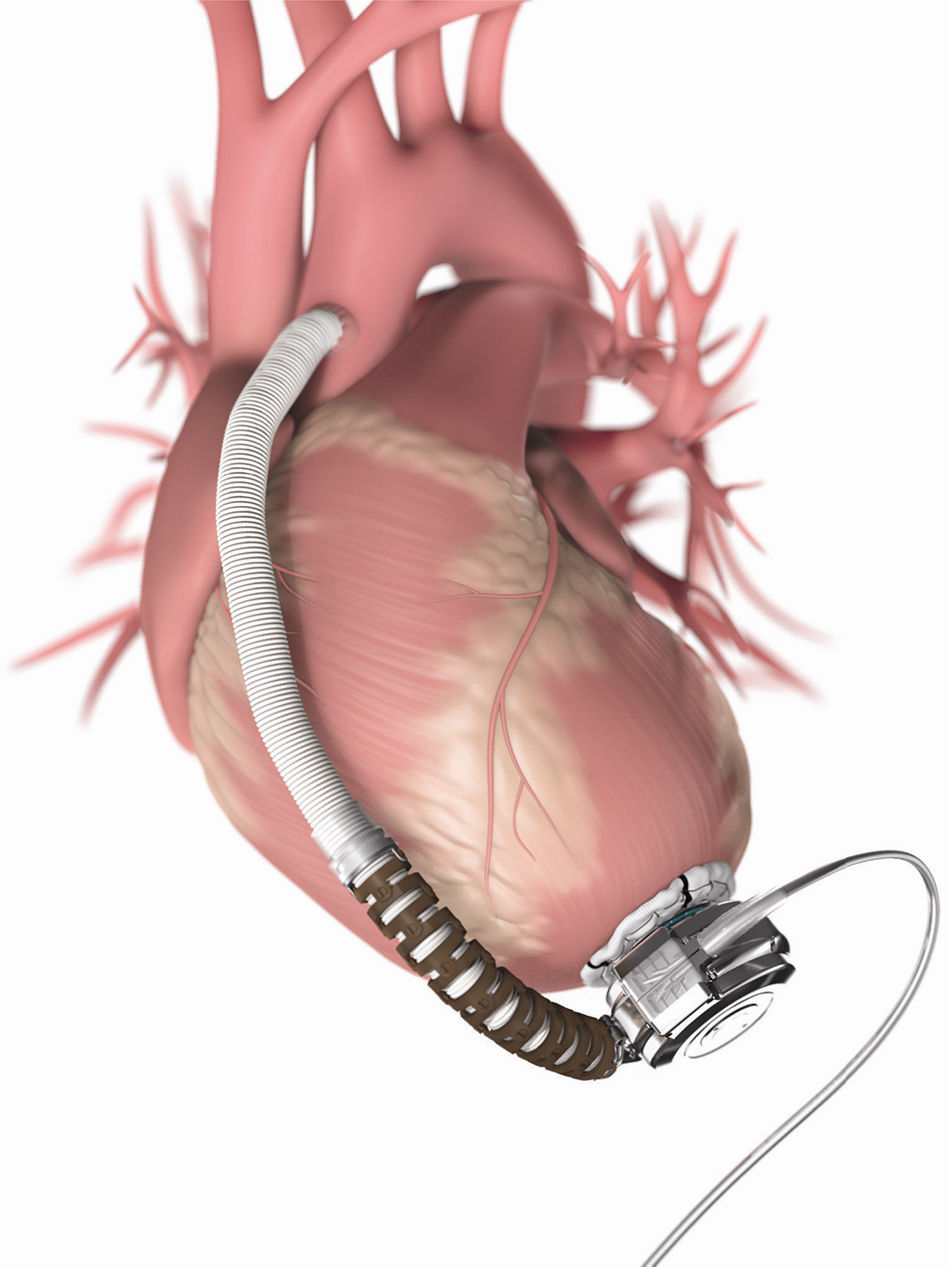
MétodosTécnica mínimamente invasivaEn 2011 nuestro grupo desarrolló una técnica mínimamente invasiva (TMI) de implantación de DAVI14. El procedimiento TMI implica 2 pasos: la inserción del DAVI a través de una toracotomía anterolateral (5.° o 6.° espacio intercostal izquierdo). En segundo lugar, se realiza una miniesternotomía en forma de «J» hasta el segundo o tercer espacio intercostal. Este acceso permite realizar la anastomosis entre el injerto de salida (outflow graft) y la aorta ascendente. Todos los pacientes recibieron el mismo sistema de asistencia ventricular izquierda (HVAD™, HeartWare Inc., Miami Lakes, EE. UU.) con el uso de circulación extracorpórea (CEC).
Diseño del ensayo clínicoSe realizó un ensayo monocéntrico, prospectivo y de un solo brazo. Entre los años 2013 y 2015, un total de 14 pacientes consecutivos mayores de 70 años, que requerían asistencia ventricular izquierda (HVAD, HeartWare Inc., EE. UU., fig. 1) como terapia de destino y no elegibles para el trasplante cardíaco fueron incluidos. Todos los pacientes fueron operados por el mismo equipo quirúrgico aplicando la TMI. Criterios de indicación clínica para la implantación de DAVI fueron: un deterioro significativo de la función cardíaca (FEVI<30%), con el índice cardíaco menor o igual a 2,2 l/min/m2, refractario al tratamiento médico, incluyendo la dependencia de inotrópicos.
El seguimiento máximo fue de 2 años después de la implantación. Todos los pacientes fueron visitados regularmente 4 veces al año en la clínica ambulatoria.
La investigación se ajusta a los principios esbozados en la declaración de Helsinki. Todos los pacientes proporcionaron por escrito un consentimiento informado y el estudio fue aprobado por la junta de revisión institucional local. La atención médica postoperatoria se gestionó de acuerdo con la práctica habitual.
Análisis estadísticoEl análisis estadístico se realizó con el programa SPSS 20.0 (SPSS Statistisics IBM, IBM Corp., Armonyk NY, EE. UU.). Se utilizó la estimación de supervivencia de Kaplan-Meier. Todos los datos continuos son mostrados como media±desviación estándar.
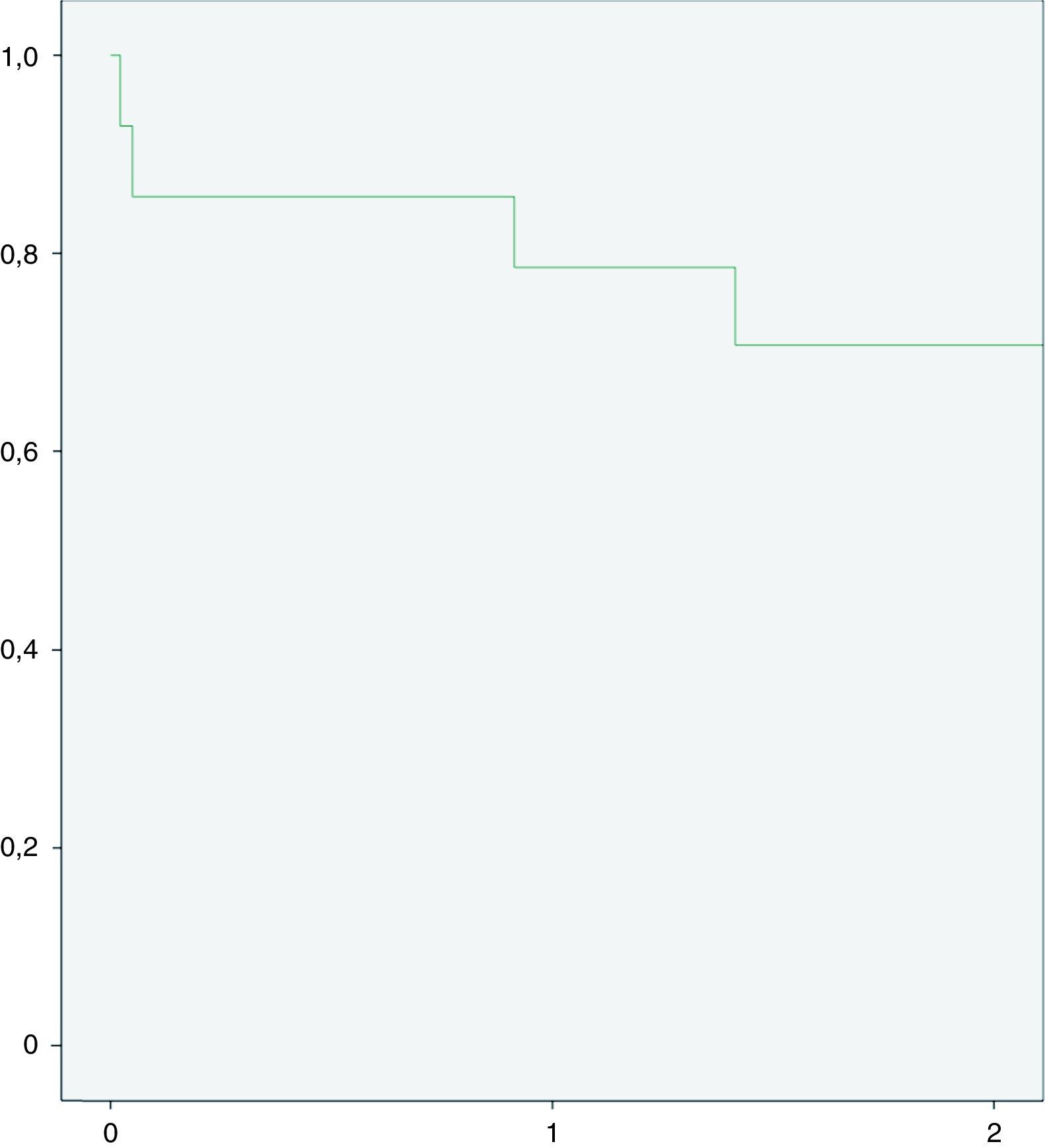
ResultadosEl total de las variables preoperatorias están resumidas en la tabla 1. Un total de 14 pacientes (100% hombres) fueron incluidos en el estudio. Todos los pacientes presentaban de una insuficiencia cardíaca crónica en estado funcional NYHA IV. Respecto a la clasificación INTERMACS, la mayoría de los pacientes correspondían a la categoría iv. Solo un paciente que había recibido soporte mecánico circulatorio previo (ECMO veno-arterial) se encontraba en la categoría INTERMACS I. La etiología de la insuficiencia cardíaca correspondía mayoritariamente (64,3%) a una miocardiopatía isquémica con un 50% de pacientes que recibieron cirugía cardíaca previa. El 50% de los pacientes presentaban de un fallo renal crónico (sin necesidad de diálisis), con niveles medios de creatinina de 135±35mg/l. Otras comorbilidades importantes fueron: diabetes (no insulinodependiente) 35,7% y enfermedad pulmonar obstructiva crónica 28,6%. Un 85,7% del total de los pacientes disponían de un desfibrilador automático implantable (DAI) previo al implante de DAVI, al restante porcentaje se le implantó un DAI en el transcurso postoperatorio. La función cardíaca previa a cirugía fue evaluada mediante ecocardiografía y cateterismo derecho en todos los pacientes. La fracción de eyección del ventrículo izquierdo promedia fue de un 22,0±5,0% con una dilatación media del ventrículo izquierdo (DdIV) de 67,4±7,3. La función longitudinal del ventrículo derecho fue estimada mediante el desplazamiento sistólico del anillo tricúspide (TAPSE) que resultó en un 15±2mm. Un 92,9% de los pacientes presentaban una insuficiencia tricuspídea leve a moderada. La saturación venosa de la arteria pulmonar media fue de un 52±7% y el índice cardíaco de 1,7±0,3 l/min/m2. Las variables intrahospitalarias y perioperatorias están resumidas en las tablas 2 y 3, respectivamente. Todas las implantaciones se realizaron mediante el uso de CEC, el tiempo medio de cirugía fue de 221±79min con un tiempo medio de CEC de 51±8min. Todos los pacientes recibieron productos sanguíneos incluyendo unidades de: concentrados de hematíes 4,7±3,2, concentrados de plaquetas 2,2±0,6 y plasma fresco congelado 1,6±0,9. Dos pacientes fallecieron durante el periodo intrahospitalario. La causa de muerte fue en ambos casos sepsis con fallo multiorgánico. Hubo 2 casos de fallo ventricular derecho que pudieron ser tratados exitosamente con inotrópicos. El tiempo promedio de estancia hospitalaria fue de 28,6±16,1 días, con una supervivencia de 30 días del 85,7%. Durante el seguimiento (tablas 3 y 4; fig. 2), la supervivencia bajó a un 78,6% (un año) y a un 70,7% (2 años). Las causas de muerte de los 2 casos durante el seguimiento fueron sepsis con fallo multiorgánico y hemorragia intracraneal (tabla 5).
Variables preoperatorias
| n=14 | |
|---|---|
| Demografía | |
| Edad al implante (años) | 71,8±1,5 |
| NYHA IV, n (%) | 14 (100) |
| INTERMACS I-III, n (%) | 5 (35,7) |
| INTERMACSIV, n (%) | 9 (64,3) |
| Miocardiopatía dilatada | 5 (35,7) |
| Miocardiopatía isquémica | 9 (64,3) |
| Hombres, n (%) | 14 (100) |
| IMC (kg/m2) | 24,4±3,5 |
| SC (m2) | 1,9±0,1 |
| Diabetes, n (%) | 5 (35,7) |
| Fallo renal crónico, n (%) | 7 (50) |
| EPOC, n (%) | 4 (28,6) |
| Historia de ACV, n (%) | 0 |
| DAI, n (%) | 12 (85,7) |
| Cirugía cardíaca previa, n (%) | 7 (50) |
| Soporte mecánico circulatorio previo, n (%) | 1 (7,1) |
| Laboratorio | |
| Sodio (mmol/l) | 137,7±5,0 |
| Creatinina (mg/l) | 134,6±35,4 |
| Bilirrubina (μl/l) | 24±19 |
| PCR (mg/dl) | 21,2±27,5 |
| NTproBNP (pg/ml) | 7.102±5.800 |
| Ecocardiografía y hemodinámica | |
| FEVI por ecocardiografía (%) | 22,0±5,0 |
| DdIV (mm) | 67,4±7,3 |
| TAPSE (mm) | 14,6±2,4 |
| Insuficiencia tricúspide (I-II), n (%) | 13 (92,9) |
| Insuficiencia tricúspide (III), n (%) | 1 (7,1) |
| Insuficiencia mitral (I-II), n (%) | 14 (100) |
| Insuficiencia aórtica (0-I), n (%) | 7 (50) |
| Presión arterial media (mmHg) | 88,4±10,4 |
| PVC (mmHg) | 17±5 |
| PCP (mmHg) | 24±7 |
| PVC/PCP (mmHg) | 0,7±0,2 |
| RVP (dyn*sec*cm−5) | 322±165 |
| RVS (dyn*sec*cm−5) | 1.532±269 |
| Saturación venosa (a. pulmonar) (%) | 52±7 |
| Índice cardíaco (l/min/m2) | 1,7±0,3 |
Los valores representan la media±deviación estándar (DE).
ACV: accidente cerebrovascular; DAI: desfibrilador automático implantable; DdVI: diámetro diastólico del ventrículo izquierdo; EPOC: enfermedad pulmonar obstructiva crónica; FEVI: fracción de eyección del ventrículo izquierdo; IMC: índice de masa corporal; PCP: presión capilar pulmonar; PVC: presión venosa central; RVP: resistencia vascular pulmonar; RVS: resistencia vascular sistémica; SC: superficie corporal; TAPSE: tricuspid annular plane systolic excursion.
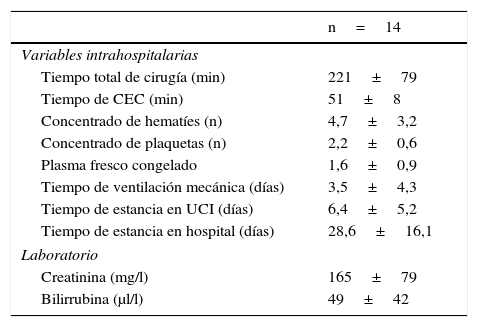
Variables perioperatorias
| n=14 | |
|---|---|
| Variables intrahospitalarias | |
| Tiempo total de cirugía (min) | 221±79 |
| Tiempo de CEC (min) | 51±8 |
| Concentrado de hematíes (n) | 4,7±3,2 |
| Concentrado de plaquetas (n) | 2,2±0,6 |
| Plasma fresco congelado | 1,6±0,9 |
| Tiempo de ventilación mecánica (días) | 3,5±4,3 |
| Tiempo de estancia en UCI (días) | 6,4±5,2 |
| Tiempo de estancia en hospital (días) | 28,6±16,1 |
| Laboratorio | |
| Creatinina (mg/l) | 165±79 |
| Bilirrubina (μl/l) | 49±42 |
Los valores representan la media±desviación estándar (DE).
CEC: circulación extracorpórea; UCI: Unidad de Cuidados Intensivos.
Eventos adversos durante el seguimiento de 2 años
| n=14 | |
|---|---|
| Eventos adversos, n (% del total) | |
| Reintervención quirúrgica por sangrado | 1 (7,1) |
| Diálisis durante el transcurso postoperatorio | 2 (14,3) |
| Fallo ventricular derecho | 2 (14,3) |
| ACV hemorrágico | 1 (7,1) |
| Sangrado gastrointestinal | 2 (14,3) |
| Infección del driveline | 1 (7,1) |
ACV: accidente cerebrovascular.
Mientras que en un inicio los DAVI tenían una indicación exclusiva para puente a trasplante, hoy en día más de un tercio de todos los pacientes tratados figuran como terapia de destino, vale decir sin opción de trasplante12. Por un lado, esto implica una ayuda importante para aquellos pacientes que sin esta opción tendrían un alto riesgo de mortalidad, por el otro lado crea nuevos desafíos para la terapia misma, ya que los pacientes terapia de destino en sí forman un grupo de alto riesgo con multicomorbilidad. El análisis de la literatura científica demuestra que la terapia de destino corresponde a una de las indicaciones más recientes de la asistencia ventricular, por lo cual existe solo un número limitado de publicaciones al respecto. Si bien un porcentaje creciente del registro INTERMACS corresponde a pacientes terapia de destino, la mayoría fue operado recientemente (falta de datos prolongados) y con un dispositivo (Heartmate II) que en Europa está perdiendo su relevancia clínica. Asimismo, los pacientes terapia de destino son un grupo bastante heterogéneo: La decisión de si un candidato a DAVI califica para terapia de destino o no no solo se basa en la edad del paciente, sino también en otros factores como la diabetes o la obesidad mórbida (entre otros) que excluyen un futuro trasplante15. Como actualmente los ensayos actuales no separan estos distintos grupos de pacientes, se dificulta la interpretación de los resultados. Es por ello que es fundamental realizar ensayos clínicos que investiguen los distintos grupos de pacientes dentro de la terapia de destino. Como actualmente en Europa nos vemos enfrentados hacia cambios demográficos importantes que implican una población cada vez mayor con un estimado aumento en la prevalencia e incidencia de insuficiencia cardíaca, el objetivo del presente estudio fue investigar los resultados del implante de DAVI en pacientes septuagenarios. En un total, 14 pacientes fueron incluidos y seguidos por 2 años. Si bien uno podría argumentar que se trata de una muestra reducida, hay que tener en cuenta que la experiencia a nivel mundial en estos pacientes es bastante limitada también. Según nuestros conocimientos, actualmente no existe una publicación que trate el tema en la literatura.
Creemos que un factor muy importante en la terapia de destino es la selección de pacientes, considerando especialmente la edad biológica de cada paciente16. En nuestro ensayo, ningún paciente fue excluido por el grupo de estudio. Sin embargo, como la mayoría de los pacientes es derivada desde centros terciarios, no se puede descartar que haya habido una preselección de pacientes. Como era de suponer, la mayoría de los pacientes tenían una miocardiopatía isquémica, con un 50% de cirugía cardíaca previa y en estado INTERMACS IV (estable en casa). Todos tenían una función ventricular izquierda muy reducida con índices cardíacos bajos. Una observación interesante fue la incidencia preoperatoria de insuficiencia aórtica leve (50% del total), en nuestro colectivo no observamos casos de empeoramiento de insuficiencia aórtica post-DAVI. Sería trascendente analizar este punto con un mayor número de pacientes y un seguimiento prolongado. Del punto de vista de la función ventricular derecha previa al implante, observamos valores medios de TAPSE y proporción PVC/PCP conservados. Mientras que la gran mayoría de los pacientes presentaba insuficiencia tricúspide ligera a moderada, hubo solo un caso de insuficiencia tricúspide severa. En todos los casos, decidimos favorecer a la cirugía mínimamente invasiva a una esternotomía completa con reparo tricúspide. Si bien sigue siendo una hipótesis, creemos que mantener el pericardio cerrado mantiene la barrera natural del ventrículo derecho evitando una sobredilatación al iniciar el DAVI. Comprobar esta hipótesis requerirá de estudios posteriores. Hubo 2 casos de fallo ventricular derecho que pudieron ser tratados con uso prolongado de inotrópicos. Respecto a otros eventos adversos importantes, observamos solo un caso de reintervención quirúrgica por sangrado con un bajo consumo total de productos sanguíneos. Mientras el 50% de todos los pacientes presentaba de fallo renal crónico sin la necesidad de diálisis, hubo 2 pacientes que requirieron diálisis de manera transitoria en el transcurso postoperatorio. La supervivencia intrahospitalaria fue de un 86,7%, bajando a 78,6% un año y a 70,7% dos años postimplante. Especialmente considerando este colectivo de alto riesgo, son resultados aceptables. En el transcurso del seguimiento un paciente falleció debido a una hemorragia intracraneal bajo régimen de anticoagulación. Además, hubo un caso de infección de driveline y 2 casos de sangrado gastrointestinal, todos los cuales fueron tratados de manera conservadora.
ConclusiónNuestros datos indican que la implantación de un dispositivo de flujo continuo miniaturizado mediante cirugía mínimamente invasiva es segura, factible y asociada a varios efectos positivos que incluyen la protección del ventrículo derecho y menor incidencia de sangrado postoperatorio. Incluso si nuestros resultados deben considerarse preliminares, nuestro estudio indica que los pacientes DT mayores de 70 años que se someten a la implantación DAVI pueden alcanzar tasas de supervivencia a 2 años iguales o superiores al 70%. Por lo tanto, consideramos que nuestro enfoque es adecuado para todos los pacientes que califican para un DAVI como terapia de destino. Además, dado que el proceso de miniaturización de los dispositivos continuará, es probable que en el futuro la mayor parte de las implantaciones se realicen utilizando técnicas mínimamente invasivas.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes y que todos los pacientes incluidos en el estudio han recibido información suficiente y han dado su consentimiento informado por escrito para participar en dicho estudio.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
Conflicto de interesesSVR es asesor para HeartWare Inc. y SJM, MA es asesor para HeartWare Inc. y SJM. JDS es asesor para HeartWare Inc. y SJM.