El síndrome de apnea-hipopnea del sueño (SAHS) pediátrico engloba alteraciones multisistémicas que afectan al estado general de salud, valorado indirectamente mediante el estudio de la demanda asistencial. Objetivo: cuantificar la frecuentación de consultas médicas en niños con SAHS durante 5 años y compararla con una población sana.
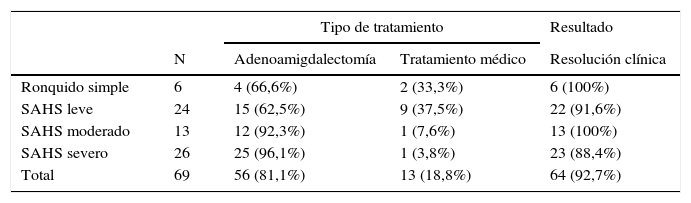
MétodosEstudio casos-control longitudinal ambispectivo en un hospital del sistema nacional de salud. Reclutamos a 69 niños remitidos por SAHS sin otras patologías para que la demanda asistencial fuera predominantemente atribuida al SAHS. Se seleccionó a otros 69 niños sanos como grupo control. Obtuvimos datos de frecuentación durante 5 años: el año en el que se realizó el tratamiento del SAHS («año 0»), 1 y 2 años antes («año –1» y «año –2»), y 1 y 2 años tras el tratamiento («año+1» y «año+2»).
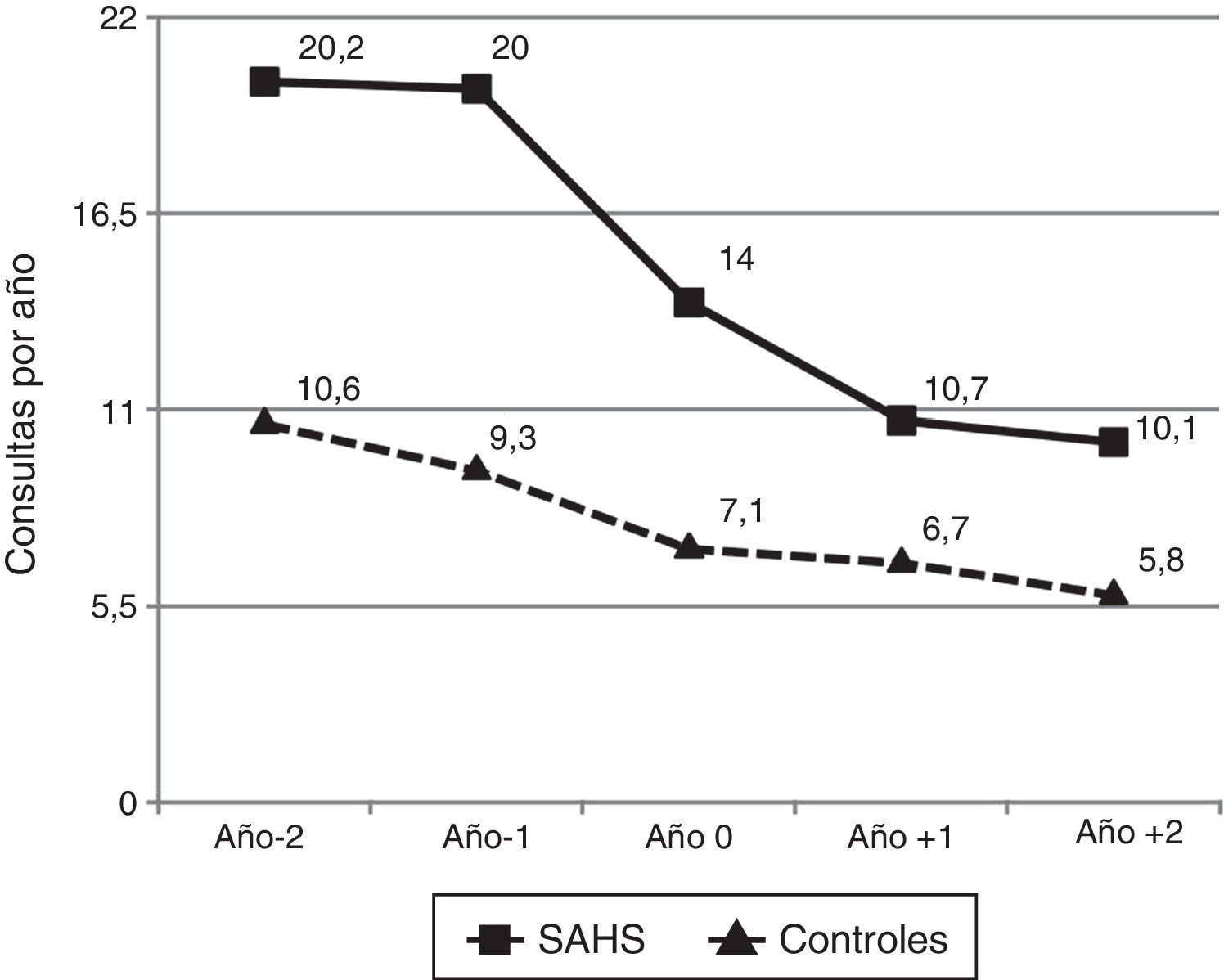
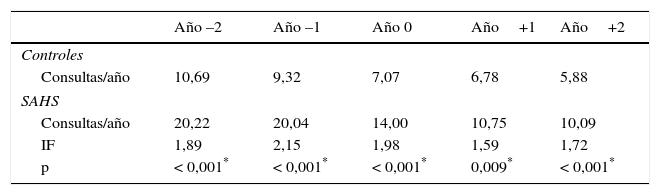
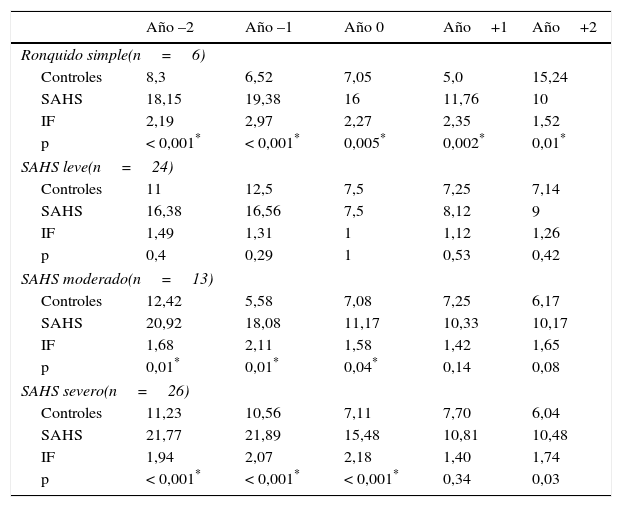
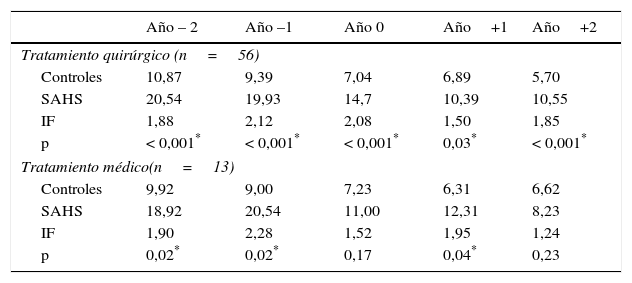
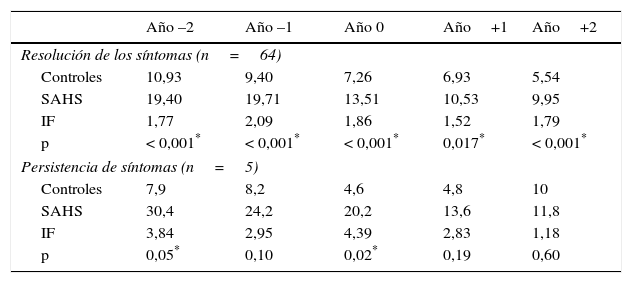
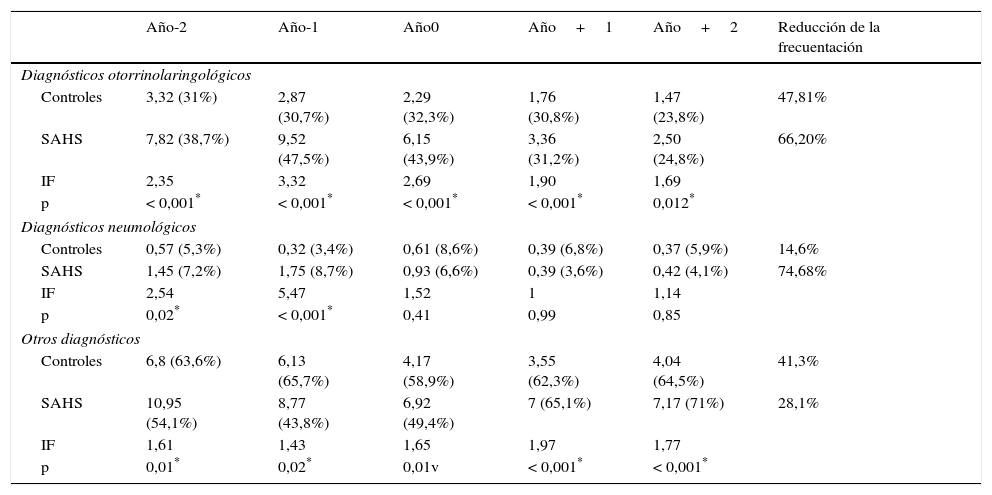
ResultadosEl índice de frecuentación (IF), descrito como cociente entre demanda asistencial por los niños con SAHS y niños sanos, fue 1,89 durante el año –2 y 2,15 durante el año –1 (p<0,05). El tratamiento disminuyó la utilización, con IF de 1,59 durante el año+1 y 1,72 en el año+2 (p<0,05). Las principales causas de sobrefrecuentación fueron otorrinolaringológicas y neumológicas.
ConclusionesLos niños con SAHS muestran mayor demanda asistencial, al menos 2 años antes del tratamiento, lo que implica un deterioro de la salud global que pudiera estar presente años antes de que la abordemos. El tratamiento repercute en una mejora, aunque permanece alta tras el tratamiento, sugiriendo enfermedad residual o secuelas.
Paediatric Obstructive Sleep Apnoea-Hypopnoea Syndrome (OSAS) is a multisystemic condition affecting child's health status that may be investigated analyzing demand for healthcare. Objective: to quantify the frequency of medical consultations in children with OSAS over a 5-year period, compared to a healthy population.
MethodsA longitudinal, case-control, ambispective study was conducted at a hospital pertaining to the national public health system. 69 consecutive children referred for OSAS were recruited with no diseases other than OSAS so that healthcare demand was purely attributed to this condition. Matched healthy control children were selected to compare these data. Data regarding frequency of the medical consultations were obtained over 5 years: the year of the treatment (“Year0”), 1 and 2 years before (“Year -1” and “Year -2” respectively), and 1 and 2 years after treatment (“Year+1” and “Year+2”)
ResultsFrequentation Index (FI), as ratio between the use of health services by OSAS children and healthy controls was 1.89 during Year-2, and 2.15 during Year-1 (P<.05). Treatment diminishes utilization, with FI of 159 during year+1 and 1.72 during year+2 (P<.05). The main causes of attendance were otolaryngological and pneumological diseases, improving after treatment.
ConclusionsChildren suffering from OSAS demand more healthcare services, at least 2 years before treatment, implying that the disease could be present years before we manage it. Therapeutic actions improve healthcare services utilization, although remain higher than for controls, which suggests OSAS sequelae or residual disease.