Transplantation (Tx) is a therapeutic alternative intervention for terminal organ dysfunction, fatal disease or, in some cases, to improve the quality of life and reduce the risk of complications from chronic diseases. One of the major limitations in performing transplants is obtaining donor organs because of the difficulties in the process of organ donation of deceased donors and the unavailability of compatible living donors. In Brazil, there are many more patients on waiting lists, especially for liver and kidney transplants, than the number of procedures performed. Therefore, non-ideal donors are sometimes considered for transplantation, including those with a higher risk of primary graft dysfunction and infection transmission, such as hepatitis C virus (HCV)-seropositive donors. HCV-seropositive donors have routinely been used by a few groups or in cases of extreme urgency. However, the safety of transplantation from HCV-positive donors has not been clearly determined and may vary according to the type of transplant. To establish a set of recommendations, we performed an analysis based on the data available in the literature. The following items were considered according to the type of transplantation: 1) the position on the list, 2) the urgency of transplantation, 3) the HCV infection status of the donor (serology, viral replication and histological activity), 4) the HCV infection status of the recipient (serology, viral replication and histological activity) and 5) the safety data available regarding the use of HCV-seropositive donors. We analyzed liver, kidney, heart, lung and hematopoietic stem cell transplants (HSCTs). The IDSA (Infectious Diseases Society of America) rating system was used to establish levels of evidence.
1. Liver Transplantation
Chronic liver disease due to HCV accounts for almost one-half of liver Tx indications. The risk of the histological recurrence of hepatitis after transplantation is approximately 70%. The graft and recipient survival is lower compared with other etiologies. Descriptive and comparative studies and case-control analyses have shown that the use of seropositive donors for seropositive recipients does not interfere with graft or patient survival.
2. Kidney Transplantation
Some descriptive studies have shown that the use of seropositive donors for seropositive recipients does not interfere with graft or patient survival. However, one publication described five cases of discordant donor and recipient genotypes: in three of these cases, elevated enzyme levels and genotype substitution or association were observed in the recipient after transplant.
3. Heart Transplantation
Little data are available regarding heart Tx. One multicenter study reported a lower survival rate in patients who received organs from seropositive donors, regardless of the HCV serostatus of the recipient.
4. Lung Transplantation
Little data are also available regarding lung Tx. However, in a multicenter survey, 72% of the participating groups considered the use of HCV-seropositive donors for HCV-seropositive recipients. Nevertheless, there have been no descriptions of liver disease progression or graft and patient survival in positive viremia recipients. It is important to consider that treatment with interferon-gamma is usually not recommended after lung Tx due to the high risk of acute cellular rejection.
5. Hematopoietic Stem Cell Transplantation (HSCT)
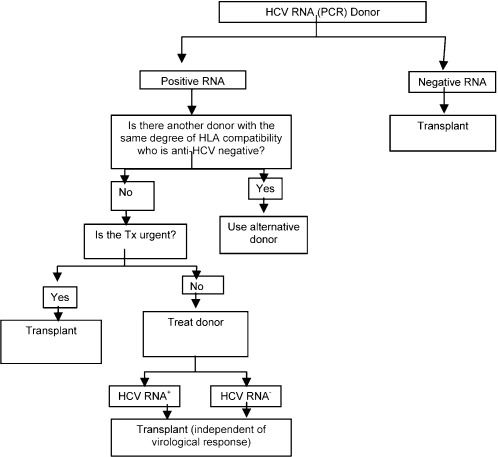
In HSCT, there have been reports of a significantly increased risk of hepatitis in HCV-seronegative recipients of seropositive donors, especially when there is evidence of viral replication. Because HSCT often involves situations in which there is an imminent risk of death and the need for an HLA-matched living donor, the decision should be based on the urgency of the Tx and level of viremia in the donor.
RECOMMENDATIONSA. General- 1.
In solid organ transplants, consider the use of HCV-seropositive donors only for HCV-seropositive recipients.
- 2.
Informed consent should be obtained in all of the cases involving HCV-seropositive organ or cell donors.
- 3.
Patients should be informed of the possibility that their donor will have a different HCV genotype, the lack of available time to determine the serotype before Tx (in cases of deceased donors) and the potential risk of HCV transmission in these cases (fact demonstrated after kidney Tx).
1. Liver Transplantation
Accept HCV-seropositive donor for HCV-seropositive recipient since donor liver biopsy has not provided evidence of liver disease in a recipient with positive HCV viremia.
2. Kidney Transplantation
Accept HCV-seropositive donors for HCV-seropositive recipients with positive viremia (BII).
3. Lung Transplantation
In centers that accept recipients with HCV-positive viremia, accept HCV-seropositive donors (CIII).
4. Heart Transplantation
Do not accept HCV-seropositive donors (DII).
5. Hematopoietic Stem Cell Transplantation
Follow the chart (CIII).
AUTHOR CONTRIBUTIONSAbdala E wrote the manuscript (Portuguese), supervised the revision of the recommendation for liver transplantation and participated in the discussion of final recommendations and the final revision of the text. Azevedo LSF prepared the recommendations for kidney transplantation and participated in the discussion of the recommendations. Campos SV was responsible for the final revision of the literature and the English translation of the manuscript. Caramori ML prepared the recommendations for lung transplantation and participated in the discussion of the recommendations. Costa SF prepared the recommendations for bone marrow transplantation and participated in the discussion of the recommendations. Strabelli TMV prepared the recommendations for bone marrow transplantation and participated in the discussion of the recommendations. Pierrotti L, Varkulja GF, and Almeida GMD participated in the discussion of the recommendations. Shikanai-Yasuda MA coordinated the presentations and discussion of the recommendations, helped to revise the final recommendations and to adequate the manuscript for submission.
The authors wish to thank Profs. José Otávio Costa Auler Júnior, Tarcísio Eloi Pessoa de Barros Filho and Eloísa Bonfá for their support as Clinical Directors of the Hospital das Clínicas da Faculdade de Medicina da Universidade de São Paulo.
O transplante (tx) consiste, atualmente, em alternativa terapêutica para doenças terminais e fatais ou, em alguns casos, para melhoria da qualidade de vida e diminuição dos riscos de complicações de doenças crônicas. Uma das principais limitações atuais para a realização de tx é a escassez de órgãos ou de doadores, por dificuldades na captação de doadores falecidos ou pela indisponibilidade de doadores vivos compatíveis. Há, no Brasil, um grande número de pacientes em lista de espera, especialmente para tx de fígado e de rim, em relação ao número de procedimentos realizados. Como consequência destas limitações, doadores considerados não ideais têm sido utilizados, incluindo-se aqueles cujo enxerto apresenta maior risco de não funcionamento após o transplante e doadores com risco potencial de transmissão de alguma infecção. Entre estes últimos encontram-se os soropositivos para o vírus da hepatite C (VHC). Doadores com sorologia positiva para VHC têm sido utilizados como rotina por alguns grupos, ou em casos de extrema urgência por outros. A segurança desta medida, entretanto, não está claramente determinada e varia conforme o tipo de transplante. Com o objetivo de estabelecer uma recomendação em nosso meio, realizamos discussões baseadas nos dados disponíveis na literatura. Os seguintes itens foram considerados, por tipo de transplante: 1. Tempo estimado de espera em lista; 2. Urgência do transplante; 3. Condição de infecção pelo VHC do doador (sorologia, replicação viral e atividade histológica); 4. Condição de infecção pelo VHC do receptor (sorologia, replicação viral e atividade histológica); 5. Dados de segurança no uso de doadores soropositivos. Foram analisados os seguintes transplantes: fígado, rim, coração, pulmão e transplante de células-tronco hematopoéticas (TCTH). Para a determinação dos níveis de evidência foi utilizado o sistema da IDSA (Infectious Diseases Society of America).
- 1.
Transplante de Fígado
A hepatopatia crônica pelo VHC corresponde a quase a metade das causas de indicação de tx de fígado. O risco de recidiva histológica da hepatite após o tx é de aproximadamente 70%. A sobrevida do enxerto e do hospedeiro é menor do que a dos transplantados por outras etiologias. Estudos descritivos e comparativos, e análises de caso controle, demonstram que o uso de doadores soropositivos para pacientes soropositivos não interfere na sobrevida do enxerto e do hospedeiro.
- 2.
Transplante de Rim
Alguns estudos descritivos demonstraram que o uso de doadores soropositivos em receptores soropositivos não interferiram na sobrevida do enxerto ou do hospedeiro. Há, no entanto, uma publicação de 5 casos de genótipos discordantes entre doador e receptor, e em 3 destes houve aumento de enzimas e substituição ou associação do genótipo no receptor após o tx.
- 3.
Transplante de Coração
Existem poucos dados disponíveis em tx de coração. Um estudo multicêntrico detectou menor sobrevida em pacientes que receberam órgãos de doadores soropositivos, independentemente do estado sorológico do receptor.
- 4.
Transplante de Pulmão
Há também poucos dados em tx de pulmão, entretanto em inquérito multicêntrico 72% dos grupos que responderam consideram o uso de doadores soropositivos para receptores soropositivos.
- 5.
Transplante de Células Tronco Hematopoéticas
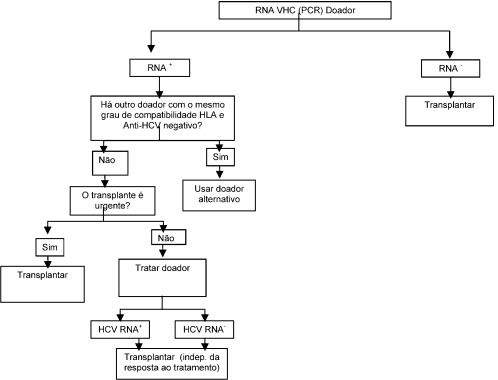
Em TCTH, há descrições de aumento significativo do risco de hepatite pelo VHC em receptores soronegativos de doadores soropositivos, especialmente se houver evidência de replicação viral. Como o TCTH envolve situações de possibilidade iminente de óbito e compatibilidade HLA de doadores vivos, a decisão deve basear-se na urgência do tx e na viremia do doador.
Uso de doadores com sorologia positiva para vírus da hepatite C em transplantes
- 1.
Em transplantes de órgãos sólidos, considerar utilizar doador soropositivo para VHC apenas para receptor também soropositivo.
- 2.
Em todos os casos de uso de órgão ou células de doador soropositivo para VHC providenciar assinatura de Termo de Consentimento Livre e Esclarecido pelo receptor ou responsável por este.
- 3.
Considerar e informar ao paciente a possibilidade de o genótipo do VHC do doador não ser o mesmo do receptor, de não haver tempo disponível para esta determinação antes do tx (doadores falecidos) e do potencial risco de transmissão nestes casos (fato demonstrado em tx renal).
- 1.
Transplante de Fígado
Aceitar doador soropositivo para VHC para receptor com doença hepática pelo VHC, desde que: biópsia hepática do doador sem evidência de hepatopatia pelo VHC e viremia do receptor positiva (BII).
- 2.
Transplante de Rim
Aceitar doador soropositivo para VHC para receptor soropositivo para VHC, desde que viremia do receptor positiva (BII).
- 3.
Transplante de Pulmão
Aceitar doador soropositivo para VHC para receptor soropositivo para VHC, desde que viremia do receptor positiva (CIII).
- 4.
Transplante de Coração
Não aceitar doador soropositivo para VHC (DII)
- 5.
Transplante de Células Tronco Hematopoéticas – Seguir fluxograma (CIII)