La introducción de la mamografía digital y la difusión de los programas de screening poblacional han ocasionado un aumento del número de procedimientos percutáneos para la caracterización de lesiones mamarias no palpables.
En una biopsia con aguja gruesa (BAG) la categoría B3 define las lesiones con potencial maligno incierto y abarca un amplio espectro de alteraciones de la unidad ductolobulillar terminal, para las cuales no existe una indicación terapéutica estandarizada1.
Debido a la posibilidad de infradiagnóstico de lesiones malignas, el manejo más aceptado para pacientes con resultado de atipia en la BAG es la realización de una biopsia quirúrgica o una rebiopsia percutánea con una técnica que obtenga más muestra. La biopsia asistida por vacío se recomienda como técnica de elección para la caracterización de microcalcificaciones –especialmente en los grupos<5mm– y como técnica de rebiopsia para caracterizar lesiones B1, B3 o B4 después de BAG con aguja 14G como alternativa a la biopsia quirúrgica2–4. Los objetivos del estudio fueron revisar retrospectivamente las BAG realizadas desde noviembre de 2006 hasta octubre de 2012 con resultado histológico de atipia del epitelio plano (AEP), hiperplasia ductal atípica (HDA), hiperplasia lobulillar atípica (HLA) y carcinoma lobulillar in situ (CLIS), revisar su presentación clinicorradiológica y analizar la correlación anatomopatológica entre BAG y cirugía en las lesiones tratadas quirúrgicamente.
Se seleccionaron 28 BAG realizadas en 27 pacientes. Dieciséis pacientes procedían del programa de screening poblacional y 11 de la actividad asistencial.
En 5 pacientes el diagnóstico se realizó mediante ecografía second-look después de resonancia magnética de estadificación locorregional de cáncer de mama. En 2 pacientes la lesión B3 se localizaba en la mama contralateral, y en 3 en la ipsilateral, sin continuidad de captación con el carcinoma, a una distancia mínima de 3cm.
Las BAG se realizaron con aguja de 14G, mediante guía ecográfica en 10 casos y mediante estereotaxia digital vertical en 18.
El diagnóstico, el tratamiento y el seguimiento se valoraron en un comité multidisciplinar de patología mamaria.
El diagnóstico histológico de las 28 BAG incluía 16 HDA (5 asociadas a AEP, una a cicatriz radial y 2 dentro de fibroadenoma), 8 AEP, 3 CLIS (uno asociado a AEP) y una HLA.
La edad media global fue de 53 años, y de 51 años en las 22 pacientes no oncológicas. La edad media en las AEP puras fue de 50 años y de 52 años en las HDA e HDA+AEP sin cáncer de mama.
Sin incluir las 5 pacientes oncológicas, solo 2 eran sintomáticas: una presentaba dolor axilar y otra secreción de pezón unilateral y uniorificial.
De las 28 lesiones, 17 (61%) fueron microcalcificaciones, 10 (36%) nódulos y una distorsión. La única distorsión correspondía a una HDA en una cicatriz radial.
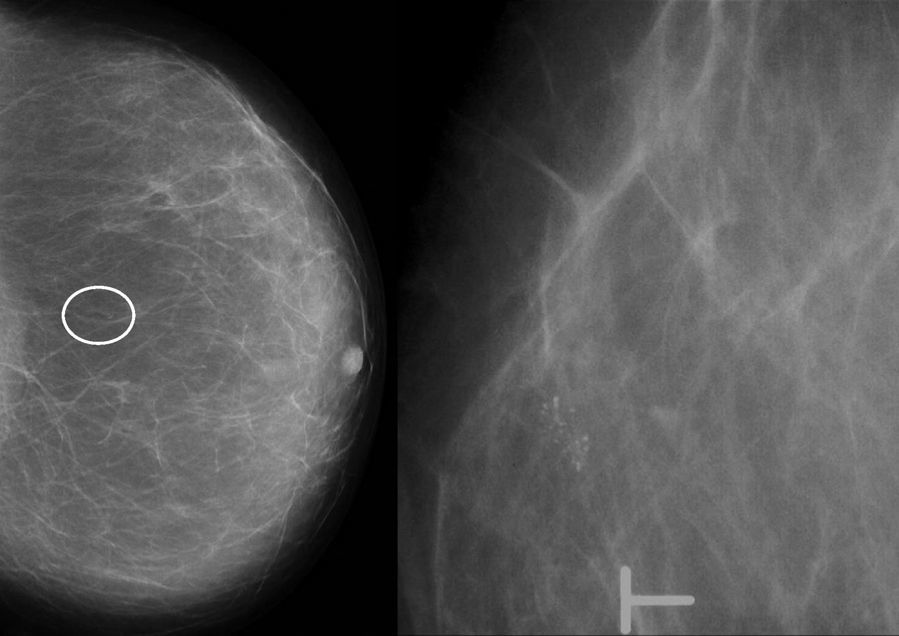
La mayoría de las microcalcificaciones eran amorfas (11/17), todas agrupadas (fig. 1). El resto eran pleomórficas (6/17): 4 con distribución segmentaria y 2 regional.
En 22 pacientes no oncológicas el 74% de las lesiones fueron microcalcificaciones.
Las 5 lesiones detectadas por resonancia magnética correspondían a nódulos en la ecografía: uno coincidía con una zona de microcalcificaciones amorfas en una mama densa y otros 4 no tenían traducción mamográfica.
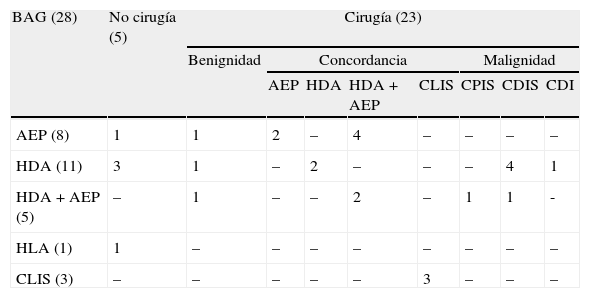
Se realizó tratamiento quirúrgico en 23 lesiones (82%) y seguimiento clinicorradiológico solo en las otras 5 (18%). La correlación con las biopsias quirúrgicas demostró concordancia con el resultado de las BAG en el 39% (9/23), lesión sin atipia en el 13% (3/23), coexistencia de otra lesión precursora/premaligna de mayor riesgo (HDA) no representada en la muestra de la BAG de 4 AEP en el 17%, y lesión maligna en el 30% (7/23). Excluyendo las pacientes oncológicas, la cirugía fue de malignidad en 5 pacientes sobre un total de 18 BAG (27%): un carcinoma ductal infiltrante de bajo grado, un carcinoma papilar in situ y 3 carcinomas ductales in situ (CDIS) grado i y grado ii (tabla 1).
El seguimiento radiológico (entre 3,5 meses y 6,2 años; media: 35,4 meses) –realizado con mamografía anual y con ecografía complementaria cuando fue necesaria– no demostró aumento ni aparición de nuevas lesiones.
La limitación más importante en este estudio es el pequeño grupo de pacientes incluido y la representación escasa de algunos tipos de lesiones B3. Otro límite de nuestro estudio es la técnica de biopsia automática y con aguja de calibre 14G, ya que otros estudios han demostrado la mayor sensibilidad diagnóstica de las biopsias percutáneas con agujas de mayor calibre (9 o 11G) y/o realizadas con biopsia asistida por vacío5,6.
Acorde con la literatura publicada, el hallazgo radiológico más frecuente ha sido el de microcalcificaciones, la lesión más habitual fue la HDA, y las pacientes con AEP pura eran más jóvenes que aquellas con HDA o HDA+AEP7–9.
La AEP es una alteración del epitelio de la unidad ductolobulillar terminal con atipia citológica de bajo grado y arquitectural no compleja, con perfiles genético e inmunohistoquímico similares a los que se hallan en el CDIS y en el carcinoma ductal infiltrante de bajo grado10. Se ha observado su frecuente coexistencia con carcinoma tubular y CDIS de bajo grado, así como con HLA y CLIS11.
El protocolo de nuestro centro indica la biopsia quirúrgica en las AEP. En nuestra serie, a pesar de utilizar agujas de calibre 14G, en ninguna de las 7 AEP puras la cirugía ha demostrado malignidad, pero el 57% de ellas se asociaba a HDA.
La HDA es una lesión que presenta algunos, pero no todos los criterios de CDIS de bajo grado y muestra un riesgo moderado de progresión a carcinoma ductal infiltrante (riesgo relativo de 3,0-5,0)10,12,13.
En nuestra serie, el 50% de las HDA e HDA+AEP (7/14) son lesiones malignas. Excluyendo las 3 pacientes oncológicas, la tasa de infradiagnóstico de HDA e HDA+AEP es del 36,3% (4/11).
La HLA y el CLIS se denominan conjuntamente neoplasia lobulillar. Se describe un riesgo relativo de desarrollo de cáncer de 4-5 para la HLA y de 8-10 para el CLIS14.
Siguiendo el protocolo propuesto por Liberman et al. y apoyado sucesivamente por Nagi et al., debe realizarse exéresis si existe discrepancia radiológica-histopatológica, si coexiste otra lesión biológicamente agresiva que requiera extirpación o si la proliferación lobulillar tiene características ductales, mientras que las formas clásicas de neoplasia lobulillar pueden manejarse únicamente con vigilancia clinicorradiológica15,16.
En nuestra serie se realizó cirugía en 3 de 4 neoplasias lobulillares (una asociada a AEP y 2 a cáncer de mama) y en los 3 casos se confirmó el diagnóstico de la BAG.
En conclusión, las lesiones B3 constituyen un grupo heterogéneo de alteraciones cuyo manejo debe ser multidisciplinar y personalizado para cada paciente. Independientemente de la tasa de infraestimación en la biopsia percutánea, el diagnóstico de este tipo de lesiones puede identificar a un grupo de mujeres tributarias de un seguimiento más estricto debido al mayor riesgo de desarrollar un carcinoma de mama a lo largo de su vida.