Conocer la prevalencia, las características epidemiológicas y la calidad del registro relativos a la sedación paliativa (SP) en un hospital universitario. Establecer áreas de mejora.
Material y métodoAnálisis descriptivo retrospectivo de los registros clínicos de pacientes oncológicos fallecidos en nuestro centro entre octubre y diciembre de 2010. Las variables analizadas incluyeron: datos epidemiológicos y ubicación de los pacientes, presencia de SP, síntoma que la motivó, grado de participación del paciente y la familia en la toma de decisiones, fármacos y dosis utilizados. El análisis cualitativo se desarrolló mediante 2rondas Delphi en las que cada participante recibió los resultados globales del grupo. Fueron seleccionados aquellos ítems en los que existía un consenso completo o elevado.
ResultadosIdentificamos 53defunciones por cáncer, el 51% recibieron SP. La edad media fue de 67años, y el 64% fueron varones. El cáncer de pulmón supuso el 32%. Quince pacientes dependían de Oncología, 7 de Hematología y 4 del Servicio de Urgencias. En el 53,85% existió intervención de cuidados paliativos. Los síntomas que motivaron la SP fueron: disnea en 11casos y delirium en 5. El tiempo medio ingreso-SP fue de 9,5días (duración media, 1,2días). La media de fármacos utilizados fue de 2,6, con empleo de morfina en el 100% y midazolam en el 98%. En 20casos constatamos el registro de consentimiento para su inicio (100% verbal). Doce profesionales participaron en el análisis cualitativo fruto del cual consensuamos una plantilla para mejorar los registros de selección, toma de decisiones y evolución en los casos de SP.
ConclusionesLa SP fue motivada por disnea o delirium y se aplicó en la mitad de los pacientes fallecidos. Las áreas de mejora detectadas afectaban al registro de los criterios de selección, al tipo de sedación y a la participación del paciente en la toma de decisiones. Por ello hemos consensuado un conjunto mínimo de datos que facilitará la recogida de información de los profesionales.
To determine the prevalence, epidemiology and registration status of palliative sedation (PS) prevalence in a teaching hospital, and to establish areas for improvement.
MethodsA descriptive retrospective analysis was designed using the records from cancer patients who died between October and December 2010. The variables included were: epidemiological, inpatient unit, refractory symptom, drugs and dosages, and patient participation in the decision making process. The qualitative analysis followed a Delphi process: each participant received the overall performance of the group referred to as mean, median, 25th and 75th percentile. Items selected were those in which there was total or a high consensus.
ResultsA total of 53deaths were identified. Just over half (51.92%) received PS. The mean age was 67.46 and 64% were males. The most frequent diagnosis was lung cancer (32.14%). Fifteen of the patient patients were in the Oncology ward, 7 in Hematology, and 4 at the Emergency Department. The PC team took part in 14 of the sedations performed. A refractory symptom was identified in 20. There were 11cases of dyspnea and 5cases of delirium. The mean time between admission and PS was 9.5days. The mean duration of PS was 1.2days, with a mean number of 2.6drugs used. There were 20informed consents which were all verbal. The mean time from last chemotherapy to death was 82days. For the Delphi process, 12 oncology or palliative care health professionals were included. A consensus was reached on the minimum data to be recorded in case of PS. This list includes: selection criteria, decision-making process and the sedation evolution.
ConclusionsPS was applied in half of the patients who died due to dyspnea or delirium. Selection criteria were identified, as well as the type of PS and patient involvement in decision making process. A consensus was also reached on a minimum dataset that would help the clinician to record relevant information in PS.
El modelo de atención de cuidados paliativos ha demostrado su capacidad para aliviar el sufrimiento de pacientes en la etapa final de su vida y de sus familias de una manera eficiente1. Y decimos aliviar el sufrimiento porque el afrontamiento de la propia muerte o de la de un ser querido genera un sufrimiento ligado a las pérdidas que excede con mucho la capacidad de tratamiento de esta y otras disciplinas médicas. Los cuidados paliativos no pueden evitar la enfermedad, la agonía ni la muerte, pero no abandonan al paciente y su familia a su suerte sino que, desde el enfoque referido anteriormente, les acompañan. Sería ingenuo pensar que el alivio del sufrimiento es óptimo en todos los casos. La experiencia de la fragilidad y la proximidad a la muerte, en el contexto de una enfermedad crónica, no se puede diseccionar en diferentes áreas: síntomas físicos, síntomas emocionales, problemas familiares o sociales, interrogantes asistenciales, etc., y abordarlos de forma separada. Unos y otros problemas se entrelazan en un complejo entramado estrechamente ligado a la biografía de esa persona y a su entorno más próximo. Cada vez disponemos de más herramientas para el control de los síntomas físicos, pero seguimos teniendo muchas limitaciones para el control de la sensación de ahogo (en las fases finales de las enfermedades que afectan al pulmón), la debilidad, etc. En la dimensión psico-socio-existencial nos ocurre lo mismo. Disponemos de estrategias y fármacos para atender la depresión y la ansiedad reactiva, pero la búsqueda de sentido, la angustia vital ante la muerte son áreas de difícil abordaje, sobre todo cuando el enfermo, durante toda su enfermedad, ha desarrollado estrategias de negación o conductas regresivas que han sido respetadas de acuerdo con el principio de autonomía. Son estas las situaciones en las que hablamos de síntomas difíciles y síntomas refractarios2. Entendemos por «síntoma refractario» aquel que no puede ser adecuadamente controlado sin comprometer la conciencia del paciente, a pesar de los intensos esfuerzos para hallar un tratamiento tolerable durante un tiempo razonable3,4.
Disponemos de pocos datos sobre requerimiento de sedación paliativa (SP). Según las series publicadas, se estima que entre el 20 y el 25% de los casos ingresados en unidades de cuidados paliativos requieren SP en la agonía5. Los síntomas refractarios más frecuentes tributarios de SP son: delirium, disnea, dolor y sufrimiento psicológico, seguidos de otros como las náuseas y vómitos o las hemorragias4,5.
La SP es una medida terapéutica potente y en muchos casos irreversible que precisa una reflexión bioética serena y profunda antes de ser iniciada y durante el procedimiento6-8. Ante todo ello, parece necesario conocer más sobre las prácticas habituales de los profesionales, así como las demandas de los enfermos al final de la vida. Es en este contexto en el que nos planteamos desarrollar nuestra investigación, con los siguientes objetivos:
- -
Conocer la prevalencia, las características epidemiológicas y el nivel de calidad del registro del proceso de toma de decisiones en torno a la SP en pacientes oncológicos que fallecen en un hospital universitario.
- -
Establecer las áreas de mejora consensuando una plantilla de registro o check list que permita corregir las deficiencias.
Realizamos un estudio en 2fases: análisis descriptivo y estudio cualitativo tipo Delphi.
Se realizó un análisis descriptivo retrospectivo de los registros de las historias clínicas de los pacientes oncológicos fallecidos en nuestro centro entre octubre y diciembre de 2010. Las fuentes de datos fueron los registros informatizados y en papel correspondientes a las historias clínicas de los pacientes.
Como criterios de inclusión y exclusión se establecieron:
Criterios de inclusión: pacientes diagnosticados de cáncer (tumores sólidos o hematológicos) fallecidos en nuestro centro en las áreas de urgencias, oncología y hematología.
Criterios de exclusión: pacientes oncológicos fallecidos en otras unidades de hospitalización o domicilio.
El análisis estadístico fue descriptivo mediante medidas centrales y proporciones.
Posteriormente realizamos un análisis cualitativo a partir de los resultados obtenidos previamente y que fueron presentados a los profesionales de oncología y cuidados paliativos. Se detectaron las áreas donde el proceso de toma de decisiones y el registro podían ser mejorados, de acuerdo con los estándares publicados por la Sociedad Española de Cuidados Paliativos (SECPAL) y las recomendaciones de la Sociedad Europea de Cuidados Paliativos (EAPC)2,3.
Una vez establecidos los puntos débiles de nuestro registro, iniciamos una investigación prospectiva siguiendo metodología Delphi. El proceso comenzó con una tormenta de ideas a partir de los resultados y la revisión bibliográfica. Quisimos consensuar un conjunto mínimo de datos que deberían ser registrados en las historias de los pacientes que precisasen SP. A partir de la agrupación y depuración de los ítems facilitados por los profesionales, se elaboró un listado inicial que fue sometido a 2rondas Delphi. Después de la primera ronda, cada participante recibió los resultados globales del grupo referidos como media, mediana y percentil25 y 75.
Fueron seleccionados aquellos ítems en los que existía un consenso completo o elevado tras la segunda ronda Delphi, siguiendo los siguientes criterios:
- •
Consenso completo: mediana de 4 (escala de Likert de 5 puntos); ≥80% de las respuestas con nivel de acuerdo «bastante o total» (3 y 4 de escala de Likert); rango intercuartil=0.
- •
Consenso elevado: mediana de >3,6 (escala de Likert de 5 puntos); ≥80% de las respuestas con nivel de acuerdo «bastante o total» (3 y 4 de escala de Likert); rango intercuartil=1.
El grupo de profesionales que participaron en el estudio cualitativo se limitó a oncología y cuidados paliativos.
ResultadosAnálisis descriptivo. Durante los meses de octubre, noviembre y diciembre de 2010 se produjeron 4.430 (93%) ingresos en el área de urgencias médicas de adultos, 198 (4,15%) en el servicio de hematología clínica y 135 (2,83%) en el servicio de oncología médica (total, 4.763). En este periodo se produjeron en estos servicios 53defunciones relacionadas con el cáncer. De ellos pudimos acceder a información completa relacionada con el último ingreso en 48pacientes y parcial en el total. La falta de acceso a la información se debió a que 4historias clínicas en formato papel no se encontraban en el archivo durante el periodo de revisión de las mismas, y en uno no se encontró la documentación necesaria dentro del sobre que reunía toda la historia clínica.
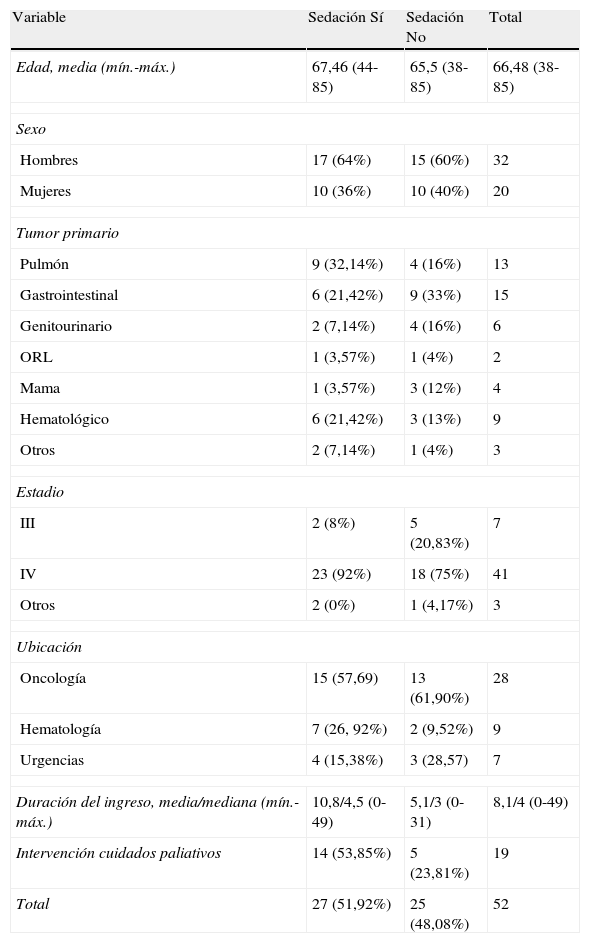
Del total de pacientes fallecidos, 27 (51,92%) recibieron SP como parte de su tratamiento. Las características demográficas y clínicas de los pacientes fallecidos (sedados y no sedados) se pueden apreciar en la tabla 1.
Características demográficas y clínicas de los pacientes analizados
| Variable | Sedación Sí | Sedación No | Total |
| Edad, media (mín.-máx.) | 67,46 (44-85) | 65,5 (38-85) | 66,48 (38-85) |
| Sexo | |||
| Hombres | 17 (64%) | 15 (60%) | 32 |
| Mujeres | 10 (36%) | 10 (40%) | 20 |
| Tumor primario | |||
| Pulmón | 9 (32,14%) | 4 (16%) | 13 |
| Gastrointestinal | 6 (21,42%) | 9 (33%) | 15 |
| Genitourinario | 2 (7,14%) | 4 (16%) | 6 |
| ORL | 1 (3,57%) | 1 (4%) | 2 |
| Mama | 1 (3,57%) | 3 (12%) | 4 |
| Hematológico | 6 (21,42%) | 3 (13%) | 9 |
| Otros | 2 (7,14%) | 1 (4%) | 3 |
| Estadio | |||
| III | 2 (8%) | 5 (20,83%) | 7 |
| IV | 23 (92%) | 18 (75%) | 41 |
| Otros | 2 (0%) | 1 (4,17%) | 3 |
| Ubicación | |||
| Oncología | 15 (57,69) | 13 (61,90%) | 28 |
| Hematología | 7 (26, 92%) | 2 (9,52%) | 9 |
| Urgencias | 4 (15,38%) | 3 (28,57) | 7 |
| Duración del ingreso, media/mediana (mín.-máx.) | 10,8/4,5 (0-49) | 5,1/3 (0-31) | 8,1/4 (0-49) |
| Intervención cuidados paliativos | 14 (53,85%) | 5 (23,81%) | 19 |
| Total | 27 (51,92%) | 25 (48,08%) | 52 |
Entre los pacientes sedados se identificó la presencia de un síntoma etiquetado como refractario como causa de la sedación en 20 de los 26casos de los que disponemos de total información (76,92%). Los síntomas más frecuentes fueron: disnea en 11casos (55%); delirium en 5casos (25%); dolor en 2pacientes (10%), sangrado masivo en un caso (5%), y otros síntomas en un caso (5%). En todos los ellos existió un tratamiento previo para el síntoma que motivó la sedación: 2exclusivamente etiológico, 3sintomático, y 16pacientes recibieron una combinación de tratamientos etiológicos y sintomáticos antes de proponer la sedación como estrategia terapéutica.
El tiempo medio entre la fecha de ingreso y el inicio de la sedación fue de 9,5días, con una mediana de 2 (0-45), y la duración media de la sedación fue de 1,2días (con un rango entre unas horas y 4días). Pudimos identificar el tipo de sedación utilizada en 25casos: sedación en la agonía en 12pacientes (48%), sedación profunda continua en 7pacientes (28%), superficial continua en 3pacientes, superficial intermitente en un paciente y progresiva en 2casos. En ninguna de estas SP existió referencia clara y precisa sobre el tipo de sedación, pero sí se describían sus objetivos.
La media de fármacos utilizados durante la SP fue de 2,6 (mínimo de 1 y máximo de 3). Ello incluía los fármacos sedantes y aquellos cuya finalidad fue controlar síntomas (secreciones, delirium, dolor, disnea). Los medicamentos utilizados fueron: morfina, con una dosis media de 40mg (5 y 120mg/día); midazolam (dosis media de 38,9mg/día, rango entre 5 y 150mg/día); el haloperidol figuraba como tratamiento en 2casos, con dosis entre 5 y 10mg/día; la escopolamina fue utilizada en 16casos, con dosis que variaban entre 0,5 y 1,5mg. La combinación más frecuente fue la asociación de morfina, midazolam y escopolamina (16 casos).
En 20pacientes (76,92%) existió un registro relativo a la solicitud de consentimiento para su inicio. En el 100% de los casos este consentimiento fue verbal. En 6casos (30%) correspondió al paciente, y en 14casos (70%) fue la familia la que otorgó el permiso.
En 22pacientes sedados se identificó un reajuste del resto de medidas terapéuticas coincidiendo con el inicio de la sedación. Ninguno de los pacientes que fueron sedados recibió alimentación parenteral o enteral y 5pacientes recibieron fármacos vasoactivos (en 4casos fueron retirados). Si el tratamiento incluía antibióticos, fueron retirados en todos los casos menos en uno. En 22 de los 26casos no se iniciaron «medidas agresivas», aunque no figuraba expresamente «no iniciar medidas terapéuticas agresivas» en las órdenes de tratamiento. Solo en 10 de los 26casos (38,4%) estaba registrada la indicación de no reanimar en caso de parada cardiorrespiratoria.
El tiempo medio entre la última dosis de quimioterapia y la defunción fue de 82días (mediana de 32días; mínimo 2 y máximo 648días) para los pacientes sedados. La intervención del equipo de cuidados paliativos se produjo en 19casos (40%). Ninguno de ellos procedía del servicio de hematología.
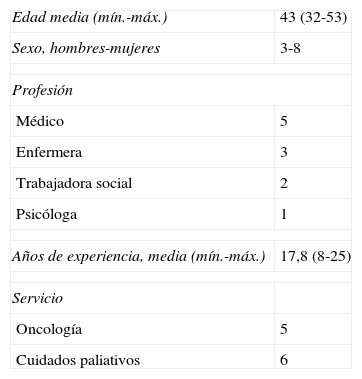
Para el análisis prospectivo cualitativo se solicitó la participaron de 12profesionales sanitarios que desarrollan su actividad en oncología o cuidados paliativos. De ellos, 11completaron el cuestionario inicial y las rondas del proceso Delphi. La tabla 2 recoge las características del grupo que completaron los cuestionarios. Cabe destacar que el perfil multidisciplinar del grupo con importante experiencia profesional. En la tabla 3 se pueden apreciar los datos referidos por los profesionales inicialmente. Se trata de un listado que recoge todas las aportaciones y que valoran los motivos de la sedación, el tipo de sedación, los tratamientos administrados con anterioridad, el grado de participación del propio paciente, y la familia. La redacción de los diferentes ítems revela diferentes sensibilidades y perfiles profesionales.
Listado completo de criterios iniciales
| Motivo de sedación |
| Causas que motivan la sedación |
| Síntoma que motiva la sedación |
| Objetivo de la sedación |
| Situación emocional e historia de pérdidas previas |
| Grado de sufrimiento espiritual/existencial |
| Tipo de sedación |
| Miembros del equipo que participan en la toma de decisiones |
| Extensión de la enfermedad de base |
| Tratamientos oncoespecíficos realizados de manera que quede justificada esta maniobra |
| Tratamientos previos del síntoma |
| Fracaso de los tratamientos previos en el control del síntoma |
| Fármacos utilizados y grado de eficacia |
| Situación cognitiva y funcional actual y previo y velocidad de la pérdida |
| Constatación de las demandas expresas del paciente o la familia |
| Consentimiento explícito o implícito del paciente |
| Titular de la información y el consentimiento |
| Información a la familia de la gravedad, de la proximidad de la muerte y de la ausencia de control sintomático |
| Autorización de la familia |
| Información al paciente y familia de las consecuencias |
| Abordaje de asuntos pendientes antes del inicio de la sedación |
| Existencia o ausencia de diálogo en torno a la sedación |
| Hora de inicio de la sedación |
| Evolución básica de la sedación |
| Soporte de la familia |
| Vivencias de la familia durante la sedación |
| Hora y fecha de la defunción |
La tabla 4 incluye los criterios en su redacción definitiva, a partir de las aportaciones de los participantes. Los ítems se han agrupado en 3 áreas: criterios de selección de pacientes, criterios relacionados con la toma de decisiones y criterios en torno al tratamiento.
Criterios definitivos agrupados en 3 áreas
| A. Criterios de selección |
| Enfermedad avanzada e irreversible |
| Muerte esperable en horas, días o semanas |
| Constatar la presencia de síntomas refractarios a otros tratamientos aceptables para el paciente y con potencial razonable para alcanzar los objetivos de bienestar y señalar cuál/cuáles motivan la sedación |
| Describir el síntoma principal que motiva la indicación de sedación paliativa |
| Abordar la existencia de asuntos pendientes antes de iniciar la sedación |
| B. Criterios en torno a la toma de decisiones y el consentimiento informado |
| Confirmar la existencia de consenso en el equipo médico/acuerdo en sesión clínica |
| Confirmar consenso entre el equipo médico y el equipo de enfermería y otros profesionales |
| Situación cognitiva del paciente y grado de participación en la toma de decisiones |
| Constatar si la familia está involucrada, informada y participa en la toma de decisiones |
| Informar a la familia de la conducta a seguir en torno a la nutrición e hidratación durante el periodo de sedación |
| C. Criterios en torno al tratamiento |
| Establecer el tipo de sedación y el objetivo |
| Selección del fármaco y de la vía |
| Reorientación de las medidas diagnósticas y terapéuticas no centradas en el bienestar (modificar el tratamiento) |
| Disponibilidad de dosis extras o pauta móvil según las necesidades |
| Monitorización del grado de sedación mediante la escala de Ramsay |
| Reevaluación de los síntomas a pesar de que el paciente esté sedado |
| Monitorización de la situación emocional de la familia |
| Cuidados de enfermería con objetivo de bienestar |
El presente trabajo ofrece información sobre el uso de SP en enfermos oncológicos fallecidos: características epidemiológicas, prevalencia y proceso de toma de decisiones. A partir de estos datos, los profesionales implicados en la atención de estos pacientes identifican áreas de mejora y establecen medidas correctoras, mediante técnicas cualitativas.
El primer dato a considerar es la tasa de SP. En los estudios publicados, este parámetro es muy variado (desde el 1 al 72%), con una frecuencia promedio del 25%9. El análisis de la literatura muestra que la frecuencia está influida por el diseño de cada estudio y las definiciones que se emplean. En España se han comunicado frecuencias tan bajas como del 6%, si la SP es solo entendida como tal cuando es profunda y continua10. En nuestro caso, siendo mucho más alta del 6%, es inferior a la descrita por Caraceni et al.4, en cuya serie retrospectiva describen una incidencia del 68% en un entorno latino, como el nuestro. La muestra seleccionada por este autor alcanza las 2.033historias clínicas correspondientes a 5años de actividad en un centro terciario especializado en oncología. La prevalencia que nosotros encontramos fue discretamente mayor a lo publicado por Stone et al.11, quienes señalan una tasa de SP del 26% en 115pacientes atendidos por equipos de cuidados paliativos en un Hospice y en un hospital de agudos de Londres. El porcentaje de SP en los pacientes atendidos en el hospital de agudos fue del 21%. Este autor matiza que hasta el 43% recibieron fármacos sedantes para el control de síntomas. Las características de nuestra revisión y la calidad de los registros no nos permiten establecer estas diferencias, y sería necesario un registro minucioso de la información clínica para poder comparar las 2series con rigor. Puede ser que hayamos calificado de sedaciones algunas maniobras destinadas al control de la angustia u otros síntomas, y que por ello nuestra incidencia sea discretamente más elevada. También los resultados de Boceta Osuna12, en su tesis doctoral, objetivan una incidencia menor a la nuestra. Este autor recoge una prevalencia de SP del 23% de los pacientes atendidos por un equipo de soporte de cuidados paliativos hospitalario. Tal vez si su muestra recogiera fallecidos no atendidos por su equipo, la incidencia sería superior. Alonso-Babarro et al.13, en una revisión retrospectiva de 370pacientes fallecidos en domicilio, encontraron una tasa de sedación del 12% (29pacientes). Posiblemente las defunciones en el domicilio corresponden a pacientes con alto nivel de control sintomático y causadas por una insuficiencia de órgano lentamente progresiva. Ello puede justificar una menor necesidad de SP. Los casos con síntomas más complejos no suelen permanecer en el domicilio, por lo que la sedación, en caso de producirse, lo hará en un entorno hospitalario o sociosanitario.
En lo relativo al síntoma que motiva la SP, nuestra serie parece coincidir con la investigación de Boceta Osuna12 que recoge, por frecuencia: disnea (75,5%), delirium (47,7%), dolor (31,1%). Este autor objetiva hasta el 21,1% de sufrimiento psicológico refractario. En la misma línea, el trabajo de Alonso-Babarro et al13. señala como principales motivos de SP: delirium (62%) y disnea (14%). Esta menor incidencia de disnea parece corroborar la idea de que el paciente con importante sintomatología respiratoria es remitido o acude por iniciativa propia a un hospital. Los resultados de Stone et al11. difieren, ya que señalan como causas de sedación y por orden de frecuencia: delirium, angustia, dolor y disnea. Sorprende que la revisión de Mercadante et al.9 presente como causa de sedación el síntoma dolor.
Estas diferencias pueden deberse a lo impreciso de la definición de «síntoma refractario» y su relación con el «sufrimiento intolerable». Estos términos no quedan completamente aclarados en las recomendaciones de la EAPC3. Para los equipos de cuidados paliativos puede no ser difícil identificar el síntoma refractario cuando se conoce la evolución del enfermo, o se analiza su trayectoria clínica y los procedimientos diagnósticos/terapéuticos desarrollados. No obstante, un síntoma difícil puede ser etiquetado de refractario en manos inexpertas2,8,14. Otra explicación que puede justificar estas diferencias puede relacionarse con las peculiaridades culturales. En el trabajo de Fainsinger et al.14 la comparación de 4unidades de cuidados paliativos situadas en 3países tan diferentes como Israel, Sudáfrica y España reconoce esta diversidad, tanto en la frecuencia de sedaciones (15% de Israel y 36% en Sudáfrica) como en los motivos de la misma (delirium de predominio en Sudáfrica, disnea y estrés existencial en España). Posiblemente cada cultura se enfrenta a la muerte de manera diferente. Los países anglosajones han sido pioneros en el desarrollo del principio de autonomía y en la participación del paciente en la toma de decisiones. Por el contrario, en la cultura latina se mantiene la idea de «proteger al enfermo» evitándole las malas noticias. Es posible que este trasfondo cultural diferente influya en la indicación de SP.
En cualquier caso, parece existir un importante consenso en torno a la indicación de SP en caso de disnea refractaria o delirium. No parece existir tanto acuerdo en cuanto al uso de SP para tratar el sufrimiento emocional o existencial15,16. La sedación por causas psicológicas plantea más dificultades de orden ético. La refractariedad de un síntoma físico es más fácil de medir y objetivar que el concepto de sufrimiento emocional. Este depende, en mayor medida, de las subjetividades, las actitudes ante la vida y las capacidades de cada sujeto, así como de la disponibilidad de profesionales capacitados para atender adecuadamente las necesidades emocionales y espirituales de los pacientes antes de considerar refractario su sufrimiento17,18.
En nuestra serie existía una referencia expresa a la solicitud de consentimiento informado en el 75% de los casos; como en el caso de Boceta Osuna12, este fue mayoritariamente otorgado por la familia en representación y tuvo carácter oral. En el trabajo de Alonso-Babarro et al.13. se señala que el 45% de pacientes y sus familias participaron en la decisión de iniciar la sedación. Este porcentaje aumenta si se tiene en consideración que en otro 45% de casos fue la familia la que directamente se involucró en la toma de decisiones. En 3casos de nuestro estudio no se encontró la documentación relacionada con el proceso de toma de decisiones. La ausencia del registro no equivale a ausencia de consentimiento, pero hace que la historia clínica pierda calidad. Diversos factores explican que sea la familia la interlocutora y la que tome las decisiones. Así, la situación de alta fragilidad del paciente, la presencia de delirio o disnea intensa (que, mantenida en el tiempo, conduce a deterioro cognitivo) y el impacto emocional constituyen circunstancias que limitan la competencia del enfermo por su vulnerabilidad física, cognitiva y emocional. Para evitar este hecho sería importante contar con una planificación anticipada de cuidados en la que el paciente, en una situación clínica de mayor estabilidad, participe en la toma de decisiones. No obstante, este proceso es hoy en día muy poco frecuente porque genera gran impacto en profesionales, enfermos y familiares. En algunos casos es entendido como un desahucio o una anticipación del final. En ninguna de las historias revisadas existía copia, registro o referencia al documento de voluntades anticipadas. En nuestro entorno, son muchos los que prefieren pensar que no morirán nunca y por tanto no desean hablar de ello. En estos casos también deberemos respetar el principio de autonomía.
En el contexto de cuidados paliativos el consentimiento escrito es difícil de obtener, y puede ser poco sensible, inoportuno o incluso nocivo. El consentimiento verbal podría considerarse suficiente, pero se considera imprescindible que quede registrado en la historia clínica19.
Es importante considerar que la SP es una maniobra terapéutica propuesta por el equipo después de un cuidadoso juicio clínico. Si el paciente es quien solicita la SP, ello suele indicar la existencia de un gran estrés, y dicha demanda debe afrontarse de forma atenta, sensible y profesional.
Los fármacos utilizados no difieren a los referidos en la literatura2,8,13,14,20. No obstante, llama la atención que, siendo el delirium la segunda causa de sedación, neurolépticos como el haloperidol fueran fármacos poco empleados. Una explicación sería que la SP se indica ante el fracaso de neurolépticos, clásicos o modernos, utilizados previamente.
Un dato que invita a la reflexión es el tiempo transcurrido entre la última quimioterapia y el inicio de la SP. La mediana de tiempo se sitúa en torno a 30días. Resulta un poco contradictorio que pacientes que fallecen sedados recibieran un tratamiento intensivo 30días antes. Es complejo planificar de forma anticipada los cuidados cuando facultativo, paciente y familia mantienen expectativas poco ajustadas a la realidad. Aunque no disponemos de herramientas capaces de establecer un pronóstico exacto21,22, deberíamos valorar a cada enfermo globalmente y pensar en términos de calidad de vida.
En lo relativo a la duración de la sedación, nuestros datos no difieren de lo publicado por Alonso-Babarro et al.13 (2días y medio, con un rango entre 1 y 10) o lo publicado por Boceta Osuna12, quien la calcula en horas, señalando una media de 54,67h, con un rango entre 4 y 576h. Estos datos también concuerdan con la revisión sistemática de Mercadante et al.9. En la comparación de varios países desarrollada por Fainsinger et al.14 la duración media oscila entre los 1,9días de Israel y los 3,2 de España. En el caso de Maltoni et al.23 la duración media es discretamente mayor: 4días.
No hemos encontrado datos relativos a la frecuencia en el ajuste del tratamiento previo o en la limitación de algunas terapias. Parece importante discutir estos aspectos con los pacientes que lo deseen y con sus familias, para evitar malos entendidos y sentimientos de abandono terapéutico o culpabilidad, como recomienda el documento publicado por la National Hospice and Palliative Care Organization20. En el caso de sedación en la agonía, todo el tratamiento debería orientarse hacia el bienestar y deberíamos revisar la indicación y vías de administración de los fármacos que cada paciente recibe. En el caso de SP, deberemos diferenciar aquellos casos en los que se prevé que la sedación se mantendrá hasta la defunción y aquellos casos en los que se establece hasta el control de un síntoma.
Los trabajos de Fainsinger et al.14, Stone et al.11, Boceta Osuna12 y Alonso-Babarro et al.13 recogen las SP desarrolladas en pacientes atendidos por equipos específicos de cuidados paliativos. Nosotros hemos ofrecido los resultados procedentes de una muestra de pacientes fallecidos en nuestro centro, atendidos o no por el equipo de cuidados paliativos. Dado que la SP tiene importantes connotaciones bioéticas, parece oportuno que la toma de decisiones en torno a ella sea consensuada dentro del propio equipo terapéutico y cuente con la validación de un observador externo habituado a la gestión del sufrimiento. En cualquier caso, la disponibilidad horaria del equipo de cuidados paliativos no es universal, por lo que asumimos que la consulta al equipo de cuidados paliativos no será nunca del 100%. Los profesionales que han acompañado al paciente y a su familia durante toda la enfermedad dispondrán de la mayor y mejor información relativa al enfermo. No obstante, la sobreimplicación que genera esta atención y el sufrimiento que produce un pronóstico infausto pueden condicionar la toma de decisiones. Los fenómenos de contratransferencia, en la proximidad de la muerte, pueden suscitar sentimientos de frustración y ansiedad que magnifiquen el sufrimiento del paciente y nos condicionen una sedación que tal vez no es precisa.
A partir de la discusión de estos resultados, consideramos que el registro era claramente mejorable y pusimos en marcha la segunda fase del proyecto. Esta discusión y el proceso de consenso de desarrolló con una parte de los profesionales (oncología y cuidados paliativos). Los profesionales de hematología y urgencias quedaron al margen del consenso para poder actuar como grupo control en el futuro. Se invitó a participar en la fase Delphi a aquellas personas habitualmente implicadas en la toma de decisiones en torno a la SP. Debido al interés del tema, la respuesta fue muy favorable. Lo reducido del grupo facilitó la participación, aunque limitó la posibilidad de discrepancias. No obstante, consideramos esta fase de la investigación como una prueba piloto, de cara a emplear esta metodología con un mayor número de servicios y profesionales en el futuro.
Las respuestas obtenidas en la fase abierta de la consulta fueron muy adecuadas y coincidentes, mayoritariamente centradas en la indicación del procedimiento, sus causas, el grado de participación de paciente y familia en la toma de decisiones y el impacto emocional que el procedimiento despierta en la familia.
Tras la primera consulta, el grado de acuerdo fue muy alto o alto en 8 de los 16ítems propuestos. En algunos ítems inicialmente existió una cierta dispersión en las respuestas, que se redujo a medida que avanzó el proceso Delphi. Las aportaciones de los participantes permitieron introducir modificaciones en la redacción de algunos criterios, así como introducir otros. El listado final de registros nos parece ponderado y respetuoso con los principios bioéticos, coherentes con las recomendaciones de la EAPC3, el Comité de Ética de Cataluña24 y la fundación Grifols i Lucas25, y comparables con los de otros autores, como Boceta Osuna12 y Alonso-Babarro et al.13.
Pese a todo lo anterior, nuestro trabajo no está exento de limitaciones, ya que se basa en una revisión retrospectiva sobre el registro escrito tanto informático como en papel. Estos resultados no reflejan directamente la actividad asistencial. Los clínicos hacemos muchas más cosas de las que registramos, y es difícil trasladar al papel todos los detalles del diálogo con un paciente y/o su familia en torno a la sedación. Si a ello añadimos la urgencia que precisa esta decisión en algunas ocasiones y la premura de tiempo con la que cuentan los profesionales para ello, es fácil entender que los registros sean, en ocasiones, casi telegráficos. Cabe añadir que el periodo temporal seleccionado corresponde, en nuestro hospital, a una fase de transición entre la historia clínica en papel y los registros informatizados, por lo que ha sido necesario revisar tanto las historias clínicas informatizadas (curso clínico e informes de alta) como los registros en papel (registros de enfermería, hojas de tratamiento, etc.). Sin duda ello dificulta una exhaustiva redacción. Otros autores también señalan estas limitaciones en trabajos de similares características8. No obstante, la historia clínica es un documento legal y somos los clínicos los máximos responsables de su calidad26. Por ello entenderemos como un síntoma de nuestra realidad clínica cotidiana los resultados de este trabajo, y por tanto un estímulo para introducir medidas de mejora.
Una segunda limitación puede residir en los criterios de selección de la muestra. Dado que la SP no es un procedimiento que requiera una notificación o codificación específica, no es posible identificar todos los pacientes sedados, y debemos buscar criterios indirectos de selección de la muestra. Seleccionar a los pacientes fallecidos excluye las posibles sedaciones intermitentes desarrolladas para el control de un síntoma y cuya evolución no se asocia a la defunción del paciente. Otra limitación es el tamaño de la muestra. Hemos seleccionado los pacientes con enfermedades oncológicas ubicados en los servicios de oncología, hematología y urgencias. Somos conscientes de que en todo tipo de pacientes y patologías, así como en muchos otros servicios, puede iniciarse una sedación. Los profesionales de oncología están más habituados a considerar los cuidados paliativos como parte de su tratamiento y pobremente son capaces de identificar los estadios avanzados de la enfermedad oncológica, frente a otras patologías como la insuficiencia respiratoria crónica o la insuficiencia cardiaca crónica. También debemos considerar que la sedación, como procedimiento terapéutico, se aplica también a nivel domiciliario, tanto por los equipos específicos de cuidados paliativos como por los médicos de familia. Nuestros resultados no son, por ello, una foto de lo que está ocurriendo en nuestro hospital o en el ámbito sanitario en general, sino una pista, o algunas piezas de un puzzle mucho más complejo y que requeriría una metodología más compleja para aportar conclusiones extrapolables.
A partir de todo lo anterior, podemos concluir:
- -
La calidad del registro clínico en torno a la selección, la toma de decisiones y el tratamiento en los casos de sedaciones al final de la vida es claramente mejorable en nuestro centro. Los registros en torno a la medicación y las vías de administración fueron rigurosos.
- -
En torno a la mitad de los pacientes oncológicos que fallecen en los servicios de urgencias, oncología o hematología clínica lo hacen sedados (SP o sedación en la agonía).
- -
En la población estudiada, el perfil más frecuente del paciente sedado corresponde a un varón de 65años, afecto de una neoplasia pulmonar o gastrointestinal avanzada que presenta disnea y/o delirium, participa poco en la toma de decisiones y fallece a las 24h de iniciada la sedación.
- -
Dada la necesidad de mejorar el registro relativo a los criterios de selección, el proceso de toma de decisiones y las opciones de tratamiento, hemos consensuado una plantilla a modo de check list que los profesionales podrán consultar cuando se planteen una sedación al final de la vida. Dicha lista contempla los requisitos de selección, del proceso de toma de decisiones con la participación del enfermo y/o sus representantes, y de la evolución de la sedación.
Nos queda pendiente incorporar el check list a nuestra práctica clínica habitual y evaluar si modifica el registro en los casos de SP, pero eso formará parte de futuras investigaciones.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Este artículo se presentó como trabajo de fin de Máster de Bioética, Universidad Ramon Llull, Barcelona, edición 2009-2011.