La reducción de la radiación ionizante (RI) en el niño es fundamental por distintas causas. Ante una exposición a la misma dosis de radiación, el riesgo de desarrollo de un tumor es mayor en la infancia. Varias estrategias pueden emplearse para reducir la RI. La fundamental es evitar la realización de pruebas innecesarias o no indicadas, elegir una prueba alternativa que no utilice RI, y/o tomar una serie de medidas que reduzcan al máximo la dosis recibida por el paciente, como evitar repetir pruebas, emplear las proyecciones correctas, usar protector, ajustar el protocolo (mAs, Kv o pitch) al volumen del paciente, etc…
En ecografía, se pueden utilizar contrastes sonográficos de uso endocavitario, aunque también se está extendiendo para uso endovascular. En fluoroscopia se deben utilizar de baja osmolaridad, como en TC donde ajustaremos la dosis y la velocidad de inyección al peso del paciente y calibre de la vía periférica respectivamente. En RM tan sólo están aprobados para utilización pediátrica tres tipos de contrastes. En ciertas situaciones clínicas es necesaria la utilización de dosis dobles o de contrastes organoespecíficos, indicaciones que aun no estando probadas en términos de seguridad farmacológica pueden emplearse como uso compasivo.
It is essential to minimize exposure to ionizing radiation in children for various reasons. The risk of developing a tumor from exposure to a given dose of radiation is greater in childhood. Various strategies can be used to reduce exposure to ionizing radiation. It is fundamental to avoid unnecessary tests and tests that are not indicated, to choose an alternative test that does not use ionizing radiation, and/or to take a series of measures that minimize the dose of radiation that the patient receives, such as avoiding having to repeat tests, using the appropriate projections, using shields, adjusting the protocol (mAs, Kv, or pitch) to the patient's body volume, etc…
When contrast agents are necessary, intracavitary ultrasound agents can be used, although the use of ultrasound agents is also being extended to include intravenous administration. In fluoroscopy, contrast agents with low osmolarity must be used, as in CT where we must adjust the dose and speed of injection to the patient's weight and to the caliber of the peripheral line, respectively. In MRI, only three types of contrast agents have been approved for pediatric use. It is sometimes necessary to use double doses or organ-specific contrast agents in certain clinical situations; the safety of contrast agents for these indications has not been proven, so they must be used off label.
Todos estamos expuestos continuamente a la radiación ionizante. El promedio de dosis efectiva en la población española es de aproximadamente 3,7 mSv/año1, de los cuales 2,4 mSv/año2 provienen de materiales radiactivos naturales y de la radiación cósmica del espacio (dosis de fondo natural). La dosis efectiva restante proviene fundamentalmente de la derivada de usos médicos, que para cada miembro de la población de un país de nivel sanitario I es de 1,28 mSv/año2, y de ellos 1,2 mSv/año se deben a técnicas de diagnóstico con rayos X y 0,08 mSv/año a medicina nuclear.
La tasa de dosis de radiación anual derivada de usos médicos está regulada por las directivas europeas vigentes (Directiva 2013/59 EURATOM), que recomiendan se encuentre en torno a 1 mSv/año per caput. Gracias al proyecto DOPOES3,4 se conoce la media per caput de dosis efectiva recibida en procedimientos diagnósticos en España (datos recogidos hasta 2010), que es de 0,97±0,35 mSv/año, similar a la de los países de nuestro entorno y que cumple la citada normativa. Esto supondría una dosis acumulada media a lo largo de la vida de unos 200 mSv.
Los efectos nocivos de la radiación a altas dosis están bien documentados. En general se trata de efectos deterministas dependientes de la dosis y consecuencia de la muerte de un gran número de células en un tejido u órgano.
En términos de protección radiológica, una dosis baja es aquella inferior a 0,2Gy (tasa de dosis inferior a 0,1 mGy/min), a la que es muy improbable que ocurra más de un evento de absorción de energía de la radiación antes de que puedan actuar en ella los mecanismos de reparación. Las medias poblacionales descritas con anterioridad, entre las que se incluyen las derivadas de usos médicos, se corresponden con tasas de dosis bajas.
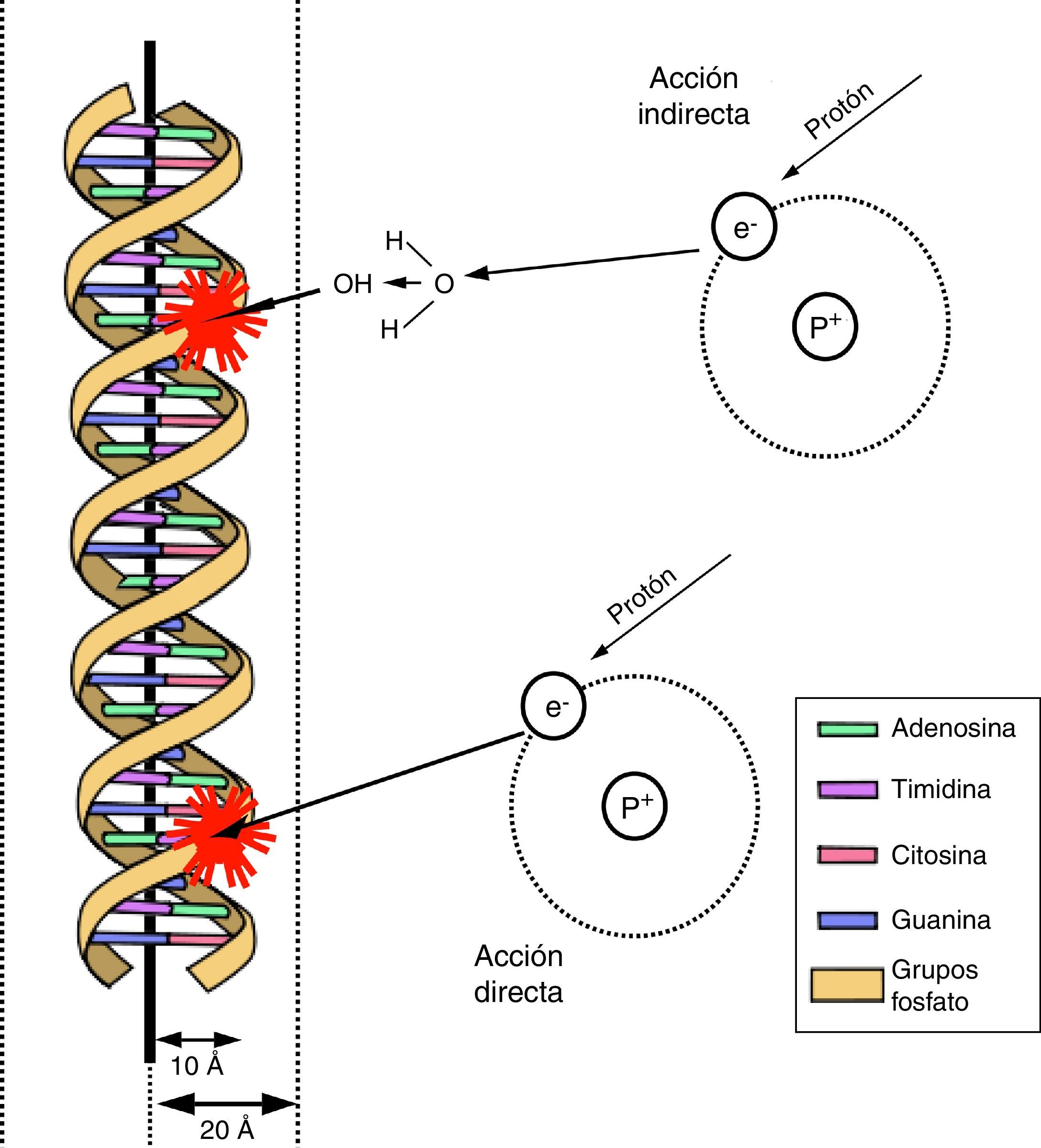
Respecto a este tipo de dosis, y para explicar sus efectos biológicos, las entidades reguladoras han adoptado un modelo conocido como «lineal sin umbral» (LNT, lineal no-threshold), que se basa en la hipótesis de que la radiación siempre es perjudicial para el ser humano, incluso a dosis infinitesimales. Para estas dosis pueden producirse efectos estocásticos o probabilísticos que se deben a mutaciones no reparadas sin muerte celular (fig. 1), de tal forma que es posible que induzcan cambios somáticos o cambios hereditarios. Esta mutación, que puede ser única o bien acumularse sin ser reparada a lo largo de los sucesivos ciclos celulares (y así sumarse a antiguas o nuevas mutaciones), puede dar lugar a la aparición de una célula que finalmente se convierta en cáncer. La probabilidad de aparición de estos efectos, aunque no su gravedad, depende de la dosis, de modo que, a mayor dosis, mayor número de mutaciones no reparadas y, por tanto, mayor probabilidad de efectos nocivos.
Mecanismo de acción de las radiaciones ionizantes. La acción directa de la radiación ionizante sobre los átomos produce un electrón secundario, resultante de la absorción de un fotón, alterando la estructura química del ADN. En la acción indirecta, un electrón secundario interacciona con la molécula de agua y produce un radical libre OH- que altera la estructura del ADN. El daño resultante puede ser reparado con cierta eficacia si solo afecta a un haz de la hélice; cuando afecta a la doble hélice resulta en un daño no reparable con eficacia.
Continuamente se está cuestionando el modelo LNT, apuntando la posibilidad de que la radiación a bajas dosis carezca de efectos perjudiciales, aunque a falta de un mayor número de resultados experimentales que lo sustenten se sigue aceptando que las radiaciones ionizantes pueden producir efectos nocivos a cualquier dosis5.
Mayor susceptibilidad a la radiación de la población pediátricaSea como fuere, parece claro que durante la edad pediátrica hay mayor susceptibilidad a ciertos efectos de las radiaciones ionizantes3,6. Esto se debe a varios factores:
- •
Cuanto menor es el tamaño de un órgano o de una parte del cuerpo, mayor es la dosis absorbida (energía depositada por unidad de masa, en Gy).
- •
Los efectos de la radiación son mayores en los organismos en desarrollo. Las tasas de crecimiento de diversos órganos durante la infancia son más altas, como las del tejido linfoide, el tejido cerebral y el tejido gonadal.
- •
Mayor esperanza de vida. Los efectos debidos a la radiación son acumulativos y pueden persistir muchos años tras un evento determinado.
Los efectos de la radiación en la edad pediátrica pueden resumirse como sigue7:
- •
En los fetos, la radiación puede inducir la muerte, la aparición de malformaciones diversas, retraso del crecimiento o retraso mental. La anomalía encontrada con más frecuencia en fetos supervivientes de accidentes nucleares ha sido microcefalia y retraso mental grave. El riesgo de desarrollar retraso mental grave se estima en un 40% de los fetos de 8-15 semanas de gestación expuestos a dosis de 1Sv, que disminuye al 10% en fetos de 16 a 25 semanas de gestación respecto a fetos no expuestos. Este efecto es determinista y posiblemente se produce a partir de 0,2Gy de umbral inferior.
- •
El óbito fetal puede producirse fundamentalmente cuando el evento de radiación se produce en la fase de preimplantación (0 a 9 días posconcepción). Es un efecto probabilístico y posiblemente carece de umbral inferior.
- •
Riesgo de cáncer radioinducido. Este riesgo es probabilístico y posiblemente carece de umbral inferior. La población general sometida a dosis bajas presenta un coeficiente de riesgo medio de cáncer radioinducido del 5%7. En la edad pediátrica este valor aumenta a un 16% por Sv en las niñas y a un 12% por Sv en los niños en la primera década de la vida. Este riesgo no se refiere a todos los tumores, sino a aproximadamente un 25% de ellos: cáncer de tiroides, cáncer cerebral, leucemia, cáncer de mama y cáncer de piel3. Parece claro también que el riesgo de cáncer sólido radioinducido persiste hasta 50 años después de la exposición8. Por debajo de 50 mSv los datos epidemiológicos resultan contradictorios, aunque muchos autores6,9 coinciden en que dosis en el rango de 5 a 125 mSv resultan en un incremento bajo, pero estadísticamente significativo, del riesgo de cáncer radioinducido.
- •
Defectos genéticos heredables: riesgo del 0,2% por Sv respecto a la población general.
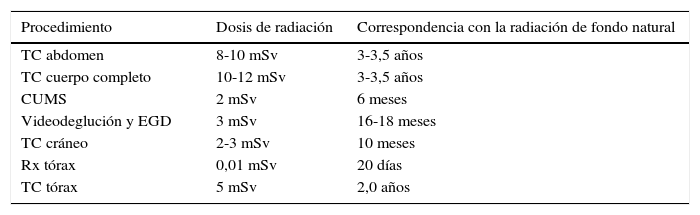
Aproximadamente el 3-10% de todos los procedimientos que utilizan radiación ionizante en los países desarrollados se realizan en niños3. En la tabla 1 se indican las equivalencias medias a la dosis natural de fondo por procedimiento radiológico.
Equivalencia de dosis de técnicas de imagen habituales que emplean radiaciones ionizantes con la radiación natural o de fondo
| Procedimiento | Dosis de radiación | Correspondencia con la radiación de fondo natural |
|---|---|---|
| TC abdomen | 8-10 mSv | 3-3,5 años |
| TC cuerpo completo | 10-12 mSv | 3-3,5 años |
| CUMS | 2 mSv | 6 meses |
| Videodeglución y EGD | 3 mSv | 16-18 meses |
| TC cráneo | 2-3 mSv | 10 meses |
| Rx tórax | 0,01 mSv | 20 días |
| TC tórax | 5 mSv | 2,0 años |
CUMS: cistouretrografía miccional seriada; EGD: esofagogastroduodenoscopia; mSv: milisievert; Rx: radiografía simple; TC: tomografía computarizada.
En los últimos años, diversas sociedades radiológicas internacionales (European Society of Radiology [ESR], American College of Radiology [ACR], Radiological Society of North America, entre otras) han puesto en marcha campañas de reducción de dosis, como Eurosafe Imaging, Image gently, Image wisely o Radiation Protection of Patients. Esa misma línea sigue la toma de posición conjunta de la Organización Mundial de la Salud y el Organismo Internacional de Energía Atómica en el documento Bonn Call-for-action, y la Estrategia de seguridad del paciente del Sistema Nacional de Salud. Periodo 2015-2020 aprobada por el Ministerio de Sanidad, Servicios Sociales e Igualdad en 2015. En este sentido, la Sociedad Española de Radiología Médica (SERAM) ha elaborado un documento, publicado en septiembre de 2015, titulado Posición SERAM sobre los riesgos asociados a las dosis de radiación utilizadas en las exploraciones practicadas en radiodiagnóstico (consultado en octubre de 2015 y disponible en la página web de la sociedad, http://www.seram.es). En la tabla 2 se exponen los axiomas fundamentales extraídos de este documento10.
Pilares básicos en radioprotección adoptados por la Sociedad Española de Radiología Médica
| Práctica radiológica adecuada | • Desarrollada en texto |
|---|---|
| Formación en radioprotección | • Formar a los técnicos para que sean capaces de aplicar protocolos de exploración que reduzcan la dosis administrada manteniendo la calidad de la misma10. • Formar, tanto a los radiólogos como a los profesionales que solicitan pruebas diagnósticas, en la conciencia de los riesgos de carcinogénesis asociados a las radiaciones ionizantes, para que extremen su diligencia en la adecuada justificación de las exploraciones y en la elección preferente o alternativa de las que no usan radiaciones ionizantes (Directiva 2013/59/EURATOM del Consejo de 5 de diciembre de 2013). |
| Información a la población | • Informar al público sobre el riesgo estimado que entrañan las pruebas de diagnóstico médico y los beneficios esperados de ellas en cada caso, y especialmente a los pacientes, dentro de los principios derivados de la Ley de Autonomía del Paciente. Esta información puede evitar una de las fuentes de exploraciones no justificadas, que es la presión del paciente y sus familiares en el marco de la medicina defensiva. • Hacer accesible al paciente la información sobre la dosis recibida con cada exploración, así como de su historia dosimétrica y lo que ello supone, siguiendo lo establecido por la Directiva 2013/59/EURATOM del consejo de 5 de diciembre de 2013. |
| Medidas sobre el equipamiento | • Utilización del equipamiento más adecuado en cada momento, y en concreto de aquel que permita una mayor reducción de la dosis al paciente. • Actualizar la tecnología para permitir obtener las exploraciones con calidad diagnóstica con la menor dosis posible. Los equipos que produzcan una exposición significativamente superior a la permitida deben ser sustituidos y su uso evitado, especialmente en la población más sensible. • Implementación y actualización del software de los equipos, de modo que permita instalar alarmas y avisos de dosis en tiempo real adecuadas a cada paciente, especialmente dirigidas a la población pediátrica. • Disponer en el historial clínico del paciente de su dosis histórica, de modo que sea accesible y obligatoriamente visible para el médico peticionario al realizar la prescripción y al radiólogo al realizar la exploración. • Optimización del equipamiento y de los protocolos de exploración para hacer que la dosis administrada en cada equipo y en cada exploración sea la menor posible. Todo equipo debe ser supervisado por un físico médico especialista. |
En lo que concierne al especialista en diagnóstico por la imagen, deberían aplicar los siguientes principios generales de radioprotección:
- –
Justificación:
- •
No realizar nunca una exploración radiológica no justificada que implique radiación ionizante, sustituyéndola siempre que sea posible por una técnica que no emplee radiación, como la resonancia magnética (RM) o la ecografía.
- •
Deben revisarse las peticiones que impliquen radiación ionizante. No aceptarlas de forma automática.
- •
Utilizar guías clínicas, protocolos o sistemas de ayuda a la decisión siempre que sea posible. De esta necesidad emanan documentos como Recomendaciones SERAM de No Hacer, publicado por la SERAM en diciembre de 2014, o Appropiateness Criteria, publicado por el ACR (consultado en octubre de 2015).
- •
- –
La aplicación del criterio ALARA (tan bajo como razonablemente sea posible): utilizar técnicas y protocolos de exploración con una dosis tan baja como sea posible para mantener una calidad de exploración suficiente.
- –
Precaución en la protección de los pacientes: ajustar los parámetros de radiación al volumen del paciente, utilizar protectores de plomo o bismuto, etc.
- –
Aplicación del modelo LNT para la evaluación de riesgos de las radiaciones ionizantes.
La radiografía simple (Rx) sigue siendo una exploración ampliamente utilizada en pediatría. En un estudio a gran escala realizado en cinco grupos poblacionales representativos en los Estados Unidos11 se comprobó que, combinando todos los estudios convencionales, un niño puede haberse sometido a siete estudios radiológicos o más antes de los 18 años de edad (asumiendo que fueran Rx de tórax, esto supone unos 140 días de radiación de fondo).
La radiología digital, en sus distintas modalidades, ha sustituido en gran medida a la radiología convencional placa-película, y aunque las imágenes digitales pueden adquirirse con dosis bajas, sin una atención cuidadosa los factores de exposición pueden aumentar con el tiempo y dar lugar a una sobreexposición. Esto se debe en gran parte al posprocesado de las imágenes, ya que las imágenes subexpuestas conllevan un ruido o granulado que puede requerir la repetición de pruebas. El aumento de la exposición reduce el ruido, y el técnico, para evitar la repetición de pruebas, puede acostumbrarse a sobreexponer las imágenes. El posprocesado de las mismas evita que el radiólogo lo reconozca, y ello resulta en una exposición innecesaria y continuada, y en un daño potencial para el paciente. Algunos estudios apuntan una sobreexposición hasta en el 43% de las radiografías digitales pediátricas12.
Otro de los problemas que se presentan con la radiología digital es la posibilidad de no colimar, ya que puede adquirirse la imagen y recortarla posteriormente. En una publicación reciente, en torno al 50% de los técnicos reconoció el uso de esta herramienta el 75% de las veces13. La ausencia de colimación incrementa de manera innecesaria la exposición en las partes que anatómicamente no estaban incluidas en el estudio, y aumenta el producto dosis por área.
Después de la exposición y la colimación, el tercer factor importante es la adecuada inmovilización. En pediatría este factor probablemente condiciona el resto de la prueba, ya que una adecuada inmovilización proporciona una mejor colimación y un mayor control de los factores de exposición, aumentando la calidad de la imagen y disminuyendo la necesidad de repetición de pruebas.
En la tabla 3 se detallan las medidas que pueden emplearse para disminuir la dosis de radiología digital en pediatría.14–17
Medidas de radioprotección en radiología digital
| Medida | Factor que disminuye |
|---|---|
| Emplear una colimación ajustada | Esto disminuye el PDA y la radiación dispersa, lo que aumenta la calidad de la imagen y mejora el posterior procesado de la imagen y la medición de dosis. |
| Inmovilización adecuada | Esto disminuye la necesidad de repetición de pruebas, y mejora la colimación y la calidad de la imagen. |
| No emplear la parrilla antidifusora en partes del cuerpo <10-12cm ni densidad aire (en Rx de tórax) | El empleo de la parrilla antidifusora duplica o triplica los factores de exposición necesarios para obtener una imagen de calidad adecuada, y no mejora el ruido en partes del cuerpo<10cm y densidad aire14. |
| Emplear las proyecciones adecuadas y reducirlas al mínimo necesario | Por ejemplo, es innecesario realizar dos proyecciones de tórax en pediatría, siendo excepcional la Rx de tórax lateral; la proyección PA en vez de AP en la pelvis y el tórax disminuye la dosis de radiación gonadal y mamaria. |
| Utilizar adecuadamente los protectores gonadales | En los varones deben emplearse siempre para proteger los testículos; en las niñas se emplearán, por ejemplo, para el estudio de las caderas, pero no en los estudios de abdomen15. |
| En general, no se recomienda para ciertos estudios pediátricos el uso de programas anatómicos prefijados ni de exposimetría automática | El uso de la exposimetría automática en radiografías de partes muy pequeñas o Rx en neonatos no es útil, debido a que en estos casos, incluso utilizando un solo foco, este es mayor que la parte del cuerpo a estudiar, de tal modo que la lectura de datos no es correcta e induce errores en la calidad de imagen, etc. En el niño es mejor el empleo de técnicas manuales controlando factores como Kvp, mA y tiempo de exposición en función del volumen corporal, creando si es posible unos parámetros o «cartas» de referencia en cada centro. Son muy útiles las dosis de referencia publicadas. |
| Familiarizarse con los factores de exposición para evitar la sobreexposición; los fabricantes deben implementar los nuevos parámetros de exposición de la IEC16 | Es de gran utilidad conocer estos parámetros en cada prueba, que deberían grabarse en el almacenamiento de imágenes DICOM para poder visualizarlas. Los fabricantes se comprometieron, en el Image Gently Digital Radiography Summit de 2010, y ha sido publicado, a adoptar los parámetros IEC17, ya que especialmente el índice de desviación es un indicador muy útil que sirve de retroalimentación a técnicos y radiólogos, e indica si la exposición ha sido correcta o no (ID ≥ −1 o ID ≤ +1). |
AP: anteroposterior; IEC: International Electrotechnical Commission; kVp: kilovoltaje-pico; mA: miliamperio; PA: posteroanterior; PDA: producto dosis área; Rx: radiografía simple.
El empleo de la tomografía computarizada (TC) para diagnóstico en pediatría ha aumentado desde la década de 1990, debido fundamentalmente a los avances técnicos. Sin embargo, se ha incrementado la dosis de radiación en la edad pediátrica, en especial por el aumento de las TC que emplean mayores dosis, como los estudios cardiacos o de abdomen/pelvis. Minglioretti et al.18 apuntan que hasta un 25% de la población pediátrica con una sola TC de abdomen/pelvis ha recibido una dosis de 20 mSv o más, lo que supone un riesgo de cáncer inducido de 1/300-390 exploraciones realizadas en niñas. Un estudio19 encontró que los niños que recibieron una dosis en el cerebro acumulada de al menos 50 mGy presentaban 2,8 veces mayor riesgo de neoplasias cerebrales.
El riesgo de aparición de cánceres inducidos por la radiación puede disminuir en gran medida si se implementan las siguientes estrategias de reducción de la dosis:
- •
Disminución del miliamperaje por segundo (mAs) en función del tamaño corporal, que presenta una relación lineal con la radiación, de tal manera que un porcentaje de reducción del mAs del 20% conlleva un porcentaje de reducción de dosis del 20%.
- •
Aumento del factor de paso o pitch por encima de 1. Un aumento del pitch de 1 a 1,5 puede reducir la dosis en un 33%. No obstante, algunos modelos de TC compensan el aumento del pitch con el mAs, permaneciendo la radiación constante20.
- •
Disminución del kilovoltaje. Diversos estudios han demostrado que al seleccionar 80kV en lugar de los 120-130kV habituales se obtienen reducciones de dosis del 25-40% sin que se afecte el diagnóstico21. Ciertos equipos disponen de una opción de selección automática del kilovoltaje, que aplica la información sobre la atenuación extraída del escanograma en función de la indicación elegida. También algunos fabricantes han incorporado un sistema de modulación automática del kilovoltaje similar a los de modulación de mAs22.
- •
Inmovilización, centrado y cobertura de estudio. En los estudios de TC pediátricos es fundamental una adecuada inmovilización, que resulta en una disminución de los artefactos por movimiento, en un cierto efecto tranquilizador, en una disminución de la necesidad de repetición y en unos adecuados centrado y selección del área anatómica a estudiar. Un centrado incorrecto puede incrementar la dosis hasta en un 13%23. Por otra parte, en muchos estudios pediátricos puede limitarse la cobertura exclusivamente al área anatómica de interés, intentando evitar el solapamiento y reduciendo así la dosis de radiación. En algunas indicaciones debería limitarse la TC al área anatómica de interés, como en las TC de tórax para pectus excavatum o las de pelvis para la displasia de caderas operada, entre otras. Con el fin de reducir la dosis de radiación procedente de los extremos de la hélice, que no contribuyen a la formación de la imagen, los equipos actuales disponen de colimadores que se abren y cierran asimétricamente de manera automática al inicio y al final de la exploración (colimación adaptativa), reduciendo la dosis un 6-16% dependiendo de la región y de la anchura del haz, y que puede alcanzar hasta un 55% en ciertos estudios de arterias coronarias24.
- •
Evitar estudios en dos o más «tiempos» de administración del contraste. Raramente el estudio multifásico aporta información adicional en pediatría, pero puede triplicar la dosis recibida20. Salvo en casos muy concretos, las fases arterial y venosa deben solaparse en una sola, o bien pueden emplearse técnicas de reconstrucción virtual de la imagen para simular el estudio basal precontraste si se dispone de TC con energía dual25.
- •
Sistemas de modulación automática de dosis (SMAD). En la actualidad, la mayoría de los aparatos de TC vienen con SMAD y el ajuste de la intensidad de corriente del tubo se hace a partir de las características morfológicas del paciente y de la zona anatómica a estudiar (longitudinal, angular o combinada según la atenuación de los tejidos en los ejes Z o XY, respectivamente), o por sincronización con la señal del electrocardiograma. Esto puede incrementar el ruido y disminuir la calidad de la imagen porque enmascara los detalles de bajo contraste, pero en pediatría habría que ser permisivo y aceptar imágenes con mayor ruido pero suficientemente diagnósticas (principio ALARA, As Low As Reasonably Achievable). En los equipos de TC multicorte para pacientes pediátricos, la efectividad de los sistemas de modulación está limitada por su pequeño tamaño. Se han publicado disminuciones de dosis del 10-61% en ciertos órganos (tiroides, pulmón, esófago y mama) de pacientes con edades comprendidas entre 1 y 10 años26.
- •
Protección selectiva de órganos. El uso de protectores de diferentes materiales, preferentemente de bismuto, colocados delante de órganos más radiosensibles, como el cristalino, las mamas, el tiroides o las gónadas, atenúa el haz de radiación en un 20-50%. Algunos aparatos incluyen protección selectiva automática de órganos. Varios estudios han mostrado que esta técnica permite reducciones de dosis absorbida en la mama o el tiroides del 20-38%, y parece que se han mostrado más eficaces que los protectores de bismuto para proteger órganos radiosensibles27.
- •
Métodos de reconstrucción iterativa de la imagen. Comparados con la reconstrucción tradicional por retroproyección filtrada, con estos métodos se reduce apreciablemente el ruido y se producen menos artefactos en la imagen, lo que posibilita la obtención de imágenes con calidad diagnóstica utilizando protocolos de menor dosis. Con este método se han publicado rangos de reducción de dosis del 23-76%28.
- •
Es conveniente el almacenamiento y la visualización de las dosis estimadas en los estudios en formato DICOM, así como el empleo de niveles de referencia. En el Reino Unido, el uso de niveles de referencia de diagnóstico ha bajado la dosis de TC29. Pueden utilizarse la ACR-AAPM practice guideline for diagnostic reference levels and achievable doses in medical x-ray imaging, publicada por el ACR en 2014, y el European Diagnostic Reference Levels for Pediatric Imaging (PiDRL), publicado en octubre de 2015 por la ESR. Las dosis de TC se expresan en unidades CTDIvol, SSDE o DLP.
- •
En los estudios híbridos, como la PET-TC, pueden aplicarse las técnicas anteriormente mencionadas para bajar la dosis de TC. Así, en algunos estudios se apuntan disminuciones de dosis de hasta el 50%, con una reducción del riesgo estimado de cáncer del 16%30. Siempre que sea posible hay que evitar su uso o intercambiar con otra técnica híbrida, como la PET-RM, aunque en la actualidad esta última es poco accesible. Se han publicado proporciones de reducción de dosis con la PET-RM en comparación con la PET-TC de hasta un 73%31.
La cantidad de radiación resultante de los estudios fluoroscópicos e intervencionistas es altamente variable32. La cistouretrografía miccional seriada (CUMS) es el procedimiento fluoroscópico más utilizado para el estudio del reflujo vesicoureteral. En un estudio realizado en 200533, el uso de un protocolo de CUMS optimizado para pacientes pediátricos reducía la dosis utilizada de 0,59-0,45 mSv a 0,07-0,05 mSv.
En la tabla 4 se expone una relación de pasos a seguir en estos estudios para disminuir la dosis de radiación. No obstante, la mejor estrategia para la reducción de dosis en los estudios fluoroscópicos es sustituirlos por técnicas que no empleen radiaciones ionizantes, especialmente la sonocistografía35–38.
Medidas de radioprotección en estudios fluoroscópicos e intervencionistas pediátricos. (Adaptada de Piscaglia et al.34.)
| Medida | Factor que disminuye |
|---|---|
| Posición adecuada del paciente | La dosis de radiación es inversamente proporcional al cuadrado de la distancia: - Intentar mantener una distancia entre la piel y el tubo de Rx de 50-66cm. - Minimizar la distancia entre el intensificador y el paciente. |
| Inmovilización | Disminuye el número de «disparos» y evita radiar zonas que no se incluyen en el protocolo de estudio. |
| Emplear fluoroscopia pulsada en vez de continua | Una fluoroscopia continua típica implica 30 imágenes por segundo, con una duración de cada pulso de 33 ms, lo que aumenta el mAs y por tanto la dosis de radiación. El tipo de fluoroscopia pulsada depende del tipo de estudio: pueden emplearse 15 imágenes por segundo en procedimientos vasculares intervencionistas, 7,5-15 pulsos por segundo en estudios de videodeglución o 3-5 por segundo en estudios gastrointestinales habituales o CUMS. |
| Emplear filtros del haz de rayos X | Elimina la radiación de baja energía que contribuye a la dosis recibida, pero no a la formación de la imagen. |
| Si se trabaja con fluoroscopia digital, evitar la parrilla antidifusora cuando se pueda | Igual que en radiología digital. |
| Emplear la colimación adecuadamente | No es necesario radiar las áreas anatómicas que no interesan en el estudio |
| Ajustar el kilovoltaje y el mAs al área anatómica y al tamaño del paciente | Cuando se utilicen los programas prefijados según área anatómica, debería tenerse en cuenta si están diseñados o no para uso pediátrico. En este sentido es muy útil el empleo de las dosis de referencia38. |
| Intentar realizar el menor número de radiografías posibles | Utilizar capturas de pantalla. La realización de radiografías aumenta la radiación y pocas veces aporta algo al diagnóstico. |
CUMS: cistouretrografía miccional seriada; mAs: miliamperaje por segundo; Rx: rayos X.
En la tabla 5 se exponen con cierto detalle algunas peculiaridades del uso de contrastes en pediatría. Además, deberían tenerse en cuenta las siguientes recomendaciones generales39:
- •
El trato con el niño y los padres es fundamental para disminuir la ansiedad asociada a los procedimientos diagnósticos. La comunicación con los pacientes pediátricos debería ser cuidadosa en todas las fases, explicando en un lenguaje que entiendan por qué se les administra el contraste y los posibles efectos leves de este, como por ejemplo la sensación de calor en el sitio de punción del contraste yodado cuando se administra por vía intravenosa. Esto reduce la necesidad de repetición de pruebas y de radiación innecesaria. En este sentido son muy útiles y amenas las iniciativas de algunos grupos hospitalarios pediátricos de crear un ambiente decorativo adaptado a la infancia en los servicios de diagnóstico por la imagen.
- •
Es importante disponer de catéteres y sondas de distintos calibres para adaptarnos al tamaño del paciente, y de personal cualificado con experiencia en el acceso de vías venosas y sondaje rectal/vesical en niños. Como norma general, en lactantes y niños pequeños podremos emplear catéteres Abbocath® de 24 a 22 G (velocidades de 1,5 a 2,5 cc/s, respectivamente). El empleo de vías centrales puede considerarse si no se consigue obtener una vía periférica adecuada40. La limitación de velocidad en los niños se aprovecha para mantener el bolo en situación intravascular en el caso de inyecciones lentas y velocidades de adquisición de TC o RM muy rápidas, lo que además puede limitar la dosis si aún no se ha introducido por completo el volumen programado. Puesto que los volúmenes a administrar son muy pequeños, hay que considerar el volumen de los catéteres y de las llaves de paso, de tal modo que el bolo de contraste intravenoso debe estar en la punta del catéter cuando se inicie el estudio, lo que se consigue empujándolo hasta esa posición con un bolo de solución salina fisiológica.
- •
Se debe evitar el uso de contrastes intravenosos en neonatos y lactantes, en especial en aquellos con insuficiencia cardiaca o renal. Esto se debe fundamentalmente a la adaptación fisiológica transitoria de la función renal a la vida extrauterina, al volumen relativo del contraste respecto al volumen intravenoso y a la osmolaridad de los contrastes yodados de uso intravenoso comercializados. A modo de ejemplo, 25ml de contraste intravenoso en un neonato de 3kg de peso, que puede tener un volumen intravascular de 255-288ml, supone un 10% del mismo. Por otra parte, en pacientes cardiópatas o con insuficiencia renal esta sobrecarga de volumen puede agravarse debido a la relativa hiperosmolaridad del contraste yodado respecto a la sangre y la consecuente movilización de fluidos desde el compartimento intravenoso al intersticial (450-800 mOsm/kg respecto a la media sanguínea de 300 mOsm/kg). La misma consideración debe tenerse con el uso oral o endorrectal de contrastes yodados de alta osmolaridad, que pueden inducir deshidratación grave con pérdida de sales por movilización de fluidos desde el compartimento intravascular al intraluminal (tabla 5).
- •
Algunos medios de contraste pueden no estar aceptados de manera específica para su uso en la edad pediátrica, aunque no estén explícitamente contraindicados. Cuando sea necesaria su administración, como es el caso de ciertos contrastes de gadolinio (Gd) o del contraste sonográfico (Sonovue®), puede hacerse como «uso compasivo», por lo que se recomienda disponer de este tipo de documento de consentimiento informado.
- •
Las reacciones adversas a los contrastes intravenosos se previenen y tratan de forma similar a como se hace en los adultos, considerando la dosificación pediátrica especial41. Si ocurriera una extravasación del medio de contraste, su tratamiento también es similar al del adulto, aunque debe tenerse en cuenta que el niño puede no avisar de ello39,41. La incidencia real de reacciones anafilactoides es difícil de estimar, entre otras razones porque disminuye con la edad (a menor edad, menos probabilidad): se encuentra en torno al 0,18% para contrastes yodados no iónicos de baja osmolaridad y al 0,04% para contrastes de Gd.
- •
Existen muy pocos datos en la literatura sobre la nefrotoxicidad inducida por contraste intravenoso en niños. Como norma general, habría que evitar el uso de cualquier contraste intravenoso en pacientes con tasas de filtración glomerular <60ml/min/1,73 m2. La tasa de filtración glomerular es la medida que debería emplearse para estimar la función renal en la edad pediátrica, y puede utilizarse la fórmula modificada de Schwartz39. Para el tratamiento y la prevención de la nefrotoxicidad inducida por el contraste intravenoso, el ACR42 recomienda seguir las guías para adultos.
- •
Existen muy pocos casos comunicados en la literatura sobre fibrosis sistémica nefrogénica relacionada con contrastes de Gd: 23 en pacientes con edades comprendidas entre los 8 y los 19 años43. El ACR recomienda seguir las mismas precauciones que para los adultos42.
- •
Todos los contrastes intravenosos de yodo o Gd atraviesan la placenta y no se conocen sus efectos en el feto, por lo que se recomienda no utilizarlos. Por otra parte, el paso de los contrastes (de yodo y basados en Gd) a la leche materna es <1% de la dosis administrada en las primeras 24 horas, y se estima que <1% de esta dosis se absorbe en el tracto gastrointestinal del lactante y pasa al torrente circulatorio, por lo que su uso es seguro y no debería interrumpirse la lactancia por este motivo39.
Uso de contrastes en estudios de imagen pediátricos
| Nombre (nombre commercial) | Uso | Dosis y vías de administración | Precauciones / peculiaridades | |
|---|---|---|---|---|
| ECOGRAFÍA | Microburbujas de hexafluoruro de azufre (Sonovue®) | Urosonografía para estudio y seguimiento de reflujo vesicoureteral. En otras indicaciones, en general estudios vasculares y parenquimatosos no hay suficiente experiencia para establecer su indicación. | A través de sonda vesical 1,5 cc previamente mezclado (agitar fuertemente) antes de su administración en bolsa de suero fisiológico 0,9% de 500 ml. Mantener infusión con presión constante (90 mmHg) | Es importante mantener el índice mecánico bajo<0,1 para evitar escindir la microburbuja. El Sonovue® no está aprobado para su uso en edad pediátrica. El uso endocavitario (urosonografía) se realiza como uso compasivo ya que ha demostrado suficiente seguridad y utilidad, evitando además radiación ionizante. No efectos indeseables en uso endocavitario. Precauciones de uso IV en cardiópatas. |
| Enemas de solución salina fisiológica | Desinvaginación con enema bajo control ecográfico. | Enemas de unos 500 ml en infusión a distintos grados de presión | ||
| FLUOROSCOPIA | Sulfato de Bario | Estudios contrastados gastrointestinales altos y bajos. | Solución con agua y edulcorante en caso de administración oral. En lactantes y niños pequeños de 40 a 100 ml (dilución 1:1 o 1:1,5). Cuidado en pacientes con dietas bajas en sal o con intolerancia a la fructosa. | No se debería utilizar en neonatos ni en sospechas de complicaciones del tubo digestivo. En lactantes es recomendable 2-4 horas de ayuno y 4-6 horas en niños mayores aunque pueden tomar agua hasta 3 horas antes. |
| Tratamiento del ileo meconial/cuadro pseudo- oclusivo. Indicación discutida. | Solución con agua 1:1 a 1:4. Enema, recomendable con sondas sin globo. | La hiperosmolaridad de este compuesto puede producir cuadros de hipovolemia y depleción electrolítica en neonatos y lactantes. Se prefiere para estas indicaciones contrastes yodados no iónicos de baja osmolaridad. | ||
| Contraste yodado no iónico de baja osmolaridad | En estudios gastrointestinales altos y bajos en neonatos y lactantes. En estudios gastrointestinales altos y bajos en pacientes postoperados o en situación clínica comprometida como sospecha de perforación, vólvulo, fístula traqueoesofágica…. En estudios de vías urinarias anterógrados o retrógrados. En fistulograma/genitografía/ estudios de malformación anorrectal/intra-articulares. | Solución de 1:1 a 1:2 en administración oral (biberón, cucharadas, aspiración con pajita) o en infusión en resto de usos endocavitarios. | El uso endocavitario es muy seguro. Precaución en alérgicos y en caso de propensión al hiper/hipotiroidismo por absorción en mucosas. | |
| TOMOGRAFÍA COMPUTARIZADA | Contrastes de yodo no iónicos iso o hipoosmolares | Cualquier indicación TC que precise el uso de CIV. MieloTC. ArtroTC | Dosis: 1,5–2ml/kg. Puede disminuirse en caso de estudios vasculares rápidos e infusiones lentas por limitación del calibre de la vía IV | Precauciones como en el adulto: hipersensibilidad, hipertiroidismo, insuficiencia renal, drepanocitosis… En neonatos y niños pequeños intentar evitar su administración por IR transitoria y posibilidad de inducir hipotiroidismo transitorio. Existen datos contradictorios sobre el efecto potenciador de estos contrastes sobre el daño celular producido por las radiaciones ionizantes. |
| Contrastes de Bario | Opacificación endoluminal de asas | Solución oral similar a estudios fluoroscópicos | Indicación cada vez más en desuso debido al excelente contraste enteronegativo que proporciona el agua con los TC multicorte de última generación. | |
| RESONANCIA MAGNÉTICA | Contraste de gadolinio macrocíclicos o de bajo riesgo (Dotarem®, Prohance®, Gadovist®) | Cualquier indicación RM que precise el uso de CIV | Dosis 0,2 ml/Kg. 0,4 ml/Kg en caso de angiografía-RM o estudios de perfusión. | Dotarem® es el único aprobado en cualquier rango de edad pediátrica aunque recomiendan utilizar con precaución en neonatos y lactantes. No sumar más de una dosis de contraste en 7-10 d: espaciar estudios TC y RM con CIV Prohance® contraindicado en menores de 2 años. |
| Otros contrastes de Gd®: excreción biliar (Primovist®, Multihance®) | Indicado en distinción de lesiones hepáticas | Dosis habitual | De riesgo intermedio: si necesario, utilizar “bajo uso compasivo” | |
| Contrastes enterográficos y endocavitarios de alta señal T2 o baja señal T2 | Estudios de enteroRM | Manitol al 5% en solución acuosa (1-1,5 l), gel ecográfico para uso endocavitario o suero fisiológico | Distensión hiperosmolar de asas para EII. Usar con Buscapina® Mejora contraste en los órganos pélvicos | |
| Opacificar asas en T2 (urografíaroRM, pancreatografía) | Solución en zumo de piña o de arándanos | El alto contenido en manganeso de la piña o los arándanos permite opacificar la señal T2 de las asas en estos estudios | ||
CIV: contraste intravenoso; EII: enfermedad inflamatoria intestinal; RM: resonancia magnética; TC: tomografía computarizada.
Los autores declaran no tener ningún conflicto de intereses.