Los linfomas y las leucemias en etapas avanzadas pueden infiltrar el útero y la vagina. Sin embargo, la localización primaria del tracto genital femenino de los tumores hematológicos es extremadamente infrecuente (1% de los extraganglionares). Se presenta un caso de un linfoma no Hodgkin difuso de células grandes B primario de vagina en estadio IE, de acuerdo con la clasificación de Ann Arbor. Tras el tratamiento quimioradioterápico se obtuvo la remisión completa y la paciente permanece libre de enfermedad 5 años después del diagnóstico.
Advanced lymphoma and leukemia can infiltrate the uterus and vagina. However, primary lymphomas affecting the female reproductive system are extremely uncommon (representing 1% of non-nodal tumors). We present a case of primary non-Hodgkin’s lymphoma of the vagina, diffuse large B cell type, stage IE according to the Ann-Arbor staging system. Complete remission was obtained after treatment with chemotherapy and radiotherapy. Five years after diagnosis, the patient is disease free.
Las neoplasias de la vagina son tumores poco frecuentes que comprenden un 1-2% de todos los cánceres ginecológicos. El cáncer vaginal celular escamoso es el más frecuente, aproximadamente el 85% de los casos, seguido del adenocarcinoma, el 14% de los casos y, con menor frecuencia, el melanoma, el sarcoma, el linfoma y los tumores carcinoides son descritos como cánceres vaginales primarios1.
Los linfomas tienen una frecuencia del 5% entre todos los cánceres. Cuando los linfomas no Hodgkin se encuentran en etapas avanzadas pueden afectar al tracto genital femenino; sin embargo, la vagina como localización primaria de este tumor es excepcional. El 25% de los linfomas tiene un origen extraganglionar, y alcanza el 40% en los linfomas difusos de células grandes, si bien sólo un 1% se desarrolla a nivel ginecológico. El ovario es la localización más frecuente y sólo 1 de cada 175 linfomas extraganglionares en la mujer se origina en el útero o la vagina2,3. La edad media de presentación está en la quinta década de la vida4,5. La histología más frecuente es el linfoma no Hodgkin de estirpe B, difuso de células grandes (LNHDCGB). El motivo por el que suelen consultar las pacientes es la hemorragia por vía vaginal anormal6.
No hay un tratamiento estándar para la enfermedad, si bien los diferentes esquemas empleados incluyen un tratamiento con quimioterapia y radioterapia, existiendo una buena respuesta en estadios iniciales de la enfermedad7.
CASO CLÍNICOPaciente de 48 años, que acudió remitida desde el centro de planificación familiar por induración del tercio inferior de vagina y dispareunia de varios meses de evolución. La última revisión ginecológica se había realizado 5 años atrás. Sus antecedentes personales eran amigdalectomía, fumadora de 20 cigarrillos/día y 2 embarazos y partos normales. En la exploración se observó un anillo fibroso de 1 cm de ancho, en semiluna, que ocupaba toda la pared lateral izquierda, a 2–3 cm de introito. El cérvix estaba bien epitelializado. Al tacto vaginal, el útero y los ovarios eran normales, así como la ecografía transvaginal. La citología cérvico-vaginal realizada en el centro de planificación fue normal.
Se practicó una biopsia de vagina, con resultado de mucosa vaginal con inflamación aguda y crónica, y fibrosis, sin evidencia de malignidad.
La paciente consultó 2 meses después por incremento del dolor vaginal, tenesmo rectal y leucorrea sanguinolenta y mal oliente; refería empeoramiento clínico desde la biopsia realizada un mes antes y no refería fiebre, sudoración o pérdida de peso. En la exploración se observó un aumento de la induración de la pared vaginal, de forma concéntrica nodular, e irregular al tacto. Con un espéculo vaginal se visualizó un nódulo de aspecto friable, rojo vinoso, en el tercio medio de la cara lateral izquierda de la vagina, lugar donde se había tomado la biopsia un mes antes. El resto de la vagina estaba epitelializada, aunque de aspecto fibroso. La impresión diagnóstica fue de tumoración extrínseca que provocaba una disminución concéntrica de la luz vaginal. Al tacto vaginal, los fondos de saco vaginales estaban respetados. Al tacto rectal, el parametrio izquierdo se encontraba ocupado por una tumoración dura e irregular de unos 8 cm. En la ecografía transvaginal y abdominal se visualizaba una masa de 8 × 6 cm, irregular, sugerente de neoplasia, que infiltraba la vagina.
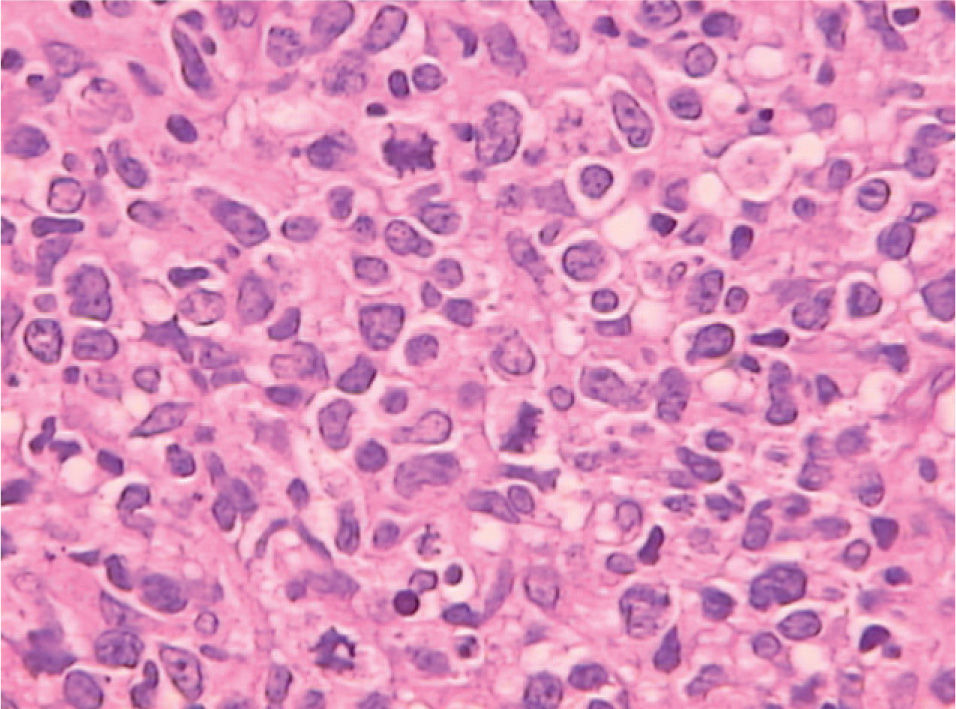
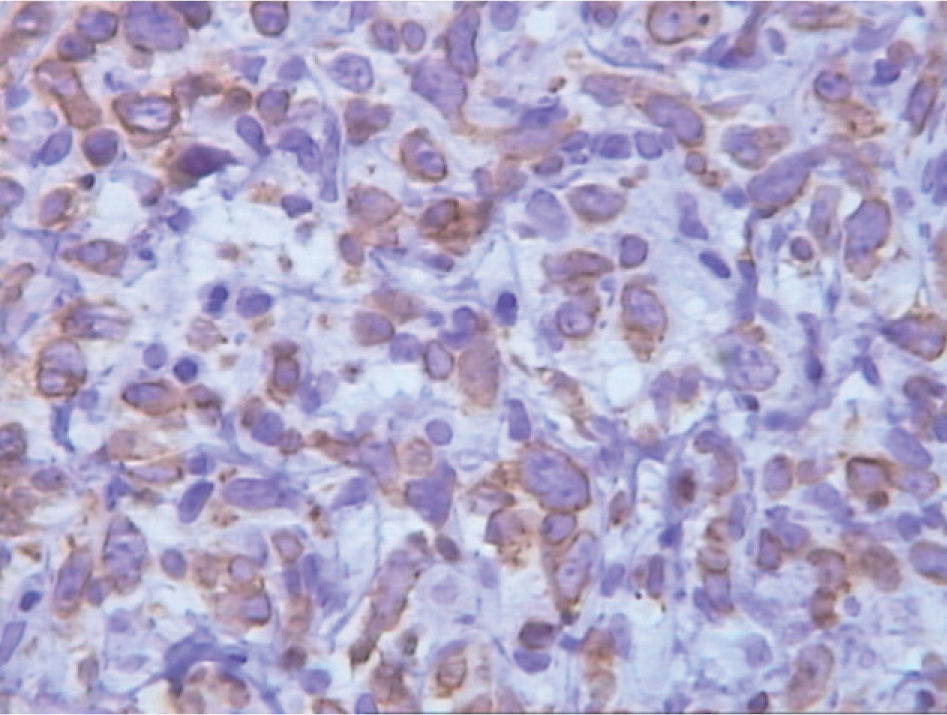
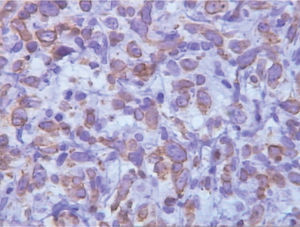
Se realizó una nueva biopsia de la tumoración cuyo estudio histológico mostró la presencia de una proliferación difusa de células de hábito linfoide de origen B. El estudio inmunohistoquímico mostró que esas células eran CD20 (+), bcl-6 (+), CD10 (−), bcl-2 (−/+), CD30 (+), CD23 (−), p53 (−) y ciclina D1 (−), con elevada fracción de crecimiento.
Se realizó una tomografía computarizada (TC) abdominopélvica que confirmó la masa sólida ya descrita, de morfología redondeada, densidad heterogénea y parcialmente cavitada, que ocupaba más de dos tercios de la vagina, de 8 × 6 cm. No había adenopatías retroperitoneales o pélvicas significativas.
En la cistoscopia se observó la vejiga con capacidad disminuida, con compresión extrínseca por masa pélvica y probable infiltración del área trigonal.
La radiografía de tórax y la colonoscopia fueron normales.
El hemograma, la cifra de deshidrogenasa láctica (LDH) sérica y beta-2 microglobulina se encontraban también dentro de la normalidad; la biopsia de médula ósea no mostró infiltración por linfoma.
Ante una mujer de 48 años con el diagnóstico de LNHDCGB en estadio localizado IE, se decidió realizar tratamiento quimioterápico con esquema CHOP (ciclofosfamida, vincristina, adriamicina y prednisona) en 5 ciclos en total y radioterapia extensa sobre el área tumoral, con un total de 39,2 Gy, y se obtuvo una respuesta completa.
La paciente continúa en revisiones periódicas, libre de enfermedad hasta la fecha.
DISCUSIÓNLa incidencia de un linfoma no Hodgkin, como el presentado en este caso clínico, es del 5% de todos los cánceres; su incidencia ajustada por edad es de 17/100.000 casos/año. Los linfomas difusos de células grandes B representan el 30-40% de los linfomas no Hodgkin del adulto en los países desarrollados. Hasta un 40% se presenta como única localización extranodal; la localización más frecuente es el tracto gastrointestinal (estómago o región ileocecal), si bien pueden aparecer en cualquier localización extranodal.
De los linfomas extraganglionares, un 1% es ginecológico y sólo 1 de cada 175 se origina en el útero o la vagina2. Sin embargo, la incidencia de estos linfomas, especialmente los de localización extraganglionar, se ha incrementado en décadas recientes6. Entre las posibles causas de este aumento, se cita una asociación de distintos agentes infecciosos, como el virus de Epstein-Barr8, el virus de la inmunodeficiencia humana (VIH)9,10, terapias inmunosupresoras11 y exposición ambiental a tóxicos y contaminantes. El aumento puede ser también resultado de los avances logrados con nuevas técnicas diagnósticas. El empleo de nuevos reactivos citoquímicos y anticuerpos monoclonales frente a diversos antígenos de diferenciación permite diferenciar la subpoblación de linfocitos involucrada.
La edad media de presentación son 50 años (20 a 80 años) y las tres cuartas partes de las pacientes son posmenopáusicas.
La forma de presentación más frecuente de esta neoplasia es la hemorragia por vía vaginal anormal, seguida del dolor abdominal o pélvico, dispareunia, dismenorrea, presión perineal y, ocasionalmente, obstrucción ureteral, síndrome de compresión de la vena cava o de médula espinal6. En nuestro caso, la paciente refirió como primer síntoma la dispareunia, seguida de dolor pélvico, presión perineal y hemorragia por vía vaginal anormal.
Típicamente se presenta con una masa de rápido crecimiento, en ocasiones grande (> 4 cm), generalmente endofítica, con invasión local de espacios paracervicales. Ocasionalmente se origina a partir de un pólipo cervical. Generalmente es asintomática, con una única localización nodal o extranodal, si bien en muchos de los casos en el momento de la estadificación el paciente tiene una enfermedad diseminada.
Para confirmar el diagnóstico en ocasiones se precisa más de una biopsia, como ocurrió en nuestro caso, ya que muestras pequeñas pueden no ser representativas de la lesión12. Asimismo se requiere una muestra suficiente para realizar los análisis inmunohistoquímicos; son necesarias otras técnicas moleculares para definir el subtipo de linfoma y sus características biológicas. La evaluación clínica de la paciente deberá incluir una hematología completa, con pruebas de funcionamiento hepático y renal, medición de LDH, beta-2 microglobulina y TC abdominopélvica. La biopsia de médula ósea debe realizarse dada la alta incidencia de afección de medula ósea. Una laparotomía estadificadora no está inicialmente indicada. La estadificación es el factor predictor más importante de supervivencia. El sistema de Ann Arbor de linfomas extraganglionales es operativamente más útil que la clasificación de la FIGO, ya que los linfomas no tienen un comportamiento locorregional como los tumores epiteliales (tabla 1). Nuestro caso correspondió a un estadio IE, de acuerdo con esa clasificación. El 75% de estos tumores está localizado (IE) y un 25% está en estadios más avanzados.
Clasificación por estadios de Ann Arbor
| I Afección de una sola región ganglionar |
| IE Afección de un solo órgano o región extralinfática |
| II Afección de dos o más regiones ganglionares situadas a un mismo lado del diafragma |
| IIE Afección de una o más regiones a un lado del diafragma y de un territorio extralinfático por contigüidad |
| III Afección de regiones ganglionares situadas a ambos lados del diafragma |
| III1 Afección limitada a la parte superior del abdomen: bazo, ganglios del hilio hepático, esplénico o tronco celíaco |
| III2 Afección de la parte inferior del abdomen: ganglios paraaórticos, ilíacos, inguinales, mesentéricos |
| IIIS Igual que III, pero con afectación del bazo |
| IIIE Igual que III, pero con afectación extralinfática por contigüidad |
| IV Afección difusa o diseminada de uno o más órganos o tejidos extralinfáticos con participación de los ganglios linfáticos o sin ella |
Recientemente la Organización Mundial de la Salud (OMS) ha establecido una nueva clasificación para las enfermedades malignas hematológicas. La OMS hace una primera estratificación de las neoplasias acorde a su linaje (estirpe) celular: mieloide, linfoide, células dendríticas/histiocitos. Dentro de cada categoría se definen distintas entidades, en función de la combinación de sus características morfológicas, inmunofenotípicas, genéticas y clínicas13,14.
El inmunofenotipo de estos linfomas se caracteriza por expresar varios marcadores B, como el CD10, CD20, CD22 y CD79a, si bien puede faltar uno o más de estos marcadores. La mayoría de los LDCGB variante anaplásico expresa CD30. Algunos expresan CD5 (10%) o CD10 (25-50%). Los LDCGB que sobreexpresan CD5 son negativos para la ciclina D1, lo que nos permite diferenciarlos de la variante blastoide del linfoma mantel. BCL2 es positivo en el 30-50% de los casos. La expresión nuclear de BCL6 se encuentra en una alta proporción de casos, mientras que la expresión de la proteína p53 sólo se halla en un pequeño grupo de pacientes. La fracción de proliferación detectada mediante Ki-67está generalmente aumentada (> 40%) y puede llegar a ser > 90% en algunos casos.
En nuestro caso, se trataba de un LDCGB que expresaba CD20(+), CD10(−), bcl-2 (−/+), bcl-6 (+), p53 (−), ciclina D1 (−) y CD30 y CD23 (−).
Los LDCGB son agresivos pero potencialmente curables con poliquimioterapia.
El índice pronóstico internacional IPI (tabla 2) es el índice pronóstico de supervivencia mejor y más ampliamente aceptado en este tipo de linfoma15. Otros factores biológicos asociados a una peor evolución son la expresión de bcl-2, la sobreexpresión de p53 y un elevado índice de proliferación. En nuestro caso, se trataba de una paciente con un IPI de 0 y otros factores de buen pronóstico, como la negatividad de p53 y bcl-2. El pronóstico global del linfoma de útero y vagina es favorable, con una supervivencia global a los 5 años del 73% (que se eleva al 89% en los estadios IE), y comparativamente mejor que el del linfoma de presentación ovárica, cuya supervivencia global a los 5 años es tan sólo del 34%. La mayor frecuencia de estadios avanzados en estos últimos puede favorecer esta evolución16.
Índice pronóstico internacional: asignación de un punto por cada una de las siguientes variables (factores pronósticos)
| Factor pronóstico | Índice de riesgo |
| Edad (> 60 años) | Bajo: score 0–1 |
| LDH elevada | Intermedio-bajo: score 2 |
| Índice de Karnofsky (> 1) | Intermedio-alto: score 3 |
| Estadio Ann Arbor III-IV | Alto: score 4-5 |
| Afectación extranodal (> 1) |
LDH: deshidrogenasa láctica sérica.
El tratamiento de este tipo de tumores no ha sido uniforme probablemente debido a su escasa incidencia. En algunos casos se ha utilizado la radioterapia como único tratamiento17, pero su eficacia limitada en las formas agresivas, como la de nuestra paciente, y su impacto sobre la función gonadal desaconsejan su uso aislado.
En otros casos se ha utilizado únicamente quimioterapia18, aunque parece que el tratamiento combinado (quimioterapia y radioterapia), el que se aplicó a nuestra pacientes, es el más aceptado7,19.
Recientemente la introducción de un anticuerpo monoclonal específico dirigido frente al antígeno CD20 (Rituximab®) ha permitido incrementar la tasa de respuestas y la supervivencia en asociación a la quimioterapia, tanto en las formas avanzadas como en las localizadas. Por ello, el tratamiento con CHOP-Rituximab® es la opción de elección en la actualidad20.