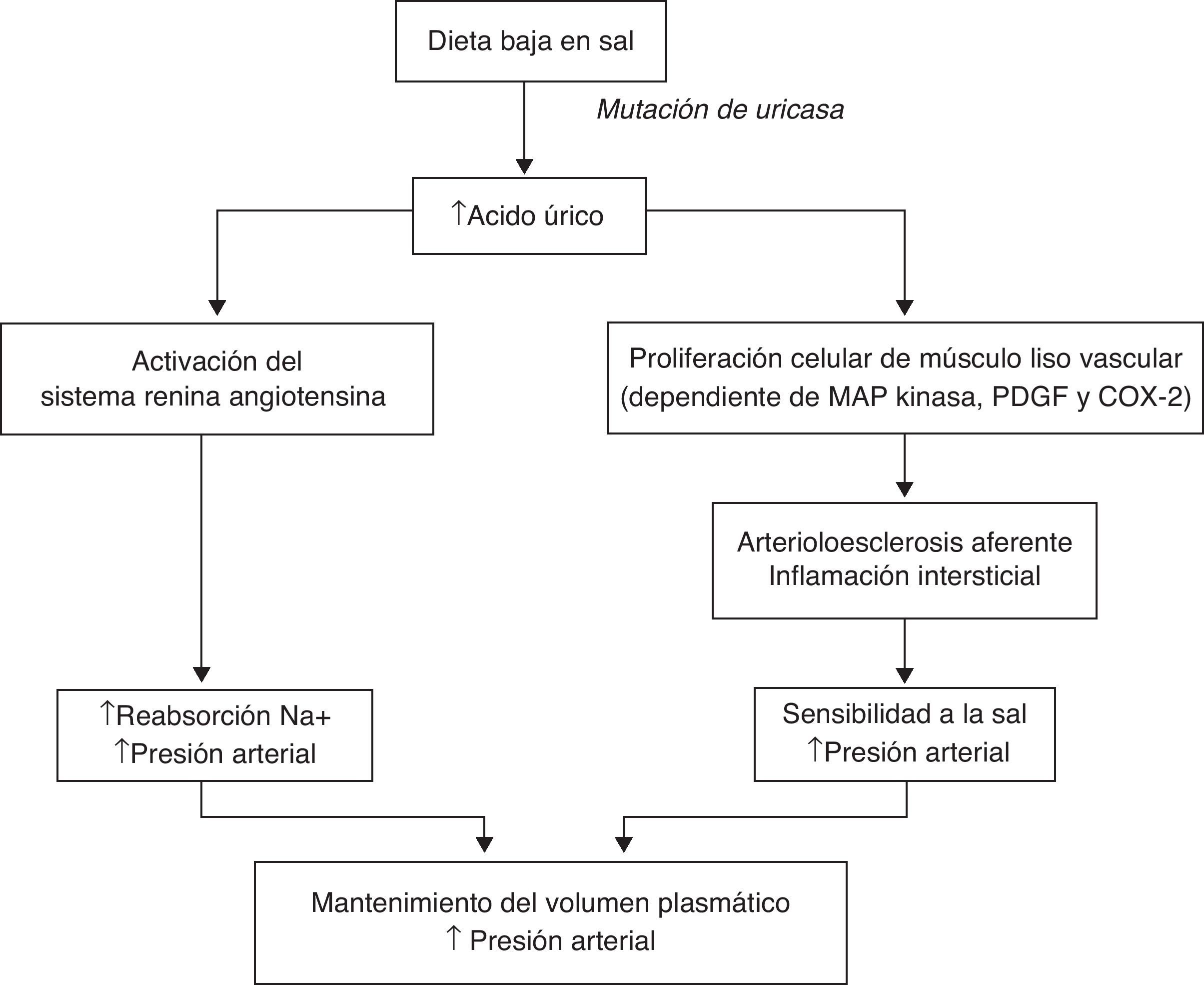
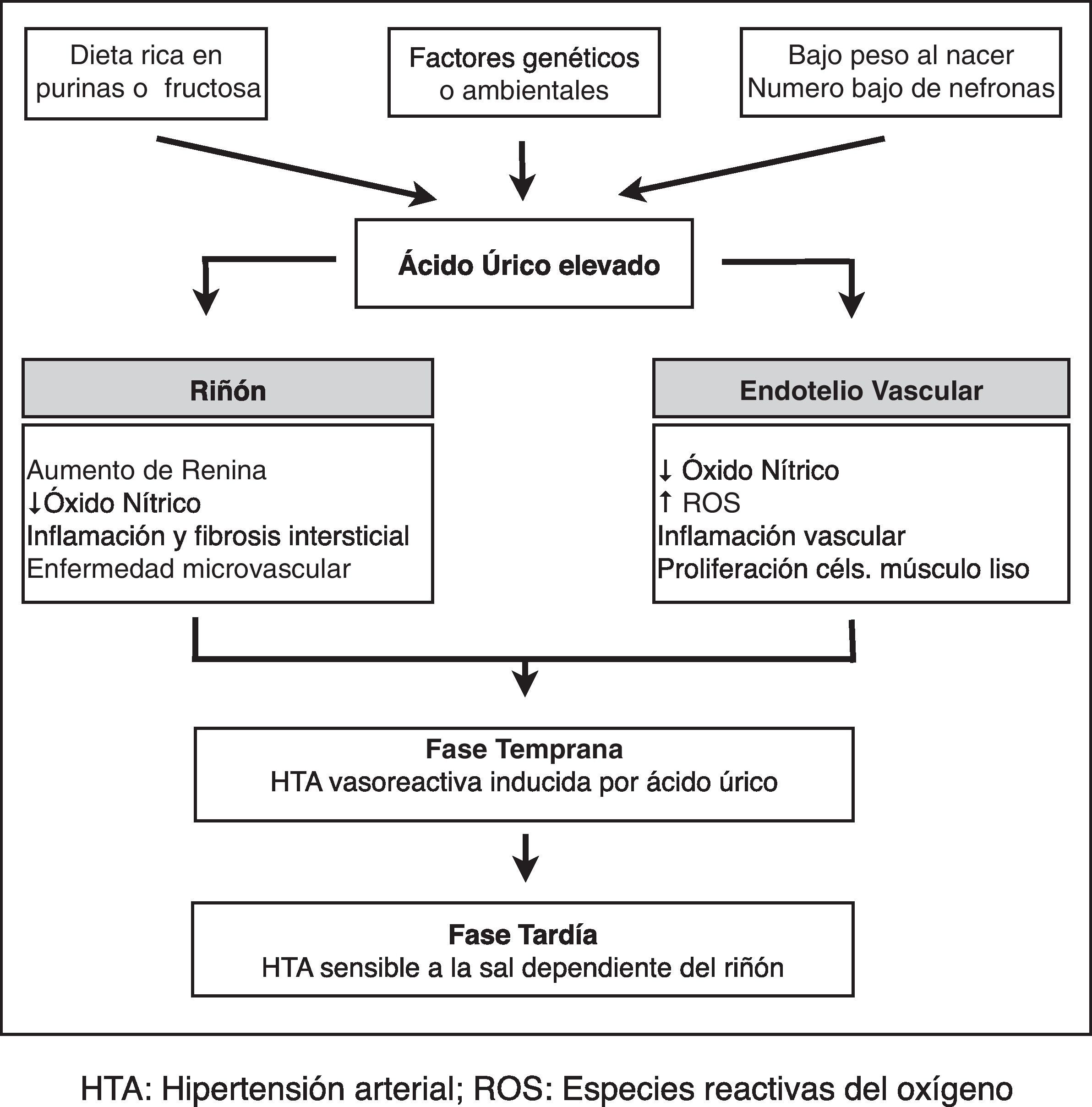
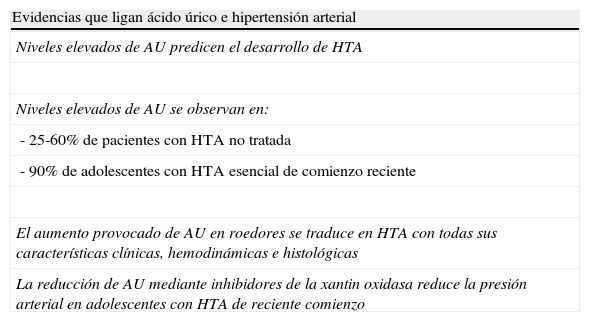
La relación entre niveles séricos de ácido úrico y enfermedad cardiovascular es conocida desde hace tiempo. Sin embargo, ha sido en los últimos años cuando hemos encontrado creciente evidencia estableciendo el posible papel patogénico del ácido úrico en las diferentes manifestaciones de la enfermedad cardiovascular. La importancia de esta relación continúa siendo motivo de controversia y el debate sobre si debemos considerar la hiperuricemia un factor de riesgo vascular independiente o si es un mero epifenómeno de la enfermedad vascular o metabólica permanece abierto.
Esta revisión pretende repasar la evidencia sobre estos aspectos y analizar las implicaciones terapéuticas que los nuevos conocimientos pudieran conllevar.
The relation between uric acid serum levels and cardiovascular disease has been known for a long time. However, it has been in recent times that we have found growing evidence that establishes the possible pathogenic role of uric acid in the different manifestations of cardiovascular disease. The importance of this relation continues to be cause of controversy and the debate is still open on whether we should consider hyperuricemia as an independent vascular risk factor or if it is a mere epiphenomenon of the vascular or metabolic disease.
This review aims to go over the evidence on these aspects again and to analyze the therapeutic implications that the new knowledge may involve.
Artículo
Comprando el artículo el PDF del mismo podrá ser descargado
Precio 19,34 €
Comprar ahora