Biriketako malformazio arteriobenosoak (MAB) entitate kliniko arraro bat dira. Gehienak sortzetikoak eta asintomatikoak badira ere, disnea, hipoxemia eta hemoptisia eragin ditzakete, baita konplikazio larriagoak ere (neurologikoak eta kardiobaskularrak). Tratamendu endobaskularra, espiralekin edo baloi desmuntagarriekin eginiko enbolizazio bidez, eraginkortasun terapeutiko handikoa bada ere, baloien migrazio distalak arazoak sor ditzake. Arazo horiei aurre egiteko, dispositibo berriak sortu dira autoerretentzioko mekanismoekin. Biriketako malformazio arteriobenoso solitario handi baten kasua aurkezten dugu, egoki enbolizatua Amplatzer® dispositibo baten bidez.
ResumenLas malformaciones arteriovenosas pulmonares son una entidad clínica rara. Aunque la mayoría son congénitas y asintomáticas también pueden causar disnea, hipoxemia, hemoptisis o incluso complicaciones más severas, neurológicas y cardiovasculares. El tratamiento intravascular mediante embolización con espirales o balones desmontables ha demostrado alta eficacia terapéutica, si bien no se encuentra exento de complicaciones derivadas de la posible migración distal de los mismos. Para evitar estos eventos adversos se han diseñado nuevos dispositivos con diversos mecanismos de autorretención. Presentamos un caso de una gran malformación arteriovenosa pulmonar solitaria embolizada satisfactoriamente con un dispositivo tipo Amplatzer®.
Pulmonary arteriovenous malformations are a rare clinical entity. Most are congenital and asymptomatic but some can cause dyspnea, hypoxemia, hemoptysis, and even more severe complications such as neurological and cardiovascular complications. Endovascular embolization with coils or detachable balloons has shown high therapeutic efficacy but is not exempt from possible complications due to distal migration of these devices. To avoid these adverse events, new devices have been designed with various mechanisms to prevent their migration. We report the case of a large solitary pulmonary arteriovenous malformation successfully treated with an Amplatzer® device.
Las malformaciones arteriovenosas pulmonares (MAVP) son comunicaciones directas anómalas entre las arterias y venas pulmonares, sin presencia de lecho capilar entre ellas. Aunque raras, son probablemente la anomalía del árbol vascular pulmonar más común, con una incidencia de 2-3 casos/100.000 habitantes. La gran mayoría son de origen congénito y, de éstas, un 47-80% se asocian al síndrome de Rendu-Osler-Weber1. Las formas adquiridas suponen menos del 20% y su etiología es muy dispar1, 2.
Las MAVP pueden ser únicas (42-74%), múltiples (8-20%), bilaterales o unilaterales, y su ubicación más frecuente es en los lóbulos inferiores (53-70%)1, 2. El tamaño puede ser muy variado, típicamente oscila entre 1 y 5cm, aunque ocasionalmente pueden llegar a superar los 10cm de diámetro2. En el 95% de los casos el aporte vascular aferente y eferente de la MAVP va a depender de la circulación pulmonar1, 2.
Entre el 13-55% de los pacientes con MAVP son asintomáticos1, 2, 3. Cuando aparece la sintomatología esta es secundaria al shunt derecha-izquierda que se crea en el interior de la MAV1, 3, siendo la disnea durante el ejercicio el síntoma más comúnmente referido (31-67%)1, 2, 3. Sin embargo, las MAVP también pueden ser responsables de complicaciones severas, tanto neurológicas (infartos, AIT, abscesos, apoplejía) desencadenadas por fenómenos de embolización paradójica1, 2, 3, como torácicas, donde pueden causar episodios de hemoptisis o hemotórax masivos motivados por la rotura de la MAVP, que aunque infrecuentes, son potencialmente mortales1, 2, 3, 4.
Son estas complicaciones graves las que se tratan de evitar con el tratamiento de las MAVP, cuya terapia de elección a día de hoy es la embolización endovascular1, 2, 3, 5. A los sistemas de embolización tradicionales, recientemente se ha añadido el dispositivo Amplatzer®, cuya ventaja principal deriva de su sistema de anclaje, desarrollado para evitar una hipotética migración distal4, 5.
Presentamos un paciente con una gran MAVP que tras tratamiento con Amplatzer® experimentó una resolución completa de su enfermedad respiratoria.
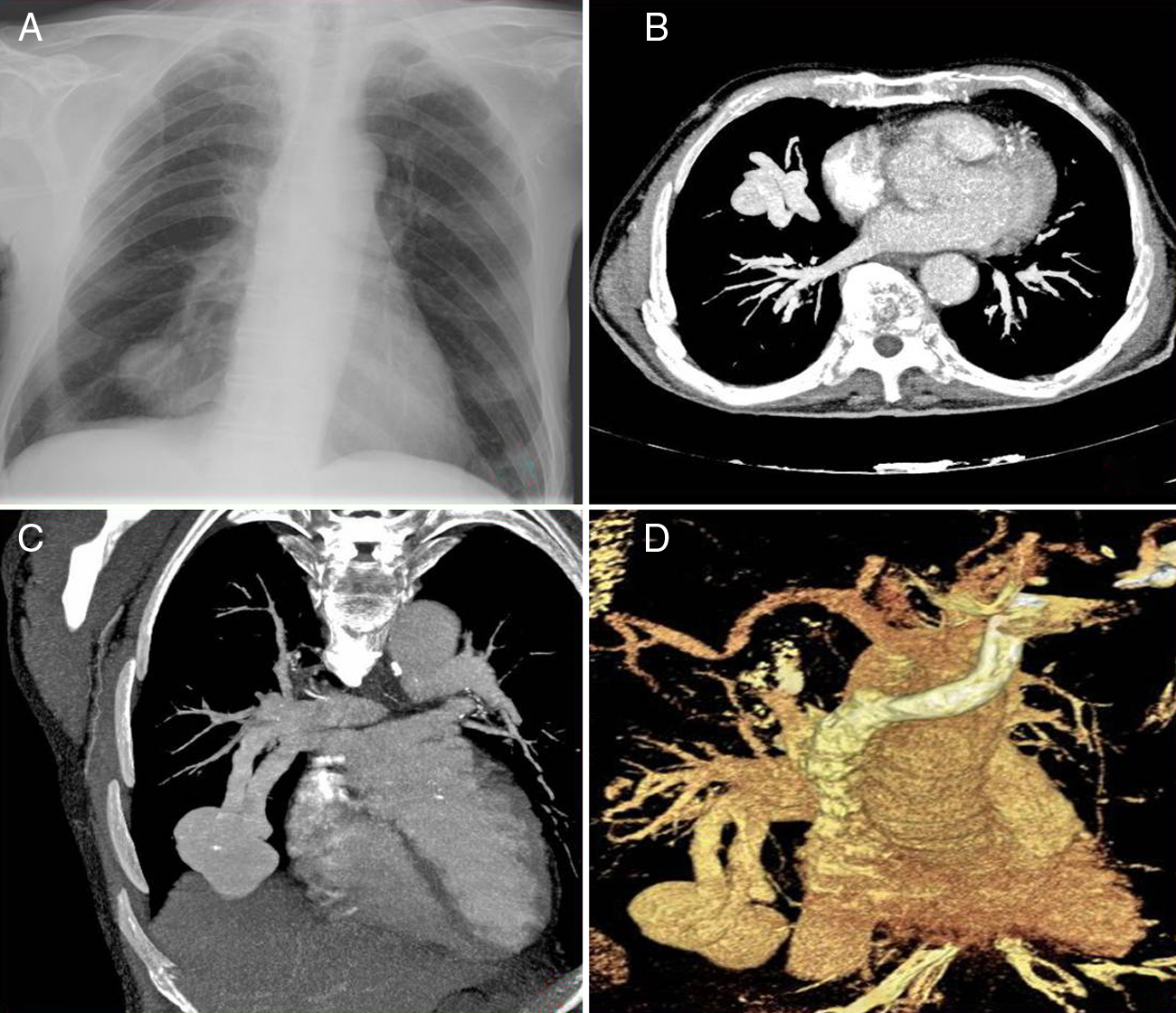
Presentación del casoVarón de 79años de edad con historia de insuficiencia respiratoria crónica y progresiva. La exploración física y analítica era normal, y llamaba la atención en la gasometría obtenida con gafas nasales a 3 l/min una saturación de O2 del 85%. En la radiografía de tórax se observó una masa de contornos bien definidos en el lóbulo inferior derecho. La tomografía computarizada multidetector (TCMD) de región torácica, con adquisición de imágenes en plano axial y posterior reconstrucción multiplanar, reveló la presencia de una lesión nodular única localizada en el segmento medial del LID, de casi 50mm de diámetro transverso, en conexión con una gran arteria nutricia (9,7mm de diámetro) y una vena de drenaje, que desembocaba en la aurícula izquierda, siendo los hallazgos compatibles con MAVP (Figura 1).
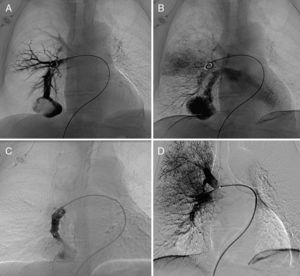
Figura 1. Radiografía de tórax (A) y TCMC tras CIV, en plano axial (B) que muestran la MAVP como una masa nodular en LID. En las reconstrucciones MIP (C) y VRT (D) se visualiza la arteria aferente pulmonar y la vena de drenaje hacia la aurícula izquierda.
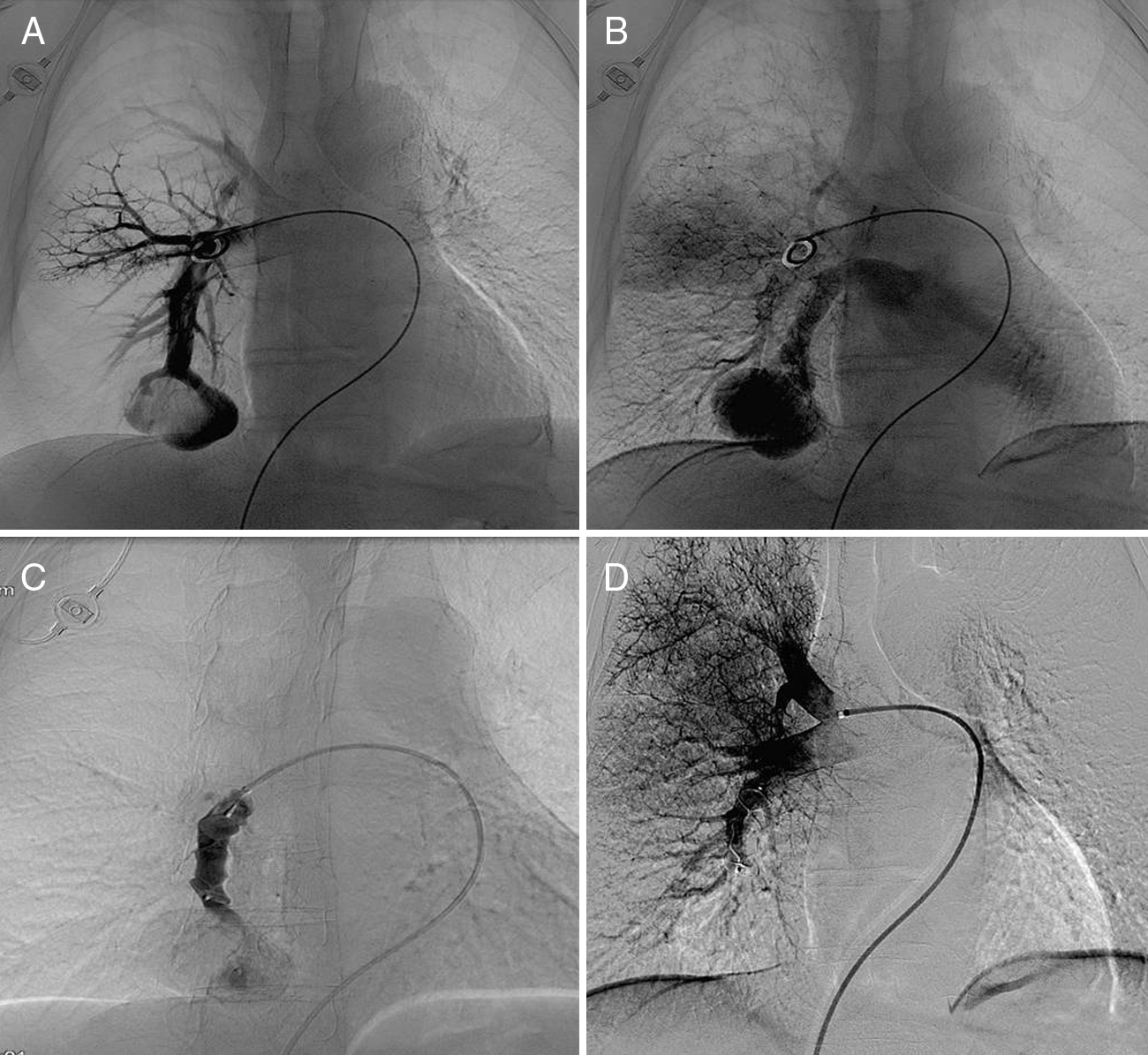
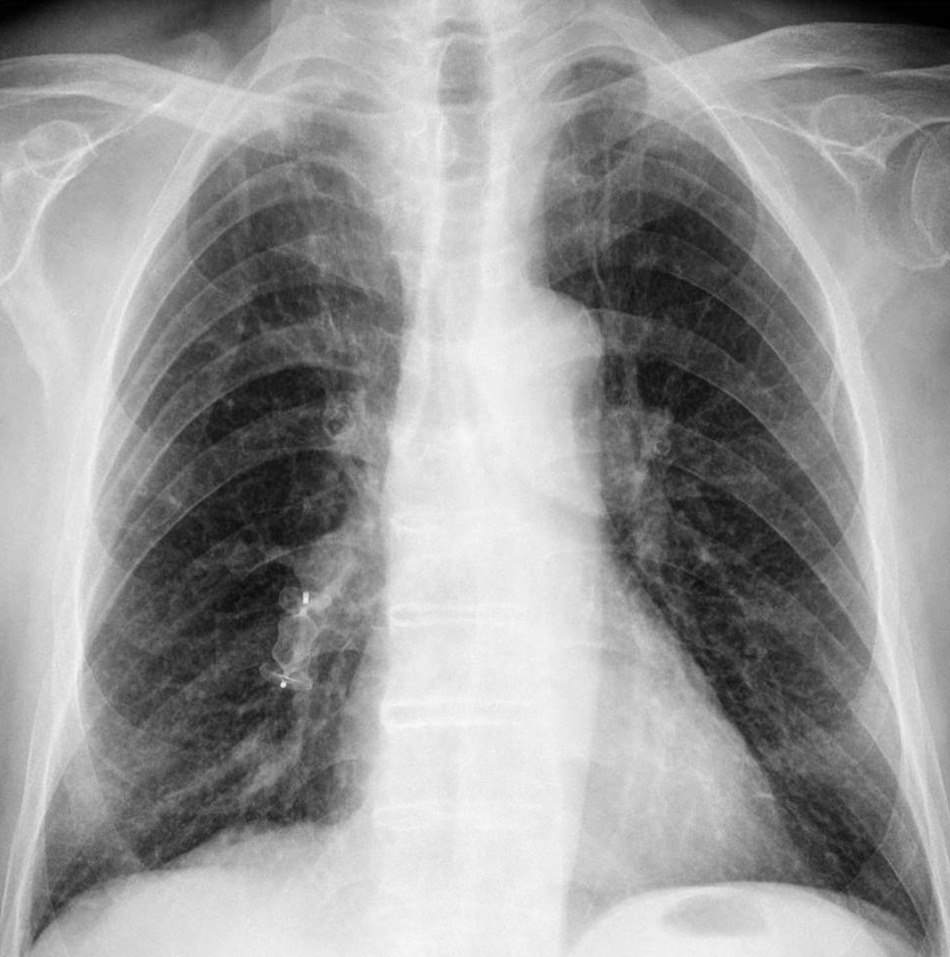
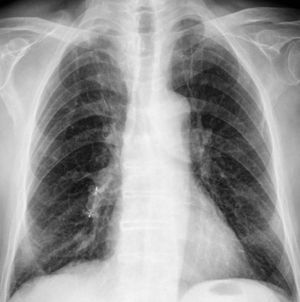
Tras los resultados de la TCMD, se realizó estudio angiográfico pulmonar y tratamiento percutáneo intravascular. A través de vena femoral común derecha, previo abordaje con introductor valvulado 6 F de Terumo®, y sobre una guía hidrofílica de 0¿035″ (Radiofocus Terumo®) de 150cm de longitud, se introdujo un catéter angiográfico tipo pigtail 5 F (Angiodynamics®) hasta la arteria pulmonar derecha, para realizar un estudio angiográfico general del pulmón derecho. Seguidamente se intercambió el introductor por un catéter introductor Ansel II 6F de 55cm (Cook®). Posteriormente, a través del catéter introductor y sobre una guía rígida Amplatz Super Stiff de 0¿035″ de 145cm de longitud (Boston Scientific®) se introdujo un catéter multipropósito 5 F (Angiodynamics®), que se avanzó sobre la guía hasta cateterizar selectivamente la arteria nutricia de la MAV. Una vez confirmada la localización exacta de la MAV, se avanzó el catéter introductor Ansel II y se introdujo el dispositivo Amplatzer® II de 16mm. Previamente a su liberación definitiva, se verificó su posición y comprobada esta, se procedió a la misma. Posteriormente se retiró el catéter introductor hasta la arteria pulmonar derecha, donde se realizó nueva comprobación angiográfica que demostró la oclusión completa de la MAV (Figura 2). El procedimiento fue bien tolerado y transcurrió sin complicaciones inmediatas. En el momento del alta, la gasometría practicada al paciente respirando aire ambiente reveló una saturación de O2 del 96%. Tras un año de seguimiento clínico, el paciente permanece asintomático y en una radiografía simple de tórax de control rutinario, se aprecia desaparición de la imagen de masa en la base derecha (Figura 3).
Figura 2. Arteriografía selectiva de la MAVP que demuestra el aporte arterial dependiente de la rama interlobar descendente de la arteria pulmonar derecha (A), y su vena de drenaje (B). Angiografía inmediata tras despliegue del Amplatzer® de 16mm, con persistencia de flujo en el interior de la MAVP (C). Angiografía de control tras liberación del dispositivo con comprobación de óptimo resultado terapéutico (D).
Figura 3. Radiografía de tórax de control un año después en el que se visualiza el dispositivo Amplatzer® con desaparición de la masa pulmonar.
DiscusiónLas MAVP son comunicaciones directas anómalas entre las arterias y venas pulmonares, sin presencia de lecho capilar entre ellas, que condicionan el desarrollo de un shunt derecha-izquierda. Aunque habitualmente son asintomáticas (13-55%) o mínimamente sintomáticas, en su desarrollo pueden provocar cuadros hemorrágicos o embólicos de riesgo e incluso potencialmente mortales para el paciente1, 2, 3, 4.
El objetivo principal del tratamiento es reducir el shunt vascular y disminuir la tasa de morbimortalidad global1, 2. El tratamiento se indica en todas las MAVP sintomáticas o con fenómenos de embolización paradójica, cuando hay un aumento progresivo de su tamaño, y también en aquellas que, aunque asintomáticas, tengan arterias nutricias con diámetro mayor o igual a 3mm1, 2.
La terapia de embolización intravascular, a día de hoy el tratamiento de elección, ha relegado la cirugía para los casos en que falla la emboloterapia1, 2, 3. Los agentes embolizantes más utilizados son las espirales y/o los balones desmontables1, 2, 3, siendo a veces necesario recurrir a ambos dispositivos para lograr un óptimo resultado terapéutico. Sin embargo, a pesar de su amplia utilización hay que valorar la posibilidad de complicación por migración, sobre todo en MAVP grandes o con alto flujo4, 5.
El Amplatzer® es un dispositivo autoexpandible formado por una malla –alambre recubierto de nitinol, que se aloja en el interior de un catéter, para luego, tras ser liberado, recuperar su forma y ocluir el vaso. Existen modelos con distintas morfologías y calibres, recomendándose utilizar un dispositivo un 30-50% más grande que el diámetro del vaso a ocluir, y que deberá liberarse tan distalmente como sea posible para conseguir un óptimo resultado terapéutico4, 5.
Entre las ventajas que ofrece este dispositivo, destaca un menor riesgo de migración y la posibilidad de recolocación. Al ser un dispositivo autoexpandible y elegir un tamaño mayor al del calibre de la estructura vascular diana, una vez liberado se consigue su óptimo anclaje. En cuanto a la recolocación, la posición del Amplatzer® puede ser fácilmente verificada mediante estudio angiográfico, de manera que si la ubicación no es correcta se puede reintroducir en el catéter y reposicionar antes de su liberación definitiva. Además de estas ventajas, este dispositivo puede usarse en MAVP con arterias nutricias de gran calibre (> 10mm) y/o que tengan alto flujo, donde la alternativa sería el uso de múltiples espirales. De esta forma, se reducirá el tiempo de procedimiento, la exposición a radiación así como el coste económico especialmente en pacientes con múltiples MAVP4, 5.
En cuanto a la recurrencia de las MAVP embolizadas con Amplatzer®, a día de hoy no ha sido reportada la tasa de reperfusión4.
En nuestro caso se trataba de una MAVP voluminosa con una arteria nutricia de gran tamaño, que suponía un alto riesgo de migración de las espirales embolizantes, por lo que se prefirió utilizar el Amplatzer®. Mediante el uso de un único dispositivo se consiguió un resultado terapéutico satisfactorio con oclusión completa de la MAV y no se encontró reperfusión en los controles posteriores. No obstante, resulta recomendable el seguimiento clínico y radiológico, ya que la recanalización puede producirse incluso años después del tratamiento.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Recibido 17 Mayo 2011
Aceptado 9 Agosto 2011
Autor para correspondencia. naroasu@hotmail.com