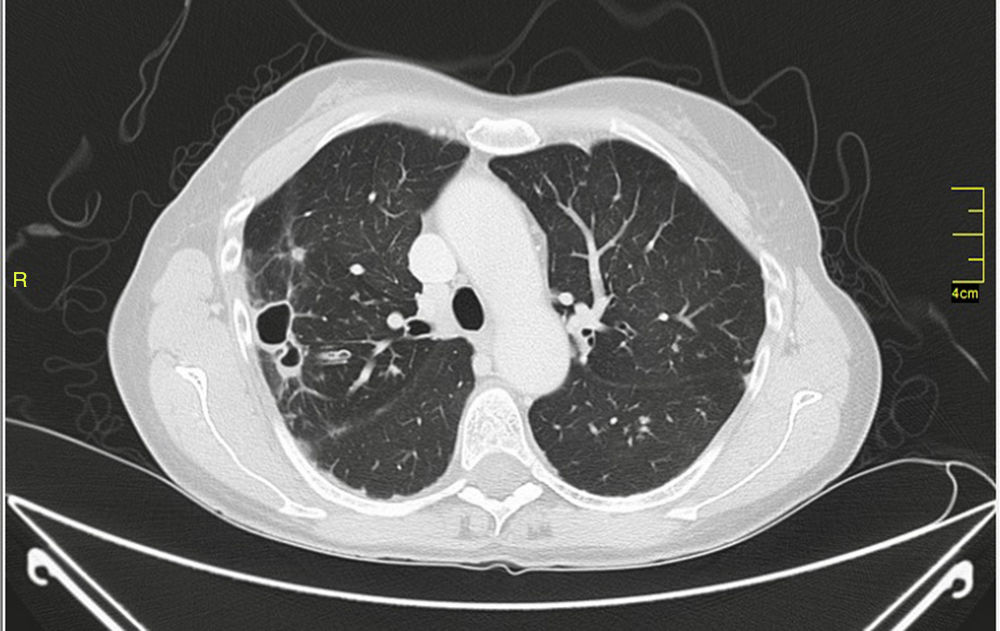
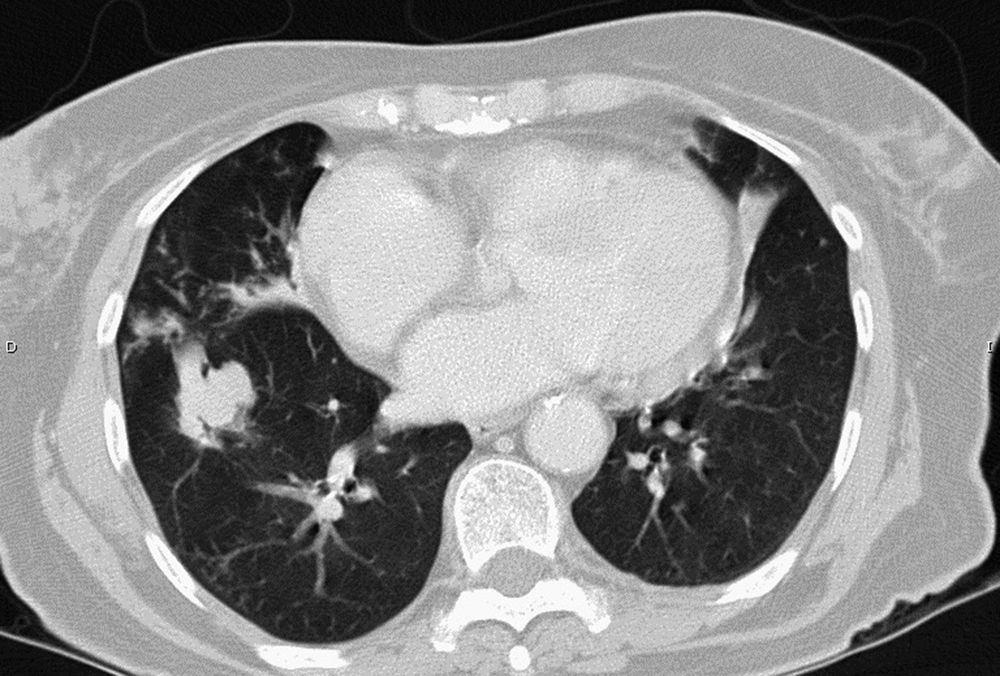
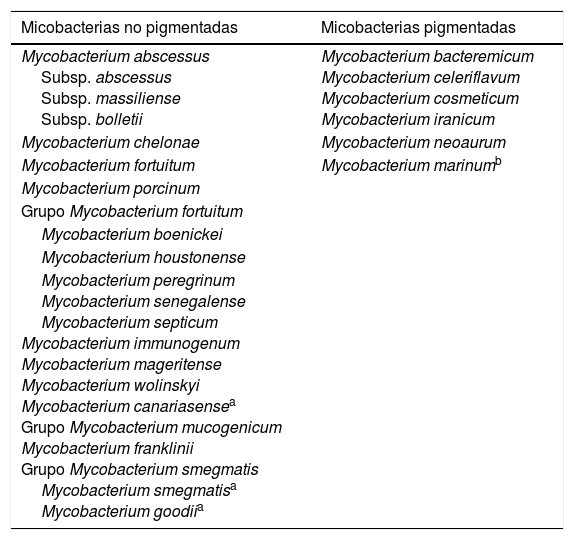
Las micobacterias no tuberculosas forman un grupo heterogéneo de microorganismos que en numerosas ocasiones son causa de infección en humanos, si bien también pueden considerarse en ocasiones como contaminantes o colonizadores. El manejo de estas infecciones debe necesariamente tener en cuenta la especie aislada y su sensibilidad in vitro (aunque no en todas ellas), así como las características del propio paciente, ya que estos tratamientos suelen ser prolongados y, necesariamente, deben ser llevados a cabo por expertos en el manejo de estas infecciones. Clásicamente divididas en micobacterias de crecimiento lento y micobacterias de crecimiento rápido, los esquemas de tratamiento y los antibióticos empleados son diferentes en ambos casos. Además, en determinadas circunstancias este tratamiento deberá necesariamente ir unido a otras medidas (retirada de cuerpos extraños, cirugía) con el objetivo de tener las máximas posibilidades de conseguir la curación del paciente.
Nontuberculous mycobacteria are a heterogeneous group of microorganisms that can often cause human infection, although they may also be considered to be contaminants or colonisers on occasions. The management of these infections must necessarily take into account the identification of isolated species and their in vitro susceptibility testing (although not for all of them), as well as the characteristics of the patient, because these treatments are usually prolonged and must be carried out by experts in the management of these infections. Classically divided into slowly growing mycobacteria and rapidly growing mycobacteria, the treatment regimens and the antibiotics used are different for both groups. In addition, in certain circumstances, this treatment must necessarily be linked to other measures (removal of foreign bodies, surgery) in order to maximise the likelihood of curing the patient.
Artículo
Socio de la Sociedad Española de Enfermedades Infecciosas y Microbiología Clínica

Para acceder a la revista
Es necesario que lo haga desde la zona privada de la web de la SEIMC, clique aquí
Comprando el artículo el PDF del mismo podrá ser descargado
Precio 19,34 €
Comprar ahora