Estudiamos la tendencia y estacionalidad de las resistencias en Escherichia coli comunitario y se cuantifica su asociación con el uso previo de determinados antibióticos.
MétodosEstudio de series temporales de las resistencias de aislados comunitarios de E. coli y su relación con el consumo de antibióticos en un área de primaria durante 2008-2012. La tendencia y estacionalidad de las resistencias se estudiaron mediante regresión de Poisson.
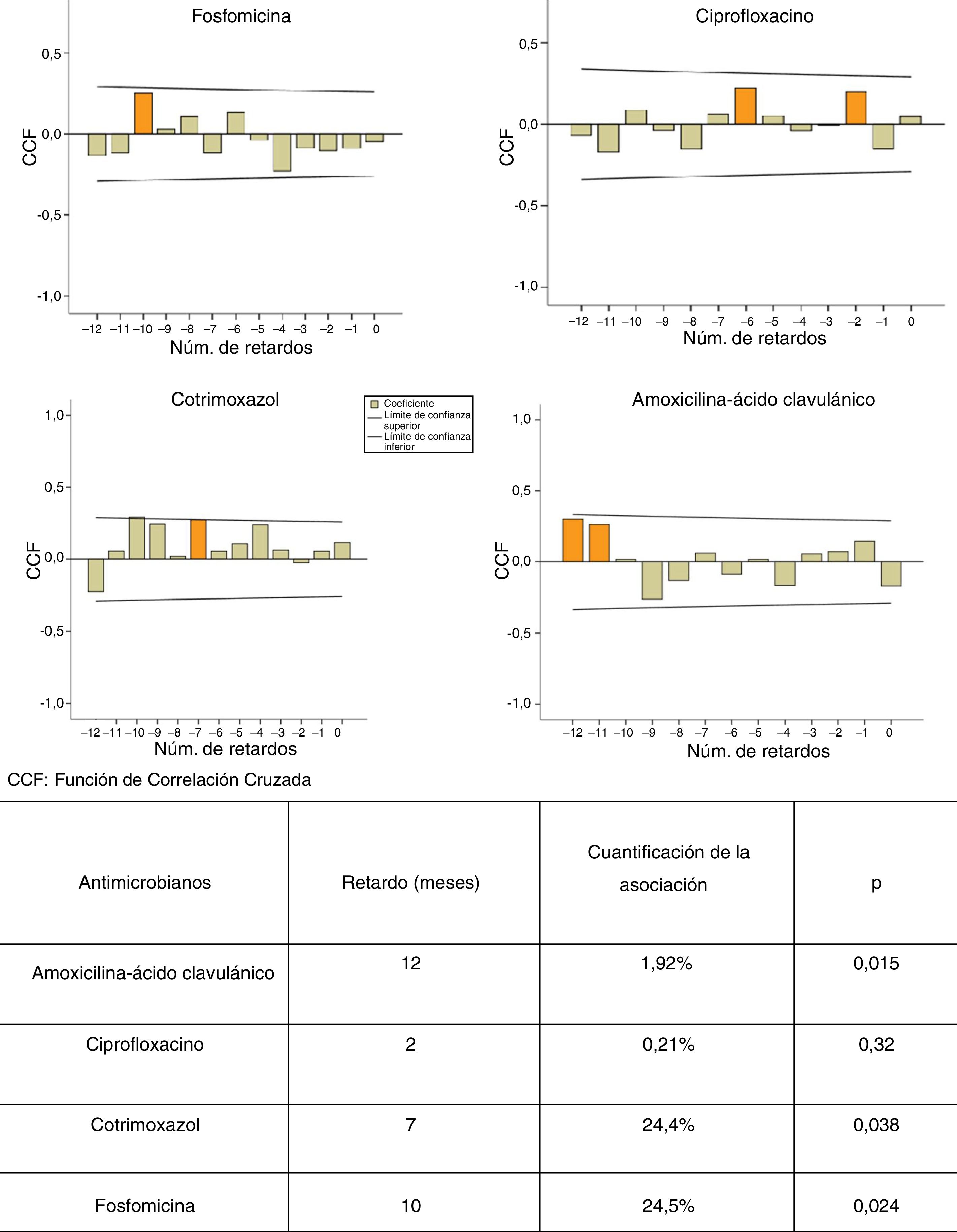
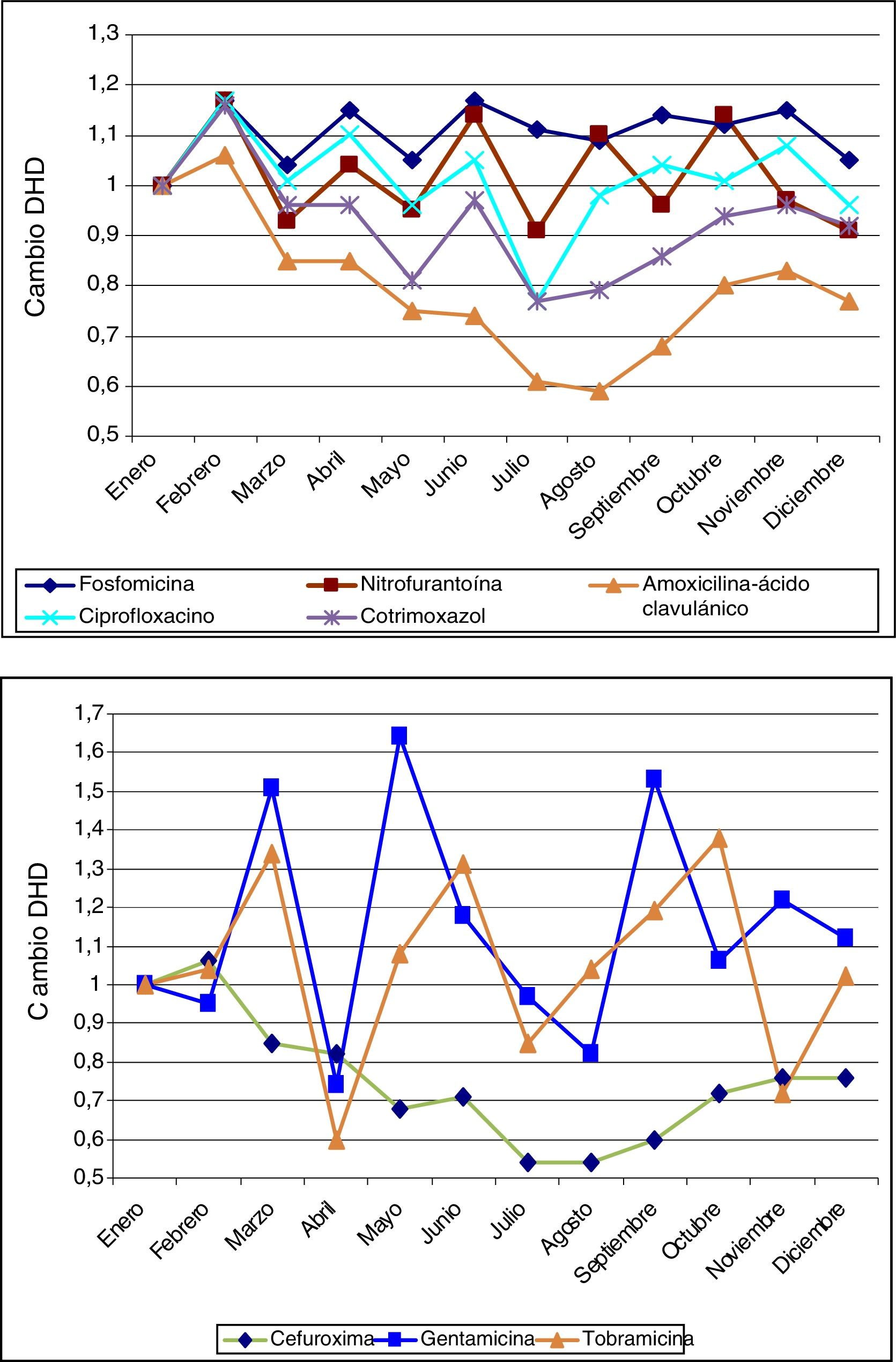
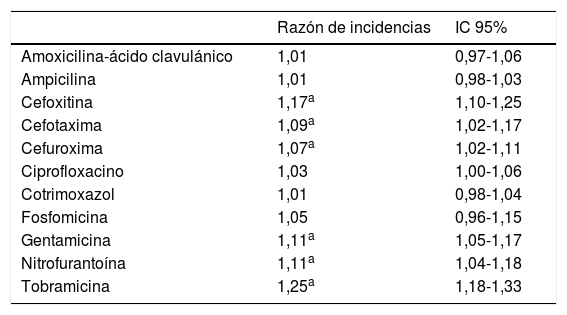
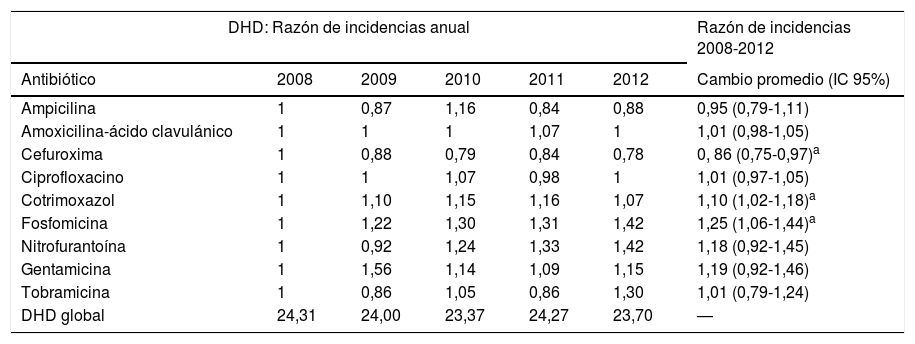
ResultadosSe observó un aumento significativo de la resistencia promedio de E. coli a cefalosporinas, nitrofurantoína y aminoglucósidos. La estacionalidad de las resistencias fue significativa en otoño-invierno para amoxicilina-ácido clavulánico y ciprofloxacino. Observamos un retardo de 7, 10 y 12 meses entre el consumo de cotrimoxazol (p<0,038), fosfomicina (p<0,024) y amoxicilina-ácido clavulánico (p<0,015), respectivamente, y la aparición de resistencias.
ConclusionesDetectamos un retardo medio de 10 meses entre la utilización de amoxicilina-ácido clavulánico, cotrimoxazol y fosfomicina, y la aparición de cepas resistentes de E. coli comunitarios.
We studied the trend and seasonality of community-acquired Escherichia coli resistance and quantified its correlation with the previous use of certain antibiotics.
MethodsA time series study of resistant community-acquired E. coli isolates and their association with antibiotic use was conducted in a Primary Health Care Area from 2008 to 2012. A Poisson regression model was constructed to estimate the trend and seasonality of E. coli resistance.
ResultsA significant increasing trend in mean E. coli resistance to cephalosporins, aminoglycosides and nitrofurantoin was observed. Seasonal resistance to ciprofloxacin and amoxicillin-clavulanic acid was significantly higher in autumn-winter. There was a delay of 7, 10 and 12 months between the use of cotrimoxazole (P<0.038), fosfomycin (P<0.024) and amoxicillin-clavulanic acid (P<0.015), respectively, and the occurrence of E. coli resistance.
ConclusionsAn average delay of 10 months between the previous use of amoxicillin-clavulanic acid, cotrimoxazole and fosfomycin and the appearance of resistant community-acquired E. coli strains was detected.
Artículo
Socio de la Sociedad Española de Enfermedades Infecciosas y Microbiología Clínica

Para acceder a la revista
Es necesario que lo haga desde la zona privada de la web de la SEIMC, clique aquí
Comprando el artículo el PDF del mismo podrá ser descargado
Precio 19,34 €
Comprar ahora