El documento incluye los aspectos clínicos para abordar el riego cardiovascular en la práctica clínica, con especial atención en el riesgo cardiovascular residual asociado a anomalías lipídicas, especialmente dislipemia aterogénica (DA).
Se propone una definición simplificada de DA para mejorar la comprensión del problema, su prevalencia y su impacto en el riesgo cardiovascular. La DA puede ser definida por aumento de los niveles de triglicéridos (≥2,3mmol/l / ≥200mg/dl) y descenso de cHDL (≤1,0 / 40 y ≤1,3mmol/l / 50mg/dl en hombres y mujeres, respectivamente) en pacientes con alto riesgo cardiovascular en tratamiento con estatinas. Se recomienda el empleo de un marcador simple para el diagnóstico y tratamiento de la DA, tal como es el colesterol-no-HDL. Para los expertos, la intervención terapéutica incluye optimización del estilo de vida y fármacos hipocolesterolemiantes (estatinas ±ezetimiba). El tratamiento de la DA residual se puede completar con la adición de fenofibrato, al objeto de mejorar el perfíl lipídico completo y reducir el riesgo de accidentes cardiovasculares en los pacientes con DA. Otras situaciones clínicas en las que se puede prescribir fenofibrato incluyen los pacientes con hipertrigliceridemias elevadas (≥5,6mmol/l / 500mg/dl), enfermos con intolerancia o resistencia a las estatinas, y pacientes con alto riesgo cardiovascular que presentan DA. Los expertos consideran que la combinación estatina-fenofibrato muestra un perfil favorable riesgo-beneficio.
En conclusión, los expertos proponen un manejo multifactorial para la prevención de la enfermedad cardiovascular aterosclerótica mediante optimización del estilo de vida, tratamiento para reducir el cLDL y tratamiento de la DA con adición de fenofibrato de forma rutinaria, al objeto de reducir el riesgo cardiovascular global del paciente.
This document has discussed clinical approaches to managing cardiovascular risk in clinical practice, with special focus on residual cardiovascular risk associated with lipid abnormalities, especially atherogenic dyslipidaemia (AD).
A simplified definition of AD was proposed to enhance understanding of this condition, its prevalence and its impact on cardiovascular risk. AD can be defined by high fasting triglyceride levels (≥2.3mmol/L / ≥200mg/dL) and low high-density lipoprotein cholesterol (HDL-c) levels (≤1,0 / 40 and ≤1,3mmol/L / 50mg/dL in men and women, respectively) in statin-treated patients at high cardiovascular risk. The use of a single marker for the diagnosis and treatment of AD, such as non-HDL-c, was advocated. Interventions including lifestyle optimization and low density lipoprotein (LDL) lowering therapy with statins (±ezetimibe) are recommended by experts. Treatment of residual AD can be performed with the addition of fenofibrate, since it can improve the complete lipoprotein profile and reduce the risk of cardiovascular events in patients with AD. Others clinical condictions in which fenofibrate may be prescribed include patients with very high TGs (≥5.6mmol/L / 500mg/dL), patients who are intolerant or resistant to statins, and patients with AD and at high cardiovascular risk. The fenofibrate-statin combination was considered by the experts to benefit from a favorable benefit-risk profile.
In conclusion, cardiovascular experts adopt a multifaceted approach to the prevention of atherosclerotic cardiovascular disease, with lifestyle optimization, LDL-lowering therapy and treatment of AD with fenofibrate routinely used to help reduce a patient's overall cardiovascular risk.
El tratamiento con estatinas es un elemento crucial en la prevención cardiovascular (CV) por su capacidad para reducir los niveles de colesterol unido a lipoproteínas de baja densidad (cLDL). Además, recientemente se ha demostrado el beneficio en la reducción de accidentes CV cuando se provoca una disminución adicional de cLDL, bien con altas dosis de estatinas o combinando una estatina con otro fármaco hipocolesterolemiante, por ejemplo ezetimiba, tal y como se demostró en el estudio IMPROVE-IT1. Sin embargo, las estatinas no eliminan el riesgo residual debido a otras alteraciones lipídicas, como es el caso de la hipertrigliceridemia y/o los niveles descendidos de colesterol unido a lipoproteínas de alta densidad (cHDL), y que es responsable de accidentes CV adicionales.
Recientemente se ha publicado un documento de consenso que incluye la opinión de expertos europeos en enfermedades CV y describe la importancia que tiene la dislipemia aterogénica (DA) en el mantenimiento de un riesgo CV elevado, así como el papel de la combinación estatina-fenofibrato para un abordaje global de la dislipemia cuando se encuentra presente una DA y el paciente requiere, además, tratamiento hipocolesterolemiante por su elevado riesgo CV2.
El presente artículo tiene como objetivo mostrar la opinión de estos expertos sobre las decisiones clínicas que afectan al manejo del riesgo CV en la práctica cuando específicamente nos encontramos con este tipo de riesgo residual asociado a la presencia de DA.
Dislipemia aterogénica y riesgo cardiovascular residualNumerosos factores contribuyen al riesgo CV, algunos de ellos no lipídicos (edad, sexo, tabaco, alcohol, diabetes mellitus, obesidad, hipertensión) y otros lipídicos (aumento de cLDL, aumento de triglicéridos y/o descenso de cHDL). Las estatinas, junto a una optimización del estilo de vida, reducen la tasa de episodios CV en muchos enfermos, pero aun así, frecuentemente los enfermos pueden presentar accidentes CV, sobre todo si persisten alteraciones en el metabolismo lipídico. Este riesgo CV se conoce como «riesgo residual», y de acuerdo con la Iniciativa para la Reducción de Riesgo Residual (R3i)3, se define como el riesgo de accidentes CV que persiste en los individuos a pesar de la consecución de los objetivos para cLDL, presión arterial y glucemia, una vez tomadas las medidas terapéuticas convencionales.
El principal obstáculo para tratar el riesgo CV residual debido a la dislipemia, particularmente a la DA (caracterizada por aumento de triglicéridos y descenso de cHDL), es precisamente la pérdida de conciencia sobre la incidencia y el impacto que puede tener la DA en el riesgo CV. De ahí la necesidad de incrementar el conocimiento sobre la importancia del riesgo residual CV asociado a la DA, y de la importancia de su tratamiento, más allá de un descenso del cLDL. Además, una vez que se establezcan y conozcan unos objetivos de tratamiento claros, así como las medidas para alcanzarlos, el médico podrá identificar y tratar mejor a los pacientes con riesgo residual, ya sea en prevención primaria o secundaria.
La DA es definida por R3i como un disbalance entre las lipoproteínas proaterogénicas ricas en triglicéridos que contienen apoB, y las lipoproteínas antiaterogénicas que contienen apoAI (como es el caso de las HDL)3. Una definición simplificada es la combinación de un exceso de triglicéridos en ayunas (≥2,3mmol/l / ≥200mg/dl) y un déficit de cHDL (≤1,0mmol/l / 40mg/dl y ≤1,3mmol/l / 50mg/dl) en hombres y mujeres, respectivamente. Aunque las concentraciones de cLDL suelen ser normales o solo moderadamente aumentadas, en la DA las partículas de LDL son típicamente pequeñas y densas.
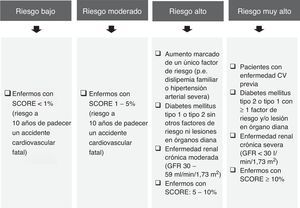
La DA es muy prevalente, especialmente en individuos de alto riesgo (criterios de la Sociedad Europea de Arteriosclerosis y de la Sociedad Europea de Cardiología) (fig. 1)4, con diabetes mellitus, síndrome metabólico5,6, enfermedad renal crónica, hiperlipemia familiar combinada7, mujeres con sobrepeso8 o mujeres con síndrome del ovario poliquístico9.
Criterios de clasificación de riesgo cardiovascular4,23.
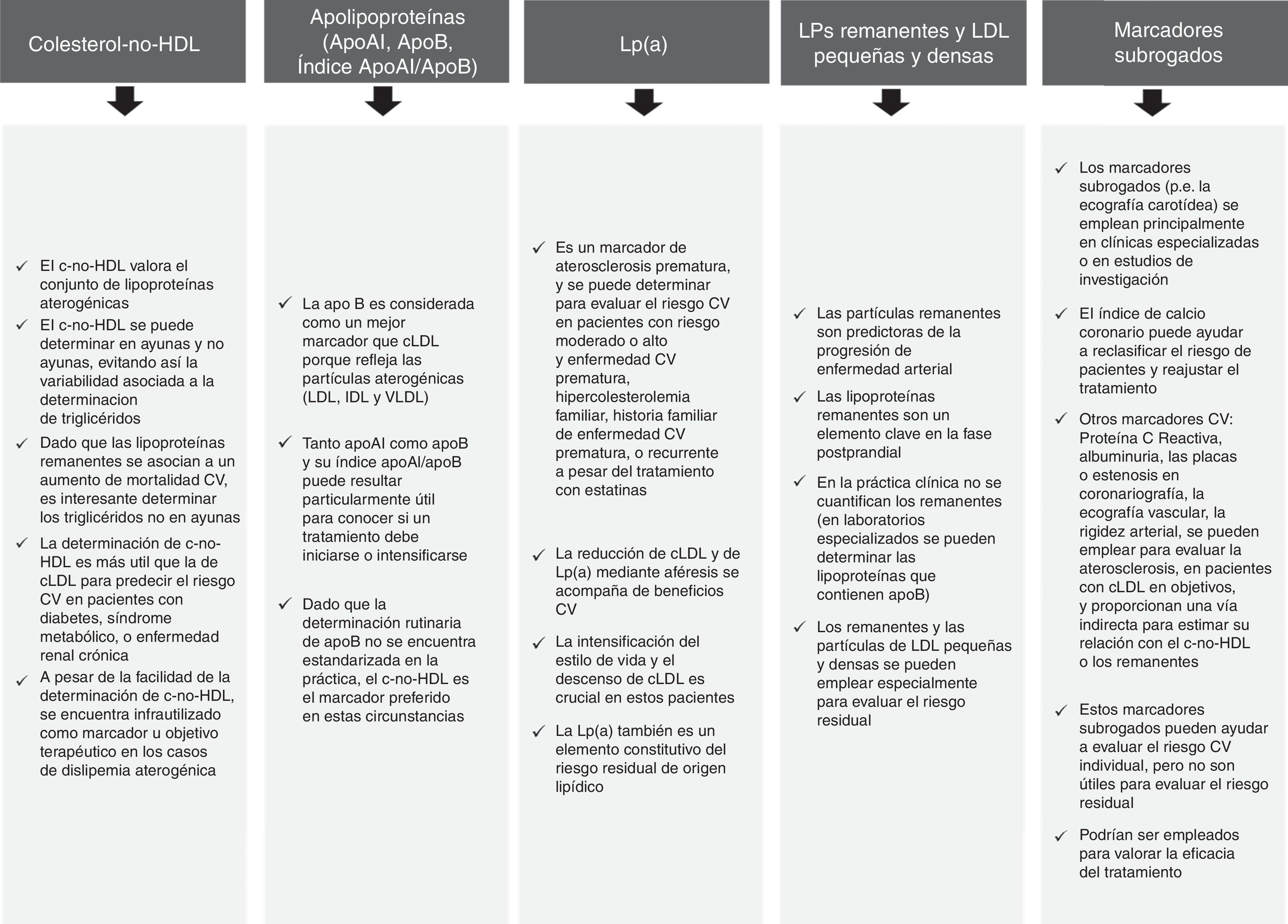
En la práctica, las determinaciones del perfil lipídico deben incluir colesterol total, cLDL, triglicéridos en ayunas y cHDL. Tanto el cLDL como el colesterol-no-HDL (c-no-HDL, calculado como colesterol total menos cHDL) son considerados como los parámetros más importantes, de tal forma que deberían ser empleados como los objetivos terapéuticos.
Adicionalmente se pueden considerar otros marcadores para abordar el riesgo residual de origen lipídico (fig. 2)10-15, si bien el empleo de uno solo de ellos, como es el c-no-HDL, puede ser particularmente útil, fácil de determinar y muy reconocido en las guías internacionales. Por este motivo, se recomienda como un objetivo terapéutico secundario en las Guías Europeas4 en los pacientes con hipertrigliceridemia y diabetes mellitus, síndrome metabólico o enfermedad renal crónica. Hay que hacer notar que en las Guía NICE16 el c-no-HDL se recomienda como un objetivo primario de tratamiento en todos los pacientes, debido a que representa la totalidad del colesterol aterogénico.
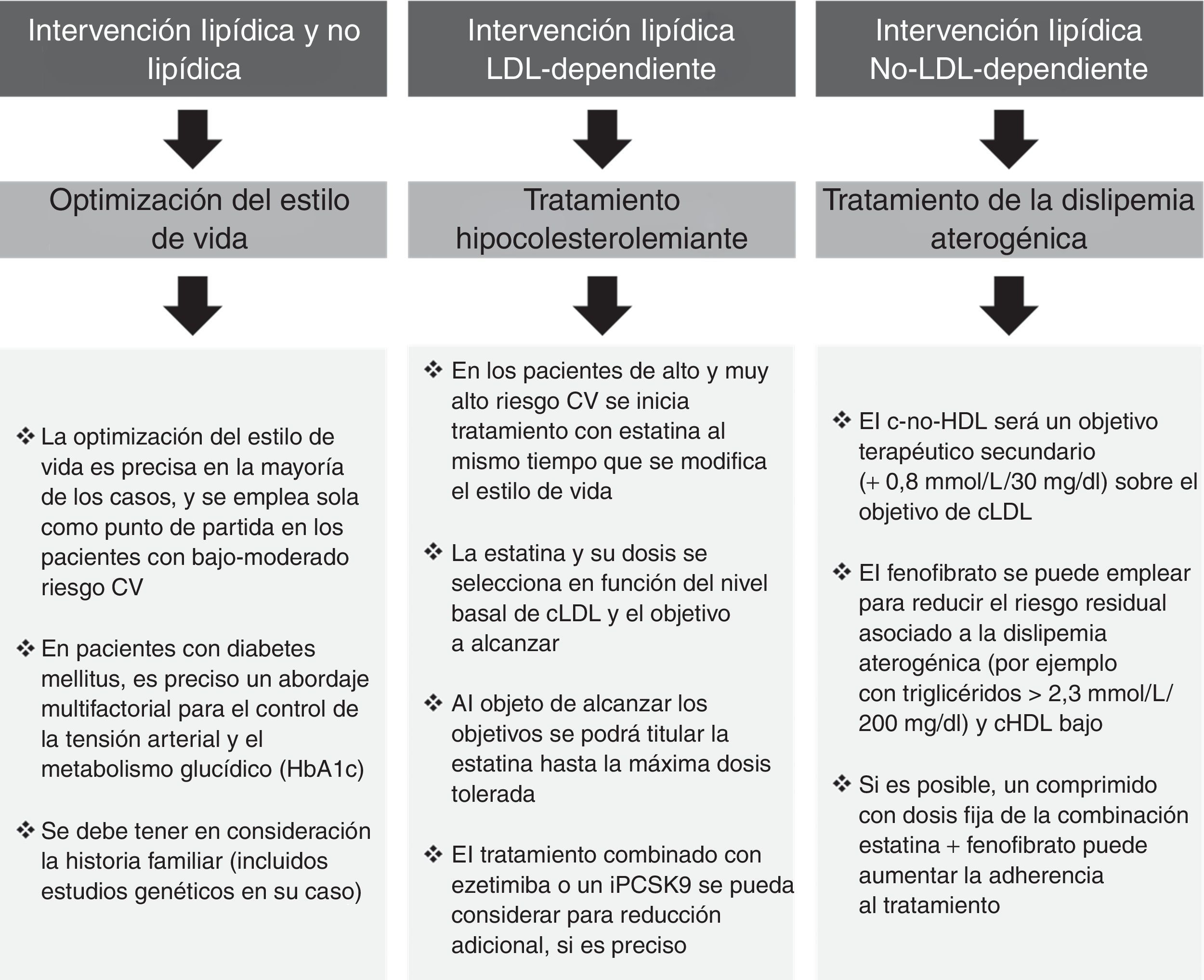
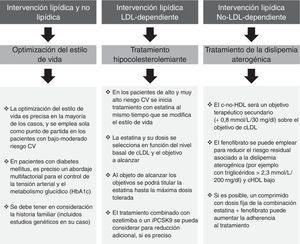
Riesgo cardiovascular globalLa naturaleza multifactorial de la enfermedad CV arteriosclerótica y de sus factores de riesgo aboca a la necesidad de un abordaje multifactorial en su prevención y en su tratamiento (fig. 3). De forma habitual, ello queda focalizado hacia 3 aspectos: 1)estilo de vida; 2)descenso de cLDL, y 3)tratamiento de la DA.
De cara a definir las actuaciones, seguiremos las recomendaciones europeas4 que proponen una individualización del tratamiento basada en el riesgo individual y en los objetivos terapéuticos, mientras que las americanas ponen énfasis exclusivamente en el descenso del cLDL17.
Optimización del estilo de vidaEs imprescindible sensibilizar al paciente de que mejore su dieta, aumente el nivel de ejercicio físico, limite la ingesta de alcohol, cese el hábito tabáquico o se valore su patrón de sueño; y todas estas medidas no deben ser infraestimadas. Los cambios en el estilo de vida pueden mejorar la DA, paralelamente a un descenso del 5-10% en el peso corporal. El impacto del estilo de vida es aún mayor en los pacientes con diabetes mellitus tipo2, incluido su efecto favorable en el control glucémico.
Tratamiento hipocolesterolemianteEn los pacientes con alto o muy alto riesgo, habitualmente se inicia el tratamiento hipolipemiante con estatinas al mismo tiempo que los cambios en el estilo de vida. En las Guías Europeas, los objetivos de cLDL se establecen de acuerdo con el riesgo CV individual: <2,5mmol/l / 100mg/dl y <1,8mmol/l / 70mg/dl para los pacientes con alto y muy alto riesgo, respectivamente4. También hay que destacar que un descenso adicional con tratamiento combinado (estatina más ezetimiba) puede llegar a ofrecer mayores reducciones de riesgo1. Este beneficio, tanto absoluto como relativo, es superior en los pacientes con diabetes mellitus18, y puede evidenciar la necesidad de incluir descensos aún más acusados en las futuras guías de práctica clínica, esto es, más allá de 70mg/dl en los pacientes de muy alto riesgo o en prevención secundaria19.
Tratamiento de la dislipemia aterogénicaEl impacto de la DA en el riesgo CV residual es de tal magnitud que incluso los pacientes en tratamiento con estatinas y con cLDL controlado tienen un 71% más de riesgo para episodios CV graves si también tienen alteraciones en los triglicéridos y/o del cHDL20. Por tanto, el tratamiento de la DA en los pacientes con alto o muy alto riesgo, incluyendo aquellos con diabetes mellitus, puede reducir significativamente los accidentes CV.
Detrás de este hecho subyace que, si bien las lipoproteínas aterogénicas más importantes son las LDL, otras lipoproteínas que contienen apoB (por ejemplo, las lipoproteínas ricas en triglicéridos y sus remanentes) pueden contribuir al depósito de colesterol en la íntima21. Además, el tamaño de las lipoproteínas es un determinante clave para la aterogénesis, de tal forma que las partículas remanentes que vehiculizan triglicéridos penetran en la íntima y son retenidas en la matriz del tejido conectivo, contribuyendo así a la formación y progresión de la placa de ateroma21. Por tanto, estos aspectos patogénicos justifican la relevancia que tiene un tratamiento adicional de la DA, incluso en combinación con estatinas, al objeto de reducir el riesgo CV residual22. En una proporción muy considerable de pacientes de alto riesgo no se alcanzan los objetivos de cLDL, incluso empleando altas dosis de estatinas o la combinación estatina y ezetimiba, o tienen una DA adicional. En estos pacientes, y con el fin de disminuir su riesgo, se ha propuesto una reducción mínima del 50% en cLDL4,23 así como el tratamiento adicional del exceso de triglicéridos y/o el déficit de cHDL, si es que existen tales alteraciones. En la práctica, estas últimas anomalías se han tratado con niacina o con fibratos, siendo el fenofibrato el fármaco que ha mostrado una interacción farmacológica más favorable para el empleo junto a las estatinas, por lo que se considera de elección para dicha combinación24. La niacina asociada a la estatina no ha mostrado beneficio adicional con respecto a la monoterapia con estatinas, y como fármaco hipocolesterolemiante es menos potente que las estatinas25; además, por los resultados de los últimos ensayos clínicos, y debido a su riesgo/beneficio y sus efectos secundarios, se ha desaconsejado su empleo en Europa. Finalmente, los inhibidores de la proproteína convertasa subtilisina/kexina tipo 9 (PCSK9) se encuentran en fase reciente de comercialización, y aunque aportan un potente efecto hipocolesterolemiante adicional, no disponemos de estudios definitivos sobre la DA, aunque sí sobre la lipoproteína(a) [Lp(a)]26.
FenofibratoEl beneficio de la combinación estatina-fenofibrato en los pacientes con DA se ha demostrado en el estudio ACCORD-Lipid20, en el que los pacientes diabéticos con DA que recibían el tratamiento combinado reducían en un 31% su riesgo de muerte por causas CV, infarto de miocardio o ictus, comparados con los pacientes que recibían estatina sola, y el NNT para conseguir este beneficio resultó ser de 20 pacientes durante 5años27. Estos datos obligan a considerar el empleo de fármacos no estatinas, como es el fenofibrato, para el tratamiento de la DA cuando esté presente, según lo que se ha comprobado también en los subanálisis del estudio FIELD28, si bien habría que conocer evidencias definitivas sobre morbimortalidad en estudios específicamente diseñados al efecto.
El fenofibrato se recomienda para disminuir la trigliceridemia4. Al objeto de evitar fluctuaciones debidas a las variaciones en las determinaciones de los triglicéridos puede resultar muy beneficioso el empleo del c-no-HDL como objetivo terapéutico (a un nivel de 0,8mmol/l / 30mg/dl más que el nivel de cLDL considerado objetivo) a la hora de iniciar tratamiento con fenofibrato en los pacientes con DA.
Importancia del tratamiento combinadoSegún lo señalado anteriormente, de cara a una mejoría en el perfil lipídico global será preciso considerar el tratamiento combinado en los pacientes de alto y muy alto riesgo, todo ello de acuerdo con los beneficios obtenidos mediante la combinación de estatinas con ezetimiba1 o con un inhibidor de PCSK929, o bien mediante la asociación de estatina y fenofibrato en los pacientes con DA20.
La adherencia es un elemento clave en el tratamiento de los factores de riesgo, tal y como se ha demostrado en la hipertensión arterial o con la diabetes mellitus. La adherencia a los tratamientos crónicos no es, ni mucho menos, óptima, y esto es especialmente comprobable con los tratamientos hipolipemiantes. Además, la adherencia al tratamiento de los factores de riesgo es crucial en los pacientes en prevención secundaria, y se ha comprobado que se acompaña de una reducción de los accidentes CV30.
En este sentido, reducir el número de comprimidos a tomar con fármacos asociados en combinación fija puede ser altamente interesante, aunque no dispongamos de datos clínicos definitivos sobre su impacto en la adherencia y cumplimiento terapéutico. De esta forma, una asociación de estatina con fenofibrato puede ser particularmente útil en los pacientes con diabetes mellitus, o en prevención secundaria, por cuanto estos pacientes suelen precisar polifarmacia31.
Empleo de fenofibrato en la práctica clínicaEl fenofibrato se emplea habitualmente en la práctica clínica para el tratamiento de la DA residual en pacientes tratados con estatinas y reducir así el riesgo asociado a la DA, ya sea en pacientes con o sin diabetes, y a pesar de que el tratamiento de la DA no sea un objetivo prioritario en sí mismo.
Las indicaciones aprobadas para el fenofibrato se encuentran bien definidas. De acuerdo con la Agencia Europea del Medicamento (EMA), el fenofibrato está indicado como tratamiento asociado a la dieta y al estilo de vida en las siguientes circunstancias:
- •
Hipertrigliceridemia severa, con o sin niveles bajos de cHDL.
- •
Hiperlipemia mixta, cuando la estatina no se tolera, o se encuentra contraindicada32.
- •
Hiperlipemia mixta en pacientes de alto riesgo CV, además de la estatina, cuando los triglicéridos y el cHDL no se encuentran debidamente controlados33.
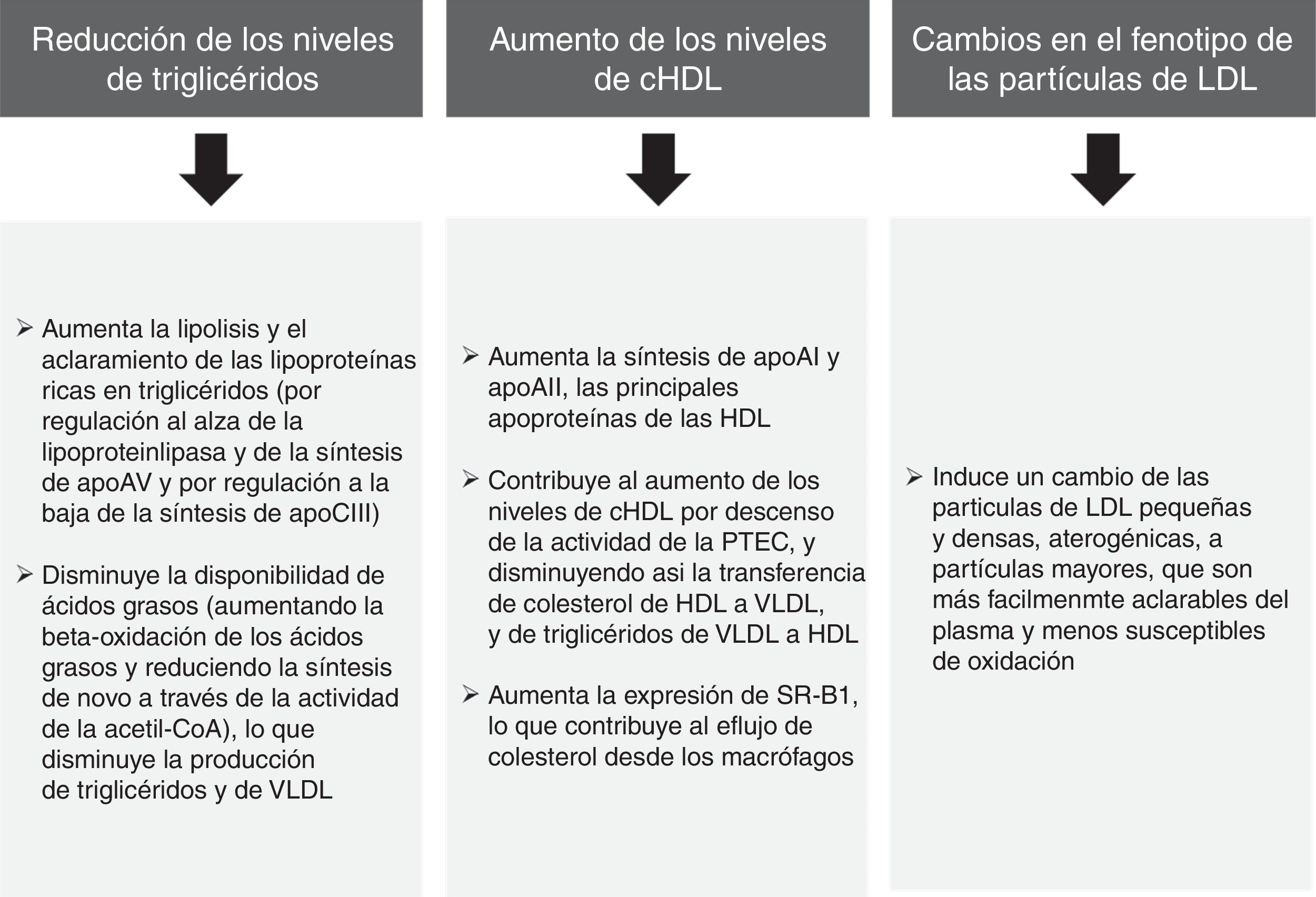
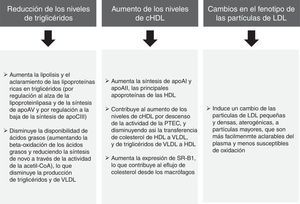
Los análisis agrupados de los ensayos clínicos en pacientes con dislipemia mixta en los que se evalúa el ácido fenofíbrico (metabolito activo del fenofibrato) en combinación con las estatinas más potentes (simvastatina, atorvastatina y rosuvastatina) ha permitido comprobar que esta combinación mejora significativamente el perfil lipoproteico global en los pacientes con DA34. El subanálisis de los pacientes con diabetes mellitus también demostró que la combinación producía un mayor beneficio en el perfil lipídico comparado con las estatinas en monoterapia35. De esta forma, hay que señalar de forma inequívoca que los efectos lipídicos del fenofibrato (fig. 4) pueden ayudar a reducir el riesgo de complicaciones macrovasculares en los enfermos con DA, y especialmente cuando existe DA.
Efectos lipídicos del fenofibrato52,53.
En la figura 5 se incluyen aquellas situaciones asociadas a las indicaciones clínicas, de acuerdo con su perfil lipídico, la presencia/ausencia de diabetes y los tratamientos concomitantes. Al margen de estas, el tratamiento con fenofibrato también se puede considerar en aquellos pacientes que no alcanzan objetivos de cLDL a pesar de tratamiento hipocolesterolemiante intensivo, y que tienen un exceso de triglicéridos y un cHDL bajo, o son pacientes de alto y muy alto riesgo, o en prevención secundaria. Esto se debe a que, aunque el efecto del fenofibrato sobre cLDL es moderado, tiene un efecto favorable disminuyendo las partículas LDL pequeñas y densas, características de la DA.
¿Cuándo se emplea fenofibrato en primera, segunda y tercera línea de tratamiento?El fenofibrato se puede emplear en monoterapia en aquellos pacientes con triglicéridos muy elevados (≥5,7mmol/l / 500mg/dl) con el objeto de disminuir el riesgo de pancreatitis aguda. También se puede prescribir en primera línea en los individuos que estando en prevención primaria o secundaria, o teniendo un alto o muy alto riesgo CV, son resistentes o intolerantes a las estatinas y tienen elevaciones moderadas de la trigliceridemia. Hay que señalar que en un consenso reciente de la Sociedad Europea de Arteriosclerosis sobre los síntomas musculares asociados a la toma de estatinas se recomienda en primer lugar añadir ezetimiba con o sin fibrato (no gemfibrocilo) para alcanzar los objetivos terapéuticos de cLDL36. El fenofibrato es empleado en segunda o tercera línea de tratamiento, después de la optimización del estilo de vida y del tratamiento con estatina asociada a ezetimiba.
Asimismo se considera la posibilidad de emplear el fenofibrato en primera línea de tratamiento en pacientes con DA y resistencia a la insulina (sin aumento de cLDL). Muchos pacientes sin historia CV previa pero con DA y síndrome metabólico, obesidad abdominal o diabetes mellitus tipo2 también pueden ser considerados como pacientes de alto riesgo y susceptibles de ser tratados con una combinación estatina-fenofibrato37.
¿Se emplea fenofibrato en diabéticos y en no diabéticos?La diabetes es una situación asociada a un incremento de riesgo CV y, como tal, los pacientes con diabetes tipo2 son considerados de alto o muy alto riesgo de acuerdo con las Guías Europeas (ESC/EAS)4 o de diabetes (EASD)38. En estos pacientes es fundamental controlar la DA, lo que se puede conseguir con fenofibrato. Sin embargo, aunque el empleo de fenofibrato es adecuado en el diabético porque frecuentemente tiene DA, hay que señalar que el empleo del fármaco es independiente de la existencia o no de diabetes, porque depende más específicamente de la existencia o no de DA. Adicionalmente, la Guía de ESC/EAS recomienda tratar con fármacos a los pacientes con alto riesgo CV y con hipertrigliceridemia >2,3mmol/l / 200mg/dl que no se controla solo con estilo de vida.
En opinión de los expertos, otras posibles aplicaciones del fenofibrato en pacientes diabéticos son la existencia de arteriosclerosis subclínica, sobrepeso u obesidad39,40. En un reciente metaanálisis41 se demuestra claramente que los pacientes con aumento de triglicéridos y descenso de cHDL que son tratados con fibratos logran reducir la tasa de enfermedad CV.
El fenofibrato puede ser especialmente útil en los pacientes con riesgo cardiometabólico. En experimentación animal, la activación de los PPAR-alfa reduce la adiposidad visceral, tiene efectos beneficiosos en las células beta-pancreáticas y mejora la acción periférica de la insulina42.
Más allá de sus efectos beneficiosos modificando el perfil lipídico, el fenofibrato también es valorado por otros efectos mediados por los PPAR-alfa, como la reducción del fibrinógeno y de los mediadores proinflamatorios, o la mejoría en la vasodilatación43. Estos hechos pueden relacionarse con la mejoría en las complicaciones microvasculares del diabético: retinopatía (demorando la necesidad de fotocoagulación con láser), neuropatía (disminuyendo la necesidad de amputaciones no traumáticas) y nefropatía (disminuyendo la albuminuria)44-46. De hecho, el fenofibrato ha sido aprobado en Australia para controlar la progresión de la retinopatía diabética, junto al control de la presión arterial, el control glucémico y el lipídico)47.
¿En qué categoría de riesgo se emplea fenofibrato?El fenofibrato se debería emplear en pacientes con alto o muy alto riesgo CV para, específicamente, controlar los triglicéridos y el cHDL4 (fig. 4). En los pacientes con riesgo moderado se debe considerar en primer lugar la intensificación del estilo de vida, antes de valorar el empleo de fármacos.
Los expertos consideran el empleo de fenofibrato en los pacientes con DA y alto riesgo cardiometabólico, así como en aquellos con DA y arteriosclerosis subclínica.
También hay que considerar que su empleo más relevante habrá de ser en prevención secundaria (por ejemplo, pacientes con cLDL controlado o no con máximas dosis de estatina o estatina más ezetimiba, pero que mantienen cifras elevadas de triglicéridos con o sin cHDL bajo). También se puede considerar su empleo en prevención primaria en pacientes con diabetes mellitus tipo2. El tratamiento combinado en un solo comprimido puede ser muy útil para aumentar la adherencia al tratamiento.
No obstante, la separación entre prevención primaria y secundaria es a veces arbitraria debido a que la arteriosclerosis es un proceso continuo23, de tal forma que puede tener más interés el cálculo del riesgo CV individual, incluso en los pacientes diabéticos en los que la lesión o la indemnidad de órganos diana puede marcar la diferencia38.
¿Cuál es la seguridad con fenofibrato a largo plazo?La opinión de los expertos es que el fenofibrato es un fármaco bien tolerado, sin que se acompañe de consideraciones de interés sobre su seguridad. Se tolera mejor que el gemfibrocilo, que se debe evitar cuando se asocia a estatinas, para evitar el riesgo de miotoxicidad24.
Aunque se ha comprobado que puede acompañarse de un aumento de los niveles de creatinina plasmática, no es seguro que se deba a un deterioro de la función renal48. Este incremento es reversible una vez que se deja de administrar el fármaco49, y tampoco se ha demostrado que provoque un incremento en la enfermedad renal avanzada20. En términos generales, se debe evitar el empleo de fenofibrato en pacientes con insuficiencia renal avanzada (eGFR<30ml/min), y ha de ser empleado con precaución en pacientes con insuficiencia renal moderada (eGFR entre 30 y 60ml/min)50.
Asimismo es preciso monitorizar los síntomas musculares, así como la función hepática y renal, muy especialmente en los enfermos con historia de sintomatología asociada al empleo de hipolipemiantes50.
También se ha comprobado un incremento en la homocisteína, que no tiene repercusión en el riesgo CV51, de tal forma que los pacientes se benefician del tratamiento a pesar de esta mencionada elevación.
ConclusiónLas alteraciones lipídicas que forman parte de la DA contribuyen al riesgo CV residual de un porcentaje significativo de pacientes en los que el cLDL ha sido adecuadamente controlado con estatinas. El control de este problema es claramente insuficiente y, por ello, es necesario promover la sensibilización sobre el mismo. Así mismo, es preciso destacar que el primer objetivo terapéutico en los pacientes con DA es el cLDL, o si no se puede disponer de este, el c-no-HDL, y en segundo lugar los triglicéridos. El tratamiento de la DA incluye optimizar el estilo de vida y las estatinas, asociadas o no a ezetimiba, y en un segundo lugar, si persiste un exceso de triglicéridos, puede ser necesaria la adición de fenofibrato. La combinación estatina-fenofibrato muestra un perfil favorable riesgo/beneficio. En los pacientes con hipertrigliceridemia grave (≥5,6mmol/l / 500mg/dl) el primer objetivo es disminuir los triglicéridos con fenofibrato para prevenir la pancreatitis.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Grupo de trabajo de Dislipemia Aterogénica de la Sociedad Española de Arteriosclerosis: Juan F. Ascaso, Mariano Blasco, Ángel Brea, Ángel Diaz, Antonio Hernández Mijares, Teresa Mantilla, Jesús Millán (Coordinador), Juan Pedro-Botet y Xavier Pintó.
Grupo Europeo de Expertos: Roberto Ferrari, Carlos Aguiar, Eduardo Alegria, Riccardo C. Bonadonna, Francesco Cosentino, Moses Elisaf, Michel Farnier, Jean Ferrières, Pasquale Perrone Filardi, Nicolae Hancu, Meral Kayikcioglu, Alberto Mello e Silva, Jesus Millan, Željko Reiner, Lale Tokgozoglu, Paul Valensi, Margus Viigimaa, Michal Vrablik, Alberto Zambon, José Luis Zamorano y Alberico L. Catapano.