La reparación de la hernia incisional gigante requiere una técnica de disección compleja, con un alto riesgo de complicaciones posoperatorias.
Presentamos un caso de eventración recidivada en el que se realizó una técnica de separación de componentes para su cierre primario. El caso se complicó con un sangrado posoperatorio secundario a la lesión inadvertida de un vaso perforante, por lo que tuvo que ser reintervenido de urgencias. A los 3 días fue dado de alta sin más complicaciones. A los pocos días reingresó por isquemia intestinal con síndrome compartimental abdominal asociado, que se trató mediante laparotomía descompresiva dejando el abdomen abierto. Posteriormente se realizó el cierre primario diferido con una segunda técnica de separación de componentes, controlando las presiones de cierre aponeurótico mediante un dinamómetro digital. Al año de seguimiento el paciente mantiene una buena calidad de vida, y se descarta recidiva herniaria mediante tac de control.
A pesar de tratarse de una dolencia benigna, no debemos menospreciar las importantes complicaciones que pueden aparecer en el posoperatorio, sobre todo cuando se trata de una hernia incisional de gran tamaño que ha precisado una disección considerable de la pared abdominal.
En el contexto de cualquier posoperatorio de cirugía abdominal, cuando un paciente presenta distensión y dolor abdominal hay que descartar la existencia de hipertensión intraabdominal para evitar la progresión al síndrome compartimental agravado con una alta mortalidad a la que este se asocia.
Large incisional hernia repair requires a laborious dissection and it is associated with a high risk of postoperative complications.
We present a case of recurrent incisional hernia in which an anatomic component separation technique was performed for primary closure. The patient presented complications with postoperative bleeding due to a perforant vessel undetected damage so he had to be reoperated. After 3 days he was discharged without complications. Afterwards he was readmitted to the hospital because of an intestinal ischaemia associated with abdominal compartment syndrome that was treated by decompressive laparotomy leaving an open abdomen. Subsequently, a delayed primary closure with a second separating components technique was carried out, controlling the tension strength edge while aponeurotic closure was performed using a digital dynamometer. After one year, the patient maintains a good quality of life with no recurrence shown in a CT scan.
Although it is a benign disease, the serious complications that can occur in the postoperative setting should not be underestimaed, especially when a large incisional hernia is present and an important dissection of the abdominal wall has been performed.
In the context of any postoperative abdominal surgery, when a patient has bloating and abdominal pain, it is mandatory to rule out the existence of intra-abdominal hypertension to prevent the development of a compartment syndrome, thus reducing the risk of mortality.
Hoy en día, el tratamiento de la hernia incisional de gran tamaño sigue siendo un complejo desafío para el cirujano, puesto que para su reparación se precisa una disección importante de la pared abdominal, que puede ocasionar un mayor número de complicaciones posoperatorias1. Además de realizar dicha disección, es necesario añadir una opción técnica para el cierre primario sin tensión, evitando –en la medida de lo posible– el riesgo de dehiscencia de la sutura. Entre las opciones se encuentra la técnica de separación anatómica de componentes (SAC) descrita por Ó. M. Ramírez et al. en 19902, reforzándose habitualmente con la colocación de material protésico para prevenir la recidiva lateral3.
Se presenta un caso de eventroplastia y técnica de SAC en una hernia incisional de gran tamaño que se complicó por una hemorragia posoperatoria que precisó la reintervención para el control hemostático. El paciente, tras el alta, reingresó en estado de shock y con un síndrome compartimental abdominal (SCA) que precisó la descompresión quirúrgica y un segundo cierre diferido mediante nueva técnica de SAC, controlando el cierre sin tensión mediante dinamometría.
La rareza y gravedad de la complicación evidenciada en el posoperatorio de la eventroplastia constituye el objetivo de la publicación del caso.
Caso clínicoVarón de 66 años, ASA III, con antecedentes de HTA, obesidad (IMC 35), EPOC severa tratada con corticoterapia inhalatoria y oxigenoterapia domiciliaria, resección de vólvulo intestinal y eventroplastia. Ingresa en la Unidad de Pared Abdominal del Servicio de Cirugía General para tratamiento quirúrgico electivo de una gran eventración recidivada multisacular de la línea media, de 20×12cm (M2M3M4W3R1 según la clasificación de la EHS4). Bajo anestesia general, y administración previa de antibioterapia parenteral profiláctica (amoxicilina y ácido clavulánico), se realizó una laparotomía media suprainfraumbilical, lisis de adherencias yeyunoileales al saco herniario, resección completa de este, cierre del defecto después de concluir una técnica de SAC nivel 13 y colocación de una malla de polipropileno supraaponeurótica de 30×30cm, fijada con sutura continua de polipropileno a modo de corona. Se colocaron dos drenajes tubulares, perforados y aspirativos tipo Redón® subcutáneos.
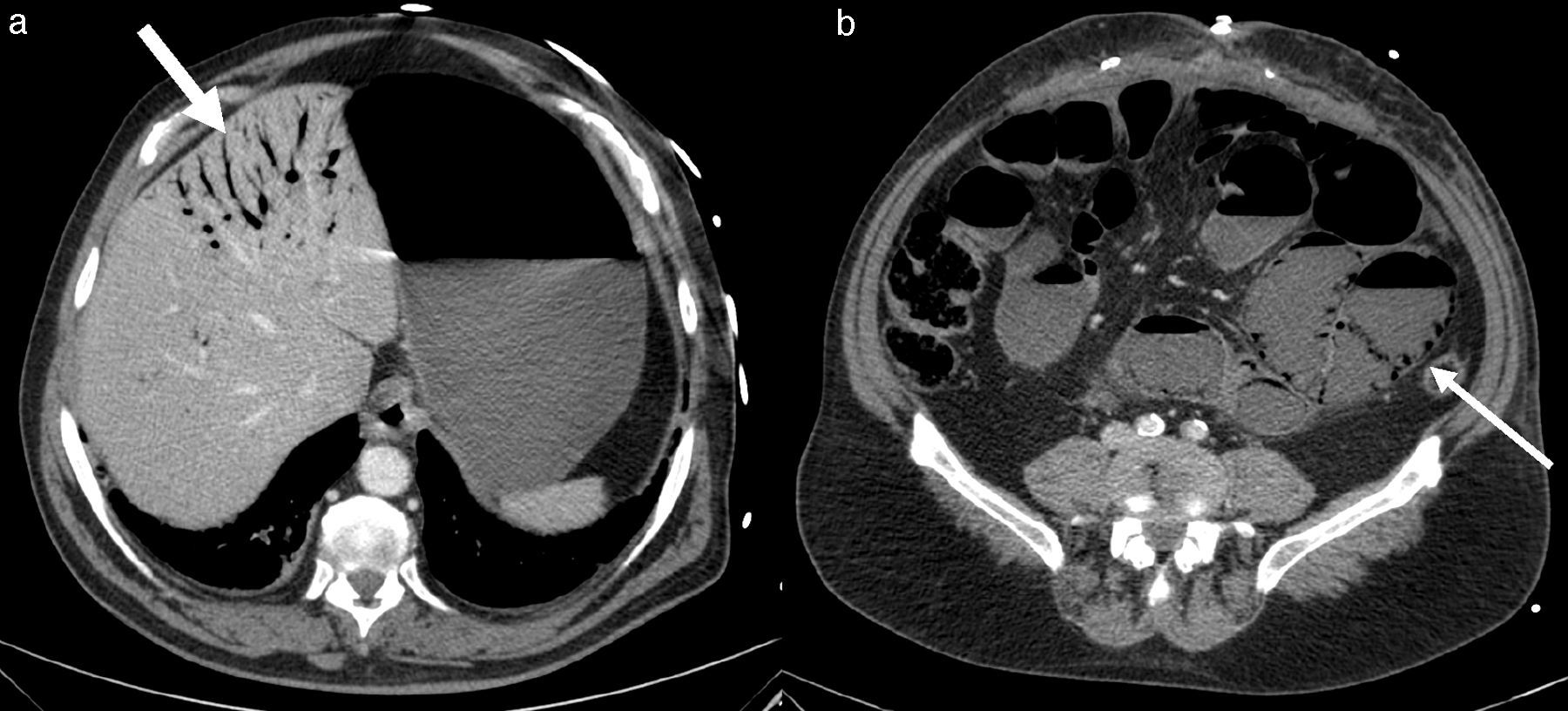
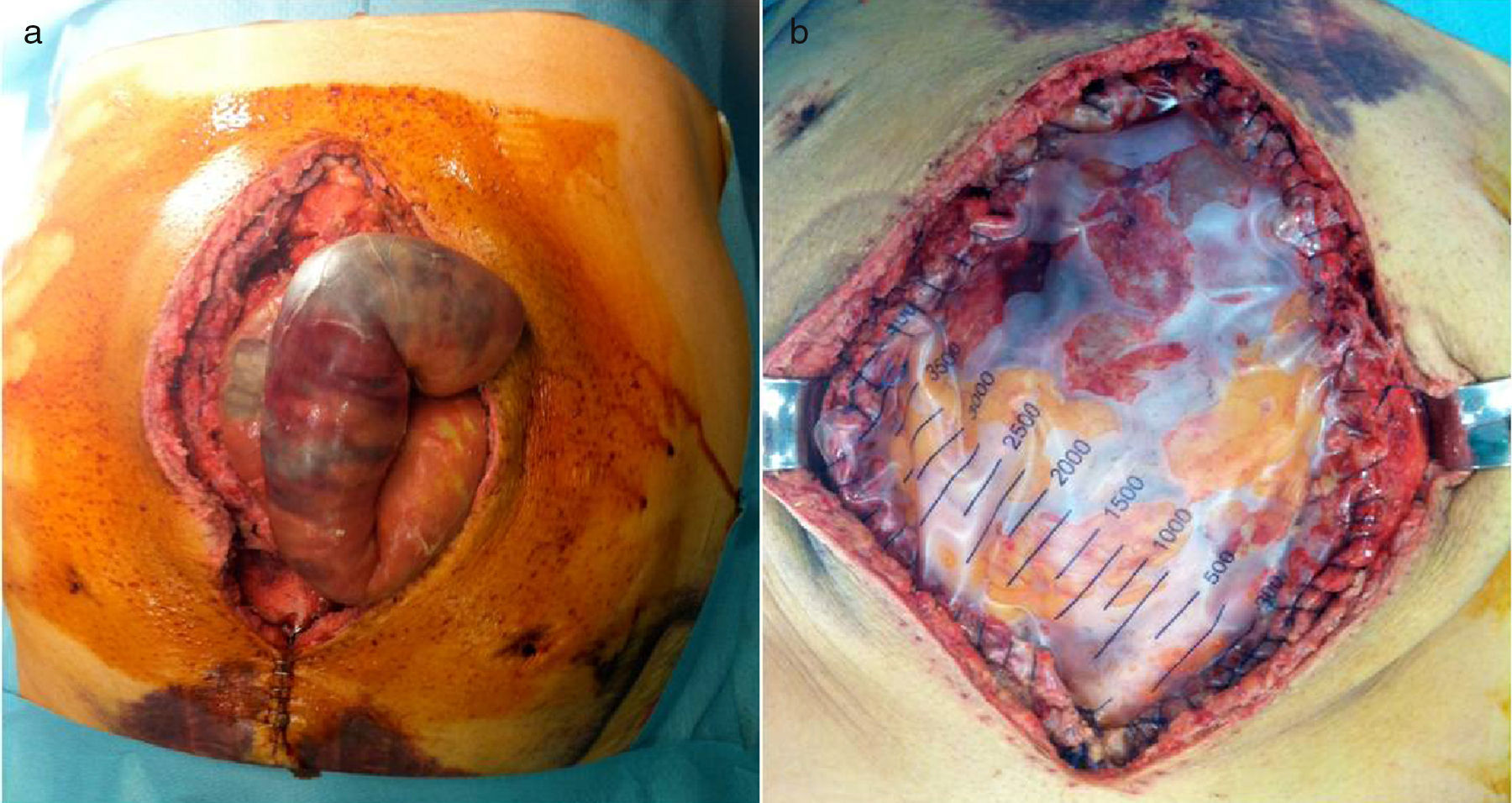
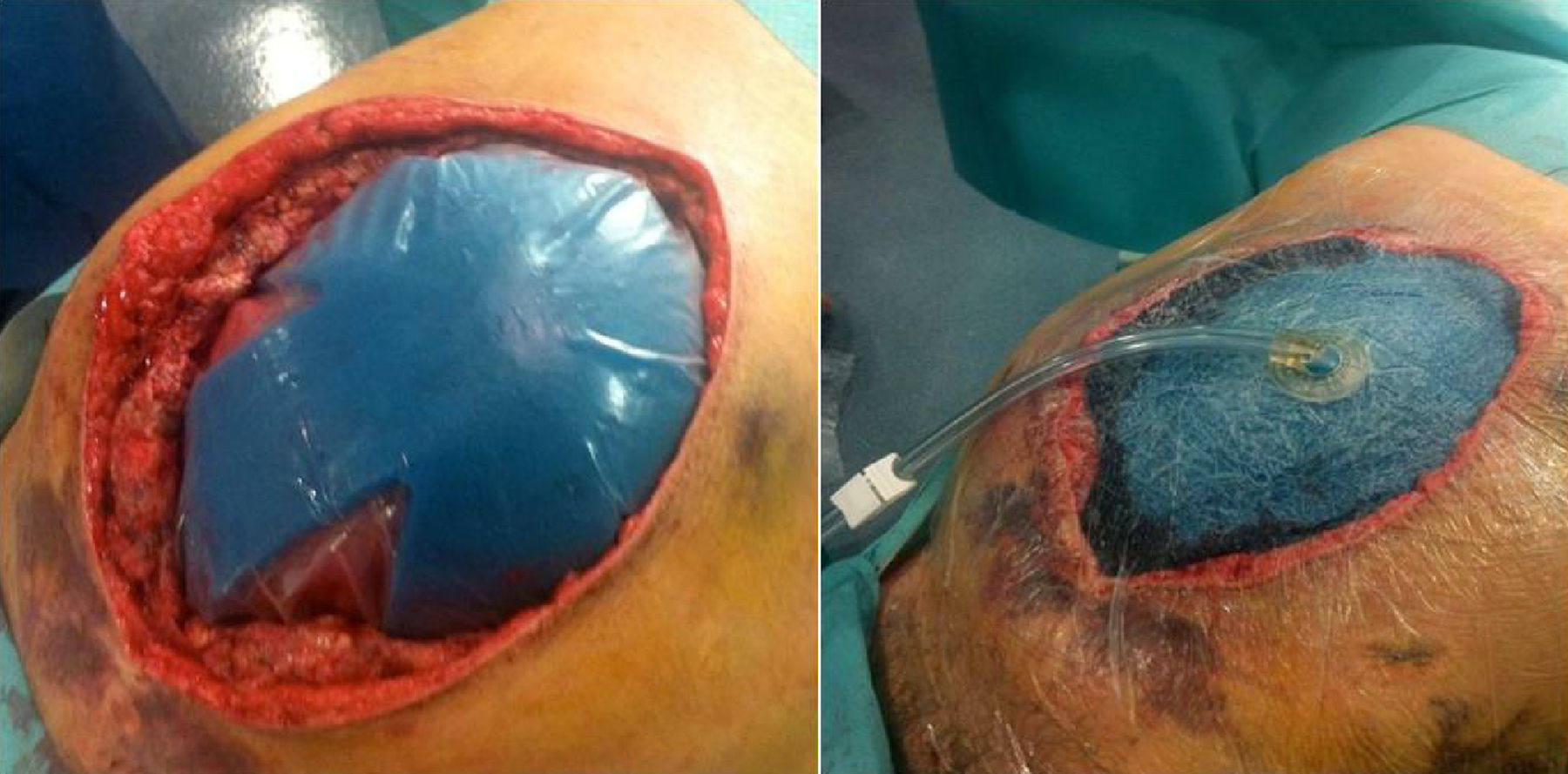
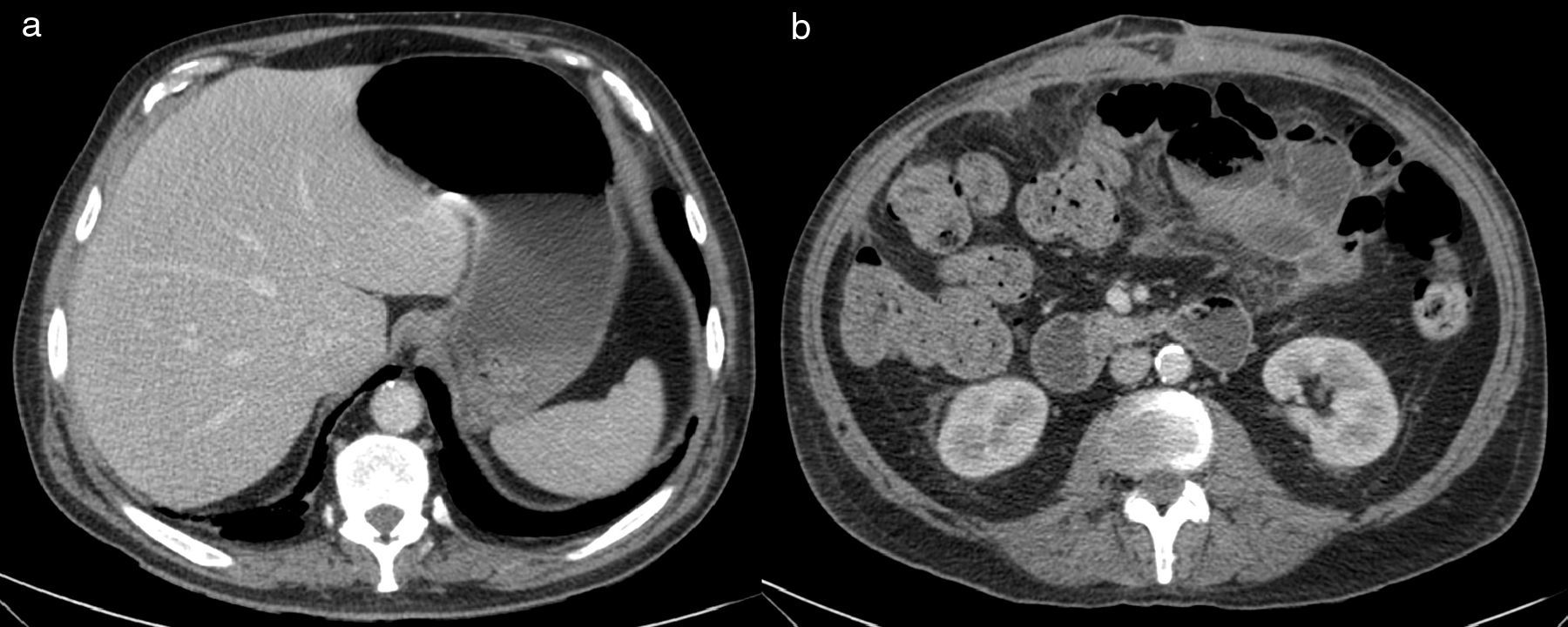
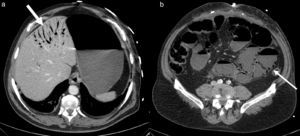
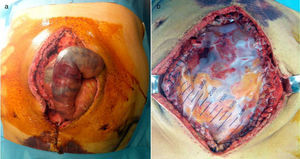
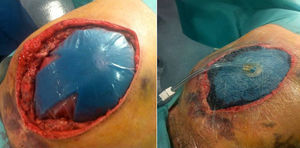
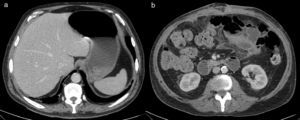
A las 24h presentó episodio de sangrado de la pared abdominal, con presencia de un gran hematoma en hemiabdomen izquierdo, que requirió transfusión de dos concentrados de hematíes. Se decidió la reintervención urgente, en la que se identificó y ligó la arteria perforante causante de la hemorragia, se llevó a cabo limpieza de los coágulos y nueva colocación de dos drenajes subcutáneos aspirativos tubulares (Redón®). Fue dado de alta al tercer día con faja de compresión abdominal, tras retirarse los drenajes por no ser productivos. El paciente se encontraba asintomático, con buena tolerancia oral y recuperación del habitual fisiologismo intestinal, con analítica de control sin alteraciones paramétricas. A las 48h del alta presentó epigastralgia, por lo que acudió a urgencias al día siguiente por aumento brusco del dolor abdominal. Manifestaba sudoración profusa, palidez mucocutánea, hipotensión arterial y oliguria. Analíticamente destacaba leucocitosis de 28 500×10×9/L, PCR 180mg/L y Hb 12g/dL. Se le realizó un tac abdominal, con el que se hallaron signos sugestivos de isquemia intestinal difusa de predominio duodenoyeyunal con dilatación y neumatosis intestinal y aire portal e intrahepático (fig. 1). Se colocó una sonda nasogástrica y se indicó cirugía urgente, sin que se evidenciaran lesiones intestinales irreversibles, según el informe operatorio, aunque en las imágenes del tac el yeyuno presentaba un estado moderadamente dilatado (por lo que se decidió volver a cerrar la pared abdominal sin realizar otro tipo de medidas). A las pocas horas, en vista del deterioro clínico del paciente (con distensión abdominal e hipotensión arterial, y aumentando los requerimientos de fármacos vasoactivos), se realizó una endoscopia digestiva alta, que informó de placas de necrosis en mucosa duodenal, sin proseguir por riesgo de perforación, y se midió la presión intraabdominal (PIA) mediante sonda vesical, que dio el resultado de 24mmHg (PIAN 0-5mmHg o <7mmHg en pacientes críticos, considerándose hipertensión intraabdominal>12mmHg5,6). Por lo tanto, ante la orientación diagnóstica de SCA con progresión a isquemia intestinal, se decidió realizar una relaparotomía urgente de descompresión, con la que se evidenciaron zonas de necrosis a nivel yeyunal (fig. 2a) que requirieron de la resección de 1m de yeyuno –aproximadamente– y se restituyó el tránsito intestinal con una anastomosis yeyunoileal terminoterminal manual, dado el buen aspecto del intestino residual. Se decidió dejar el abdomen abierto aplicándole, para la cobertura visceral, una bolsa de Bogotá (fig. 2b), que posteriormente se cambió por un dispositivo de terapia de presión negativa (TPN) (fig. 3) para mejor manejo de los fluidos intraabdominales y control de la anastomosis intestinal y la progresiva granulación del campo quirúrgico.
En el posoperatorio inmediato ingresó en la Unidad de Cuidados Intensivos con fracaso multiorgánico que revirtió con fármacos vasoactivos, diuréticos, fluidoterapia, antibioterapia parenteral de amplio espectro y profilaxis antitrombótica con heparina de bajo peso molecular que se mantuvo durante la totalidad del ingreso, y fue dado de alta a la planta de cirugía a los 10 días. Durante la estancia en la Unidad de Cuidados Intensivos se realizaron cambios del sistema de TPN cada 3-4 días según los requerimientos.
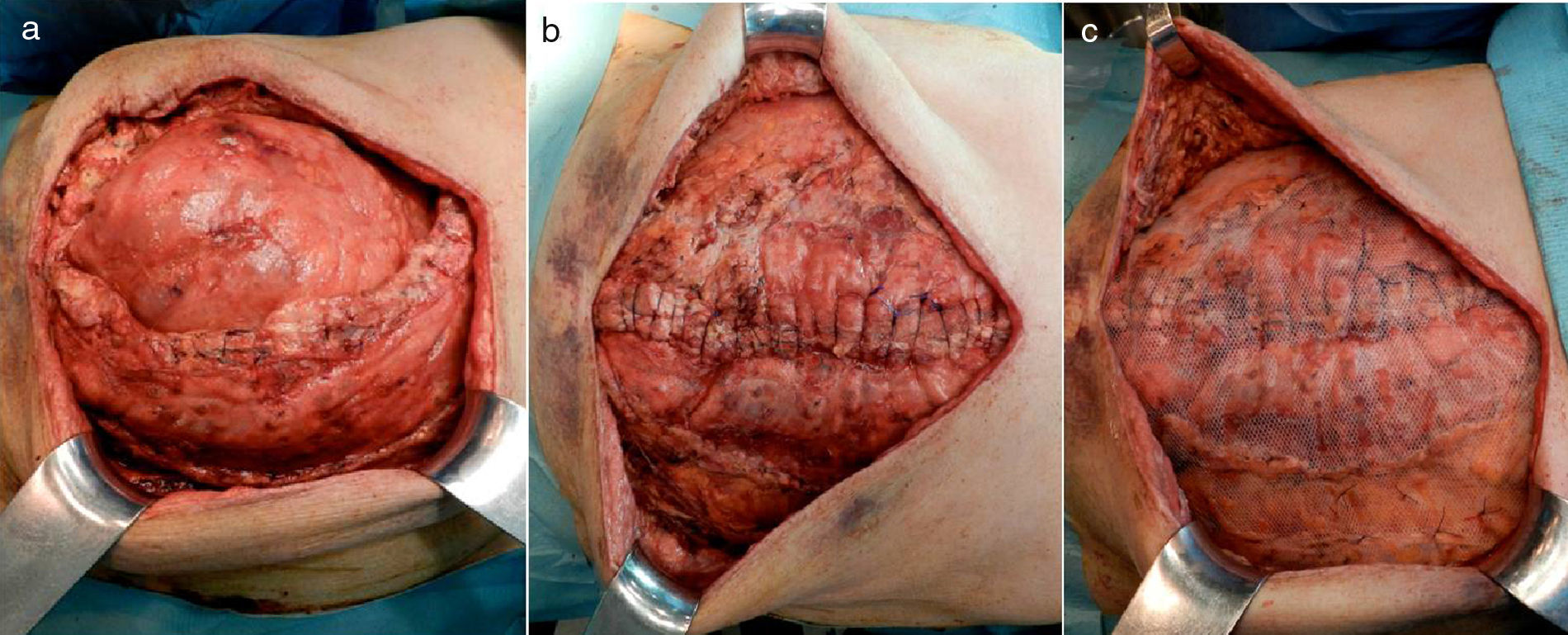
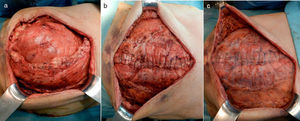
El 13.er día se procedió al cierre definitivo de la pared abdominal, realizándole una nueva SAC tomando como referencia el borde lateral de la malla previa para incidir sobre el músculo oblicuo externo (fig. 4a), además de la desinserción de los músculos rectos de las costillas, controlando la fuerza de tracción de cierre de la pared abdominal mediante un dinamómetro digital (AFG 1000N de Mecmesin®) (fig. 5). La medición se realizó en tres puntos, a cada lado de la laparotomía, aproximando el borde aponeurótico a la línea media. Posteriormente se colocó otra malla de polipropileno de 30×30cm supraaponeurótica (fig. 4c) y cuatro drenajes aspirativos subcutáneos de tipo Redón®. A las 24h de la intervención se le colocó una faja abdominal ortopédica para la sedestación, y el paciente inició tolerancia oral progresiva a las 72h. Presentó un curso posoperatorio favorable, manteniendo PIA por debajo de 10mmHg. En la endoscopia digestiva alta de control no se evidenciaron las lesiones supuestamente «necróticas» en el duodeno observadas en la gastroscopia previa. Fue dado de alta a los 14 días de la última intervención, tras comprobar con un tac la ausencia de defectos en la pared abdominal y aire portal (fig. 6).
Actualmente el paciente se encuentra en buen estado general, y se ha descartado la recidiva herniaria mediante un tac de control al año del alta.
DiscusiónLa eventración compleja es aquella que, entre otras características, presenta un defecto herniario de gran tamaño1 que requiere una técnica elaborada de disección de las diversas estructuras de la pared abdominal para su reparación anatómica y funcional. Por lo tanto, las eventroplastias en este tipo de hernias presentan un mayor riesgo de complicaciones, siendo una de las más frecuentes la hemorragia posoperatoria7 producida por la lesión inadvertida de un vaso perforante, tal como ocurrió en el caso descrito. La isquemia intestinal, diagnosticada en nuestro caso por tac y esofagogastroscopia, podría haber sido secundaria a un bajo gasto cardíaco por el episodio de sangrado en el posoperatorio inmediato, aunque no se ha descrito en la bibliografía publicada ningún otro caso de isquemia mesentérica causada por esta complicación poseventroplastia. El tac con contraste es la prueba complementaria no invasiva más sensible (79-100%)8 para el diagnóstico de una isquemia intestinal. Los hallazgos visibles son más frecuentes: una pared intestinal adelgazada sin captación parietal de contraste, distensión intestinal por íleo adinámico secundario a disfunción de los plexos autonómicos, ausencia de afectación mesentérica, neumatosis intestinal y gas portomesentérico (fig. 1). Estos dos últimos hallazgos se asocian a necrosis transmural en el 78-81% de los casos8,9, por lo que frecuentemente acompañan a la isquemia intestinal grave. A pesar de que la existencia de gas en el territorio venoso portal en el adulto se asocia tradicionalmente a isquemia intestinal (43%), también está descrita en otras entidades clínicas, como en la dilatación del tracto digestivo (12%), abscesos intraabdominales y retroperitoneales (11%), enfermedad inflamatoria intestinal, ulcus gástrico, diverticulitis, traumatismo abdominal severo sin perforación intestinal, SCA e incluso en algún caso de apendicitis aguda9.
La isquemia intestinal es una de las causas de SCA; el tratamiento de este último es la descompresión quirúrgica sin cierre primario, dejando el abdomen abierto para intentar reducir la elevada morbimortalidad de este síndrome. La nueva guía de práctica clínica de la Sociedad Mundial del Síndrome Compartimental Abdominal, publicada en 2013, utiliza la definición de abdomen abierto como sinónimo de cierre temporal abdominal5,6. Existen diversos métodos de cierre temporal, como la bolsa de Bogotá (fig. 2)10, Wittmann Patch11,12, la utilización de una malla como puente13,14, la técnica de sándwich15,16 y la TPN. Inicialmente se coloca una bolsa de Bogotá con la pretensión de realizar una revisión quirúrgica a las 24h. Una vez comprobado el buen aspecto de las asas intestinales y de la anastomosis realizada, se emplea un sistema de TPN (ABthera® KCI)17,18 (fig. 3), puesto que tiene las ventajas de permitir el control de fluidos, favorecer la cicatrización y disminuir la retracción de la aponeurosis, y se obtienen mayores tasas de cierre primario diferido según algunos artículos en los que se comparan los distintos métodos de cierre temporal19–21, aunque las conclusiones de estas publicaciones son controvertidas, debido a la existencia de numerosos sesgos en los diseños y a la heterogeneidad de estos. Las revisiones se realizaron cada 3 días, tal como está recomendado, aunque la tendencia actual es hacerlas a demanda hasta la recuperación de los parámetros fisiológicos del paciente, para plantear después el cierre definitivo.
En nuestro caso, para la reparación de la eventración se utilizó la técnica de SAC3 en la primera y segunda intervención. En la primera se trataba de una hernia con un defecto grande, resuelta mediante SAC (nivel 1), con lo que se logró una reparación sin tensión, ya que con dicha técnica se consigue un avance significativo de los rectos con preservación de los elementos neurovasculares2,3. Además, se colocó una malla en posición supraaponeurótica como medida de refuerzo. En el cierre definitivo de la pared abdominal, tras el episodio de SCA, se realizó una segunda SAC a través de la antigua malla (fig. 4a), además de la desinserción de los músculos rectos de las costillas y una nueva colocación de malla como refuerzo (fig. 4c), controlando en todo momento la tensión de cierre de la pared abdominal mediante un dinamómetro digital (fig. 5). En estudios previos, como el de Klein et al.22, se ha demostrado que el cierre primario de la pared abdominal es seguro cuando se obtienen unas tensiones intraoperatorias de cierre aponeurótico inferiores a 15N. Asimismo, con tensiones superiores a 35N no se recomienda cerrar la pared abdominal23,24.
A pesar de que la tendencia actual del tratamiento del abdomen abierto es la técnica con cierre progresivo de este, en nuestro caso realizamos un cierre primario diferido definitivo en un tiempo con una segunda técnica de separación de componentes en un paciente en el que ya se había realizado una separación de componentes previa, y logramos una aproximación sin tensión del defecto abdominal. Esta segunda SAC se pudo realizar porque en la primera intervención no se solapó la malla por debajo del músculo oblicuo externo, por lo que el tejido estaba indemne y se pudo disecar fácilmente. Esta técnica de reseparación anatómica de componentes en una SAC previa no la hemos encontrado descrita en la bibliografía publicada y, por el resultado final satisfactorio en este paciente, pensamos que podría ser de ayuda para el cierre definitivo de este tipo de casos. Por otro lado, la ayuda de un dinamómetro digital para medir la tensión del cierre aponeurótico fue importante para obtener con notable seguridad un cierre sin tensión.
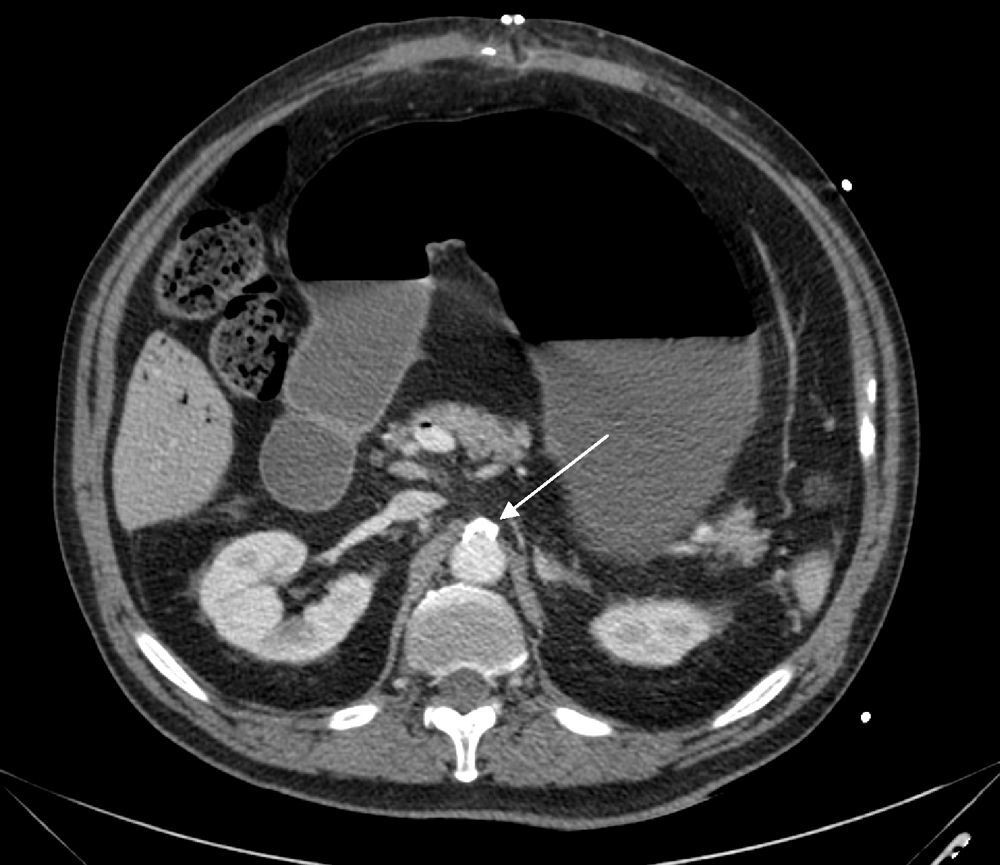
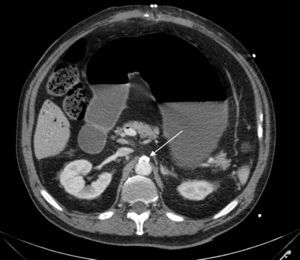
El caso presentado resulta demostrativo de que una eventración compleja es algo frecuente y de comportamiento benigno, pero las complicaciones posoperatorias son graves, incluso mortales25. Las medidas quirúrgicas precoces y agresivas, junto con el apoyo de un equipo médico interdisciplinar, permitieron resolver el grave problema de este paciente. En este caso no fue un aumento de la PIA lo que originó la isquemia intestinal, como se ha descrito en la bibliografía publicada26,27, sino que la progresión de la isquemia intestinal secundaria a un sangrado posoperatorio importante causó el aumento de esta PIA y, como consecuencia, un SCA. Revisando las imágenes del tac de reingreso se evidencia una placa de ateroma en el origen de la AMS que ocupa el 70% de la circunferencia (fig. 7), así como varias placas más pequeñas en todo el recorrido de esta, por lo que creemos que a pesar de que el sangrado posoperatorio no fuera abundante, el hecho de tener esta ateromatosis predispuso al desarrollo posterior de una isquemia intestinal.
Debemos concluir subrayando que la disección minuciosa de la pared abdominal en la reparación de una eventración compleja puede suponer una medida de vital importancia para prevenir posibles complicaciones que modifican el deseable curso posoperatorio de los pacientes.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
CONGRESO: Parte de la información del manuscrito se presentó en la XIX Reunión Nacional de Cirugía (23-25 de octubre de 2013, Burgos) en formato póster.