Journal Information
Vol. 124. Issue 11.
Pages 423-426 (March 2005)
Vol. 124. Issue 11.
Pages 423-426 (March 2005)
DOI: 10.1157/13072856
Desarrollo de enfermedades endocrinológicas sistémicas en el adulto desde la hipótesis de la programación fetal
Development of endocrinological systemic diseases in the adult, the fetal programming hypothesis
Visits
4655
This item has received
Article information
Full Text
Bibliography
Download PDF
Statistics
Tables (2)
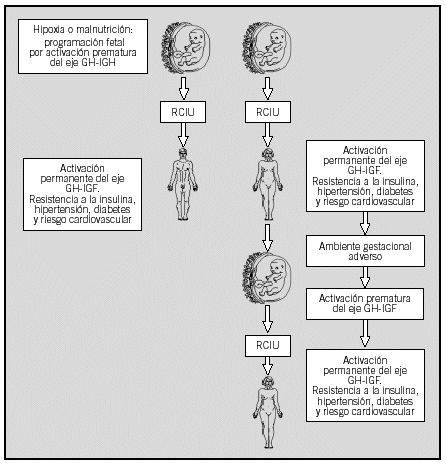
Fig. 1. La agresión inicial genera la activación del eje GH-IGF, que desencadena la programación fetal que tendrá consecuencias en la vida adulta. En la mujer afectada crearán un ambiente adverso al feto en desarrollo que pondrá nuevamente en activación el eje y perpetuará la programación. En el varón sólo se presentarán las consecuencias de la programación.GH-IGF: hormona de crecimiento; factor de crecimiento insulinoide.RCIV: retraso del crecimiento intrauterino.
Show moreShow less
These are the options to access the full texts of the publication Medicina Clínica
Subscriber
Subscribe
Purchase
Contact
Phone for subscriptions and reporting of errors
From Monday to Friday from 9 a.m. to 6 p.m. (GMT + 1) except for the months of July and August which will be from 9 a.m. to 3 p.m.
Calls from Spain
932 415 960
Calls from outside Spain
+34 932 415 960
E-mail