Establecer el estado actual de las unidades de patología mamaria (UPM) en la utilización de indicadores de calidad del manejo del cáncer de mama.
Material y métodosSe efectuó una búsqueda bibliográfica de indicadores del manejo del cáncer de mama. Con los resultados se confeccionó una encuesta electrónica de 27 preguntas que se envió a 167 UPM censadas en el Grupo de Estudios Senológicos. Se consideraron las respuestas de 33 de las UPM.
ResultadosSolo 9 de las UPM que respondieron estaban acreditadas por la SESPM. Los indicadores más utilizados fueron: utilización de informes siguiendo guías estandarizadas en diagnóstico por la imagen, pacientes con cáncer orientadas para tratamiento por un comité multidisciplinar, determinación de factores pronósticos y predictivos en carcinoma infiltrante, y especificación en el informe de la distancia al margen más cercano de la lesión. Por grupos de indicadores los más utilizados fueron los del procedimiento general y anatomía patológica. Las UPM acreditadas utilizan los indicadores con mayor frecuencia que las no acreditadas. Solo 8 de los 20 indicadores eran utilizados por más del 70% de las UPM para el control de calidad de la unidad y no solo del servicio que los origina.
ConclusiónEl uso de indicadores para el control de calidad es una herramienta ampliamente utilizada en las UPM que han contestado la encuesta, si bien en muchas ocasiones el indicador solo se usa en el servicio que lo origina y no para la evaluación del funcionamiento de la unidad de forma integral.
To determine the current state of breast pathology units (BPU) in the use of quality indicators in breast cancer management.
Material and methodsAfter a literature research of breast cancer management indicators, a 27-question survey was designed and sent on-line to 167 BPU from the Group for Senology Studies. Completed surveys were considered from 33 BPU.
ResultsOnly 9 of the BPU that responded were accredited by the SESPM. The most commonly used indicators were the following: use of standardised reporting guidelines in imaging diagnosis, patients with breast cancer treated by a multidisciplinary committee, determination of prognostic and predictive factors in invasive carcinoma, and specification of margin distance in the pathologic report. The most widely used indicators were those of the general process and pathology. Use of the indicators was more frequent in accredited than in non-accredited BPU. Only 8 of the 20 indicators were used by more than 70% of BPU for unit quality control and not only by the service creating them.
ConclusionsThe use of indicators for quality control is a widely used tool in the BPU responding to the survey. However, indicators are often only used in the service creating them and not for integral quality assessment of the BPU.
El tratamiento de las enfermedades oncológicas ha de llevarse a cabo de forma imprescindible bajo un enfoque multidisciplinar. Ello se consigue mediante la creación de unidades destinadas al manejo de enfermedades específicas, integradas por diversos especialistas relacionados con la enfermedad1. En España, con esta finalidad, existen unidades de patología mamaria (UPM), muchas de ellas acreditadas por la Sociedad Española de Senología y Patología Mamaria (SESPM) siguiendo unos estándares establecidos por la comisión de acreditación2,3. Lo mismo sucede a nivel europeo con organismos como el EUSOMA4,5.
Las condiciones mínimas para que una UPM sea acreditada consisten en establecer una serie de requisitos, sobre todo asistenciales y de procedimiento, para llevar a cabo todo el proceso en el que se involucra a las pacientes con cáncer de mama. El objetivo final de esta acreditación es alcanzar unos estándares de calidad que garanticen que estas unidades desarrollen su labor en niveles de excelencia para el manejo de la paciente con cáncer de mama.
En el procedimiento del control de calidad, juegan un papel preponderante los indicadores de calidad que permiten la evaluación y el control del proceso. Por definición un indicador debe6:
- -
Ser creíble y tener el mínimo de error.
- -
Medir de forma precisa lo que quiere medir y no otros parámetros.
- -
Ser accesible: deben de poder consultarse fácilmente los datos del indicador.
- -
Ser oportuno: poder ser actualizado periódicamente.
- -
Ser práctico: monitorizable de forma simple y a ser posible de forma automática.
- -
Ser sensible: ha de ser capaz de detectar cambios significativos que puedan suponer una desviación en el proceso.
- -
Ser alcanzable: el indicador ha de reflejar aquellos factores con impacto en los estándares de referencia.
Existe poca uniformidad a la hora de establecer qué indicadores y sus correspondientes valores expresan de forma óptima el buen funcionamiento de una UPM. Muchas veces los indicadores están establecidos de forma individualizada en los servicios que forman parte de la UPM sin englobarse y considerarse todos ellos en un conjunto para una valoración transversal del proceso en el contexto de la unidad.
La finalidad de este estudio fue llevar a cabo una revisión de la literatura de los indicadores utilizados en el proceso de diagnóstico, tratamiento y control de la paciente con cáncer de mama, y establecer el estado actual de las UPM acreditadas o no por la SESPM en lo que a utilización de indicadores en el proceso del manejo del cáncer de mama se refiere, y ver cuáles de estos se utilizaban solo en los servicios integrantes de la unidad que los origina y cuáles se utilizaban como indicadores de control de calidad de la UPM.
Material y métodosSe efectuó una búsqueda bibliográfica de revisiones sobre indicadores en el diagnóstico y tratamiento del cáncer de mama de la cual se seleccionaron 17 publicaciones3–19. De estas, se recogieron 149 indicadores, muchos de ellos repetidos en más de una revisión, que se agruparon en las siguientes categorías: procedimiento general, diagnóstico por la imagen, diagnóstico anatomopatológico y tratamiento.
En cada una de las categorías se agruparon indicadores y se seleccionaron los que el grupo de autores consideró más significativos, de forma que con ellos se confeccionó una encuesta on-line.
El estudio es descriptivo observacional a partir de datos recogidos mediante una encuesta de 27 preguntas que se envió a los 167 centros con UPM censados en el Grupo de Estudios Senológicos de la SESPM. El envío se llevó a cabo mediante un enlace para rellenar la encuesta de forma electrónica. La encuesta se envió el 7 de noviembre de 2016 y se cerró el 12 de diciembre de 2016.
Los resultados se han expresado en número de respuestas y en porcentaje respecto al total.
Se recibieron 48 respuestas en el sistema on-line. De estas, se excluyeron aquellas que mostraban datos erróneos, que no identificaban la unidad o su procedencia geográfica o que no tenían contestadas todas las preguntas sobre los indicadores (de la 3 a la 22). El total de respuestas que se consideraron en el estudio fueron 33.
ResultadosDel total de 33 encuestas incluidas en el estudio, 9 pertenecían a UPM acreditadas por la SESPM, 11 (33%) diagnosticaban menos de 150 cánceres anuales y 16 (48%), entre 150 y 300 casos.
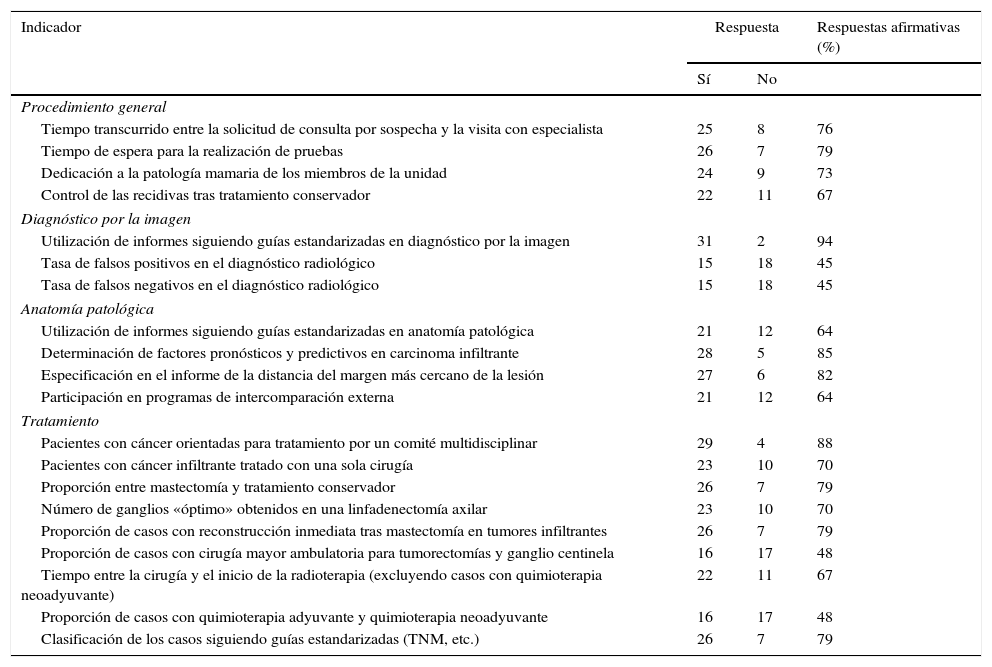
En la tabla 1 se expresa el número de UPM que utilizan o no cada uno de los indicadores planteados.
Respuestas a la utilización o no de cada uno de los indicadores
| Indicador | Respuesta | Respuestas afirmativas (%) | |
|---|---|---|---|
| Sí | No | ||
| Procedimiento general | |||
| Tiempo transcurrido entre la solicitud de consulta por sospecha y la visita con especialista | 25 | 8 | 76 |
| Tiempo de espera para la realización de pruebas | 26 | 7 | 79 |
| Dedicación a la patología mamaria de los miembros de la unidad | 24 | 9 | 73 |
| Control de las recidivas tras tratamiento conservador | 22 | 11 | 67 |
| Diagnóstico por la imagen | |||
| Utilización de informes siguiendo guías estandarizadas en diagnóstico por la imagen | 31 | 2 | 94 |
| Tasa de falsos positivos en el diagnóstico radiológico | 15 | 18 | 45 |
| Tasa de falsos negativos en el diagnóstico radiológico | 15 | 18 | 45 |
| Anatomía patológica | |||
| Utilización de informes siguiendo guías estandarizadas en anatomía patológica | 21 | 12 | 64 |
| Determinación de factores pronósticos y predictivos en carcinoma infiltrante | 28 | 5 | 85 |
| Especificación en el informe de la distancia del margen más cercano de la lesión | 27 | 6 | 82 |
| Participación en programas de intercomparación externa | 21 | 12 | 64 |
| Tratamiento | |||
| Pacientes con cáncer orientadas para tratamiento por un comité multidisciplinar | 29 | 4 | 88 |
| Pacientes con cáncer infiltrante tratado con una sola cirugía | 23 | 10 | 70 |
| Proporción entre mastectomía y tratamiento conservador | 26 | 7 | 79 |
| Número de ganglios «óptimo» obtenidos en una linfadenectomía axilar | 23 | 10 | 70 |
| Proporción de casos con reconstrucción inmediata tras mastectomía en tumores infiltrantes | 26 | 7 | 79 |
| Proporción de casos con cirugía mayor ambulatoria para tumorectomías y ganglio centinela | 16 | 17 | 48 |
| Tiempo entre la cirugía y el inicio de la radioterapia (excluyendo casos con quimioterapia neoadyuvante) | 22 | 11 | 67 |
| Proporción de casos con quimioterapia adyuvante y quimioterapia neoadyuvante | 16 | 17 | 48 |
| Clasificación de los casos siguiendo guías estandarizadas (TNM, etc.) | 26 | 7 | 79 |
Más del 80% de las unidades manejan los siguientes indicadores: utilización de informes siguiendo guías estandarizadas en diagnóstico por la imagen (94%), pacientes con cáncer orientadas para tratamiento por un comité multidisciplinar (88%), determinación de factores pronósticos y predictivos en carcinoma infiltrante (85%) y especificación en el informe de la distancia al margen más cercano de la lesión (82%). Los indicadores que usan entre el 50 y el 80% de las UPM fueron: tiempo de espera para la realización de pruebas (79%), proporción entre mastectomía y tratamiento conservador (79%), proporción de casos con reconstrucción inmediata tras mastectomía en tumores infiltrantes (79%), clasificación de los casos siguiendo guías estandarizadas (79%), tiempo transcurrido entre la solicitud de consulta por sospecha y la visita con especialista (76%), dedicación a la patología mamaria de los miembros de la unidad (73%), pacientes con cáncer infiltrante tratado con una sola cirugía (70%), número de ganglios óptimo obtenidos tras linfadenectomía axilar (70%), control de las recidivas tras tratamiento conservador (67%), tiempo entre la cirugía y el inicio de la radioterapia (excluyendo casos con quimioterapia neoadyuvante) (67%), participación en programas de intercomparación externa (64%) y utilización de informes siguiendo guías estandarizadas en anatomía patológica (64%). Los indicadores empleados en menos del 50% de las unidades fueron: proporción de casos con cirugía mayor ambulatoria para tumorectomías y ganglio centinela (48%), proporción de casos con quimioterapia adyuvante y quimioterapia neoadyuvante (48%), tasa de falsos positivos en el diagnóstico radiológico (45%) y tasa de falsos negativos en el diagnóstico radiológico (45%). Solo 3 UPM utilizaban todos los indicadores reseñados en la encuesta.
Por grupos de indicadores, los más utilizados son los del procedimiento general y anatomía patológica, seguidos por los de tratamiento y, finalmente, diagnóstico por la imagen.
Al comparar el uso de indicadores entre las UPM acreditadas y no acreditadas, la utilización fue superior en las unidades acreditadas en todos los indicadores a excepción de la participación en programas de intercomparación externa, el número de ganglios «óptimo» obtenidos en una linfadenectomía axilar y la proporción de casos con cirugía mayor ambulatoria para tumorectomías y ganglio centinela.
Los valores utilizados para cada uno de los indicadores en las UPM que respondieron, fueron:
- -
Tiempo transcurrido entre la solicitud de consulta por sospecha y la visita con el especialista: en 7 de 21 unidades es de 7 días o menos. El periodo oscila entre 5 y 15 días.
- -
Tiempo de espera para la realización de pruebas: en 6 de 21 unidades es de una semana. El periodo oscila entre 2 y 15 días.
- -
Dedicación a la patología mamaria de los miembros de la unidad: en 16 de 17 unidades el tiempo que dedican los miembros de la unidad a la patología mamaria es preferente o completo.
- -
Control de las recidivas tras tratamiento conservador: en 3 de 12 unidades se acepta hasta el 3-5% a los 5 años.
- -
Utilización de informes siguiendo guías estandarizadas en diagnóstico por la imagen: en 15 de 15 unidades se utiliza la clasificación BIRADS.
- -
Tasa de falsos positivos en el diagnóstico radiológico: en 2 de 8 unidades se utiliza una tasa inferior al 2%.
- -
Tasa de falsos negativos en el diagnóstico radiológico: solo una unidad de 9 especifica que utiliza una tasa inferior al 5%.
- -
Utilización de informes siguiendo guías estandarizadas en anatomía patológica: 7 unidades especifican que sí utilizan estas guías.
- -
Determinación de factores pronósticos y predictivos en carcinoma infiltrante: el indicador queda reflejado en todos los casos en las 11 unidades que han contestado este apartado.
- -
Especificación en el informe de la distancia al margen más cercano de la lesión: las 12 unidades que han contestado lo utilizan.
- -
Participación en programas de intercomparación externa: las 4 unidades que han respondido participan en programas de intercomparación.
- -
Pacientes con cáncer orientadas para tratamiento por un comité multidisciplinar: en 9 unidades que han respondido el porcentaje de casos orientados por un comité multidisciplinar supera el 90%.
- -
Pacientes con cáncer infiltrante tratado con una sola cirugía: en 3 de 9 unidades es superior al 80%.
- -
Proporción entre mastectomía y tratamiento conservador: en 8 de 14 unidades el porcentaje de tratamiento conservador es superior al 70%.
- -
Número de ganglios óptimo obtenidos tras linfadenectomía axilar: en 8 de 11 unidades el número es de 10 o más.
- -
Proporción de casos con reconstrucción inmediata tras mastectomía en tumores infiltrantes: en 5 de 13 unidades es del 100% de los casos, en otras es del 10, 45 y 70%.
- -
Proporción de casos con cirugía mayor ambulatoria para tumorectomías y ganglio centinela: en 7 de 12 unidades es de más del 80% de los casos.
- -
Tiempo entre la cirugía y el inicio de la radioterapia (excluyendo casos con quimioterapia neoadyuvante): en 9 de 12 unidades es inferior a 45 días.
- -
Proporción de casos con quimioterapia adyuvante y quimioterapia neoadyuvante: oscila entre el 10 y el 60% en 3 unidades de 9 que lo han especificado.
- -
Clasificación de los casos siguiendo guías estandarizadas: en las 9 unidades que han contestado es superior al 95%.
Otros indicadores planteados por los encuestados estaban relacionados con la satisfacción de las pacientes, el porcentaje de tratamientos neoadyuvantes que permiten tratar de forma conservadora posteriormente, el tiempo de indicación de la quimioterapia tras cirugía y el índice de reingresos.
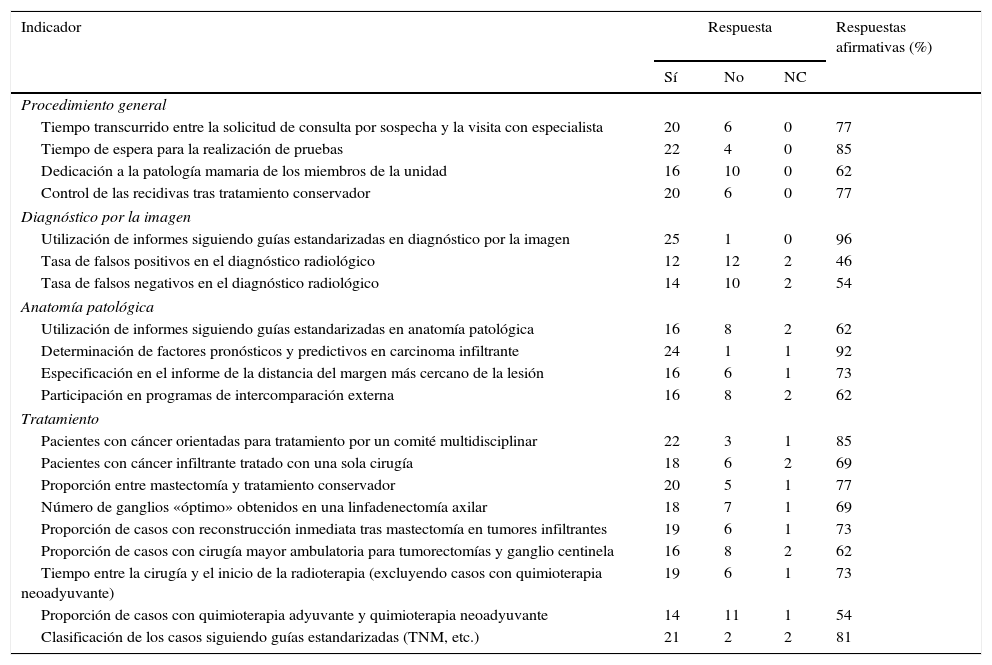
En la pregunta 26 se planteaba si los indicadores eran utilizados en el servicio, en el que se aplicaban o se usaban para el control de calidad de la UPM (tabla 2). Más del 75% de las unidades empleaban los siguientes indicadores como control de calidad de la unidad: utilización de informes siguiendo guías estandarizadas en diagnóstico por la imagen, determinación de factores pronósticos y predictivos en carcinoma infiltrante, tiempo de espera para la realización de pruebas, pacientes con cáncer orientadas para el tratamiento por un comité multidisciplinar, clasificación de los casos siguiendo guías estandarizadas, tiempo transcurrido entre la solicitud de consulta por sospecha y la visita con especialista, control de las recidivas tras tratamiento conservador y proporción entre mastectomía y tratamiento conservador.
Respuesta a la utilización o no de cada indicador en el control de la unidad
| Indicador | Respuesta | Respuestas afirmativas (%) | ||
|---|---|---|---|---|
| Sí | No | NC | ||
| Procedimiento general | ||||
| Tiempo transcurrido entre la solicitud de consulta por sospecha y la visita con especialista | 20 | 6 | 0 | 77 |
| Tiempo de espera para la realización de pruebas | 22 | 4 | 0 | 85 |
| Dedicación a la patología mamaria de los miembros de la unidad | 16 | 10 | 0 | 62 |
| Control de las recidivas tras tratamiento conservador | 20 | 6 | 0 | 77 |
| Diagnóstico por la imagen | ||||
| Utilización de informes siguiendo guías estandarizadas en diagnóstico por la imagen | 25 | 1 | 0 | 96 |
| Tasa de falsos positivos en el diagnóstico radiológico | 12 | 12 | 2 | 46 |
| Tasa de falsos negativos en el diagnóstico radiológico | 14 | 10 | 2 | 54 |
| Anatomía patológica | ||||
| Utilización de informes siguiendo guías estandarizadas en anatomía patológica | 16 | 8 | 2 | 62 |
| Determinación de factores pronósticos y predictivos en carcinoma infiltrante | 24 | 1 | 1 | 92 |
| Especificación en el informe de la distancia del margen más cercano de la lesión | 16 | 6 | 1 | 73 |
| Participación en programas de intercomparación externa | 16 | 8 | 2 | 62 |
| Tratamiento | ||||
| Pacientes con cáncer orientadas para tratamiento por un comité multidisciplinar | 22 | 3 | 1 | 85 |
| Pacientes con cáncer infiltrante tratado con una sola cirugía | 18 | 6 | 2 | 69 |
| Proporción entre mastectomía y tratamiento conservador | 20 | 5 | 1 | 77 |
| Número de ganglios «óptimo» obtenidos en una linfadenectomía axilar | 18 | 7 | 1 | 69 |
| Proporción de casos con reconstrucción inmediata tras mastectomía en tumores infiltrantes | 19 | 6 | 1 | 73 |
| Proporción de casos con cirugía mayor ambulatoria para tumorectomías y ganglio centinela | 16 | 8 | 2 | 62 |
| Tiempo entre la cirugía y el inicio de la radioterapia (excluyendo casos con quimioterapia neoadyuvante) | 19 | 6 | 1 | 73 |
| Proporción de casos con quimioterapia adyuvante y quimioterapia neoadyuvante | 14 | 11 | 1 | 54 |
| Clasificación de los casos siguiendo guías estandarizadas (TNM, etc.) | 21 | 2 | 2 | 81 |
Han sido muchas las iniciativas de recomendar e implementar el uso de indicadores que mejoren la asistencia de las pacientes con cáncer de mama, demostrándose que el uso de sistemas que aseguren la calidad mejora los resultados en la atención al paciente6,17,18,20. El establecimiento y el cálculo de estos indicadores requiere de un sistema organizado de recogida de datos para poder determinarlos, lo que se consigue bajo una estructura organizada16,18. Son muchas las organizaciones y los sistemas sanitarios que utilizan metodología específica para establecer la viabilidad y la aplicabilidad de los indicadores más representativos de forma que puedan ser utilizados por los distintos centros destinados a tratar el cáncer de mama4,6,8,17,18,21. Además, el uso de indicadores de calidad hace que puedan compararse los resultados obtenidos entre distintas UPM de forma objetiva2,6,7,20. Hay estudios que demuestran que este campo está poco desarrollado en nuestro país22.
Según los resultados de esta encuesta nacional, la mayoría de las UPM que la han contestado utilizan indicadores de calidad para monitorizar su actividad y resultados. Solo 4 de los indicadores planteados (proporción de casos con cirugía mayor ambulatoria para tumorectomías y ganglio centinela, proporción de casos con quimioterapia adyuvante y quimioterapia neoadyuvante, tasa de falsos positivos en el diagnóstico radiológico y tasa de falsos negativos en el diagnóstico radiológico) eran utilizados por menos del 50% de las unidades encuestadas.
Los valores de indicadores utilizados por las UPM encuestados que presentan un valor estandarizado en la literatura están dentro de los parámetros recomendados. El tiempo transcurrido entre la solicitud por sospecha y la visita con el especialista está descrito en menos de 5-7 días3, la utilización de informes siguiendo guías estandarizadas en diagnóstico por la imagen es superior al 98% de los casos5, y en anatomía patológica, superior al 96% de los casos5, la determinación de factores pronósticos y predictivos en carcinoma infiltrante, entre el 90 y el 95% de casos3,5,10, la especificación en el informe de la distancia del margen más cercano de la lesión se realiza en más del 95% de los casos4, el porcentaje de pacientes con cáncer orientadas para tratamiento por un comité multidisciplinar ha de ser superior al 90-95% de los casos4,10, la proporción entre mastectomía y tratamiento conservador cuando este está indicado ha de ser superior al 85% de los tratamientos de forma conservadora10, el número de ganglios «óptimo» obtenidos en una linfadenectomía axilar se estima en 10 en más del 85-95% de los casos4,5,10, la proporción de casos con cirugía mayor ambulatoria para tumorectomías y ganglio centinela se cifra en el 80% de los casos10 y el tiempo entre la cirugía y el inicio de la radioterapia (excluyendo casos con quimioterapia neoadyuvante) se estima en menos de 4 semanas.
El establecer estos valores es orientativo y en muchas ocasiones depende de los recursos y las características de cada unidad2. El disponer de un grupo multidisciplinar integrado en una UPM, y sobre todo si esta está acreditada siguiendo unos estándares por un organismo reconocido, repercute en una mejor atención2,4,5,8,10,12,14,17,18,20. Una señal de esto sería que en la encuesta realizada las unidades acreditadas utilizan con mayor frecuencia los indicadores recomendados que las unidades no acreditadas. Así mismo, la utilización de indicadores hace que el proceso mejore con el tiempo, pues existen unas cifras de referencia para los actos asistenciales7,9,14,17,18,20.
Es de destacar que solo 8 de los 20 indicadores planteados se utilizan en más del 75% de las UPM como control de calidad de la unidad y no del servicio, integrante de la unidad, que los proporciona. Ello pone de manifiesto que aún quedan opciones de mejora integrando en la unidad todos los recursos de cada uno de sus servicios.
En conclusión, el uso de indicadores para el control de calidad es una herramienta ampliamente utilizada en las UPM que han contestado la encuesta, si bien en muchas ocasiones el indicador se usa en el servicio o unidad clínica que lo origina y no para la evaluación del funcionamiento de la unidad de forma integral.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
FinanciaciónEste trabajo ha sido realizado bajo los auspicios de la Càtedra d’Investigació en Obstetrícia i Ginecologia de la Universitat Autònoma de Barcelona.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
A todas las unidades de mama que han participado en la encuesta: Hospital Universitario Ramón y Cajal (Madrid), Hospital Universitario Dr. Negrín (Las Palmas de Gran Canaria), Hospital Universitario de La Ribera (Alzira, Valencia), Hospital Universitario de Tarragona Joan XXIII (Tarragona), Complejo Hospitalario Torrecárdenas (Almería), Hospital Universitario Lucus Augusti (Lugo), Hospital Reina Sofía (Córdoba), Hospital Abente y Lago (La Coruña), Hospital Universitario Doctor Peset (Valencia), Hospital Francesc de Borja (Gandía), Hospital Universitario Virgen del Rocío (Sevilla), Hospital General (Valencia), UPMGAP (Sant Pere de Ribes/Vilafranca del Penedès), Hospital Nuestra Señora de Gracia (Zaragoza), CHN (Pamplona), Institució Font Sastre (Mataró), Hospital Central de la Defensa (Madrid), Hospital Universitario de León (León), Hospital Universitario Dexeus (Barcelona), Complejo Asistencial de Zamora (Zamora), Complejo Hospitalario de Jaén (Jaén), Hospital Universitario central de Asturias (Oviedo), Hospital Clínico Universitario Virgen de la Arrixaca (Murcia), Hospital General Universitario de Castellón (Castellón), Hospital Universitario Puerta de Hierro (Majadahonda, Madrid), Hospital La Paz (Madrid), Hospital Punta de Europa (Algeciras), Hospital Universitario Valme (Sevilla), Onkologikoa (San Sebastián), Clínica Universidad de Navarra (Pamplona), Hospital General de Teruel Obispo Polanco (Teruel), Fundación Instituto Valenciano de Oncología (Valencia) y Hospital Universitario Miguel Servet (Zaragoza).
Al Grupo de Estudios Senológicos de la SESPM por el auspicio y la distribución de la encuesta entre la Unidad de Patología Mamaria. A Teresa Martí, secretaria de presidencia de la SESPM; a Ana Turanzo, gerente de la SESPM, por su labor de coordinación con las distintas unidades de mama.