Los datos internacionales disponibles sobre uso de clozapina recogen en general una baja prescripción, infradosificación y retraso en el inicio del tratamiento, y han originado diversas iniciativas para mejorar su uso y disminuir la llamativa variabilidad. No disponemos de estudios que valoren estos aspectos en población española, por lo que nos hemos planteado una primera y modesta aproximación a través de 4 muestras territoriales. Nuestra hipótesis es que, al igual que las referencias comentadas, en nuestro país el consumo de clozapina podría ser bajo y variable. Nuestro objetivo, en caso de confirmarse la hipótesis, sería iniciar una reflexión sobre posibles estrategias a plantear.
Material y métodosLos autores han accedido a datos de consumo de clozapina en Cataluña, Castilla y León, País Vasco y un Área de Madrid (el Área de Gestión Clínica PSM del Hospital 12 de Octubre).
ResultadosLos pacientes con diagnóstico de esquizofrenia en tratamiento en los territorios estudiados oscilan en torno al 0,3%; los tratamientos con clozapina/10.000 habitantes entre el 33% y 57%; y los pacientes diagnosticados como esquizofrenia en tratamiento con clozapina suponen entre el 13,7% y 18,6% de los tratados. El coeficiente de variación entre centros y prescriptores es frecuentemente superior al 50%.
ConclusionesAunque por debajo de las cifras indicadas por la literatura, los datos globales de prescripción de clozapina en los territorios que hemos estudiado no son tan bajos como los recogidos en otros trabajos internacionales, y se sitúan en el rango de países de nuestro entorno. Sin embargo, la variabilidad en la prescripción es muy importante, aparentemente no justificada; y aumenta a medida que analizamos zonas menores, hasta una gran heterogeneidad de la prescripción individual.
International studies on clozapine use usually show lower than expected prescription proportions, under-dosing and delayed initiation of treatment, which has led to a number of initiatives aimed at improving its use and reducing the striking variability observed among practitioners. There are no similar studies on the Spanish population. Therefore we planned initial data collection from 4 territorial samples. We hypothesized that clozapine prescription would also be low and variable in our country. If this hypothesis were confirmed, a reflection on possible strategies would be necessary.
Material and methodsWe accessed data on clozapine prescription in Catalonia, Castile and Leon, the Basque Country and the Clinical Management Area of the Hospital 12 de Octubre (Madrid).
ResultsPatients diagnosed with schizophrenia under treatment in these territories comprise around .3% of their total population; treatment with clozapine ranges between 33.0 and 57.0 per 10000 inhabitants; patients diagnosed with schizophrenia on current treatment with clozapine range between 13.7% and 18.6% of the total number of patients with this diagnosis. The coefficient of variation between centres and prescribers is often higher than 50%.
ConclusionsAlthough below the figures suggested as desirable in the literature, global prescribing data for clozapine in the areas we studied are not as low as the data collected in other international studies, and are in the range of countries in our environment. However, the variability in prescription is large and apparently not justified; this heterogeneity increases as we focus on smaller areas, and there is great heterogeneity at the level of individual prescription.
Aunque conceptualmente cuestionado1 el síndrome psicótico que desde hace un siglo hemos venido llamando esquizofrenia sigue siendo el paradigma de la enfermedad mental2. El tratamiento con fármacos antipsicóticos (AP) atenúa en parte algunas de sus manifestaciones, y se considera un ingrediente necesario de actuaciones más complejas3; aunque también se encuentra sometido a una intensa y rica reflexión4–7. La primera generación de AP ha sido desplazada por los denominados «antipsicóticos atípicos» (AA)8. A pesar de que el concepto de «atipicidad» es confuso, la diferencia de eficacia no está demostrada9–13, y la homogeneidad del grupo de los AA resulta insostenible14–18; los nuevos AP han incrementado el consumo de modo exponencial, al aceptarse nuevas indicaciones, o por su uso fuera de indicación19,20.
La clozapina fue el primer AP calificado como «atípico», en base a su mecanismo de acción, no provocador de catalepsia en modelos animales, ni de efectos extrapiramidales en pacientes. Estos elementos fueron imitados en su diseño, o al menos en su comercialización, por los AA que surgieron en su estela
Los datos de eficacia global en esquizofrenia muestran superioridad de la clozapina frente a otros AP13,15,21–27; específicamente frente a la primera generación de estos fármacos21,14 y, en general, sobre el resto de los denominados «atípicos»10,18,25,28–30. Las tasas de rehospitalización con clozapina son menores31–34 y la adherencia superior a otros AP32,35,36, así como el rendimiento cognitivo, nivel de actividad laboral, vida independiente y tratamiento voluntario37,25. La clozapina muestra especial eficacia en ciertas situaciones diferenciadas, como el riesgo suicida en esquizofrenia38–42, agresividad en psicosis43 y disminución del consumo de tóxicos en pacientes con diagnóstico de esquizofrenia44–46. Muestra además eficacia en trastorno bipolar47,48 y en psicosis en pacientes parkinsonianos49.
La ausencia de la respuesta esperable a fármacos adecuadamente administrados en tiempo y dosis es denominada actualmente «esquizofrenia resistente», y se recoge en el 18-30% de los casos50–54. Se trata de un concepto muy cuestionable por su simplificación, que se centra en los denominados «síntomas positivos», y no considera la gradación en los niveles de respuesta55, ni la funcionalidad36,56,57. La variabilidad de criterios empleados se traduce en estimaciones de prevalencia muy distintas5,58, de forma que trabajos muy recientes nos recuerdan la necesidad de estudios independientes de la industria y, por fin, con criterios de inclusión y herramientas de evaluación homogéneos59, especialmente respecto al seguimiento14,60. En este tipo de situaciones, la clozapina se muestra claramente superior a otras sustancias10,24,28,51,54,61–64, con tasas de respuesta sintomática en torno al 60-70%65 siendo la única sustancia aprobada en esta indicación53.
En el actual marco de abierto cuestionamiento al uso masivo, indiscriminado e indefinido de AP6,5 y más allá de la simplista perspectiva descriptiva de «resistencia», cuyo sustrato neurobiológico seguimos sin conocer66; la clozapina se propone como alternativa4 en los pacientes que no responden al tradicional bloqueo D2 de los AP67,68, o que parecen perder eficacia con el tiempo y uso masivo, tal vez en relación con una situación de hipersensibilidad secundaria a un proceso de sobrerregulación receptorial69,57,70
La clozapina no está libre de riesgo, pero ha de dimensionarse adecuadamente. La rigurosa monitorización hematológica ha permitido que, con una prevalencia de agranulocitosis estimada de 1,3%71,72,73, la tasa de mortalidad sea del 0,1-0,3%. La incidencia de cetoacidosis diabética oscila entre el 1,2-3,1%, y la de hipomotilidad gastrointestinal es del 4%. El interés por la miocarditis es creciente, las tasas de incidencia entre países son dispares, con una media mundial de 0,02-1%; un 7% en Australia, probablemente por el mayor rigor en la monitorización71,74,75. En conjunto, la clozapina podría estar asociada con menor mortalidad global comparada con cualquier otro AP76,77,78, siempre menor al riesgo de muerte por esquizofrenia38.
El consumo de clozapina es menor del previsible considerando sus indicaciones79–81. En concreto, la proporción de pacientes con diagnóstico de esquizofrenia que reciben clozapina es habitualmente inferior a los aludidos porcentajes esperables de resistencia79,82–88: un 6,7% en Québec80, un 10,2% en Dinamarca89, un 12,7% en India, o un 11% en Hong Kong90 como ejemplos, llegando al 23% en Inglaterra y Gales91,92. En general las tasas de uso de clozapina han ido en aumento a lo largo de la pasada década90,93, solo se encuentra descenso de prescripción en Colombia y en población con seguros públicos de EE. UU.94 donde, en 199986 el 6,1% de los pacientes con este diagnóstico recibían clozapina, el 5,7% en 2006; el 4,9% en 2007; el 4,6% en 2008; y el 4,3% en 200995. En 2014 la población de EE. UU. con seguros privados era, junto con Japón, la que menores tasas de prescripción recogía (14/100.000 habitantes. y 0,6/100.000 respectivamente). La distancia con el extremo opuesto en el que se sitúan Finlandia (189,2/100.000) y Nueva Zelanda (116,3/100.000) es abrumadora94.
La prescripción de clozapina oscila entre el 1 y el 2% del total de AP en numerosos países96, pero la variabilidad geográfica es muy importante; así, en EE. UU. las diferencias entre estados van del 2% de Luisiana al 15,6% de Dakota del Sur88,97; en Quebec, las variaciones entre regiones oscilan entre el 3,9 y el 9%80; y en Gran Bretaña, la elevada variabilidad entre territorios del Sistema Nacional de Salud se redujo entre 2000 y 2006 drásticamente, tras la definición de guías al respecto98 y el descenso de precio de la sustancia99. En un muy reciente análisis internacional, las diferencias entre los países estudiados llegan a un factor de 315 veces94.
Las indicaciones de protocolos y guías respecto a dosis y criterios de indicación3,100–102 se incumplen sistemáticamente, retrasándose el inicio una media de 5 años84,89,103–106, 8,9 años en varones35,107. Durante ese tiempo la mayor parte de los pacientes (68%35) reciben numerosos AP y combinaciones a pesar de la escasa evidencia que sostiene esta práctica86,103, empeorando el pronóstico y elevando los riesgos108. La prescripción no solo es escasa y tardía, también parece en ocasiones arbitraria o condicionada por factores raciales109–111; así, Manuel et al. encuentran en Nueva York que, sorprendentemente, el consumo de drogas se asocia a menor prescripción de clozapina, y negros e hispanos la reciben menos que blancos112, tendencias exactamente replicadas en todo EE. UU.88. La edad y el sexo también condicionan el acceso a la sustancia: jóvenes y mujeres reciben globalmente menos prescripciones de clozapina que los varones entre 40 y 59 años94 .Finalmente, la infradosificación es frecuente53, y no solo en la asistencia habitual, donde raramente se individualizan las dosis mediante niveles plasmáticos, sino en los ensayos en que se compara clozapina con otros fármacos12,113. A diferencia de la sucesión de aprobaciones de nuevas indicaciones para los demás AA, las indicaciones específicas de clozapina señaladas, como riesgo suicida, consumo de sustancias o agresividad, no son oficialmente aceptadas.
En conjunto los datos internacionales disponibles indican en general una baja prescripción, infradosificación y retraso en el inicio del tratamiento. No disponemos de estudios que valoren estos aspectos en población española, por lo que nos hemos planteado una primera aproximación a través de 4 muestras territoriales. Nuestra hipótesis es que, al igual que las referencias comentadas, también en nuestro país el consumo de clozapina podría ser bajo y variable. Nuestro objetivo, en caso de confirmarse la hipótesis, sería iniciar una reflexión sobre posibles estrategias a plantear.
Material y métodosLos autores han accedidos a datos de consumo de clozapina en Cataluña, Castilla y León, País Vasco y un Área de Madrid (el Área de Gestión Clínica de Psiquiatría y Salud Mental del Hospital 12 de Octubre, AGCPSM H12O), con un nivel de detalle mayor en País Vasco y Madrid, donde, además del consumo en pacientes diagnosticados como esquizofrenia en un periodo temporal, se pudieron diferenciar subterritorios (provincias del País Vasco, centros de salud mental de Usera, Villaverde y Carabanchel) e incluso profesionales en el último caso. La fuente fue, en el caso de Cataluña «Salut Mental i Addiccions Resum executiu 2015, Xarxa de Salut Mental de Catalunya»; en el País Vasco «Proyecto Uso de clozapina en el tratamiento de pacientes con esquizofrenia en la CAV», en Castilla y León y en Madrid los datos del AGCPSM H12O y servicio de Farmacia de dichos territorios.
ResultadosEn la tabla 1 se presentan los resultados globales.
Resultados globales
| Población de referencia 2015 | Pac.Dx.Esquz. atendidos | Pac.Dx.Esquz. en tto/100 hab | Ttos cloza | Ttos cloza/100.000 hab | % Pac.Dx.Esquz. con clozapina | ||
|---|---|---|---|---|---|---|---|
| 2015 Cataluña | (ver gráf. CSMA) | 6.109.571 | 22142 | 0,36 | 3033 | 49,6 | 13,7 |
| 2017 País Vasco | Vizcaya | 1.138.852 | 3.122 | 0,27 | 776 | 68,1 | 16,17 |
| Guipúzcoa | 710.699 | 1.910 | 0,26 | 317 | 44,6 | 12,25 | |
| Álava | 322.335 | 503 | 0,15 | 213 | 66,08 | 17,30 | |
| Total | 2.171.886 | 5.535 | 0,22 | 1306 | 59,59 | 15,24 | |
| 2015 Área del H12O | Usera | 132.744 | 512 | 0,38 | 104 | 78,3 | 20,31 |
| Villaverde | 140.599 | 378 | 0,26 | 82 | 58,3 | 21,69 | |
| Carabanchel | 240.230 | 386 | 0,16 | 46 | 19,1 | 11,91 | |
| Total | 491.129 | 1.276 | 0,25 | 232 | 47 | 17,9 | |
| 2016 Castilla y León | Valladolid | 523.679 | 104 | 19,8 | |||
| Segovia | 155.652 | 33 | 21,2 | ||||
| León | 473.604 | 153 | 32,3 | ||||
| Salamanca | 335.985 | 114 | 33,9 | ||||
| Zamora | 180.406 | 63 | 34,9 | ||||
| Ávila | 162.514 | 65 | 39,9 | ||||
| Burgos | 360.995 | 160 | 44,3 | ||||
| Palencia | 164.644 | 75 | 45,5 | ||||
| Soria | 90.040 | 42 | 46,6 | ||||
| Total | 2.447.519 | 809 | 33 |
CSMA: centros de salud mental de adultos, Cataluña; Pac.Dx.Esquz.: pacientes diagnosticados como esquizofrenia atendidos; Ttos cloza: tratamientos con clozapina.
Considerando la población de referencia en Cataluña en 2015 (6.109.571 habitantes), habitantes, la tasa de diagnósticos de esquizofrenia supondría un 0,36%; y la tasa de tratamiento con clozapina un 4,9 por 10.000 habitantes.
Un 13,7% de los pacientes en tratamiento por diagnóstico de esquizofrenia en Cataluña en 2015 recibieron tratamiento con clozapina (el 11,6% mujeres, el 15% hombres), con un coeficiente de variación entre centros prescriptores superior al 50%, como se recoge en el gráfico. Se trata de un objetivo de calidad de prescripción farmacéutica de la Red de Salud Mental de Cataluña (fig. 1).
País VascoConsiderando la población del País Vasco en 2017 (2.171.886 habitantes), las personas en tratamiento diagnosticadas como esquizofrenia fueron 5.535, lo que supone un 0,22% de la población (un 0,26% en Guipúzcoa; un 0,27% en Vizcaya y un 0,15% en Álava).
En julio de 2017 se recogían 1.306 pacientes en tratamiento con clozapina en el conjunto del País Vasco, sin especificarse diagnósticos. En conjunto, la tasa de tratamientos con clozapina en la comunidad autónoma del País Vasco sería de 59,59/100.000 habitantes, aunque su distribución no resulta homogénea, pues la tasa en Vizcaya es de 68,1 tratamientos/100.000 habitantes, en Guipúzcoa de 44,6 y en Álava de 66,08.
Si se consideran los pacientes en tratamiento por diagnósticos de esquizofrenia y el número de tratamientos con clozapina, las tasas oscilarían entre el 12,25% de pacientes en tratamiento con la sustancia en Guipúzcoa, y el 17,30% en Álava, con un 16,17% para Vizcaya, con una media de 15,24%.
Castilla y LeónHemos obtenido únicamente el número de pacientes en tratamiento con clozapina en cada provincia en 2016, deduciendo la tasa de tratamientos en función de la población que, globalmente, se sitúa en 3,30/10000 habitantes, con diferencias entre provincias (del 1,98 de Valladolid al 4,66 Soria).
Área del Hospital 12 de Octubre de MadridLa población atendida en el conjunto del Área del H12O de Madrid era en 2015 de 491.129 habitantes, de 137.914 en Usera, de 156.527 en Villaverde, y de 196.688 en Carabanchel; las tasas de diagnóstico de esquizofrenia supondrían el 0,25% (0,37% en Usera; 0,24% en Villaverde; 0,19% en Carabanchel) y las de tratamiento con clozapina serían de 4,7/10.000 (5,9/10.000 en Usera; 5,2/10.000 en Villaverde; 2,3/10.000 en Carabanchel)
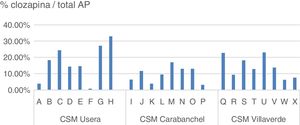
Un 17,97% de los pacientes en tratamiento por diagnóstico de esquizofrenia en el conjunto del Área recibieron tratamiento con clozapina en 2015 (un 20,31% en Usera, un 21,69% en Villaverde, y un 11,91% en Carabanchel), como se recoge en la tabla 1.
Las dosis diaria definidas (según la norma del Collaborating Centre for Drug Statistics Methodology) prescritas en 2015 en el Área del H12O por parte de especialistas psiquiatras en los centros de salud mental (unidades de tratamiento extrahospitalario que asumen la práctica totalidad de los seguimientos especializados, pero no incluye por lo tanto la prescripción asumida por atención primaria), oscilaron entre las 10.239 y 20.963 en los distritos aludidos, representando entre el 11,36% y el 18,26% del total de AP indicados, como se recoge en la tabla 2.
Dosis diarias definidas de antipsicóticos prescritas en los centros de salud mental del AGCPSM H12O
| Unidad funcional | DDD clozapina | DDD AP | % Clozapina/Total AP |
|---|---|---|---|
| CSM-Usera | 20.963 | 114.779 | 18,26 |
| CSM-Villaverde | 17.223 | 95.158 | 18,10 |
| CSM-Carabanchel | 11.598 | 109.572 | 10,58 |
| Suma actividad no hospitalaria | 49.794 | 319.5010 | 15,64 |
AGCPSM H12O: Área de Gestión Clínica de Psiquiatría y Salud Mental del Hospital 12 de Octubre, AP: antipsicóticos; CSM: centro de salud mental; DDD: dosis diarias definidas.
Dentro de un mismo centro la diferencia en las prescripciones entre facultativos que atienden perfiles de pacientes similares fueron también notables (fig. 2):
DiscusiónLos datos globales de prescripción de clozapina en los territorios estudiados no son tan bajos como los recogidos en otros trabajos internacionales, y se sitúan en el rango de países de nuestro entorno. Sin embargo, la variabilidad en la prescripción es muy importante y aumenta a medida que analizamos zonas menores, hasta llegar a una gran heterogeneidad de la prescripción individual.
Como señalábamos, entre el 18 y el 30% de los pacientes diagnosticados como esquizofrenia cumplirían los criterios de resistencia habitualmente empleados, y serían candidatos a recibir clozapina. De ellos el 60-70% respondería a al fármaco, por lo que deberíamos encontrar unas tasas mínimas del 20% de los pacientes en tratamiento por ese diagnóstico, recibiendo clozapina114.
Sin llegar a ese mínimo, los datos globales se aproximan en el H12O (17,9%); en menor medida en País Vasco (15,24%) y Cataluña (13,7%). Se trata de niveles por encima de buen número de países aludidos, aunque alejados de los datos británicos o neocelandeses. Pero estas cifras varían notablemente cuando observamos territorios menores: las 3 provincias vascas oscilan entre el 17,30% y 16,17% de Álava y Vizcaya y el 12,25% de Guipúzcoa; variaciones muy similares a los 3 distritos del H12O: del 21,69% de Villaverde o el 20,31% de Usera, al 11,91% de Carabanchel. En Cataluña las diferencias entre centros de salud mental de adultos llegan a oscilar entre un 0,0% y un 33,5%.
La llamativa variabilidad entre nuestros territorios, sin grandes diferencias sociodemográficas, con una normativa en uso de clozapina común, y con una proporción de pacientes en tratamiento por diagnóstico de esquizofrenia no muy diferentes (entre el 0,22% y el 0,36%; menores de la prevalencia esperable teórica de 0,5-0,7%115) se confirma si, en lugar de pacientes en tratamiento, estudiamos las prescripciones. Globalmente, nuestras tasas de tratamientos con clozapina/100.000 habitantes oscilan entre 33 y 59/100.000 habitantes, en el rango de países como Francia (43,1), Italia (41,8), Dinamarca (58,3) o Noruega (50,1); pero lejos de Nueva Zelanda (116,3) u Holanda (103,1); y muy lejos de los estándares teóricos (200/100.000 habitantes)94.
Pero, a medida que analizamos las prescripciones en territorios menores, la variabilidad aumenta. Así, en Castilla y León las diferencias entre provincias van del 19,8 al 46,6/ 100.000 habitantes; en el País Vasco, del 44,6 al 68,1/100.000 habitantes. La proporción de tratamientos de clozapina (dosis diaria definidas) frente al total de AP que encontramos en los distritos del H12O pasa del 18,26% o el 18,10% de Usera y Villaverde al 10,58% de Carabanchel; y cuando analizamos la prescripción por facultativos diferentes, contando con perfiles de consulta similares y población homogénea en número y cualidad, las diferencias entre ellos llegan a oscilar entre el 0,88% y el 33,03% en un mismo centro.
La variabilidad en la práctica no es una situación exclusiva de la psiquiatría116,117, ni afecta solo a la prescripción farmacológica118. En ocasiones, las circunstancias económicas, sociales y culturales pueden condicionar esa variabilidad; así encontramos el importante cambio en la prescripción de clozapina en Inglaterra tras disponer de genéricos más económicos99, o el descenso de uso en China que, aunque sigue siendo elevado por su menor precio y diferente regulación de uso119, está disminuyendo en las provincias más desarrolladas y en familias con mayor nivel económico120,121. En EE. UU. el uso de clozapina en pacientes con seguros privados es escaso frente al sistema público; probablemente por la escasa proporción de pacientes susceptibles de ser tratados con clozapina, que trabajan y por lo tanto que disfruten de seguros privados94. Consideramos que, en nuestro caso, aunque hemos estudiado territorios con indudables diferencias socioculturales y económicas, el peso de estos factores no explica la variabilidad; especialmente si observamos que las diferencias mayores se encuentran en los menores territorios, como los centros de salud mental de adultos de Cataluña; e incluso entre prescriptores de un mismo distrito en el caso del H12O.
Aunque tampoco explica nuestros datos, la heterogeneidad es también llamativa en las normas que regulan el uso de la sustancia en distintos países, y se propone como causa de las diferencias. Es variable la autorización al médico general para prescribirla, la disponibilidad de formulaciones no orales, su suministro en farmacias normales, la dosis máxima permitida, la definición de «esquizofrenia resistente» que autoriza su empleo, o las indicaciones aceptadas fuera de esquizofrenia resistente, entre otros muchos aspectos. La mayor parte de estas diferencias no tienen una clara justificación clínica y suponen una notable inequidad en el acceso al fármaco. Pero, aunque parece probable que las normas restrictivas disuadan a clínicos y pacientes de utilizar el tratamiento, al menos con regulaciones tan extremas como Japón (que presenta 0,6 tratamientos/100.000 habitantes)94, no hay datos objetivos sobre el efecto de las distintas regulaciones en el consumo122, y no puede considerarse el factor esencial, como ilustra el caso de Colombia, sin restricción de uso por indicaciones y sin exigencia de control hematológico, pero con prescripciones modestas94.
Como marco general de nuestra prescripción, el mercado de los AP cambia radicalmente a partir de los 90, con la irrupción de nuevas sustancias diseñadas bajo su influencia55 sin sus riesgos123, y que se ofrecen de entrada tan eficaces como clozapina. Los nuevos AP han desplazado del mercado a sus antecesores a pesar de su mayor precio124–127, con campañas de comercialización agresivas frente al escaso interés económico de clozapina88, aspectos que podrían complementar la explicación de esta variabilidad de prescripción111.
Pero, aunque menos definidos que los anteriores, los factores más frecuentemente relacionados con la variabilidad de uso son tan groseros como la tradición en el uso de un tratamiento en determinado territorio, y las diferencias en criterio y conocimientos de los prescriptores88,95. En nuestro caso, la relativa homogeneidad social de los territorios estudiados, la identidad de marco normativo, y el aumento de las diferencias a medida que nos acercamos al nivel individual de prescriptor, nos hacen pensar que estos son los ingredientes que más influyen en los hallazgos.
Hasta la fecha, se han realizado pocas investigaciones empíricas sobre las razones de la infraprescripción de clozapina por los psiquiatras128. Los argumentos habitualmente esgrimidos son las complicaciones que las normas imponen, la falta de capacitación para su manejo, y el temor a los efectos secundarios de médicos y pacientes o familias129. La percepción de riesgo en los médicos es desmesurada114, y paralela a la falta de conocimiento sobre su uso130,131.
En los últimos años se han puesto en marcha diversas iniciativas de las administraciones de algunos países, que proponen un uso de clozapina ajustado al volumen de pacientes que, con un balance riesgo-beneficio apropiado, podrían beneficiarse del tratamiento95. Estas acciones parecen influir decisivamente en la prescripción: así, en Holanda se puso en marcha en 2004 el Dutch Clozapine Collaboration Group (DCCG), promoviendo una guía y otras acciones entre profesionales y pacientes; en 2014 se había logrado un incremento del 56% de tratamientos con clozapina114. En Nueva Zelanda entre 2000 y 2004 el uso de clozapina en los pacientes con diagnóstico de esquizofrenia se incrementó del 21% al 32,8%10,15,31. En 2010 se puso en marcha en el estado de Nueva York la «Best Practices Initiative—Clozapine», que desarrolló acciones facilitadoras para los prescriptores, y herramientas de ayuda en la elección para los pacientes, en el marco de un modelo de decisión compartida . Las nuevas prescripciones se incrementaron en un 40% entre 2009 y 2013132.
La definición de un marco de conocimiento claro es la base necesaria pero no suficiente; los enfoques puramente didácticos tienen poco impacto en el comportamiento del médico133, e incluso se plantea el riesgo de que las guías actúen como un freno más122. Es preciso plantear acciones en todos los niveles de la atención, implicando a los equipos de salud mental y de salud en general, responsables políticos y pacientes y familiares28,134 con apoyo administrativo135–137; en modelos de cuidados integrados con sistemas definidos de coordinación de cuidados y apoyo a la implementación del tratamiento. La creación de dispositivos específicos131 es controvertida. Respecto a la normativa, a pesar de ser extraordinariamente restrictiva no llega a cumplirse, y varía sin fundamento sólido en distintos países. Es preciso generar una iniciativa que dé coherencia a las regulaciones122 y asegurar su cumplimiento.
Parece pues de interés establecer programas educativos para los profesionales, pero también para pacientes y familiares; siempre en el marco de modelos cuidados integrados, decisión compartida, coordinación de cuidados y apoyo a la decisión e implementación131,138. En esta línea se ha desarrollado en el AGCPSM H12O a lo largo de 2016, una iniciativa que pretende un uso apropiado de clozapina. La primera etapa ha consistido, en paralelo al presente análisis de la situación de prescripción, en el desarrollo de una guía práctica de uso de clozapina ajustada a nuestro medio, difundida en varias acciones entre todos los profesionales del Área. Se ha organizado asimismo un sistema centralizado y homogéneo de recogida de protocolos hematológicos accesibles desde cualquier punto de la red, incluido urgencias. En una segunda fase se plantea la difusión en atención primaria y de modo individualizado entre pacientes y familiares mediante material específico. Se estudiarán los efectos de estas acciones sobre la prescripción.
LimitacionesComo hemos señalado, este trabajo únicamente pretende ser una primera acción movilizadora de otros estudios cuantitativos más amplios y homogéneos; y de acciones para una correcta prescripción en su caso. Aunque consideramos que las conclusiones principales sobre uso global y variabilidad son válidas, las fuentes de datos son heterogéneas en algunos aspectos: las fechas de recogida son diferentes; Cataluña y País Vasco recogen datos de prescripción en pacientes diagnosticados de esquizofrenia mientras que, aunque probablemente el grueso de las prescripciones sean en ese diagnóstico, el H12O no lo especifica. Asimismo, los datos de prescripción de País Vasco y H12O se refieren a actividad no hospitalaria; Cataluña nos ofrece datos globales. A diferencia del País Vasco, los datos de prescripción de Cataluña y H12O se refieren atención especializada, sin contar con las prescripciones asumidas por los médicos de familia en cada territorio. Los datos de Castilla y león se refieren únicamente a prescripciones, sin considerar diagnóstico. Nos proponemos resolver estas diferencias en próximos y más amplios trabajos.
FinanciaciónEste trabajo no ha recibido financiación pública o privada.
Conflicto de interesesEl Dr. Bernardo ha sido consultor o ha recibido honorarios o fondos de investigación de ABBiotics, Adamed, Eli Lilly, Ferrer, Forum Pharmaceuticals, Janssen-Cilag, Lundbeck, CIBERSAM, Instituto de Salud Carlos III, Ministerio de Ciencia e Innovación, Ministerio Economía y Competitividad, Ministerio de Educación Cultura y Deporte, 7th Framework Program of the European Union, Foundation Group for Research in Schizophrenia (EGRIS).
Agradecemos al Dr. Jiménez Arriero y Dr. Francisco Rivas sus facilidades e impulso en la coordinación de intereses; al Dr. Oscar Pinar del Servicio de Farmacia del H 12 de Octubre, y los Dres. Luis Agüera y Javier Rodríguez su esfuerzo en la obtención de datos.