La cirugía continúa siendo el pilar fundamental del tratamiento del carcinoma de tiroides. El mayor acceso a estudios de imágenes permite hoy el diagnóstico de nódulos en etapas más precoces, lo que, si bien constituye una mejoría en el diagnóstico, hacen a la vez necesaria su juiciosa evaluación para evitar el sobre diagnóstico y sobre tratamiento. En ese contexto en los últimos años han cobrado relevancia conductas quirúrgicas menos agresivas, como la lobectomía o la tiroidectomía parcial, o con abordajes menos invasivos. Para ello resulta fundamental un equipo médico multidisciplinario junto a la adecuada evaluación y planificación preoperatoria por parte del cirujano con el fin de ofrecer un tratamiento personalizado a cada paciente. Los avances en anestesia, el uso de instrumentos de energía para hemostasia y la monitorización intraoperatoria del nervio laríngeo han mejorado la seguridad quirúrgica, aunque no sustituyen la técnica meticulosa ni el juicio clínico del cirujano. Vías de abordaje remoto y técnicas de ablación por radiofrecuencia, representan alternativas de manejo quirúrgico para casos seleccionados de pacientes con cáncer de tiroides. El objetivo de esta revisión es analizar el estado actual del diagnóstico y el tratamiento quirúrgico de esta patología.
Surgery remains the cornerstone of thyroid cancer treatment. Greater access to imaging studies now allows for the diagnosis of nodules at earlier stages. While this improves diagnostic performance, it also requires careful evaluation to avoid overdiagnosis and overtreatment. In this context, less aggressive surgical procedures, such as lobectomy or partial thyroidectomy, or less invasive approaches, have gained relevance in recent years. Proper preoperative evaluation and planning by the surgeon and a multidisciplinary team is essential to offer personalized treatment to each patient. Advances in anesthesia, the use of energy instruments for hemostasis, and intraoperative monitoring of the laryngeal nerve have improved surgical safety, although they do not replace the surgeon's meticulous technique or clinical judgment. Remote access routes and radiofrequency ablation techniques represent surgical management alternatives for selected cases of patients with thyroid cancer. The objective of this review is to analyze the current status of diagnosis and surgical treatment of this pathology.
Debido a su alta prevalencia, este artículo se centrará en el carcinoma papilar de tiroides, y no se referirá a otras variantes menos frecuentes como el carcinoma folicular, medular y anaplásico.
La cirugía sigue siendo la piedra angular en el tratamiento de los nódulos tiroideos malignos, mediante tiroidectomía, ya sea total o parcial1–3. Los primeros reportes de la literatura médica en relación con la extirpación de la tiroides mostraban una elevada morbilidad y mortalidad, debidas a hemorragias incontrolables, la falta de sustitución de hormona tiroidea o por la afectación de las glándulas paratiroides cuya función y relaciones eran aún poco conocidas. Fue a fines del siglo XIX cuando el cirujano suizo Theodor Kocher introdujo modificaciones en la técnica que fueron la base de la cirugía tiroidea moderna4. Actualmente es llevada a cabo por equipos especializados que realizan un alto volumen de cirugías. La tiroidectomía es una intervención segura, con baja tasa de complicaciones, la mayoría de ellas, transitorias1–3.
El desarrollo de técnicas de anestesia, así como la incorporación de tecnología avanzada en pabellón, como el uso de electrobisturí, dispositivos de energía para hemostasia, el uso de lupas de magnificación, y equipos de monitorización de nervio laríngeo nos ayudan hoy a realizar cirugías con menos complicaciones y tiempos quirúrgicos y de hospitalización más acotados. Sin embargo, estos avances no sustituyen lo esencial; el correcto estudio y selección de los pacientes, con la participación de un equipo médico multidisciplinario que, junto al apoyo de laboratorio, imágenes y biopsia, sumado a una técnica quirúrgica meticulosa, nos permiten ofrecer hoy un tratamiento quirúrgico racional, seguro, e individualizado acorde a las condiciones de cada paciente y a la etapa de evolución de la enfermedad5.
Consideraciones diagnósticasLa alta prevalencia de enfermedad nodular tiroidea, así como la proporcional baja incidencia de cáncer dentro del universo de pacientes portadores de nódulos tiroideos, junto al muy buen pronóstico vital de estos pacientes cuando se diagnostican en etapas precoces, hacen que no se recomiende el uso masivo de métodos de cribado para el diagnóstico de cáncer de tiroides6. No obstante, es cada vez más frecuente la consulta de pacientes, con nódulos de pequeño tamaño y con crecimiento limitado al interior de la glándula, en quienes se ha hecho el diagnóstico de sospecha en forma incidental en una ecografía cervical7. Es en esos casos donde es fundamental la evaluación clínica del endocrinólogo y/o el cirujano de cabeza y cuello, con el fin de entregar información al paciente acerca de las posibilidades diagnósticas y de tratamiento que eventualmente requiera. Lo anterior, no solo es importante para controlar la ansiedad y el temor del paciente con relación a la sospecha de un diagnóstico de cáncer, sino también para no sobrecargar el sistema de salud con estudios diagnósticos y biopsias que pueden redundar en un sobre-diagnóstico y sobre-tratamiento7,8.
El diagnóstico de un carcinoma de tiroides parte con la evaluación clínica, examen físico dirigido, y una ecografía tiroidea, que, en manos de radiólogos experimentados en tiroides, puede entregar valiosa información en cuanto a tipificar la naturaleza de los nódulos (sólido, quístico o mixto), su número, tamaño, ubicación dentro de la glándula, relación con estructuras vecinas, presencia de microcalcificaciones, su vascularización al Doppler, presencia de adenopatías o signos de extensión extra tiroidea.
Con toda esta información el radiólogo categoriza el nódulo de acuerdo con la clasificación TI-RADS (Thyroid Imaging Reporting and Data System), en uso desde 2009 (tabla 1)6,9.
Patrones de riesgo ecográfico de la Asociación Americana de Tiroides (ATA) para nódulos tiroideos y riesgo de malignidad
| TI RADS | Riesgo de malignidad |
| TI RADS 1 | <1% (benigno) |
| TI RADS 2 | <3% (muy baja sospecha) |
| TI RADS 3 | 5-10% (baja sospecha) |
| TI RADS 4 | 10-20% (sospecha intermedia) |
| TI RADS 5 | 70-90% (alta sospecha) |
De acuerdo con los hallazgos clínicos y ecográficos, el clínico determinará en qué paciente es recomendable realizar un estudio histológico dirigido, mediante una punción aspirativa con aguja fina (PAAF), procedimiento ambulatorio realizado bajo ecografía, idealmente por un especialista en patología tiroidea, con el fin de asegurar la toma de una muestra adecuada en cantidad y calidad, que aumente su rendimiento (figura 1).
Esta punción obtiene muestra celular que posteriormente es analizada, idealmente también por patólogos experimentados o dedicados preferentemente a patología tiroidea. El reporte se realiza según las categorías diagnósticas del Sistema Bethesda (The Bethesda System for Reporting Thyroid Cytopathology). Se obtiene así un diagnóstico citopatológico y una determinación de riesgo de malignidad1,2,10 (tabla 2).
Adaptado de protocolo clínico cáncer diferenciado de tiroides SOCHED 2020
| Bethesda | Categoría diagnóstica | Riesgo de malignidad | Conducta |
|---|---|---|---|
| I | No diagnóstica o insatisfactoria | 1-4% | Repetir |
| II | Benigna | 0-3% | Observar |
| III | ASI* o LFSI** | 5-15% | Repetir/Test genético/Cirugía/Observación |
| IV | Neoplasia folicular | 15-30% | Repetir/Test genético/Cirugía/Observación |
| V | Sospechoso de malignidad | 60-75% | Cirugía |
| VI | Maligna | 97-99% | Cirugía |
Clasificación de Bethesda
- •
Bethesda I no diagnóstica/insatisfactoria: la muestra no es adecuada para diagnóstico.
- •
Bethesda II benigna: características citológicas de lesiones benignas como tiroiditis linfocítica o hiperplasia nodular
- •
Bethesda III atipia de significado indeterminado/lesión folicular de significado indeterminado (AUS/FLUS): atipia en células foliculares sin indicios claros de malignidad
- •
Bethesda IV neoplasia folicular o sospecha de neoplasia folicular (FN/SFN): proliferación folicular que podría corresponder a un carcinoma folicular.
- •
Bethesda V sospechosa de malignidad: características citológicas altamente sospechosas de malignidad.
- •
Bethesda VI maligna: características citológicas concluyentes de malignidad, como en el carcinoma papilar (figuras 2 y 3).
En aquellos pacientes en que el diagnóstico histológico obtenido por PAAF sea concluyente o de alta sospecha de malignidad, estará indicado el tratamiento quirúrgico, una tiroidectomía, cuya extensión, total o parcial, dependerá de una serie de consideraciones, en relación con el o los nódulos, la extensión local del tumor, la presencia de compromiso linfonodal cervical y también con las características particulares de cada paciente.
Ecografía de etapificaciónPrevio al tratamiento quirúrgico resulta fundamental la realización de una ecografía de etapificación1,2,11. Dicho estudio, debe ser realizado por radiólogos experimentados en esta patología. Entrega valiosa información al equipo tratante y al cirujano en cuanto a las características del tumor primario, su ubicación, signos sugerentes de extensión extra tiroidea, y el estado de los linfonodos cervicales. Esto ayuda a planificar la cirugía más apropiada para el paciente, su extensión y la eventual necesidad de disección ganglionar, lo que puede tener un impacto en la re-etapificación postoperatoria, evolución y pronóstico del paciente11–13.
Es recomendable adjuntar un esquema que detalle la ubicación de los linfonodos sospechosos (figura 4).
Las características ecográficas que sugieren compromiso ganglionar metastásico, entre otras, son: presencia de microcalcificaciones, cambios quísticos intranodales, hiperecogenicidad cortical o alteraciones en su vascularización1,2,11,12. En casos seleccionados por duda diagnóstica o que implique cambios en el enfrentamiento quirúrgico, es recomendable realizar una PAAF de la adenopatía con estudio citológico y medición de tiroglobulina (Tg) en el aspirado, especialmente en adenopatías en compartimentos laterales1–3,13.
Ante sospecha de compromiso tumoral extratiroideo a tráquea o esófago, o ante la presencia de metástasis linfáticas extensas o de gran volumen es aconsejable realizar una tomografía computada o resonancia magnética con medio de contraste endovenoso1–3,13.
Así la determinación preoperatoria de la presencia de metástasis ganglionares cervicales, en cuanto a su número, tamaño y ubicación, junto a la evaluación dirigida de compromiso local extratiroideo, resultan fundamentales para planificar el tratamiento quirúrgico más adecuado y así reducir la posibilidad de requerir reintervenciones quirúrgicas a mediano y largo plazo, así como también para determinar en mejor forma la estratificación de acuerdo a grupos de riesgo de recurrencia, y con ello, la mejor planificación de terapia complementaria con radioyodo y seguimiento posterior1,11–13.
Con estos antecedentes el paciente debe ser presentado en Comité de Tiroides, que incluye a un equipo multidisciplinario conformado por endocrinólogo, cirujano de cabeza y cuello, patólogo, radiólogo, médico nuclear y, en casos avanzados con necesidad de terapia sistémica, de un oncólogo médico1,13.
Actualmente en Chile el cáncer diferenciado de tiroides (CDT) corresponde a una patología de las Garantías Explícitas en Salud (GES) y eso enmarca conductas y grupos de tratamiento preestablecidos por la normativa nacional13.
Cirugía del cáncer diferenciado de tiroidesCuando nos enfrentamos al diagnóstico de un CDT, la cirugía nos presenta como objetivos principales1–3:
- a)
La remoción total del tumor primario.
- b)
Remoción del tejido adyacente comprometido, frecuentemente tejido adiposo o muscular peritiroideo, o en estadios avanzados, el compromiso de pared traqueal, esófago o del nervio laríngeo.
- c)
Remoción de los linfonodos cervicales con compromiso tumoral demostrado o de alta probabilidad.
- d)
Facilitar el seguimiento a largo plazo con ecografía y medición de tiroglobulina.
- e)
Mejorar el efecto de la terapia ablativa con radioyodo que requiere, en lo posible, de ausencia de tejido tiroideo remanente.
- f)
Al mismo tiempo, minimizar los riesgos de morbilidad y complicaciones de la cirugía, en especial en cuanto a preservar la función de las glándulas paratiroides y de los nervios laríngeos.
La extensión de la tiroidectomía ha sido un tema de controversia por largo tiempo. La tendencia ha sido realizar lobectomías o tiroidectomías parciales, fundamentalmente para reducir los riesgos de complicaciones derivadas de la cirugía, que, aunque poco frecuentes, pueden ocasionar morbilidad por tiempo prolongado, como la disfonía o los síntomas derivados de un hipoparatiroidismo. Junto a ello, está también el deseo de pacientes y médicos de mantener al menos en parte la función de la tiroides5,13,14.
Por otro lado, hay consideraciones que en muchos casos favorecen la decisión de realizar una tiroidectomía total; la presencia de multinodularidad, el tamaño de los nódulos, la sospecha de extensión extratiroidea, así como la necesidad de no dejar tejido tiroideo remanente para optimizar una posterior terapia con radioyodo, y el seguimiento con tiroglobulina. Al mismo tiempo, la dificultad de acceso a pabellón por la gran sobrecarga de los sistemas de salud, hacen que también se haga necesario realizar una cirugía lo más completa y definitiva posible, para disminuir la posibilidad de necesitar futuras reintervenciones de pacientes por enfermedad recurrente o persistente13,15,16.
Hoy en día, y considerando el aumento del diagnóstico en etapas precoces, con lesiones intratiroideas, de pequeño tamaño, sin evidencia de diseminación ganglionar en el cuello, y teniendo en cuenta el excelente pronóstico de esta patología, se hace cada día más frecuente optar por cirugías menos invasivas, o con conservación de parte de la glándula14–18.
Generalidades y perioperatorioEl paciente con diagnóstico presuntivo o certeza de cáncer de tiroides es presentado en un comité de tiroides, (ya descrito). Allí se deben evaluar sus antecedentes y planificar su tratamiento médico y quirúrgico. En el preoperatorio se deben evaluar también los exámenes preoperatorios generales que correspondan de acuerdo con su edad y patologías asociadas (enfermedades cardiovasculares, tabaquismo, enfermedades respiratorias, trastornos de coagulación). Fundamentalmente, en mayores de 40 años, contar con un electrocardiograma, perfil de función tiroidea (TSH, T3, T4) y pruebas de coagulación. Especial consideración para pacientes con carcinoma tiroideo asociado a hipertiroidismo, condición poco frecuente, que requiere tratamiento farmacológico previo específico con medicamentos antitiroideos, betabloqueadores y en ocasiones con tratamiento corticoidal con el fin de conseguir la estabilización de la función tiroidea y evitar así complicaciones relacionadas con el evento quirúrgico, en especial del punto de vista cardiovascular, como crisis hipertensiva y arritmias graves. Es importante también medir niveles de Vitamina D y suplementar los casos de déficit para minimizar los trastornos en el metabolismo del calcio ante un eventual hipoparatiroidismo postquirúrgico, como se detalla más adelante1,13,19.
El paciente ingresa a hospitalización el mismo día de la cirugía, cumpliendo con el período de ayuno recomendado de al menos 6 horas. La cirugía se realiza bajo anestesia general, y cuando se trata de una tiroidectomía total exclusiva, tarda habitualmente entre 60-90 minutos. Al salir de pabellón, el paciente permanece un período variable de tiempo en una sala de recuperación de anestesia bajo observación estricta y monitorización por personal de enfermería, tras lo cual retorna a su habitación.
El periodo de hospitalización por lo general es de dos días, debido a que algunas complicaciones, aunque muy infrecuentes, ocurren generalmente dentro de las primeras 24-48 horas, y requieren de una identificación y manejo oportuno, en especial el hematoma cervical1,13,20,21.
La incisión quirúrgica, habitualmente de alrededor de 4-5 centímetros, no requiere cuidados especiales en los primeros días, y habitualmente se hace poco perceptible a las pocas semanas de la cirugía. El postoperatorio, habitualmente es muy bien tolerado, con un dolor que la mayoría de los pacientes califican de muy leve, en parte ocasionado por la posición de hiperextensión del cuello durante la cirugía. El paciente por lo general, al día siguiente puede estar deambulando, alimentándose y hablando sin dificultad.
La incapacidad laboral es por lo general de unas dos o tres semanas, dependiendo de la evolución postoperatoria y de la actividad que realice cada paciente, en especial con cierta limitación a la actividad física y deportiva, aunque manteniendo por lo demás un reposo relativo.
Tiroidectomía total, técnica quirúrgica y relaciones anatómicasIrrigación: la glándula tiroides es un órgano que posee una extensa irrigación arterial y venosa, que proviene de los grandes vasos del cuello, arteria carótida, y vena yugular interna, y de los vasos subclavios. Así, los vasos sanguíneos que debemos disecar, aunque de pequeño calibre, poseen un alto flujo, por lo que resulta de suma importancia una disección prolija, con una técnica quirúrgica meticulosa. En la actualidad son ampliamente usados diversos dispositivos de sellado de vasos mediante el uso de energía, reduciendo al mínimo el sangramiento intraoperatorio y reduciendo en forma importante la duración de la cirugía22. Existen dispositivos de energía para sellado y corte de tejidos o vasos de hasta 7mm, ya sea por fusión celular o por energía ultrasónica.
De todas formas, debe siempre realizarse una revisión de la hemostasia antes del cierre bajo visión directa y realizando el anestesiólogo una maniobra de Valsalva que simule los aumentos de presión venosa que pueden ocurrir una vez terminada la anestesia. El uso de drenaje, hoy en día se reserva solo para aquellos casos de cirugías con disecciones extensas, o con tumores y nódulos tiroideos de gran tamaño23,24, siendo por lo general retirado en el postoperatorio previo al alta.
A pesar de todas estas consideraciones, puede producirse en un reducido porcentaje de casos, un hematoma cervical postoperatorio. Su incidencia es muy variable en la literatura, pero en general oscila en rangos de 0,6% y 1,8%25,26. Esta complicación, tiene una connotación distinta al que se puede producir posterior a cirugías de otros sitios anatómicos. Al ser el cuello un espacio anatómico compartimentalizado, el hematoma cervical ejerce una presión progresiva sobre los tejidos vecinos, colapsando vasos venosos y linfáticos, lo que se traduce en edema laríngeo, y el riesgo potencial de obstrucción de la vía aérea. Cuando se produce esta complicación, se debe actuar rápidamente, debiendo incluso en algunos casos abrir la herida operatoria en la habitación para descomprimir el cuello mientras el paciente se traslada a pabellón para re-explorar y hacer hemostasia. En la mayor parte de los casos, el hematoma se produce dentro de las primeras 4 horas del postoperatorio, siendo en su gran mayoría originado en sangramiento de vasos arteriales. El sangramiento de origen venoso tiende a ser de instalación más lenta y ocurre más frecuentemente dentro de 4-12 horas de postoperado26. Junto a la extensión de la cirugía, y al igual que otras potenciales complicaciones, ésta se ha asociado a la experiencia del cirujano tratante, medido como el volumen de tiroidectomías/año realizadas27.
Este es el principal motivo por el que se hace poco aconsejable el alta precoz, antes de 24 horas en pacientes post tiroidectomía.
Glándulas paratiroides: Otro punto importante en la técnica de una tiroidectomía total es lograr preservar la indemnidad de las glándulas paratiroides. Estas glándulas, por lo general dos por lado, tienen un tamaño que oscila entre unos 5 y 8mm, y se encuentran en íntima relación o incluso dentro de la cápsula tiroidea. Su adecuado funcionamiento es fundamental en los procesos de regulación de los niveles de calcio en la sangre, por lo que es de suma importancia su adecuada preservación. Para ello deben ser manipuladas en forma cuidadosa, en especial cuidando de preservar su irrigación, arterial y venosa, que depende en su mayor proporción de vasos provenientes de la arteria tiroidea inferior. La sección de estos vasos debe realizarse lo más distal posible, de lo contrario se producirá isquemia y congestión de su drenaje venoso que alterará en grado variable su función con la subsecuente hipocalcemia postoperatoria, que, aunque en la gran mayoría de los casos es transitoria, puede resultar en sintomatología molesta y muy limitante, dada por sensación de parestesias en cara y extremidades, que en casos severos puede derivar a fenómenos de espasmo muscular progresivos.
Por lo general, se indica aporte oral de carbonato de calcio en el postoperatorio, con lo cual estos síntomas son muy leves o no aparecen. Este aporte es suspendido en los días sucesivos de acuerdo con la evolución clínica del paciente y el control de niveles de calcio en sangre. Es importante también a este respecto, como ya fue mencionado, el evaluar en el preoperatorio los niveles de Vitamina D en sangre, cuyo déficit puede dificultar el adecuado manejo de este cuadro. Se recomienda tener un nivel de al menos 20 ng/ml o idealmente>30ng/ml28,29.
Cabe señalar que la hipocalcemia es una condición casi habitual en el postoperatorio de una tiroidectomía y que como ya se ha dicho, es generalmente transitoria y que puede ser asintomática o muy poco sintomática, siendo los casos de hipoparatiroidismo severo y prolongado, muy poco frecuentes. La incidencia del hipoparatiroidismo postquirúrgico tiene en la literatura una amplia variación que va desde un 7 a un 37%30,31. Esto se da principalmente por las diferencias en los criterios diagnósticos en base a los exámenes de laboratorio y en el tiempo de seguimiento.
El hipoparatiroidismo prolongado se define como la necesidad de aporte de calcio-vitamina D3 por más de un mes desde la cirugía, asociado a niveles persistentemente bajos de PTH, mientras que la necesidad de aporte de calcio-vitamina D3 por más de 12 meses post cirugía, se considera como hipoparatiroidismo persistente32.
El hipoparatiroidismo que puede producirse en el postoperatorio de una tiroidectomía total es un proceso dinámico y evolutivo en el tiempo30–32.
La evolución clínica, y el seguimiento de exámenes de laboratorio (calcemia - PTH), dan una buena aproximación a la evolución que tendrá el paciente en el tiempo (figura 5).
Evolución del hipoparatiroidismo post tiroidectomía.
Diagrama de flujo hipotético que muestra las diferentes etapas del hipoparatiroidismo postoperatorio (vía roja) o la recuperación de la función paratiroidea (vía azul) después de 100 tiroidectomías totales realizadas en una unidad quirúrgica experimentada y de alto volumen. Traducido de Sitges-Serra A. 202131. Con licencia: CC BY 4.0
iPTH: intact parathyroid hormone.
Es necesario recalcar que la causa de este cuadro en la mayoría de los casos, no se debe solamente a la extirpación advertida o inadvertida de una o varias glándulas, sino más bien al compromiso de la irrigación y drenaje venoso de las mismas durante la disección de la tiroides. Junto con la adecuada técnica quirúrgica, el uso de lupas de magnificación se ha asociado a mejores resultados y menor incidencia de hipoparatiroidismo, dado que permite una mejor visualización de las glándulas y de los diminutos vasos que las irrigan33,34. Algunos autores recomiendan también el uso de técnicas de detección como por ejemplo el de fluorescencia con verde de indocianina, aunque ésta y otras técnicas se encuentran aún en desarrollo y con un uso limitado por lo que sus resultados en cuanto a costo efectividad deben seguir evaluándose35,36.
A pesar de todas estas consideraciones, y a pesar de una disección prolija, en ocasiones el cirujano puede apreciar que existe una devascularización importante de una paratiroides. En ese caso puede realizarse un autoimplante de esa glándula en pequeños fragmentos en bolsillos musculares del cuello, similar a la técnica empleada en algunas cirugías de hiperparatiroidismo secundario Es por ello, por lo que esta cirugía debe ser realizada por cirujanos y equipos quirúrgicos experimentados y con un alto volumen de cirugías, con el fin de procurar los mejores resultados oncológicos y funcionales35,36.
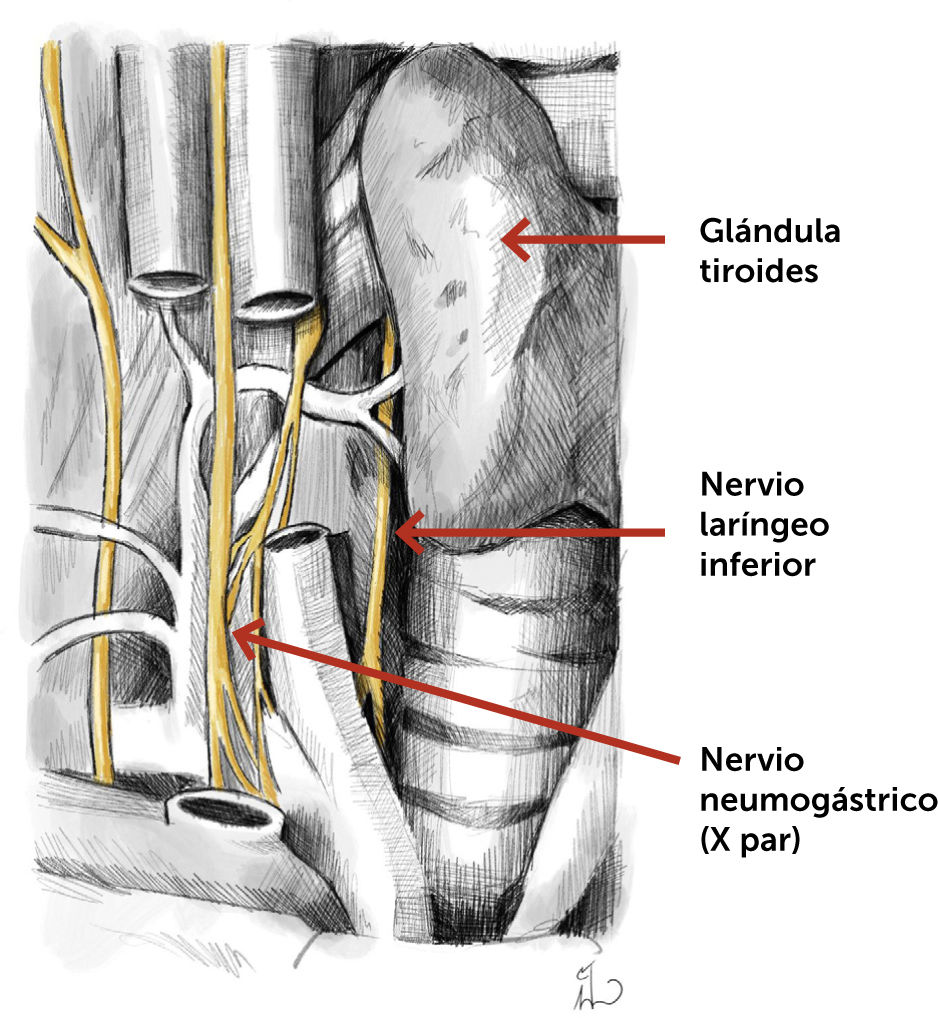
Nervios laríngeos: Otro punto relevante en relación con una cirugía de tiroides es la preservación anatómica y funcional de los nervios laríngeos, que son los responsables de la inervación motora de la musculatura laríngea que permite la movilidad de las cuerdas vocales y por ende la función de fonación.
- •
Nervio laríngeo inferior (NLI): Es también denominado nervio laríngeo recurrente, debido a su trayecto ascendente tras emerger del nervio vago (X par), y hacer un asa por debajo de la arteria subclavia al lado derecho y por debajo del cayado aórtico a la izquierda (figura 6).
Sólo en muy raros casos, especialmente a derecha, el NLI puede tener un trayecto no recurrente. Su calibre es de apenas un par de milímetros y se encuentra localizado profundamente junto al borde lateral de la tráquea, en el surco traqueoesofágico por donde asciende dividiéndose habitualmente en dos ramas antes de ingresar en la laringe donde le da inervación motora a la cuerda vocal del lado correspondiente.
En la actualidad, en muchos centros de alto volumen de tiroidectomía se cuenta con el apoyo de tecnología de neuromonitorización intraoperatoria de forma rutinaria o selectiva en este tipo de cirugías. Con ello y en especial al usar la monitorización continua, queda documentado en forma gráfica y en tiempo real que no sólo basta con la correcta identificación y preservación de la integridad anatómica del nervio durante todo su trayecto, lo que sigue siendo el gold standard en este respecto37, sino también, la preservación de su conducción nerviosa mediante una manipulación meticulosa y cuidando las maniobras de tracción o de trauma térmico. Con la ayuda del neuromonitor, hoy en día se puede reducir la posibilidad de lesiones transitorias o definitivas de NLI36–38. Sin embargo, desde el punto de vista de costo-efectividad, las guías clínicas (American Thyroid Association y la American Academy of Otolaryngology-Head and Neck Surgery) no avalan su uso en forma rutinaria en toda tiroidectomía, recomendándose preferentemente su uso ante casos de mayor complejidad de acuerdo con la ubicación y tamaño del tumor, o de las metástasis linfáticas, así como también en casos de reintervenciones, que ofrecen por lo general una dificultad técnica mayor38,39.
Tipos de neuromonitorización intraoperatoria del nerviol laringeo inferior (NLI)
- -
Monitorización intermitente del nervio laringeo inferior (I-IONM)
- -
Monitorización continua del nervio laringeo inferior (C-IONM)
Se utiliza un tubo endotraqueal que tiene incorporados dos electrodos que quedan apoyados en las cuerdas vocales, lo que debe ser verificado por el anestesista al momento de su fijación. Se debe considerar el uso restringido de relajantes musculares durante la cirugía, para no atenuar el efecto motor en la cuerda vocal del nervio estimulado (figura 7).
- -
Monitorización intermitente (I-IONM): Además de facilitar la identificación del NLI, se realizan pruebas sucesivas con una delgada sonda de estimulación (figura 8), para verificar la indemnidad del nervio y que las maniobras quirúrgicas como sección, ligadura o sellado de vasos no esté comprometiendo su conducción. Esto genera una onda en la gráfica del monitor acompañado de un sonido pulsátil, que evidencia en el momento la calidad de la conducción del nervio. Se pueden tomar y guardar imágenes de dicho registro en la memoria del equipo, lo cual también tiene relevancia desde el punto de vista medicolegal.
- -
Monitorización continua (C-IONM): En este método, se instala un electrodo siliconado en el nervio vago, comúnmente denominado por su forma como “saxofón”, (figura 9), que realiza una estimulación permanente a una periodicidad conocida que genera un registro basal continuo y un sonido pulsátil que ayuda al cirujano a detectar en tiempo real cualquier eventual pérdida o deterioro de la señal en cuanto a amplitud y latencia, y por ende de la calidad de la conducción nerviosa del NLI durante las maniobras quirúrgicas que se están realizando. Ante cualquier pérdida o atenuación de la señal, el cirujano debe detener la cirugía e identificar y corregir la acción o maniobra que lo está provocando. En varios estudios comparativos se evidencia un mejor rendimiento de la monitorización continua sobre la intermitente, en cuanto a los resultados funcionales inmediatos y alejados de la preservación de la función vocal39,40.
Figura 9.Esquema de monitorización continua del NLI.
Evidencias funcionales y dinámicas obtenidas mediante neuromonitorización intraoperatoria mejorando los estándares de la tiroidectomía. Permiso de reutilización bajo la licencia: CC BY-NC
Nurcihan Aygun.SiSli Etfal Hastanesi Tip Bulteni/The Medical Bulletin of Sisli Hospital 2021 Jul 2;55(2):146-155.
- -
- •
Nervio laríngeo superior (NLS): Este nervio, y específicamente su ramo externo, (RENLS), es el responsable de la inervación motora de los músculos cricotiroideos, cuya función es dar la tensión a la cuerda vocal correspondiente, que permite la emisión de los tonos altos de la voz (figura 10). Su trayecto está en la vecindad de los vasos del pedículo superior de la tiroides, haciendo un asa de concavidad superior que puede estar localizada a una altura bastante variable41. Esta referencia anatómica es importante al momento de la disección y sección de los vasos del pedículo superior, debiendo procurar no incluirlo en alguna ligadura o clampeo/sellado de vasos, la que debe realizarse por parcialidades para asegurar se preservación.
Para ello resulta también de utilidad el apoyo de la monitorización intraoperatoria39,40. En este caso se realiza estimulación directa en el tejido circundante a los vasos del pedículo superior durante el proceso de sección y sellado, permitiendo en algunos casos la visualización del RENLS o bien objetivando la contracción muscular producida en el músculo cricotiroideo.
Si bien, el objetivo principal de una tiroidectomía por cáncer de tiroides es la remoción completa del tumor, resulta a la vez fundamental asegurar la preservación de la voz del paciente. Por ello, y al igual que lo antes comentado en cuanto a la preservación funcional de las paratiroides, es que la tiroidectomía debe ser realizada por cirujanos entrenados y con un alto volumen de cirugías ya que el uso de tecnología no reemplaza a la experiencia y la meticulosa técnica quirúrgica.
Como se ha señalado antes, y tal como se reporta en las Guías ATA1 la aparición de complicaciones en el postoperatorio de una tiroidectomía se asocia fuertemente con la experiencia del equipo quirúrgico (tabla 3). Así se encuentran definidas distintas tasas de complicaciones post tiroidectomía comparando “cirujanos de alto volumen” (más de 50 tiroidectomías/año) comparados con cirujanos de volumen intermedio y bajo.
Consideraciones técnicas de lobectomía y tiroidectomías subtotalesSe entiende por lobectomía tiroidea, a la extirpación de uno de los lóbulos tiroideos, realizando la misma disección antes descrita para una tiroidectomía total, pero limitado a solo un lóbulo, realizando una transección a nivel del istmo de la tiroides, dejando el lóbulo contralateral indemne y sin manipulación. Como es de suponer, la principal ventaja comparativa es la disminución de la morbilidad quirúrgica, y de eventuales complicaciones al intervenir solo un lado de la glándula.
En contra de esta conducta está la posibilidad de dejar enfermedad persistente, a veces microscópica, en el lóbulo contralateral, ya que es sabido que el carcinoma papilar de tiroides puede presentar multifocalidad en un porcentaje de casos que se estima en sobre un 30% de los pacientes sometidos a tiroidectomía total por carcinoma papilar de bajo riesgo42. Esto muchas veces es inaparente al examen clínico, al estudio ecográfico preoperatorio o a la inspección intraoperatoria.
El impacto de esta condición en la sobrevida de los pacientes no se ha demostrado como significativa en especial en pacientes con tumores en estadios iniciales de la enfermedad. Sin embargo, sí se ha asociado a la multifocalidad con un mayor riesgo de recurrencia de la enfermedad42–44, lo que hace que en algunos casos se pueda recomendar la totalización de la tiroidectomía, principalmente de acuerdo con los hallazgos de la biopsia diferida de la lobectomía ya realizada, tales como:
- •
Tumor primario>4cm.
- •
Márgenes de resección comprometidos
- •
Variables histológicas de comportamiento biológico más agresivo
- •
Extensión extra tiroidea
- •
La presencia de invasión vascular o peri neural
- •
Metástasis linfáticas macroscópicas.
En dichas situaciones, es necesario reevaluar en Comité la eventual indicación de terapia complementaria con yodo radioactivo, para lo cual es recomendable la resección del lóbulo tiroideo remanente, para así aumentar el efecto sistémico de dicha terapia45. Otro factor para considerar es la necesidad de seguimiento con tiroglobulina, lo que requiere la ausencia de tejido tiroideo remanente.
Aun así, la totalización de una tiroidectomía no aumentaría las complicaciones ni empeoraría el pronóstico a largo plazo46,47. La lobectomía tiroidea constituye así una muy buena herramienta terapéutica en un grupo seleccionado de pacientes, tomando previamente en cuenta sus características individuales, la viabilidad del seguimiento a largo plazo, las características y etapa clínica de su patología, sus preferencias y la opinión al interior de un equipo multidisciplinario de profesionales, pudiendo obtener buenos resultados oncológicos, con menor morbilidad operatoria y con una mejor relación de costo-efectividad1,2,13,48–50.
Cirugía del cáncer papilar de tiroides con extensión extratiroidea (EET)Dependiendo del tamaño y especialmente de la ubicación del carcinoma, puede evidenciarse o al menos sospecharse el posible compromiso tumoral hacia estructuras adyacentes mediante el estudio ecográfico preoperatorio. Si el carcinoma se ubica hacia ventral, y está en íntimo contacto con la cápsula tiroidea, puede existir extensión tumoral hacia los tejidos blandos peri tiroideos, como tejido adiposo o músculos pretiroideos. En dicho caso, la resección quirúrgica debe procurar incluir la resección de estos tejidos en conjunto con la pieza de tiroidectomía. Si el tumor tiene una localización más dorsal (posterior) o muy cercano a la pared traqueal, puede producirse extensión tumoral hacia la pared esofágica, hacia la tráquea o comprometer el nervio laríngeo recurrente.
En ese caso una tomografía computada de cuello otorga una imagen más detallada del sitio y la extensión del compromiso tumoral, lo que ayuda a una mejor planificación de la cirugía. Esto debe correlacionarse con los hallazgos intraoperatorios del cirujano que deben quedar debidamente documentados en el protocolo operatorio.
De acuerdo con el tipo de tejido y a la cuantía de su compromiso, la “extensión extratiroidea” (EET) se puede clasificar en:
EET mínima o microscópica: existe compromiso de células neoplásicas en tejidos blandos peritiroideos (músculos o tejido adiposo). Este tipo de extensión extratiroidea se asocia a un riesgo intermedio de recurrencia que oscila entre un 3 y 9%. Sin embargo, no es un factor que se considere para modificar la etapificación según el American Joint Committee on Cancer (AJCC) en su 8° edición1,2,51,52.
EET extensa o macroscópica: existe compromiso neoplásico de esófago, pared traqueal o nervio laríngeo inferior. En este caso, se estima un aumento en el riesgo de recurrencia tumoral a un 23-40%, modificando la etapificación de la enfermedad y pudiendo alterar también la conducta terapéutica1,2,51.
La confirmación de este compromiso en la biopsia diferida constituye el gold standard para el diagnóstico de EET, constituyéndose en el factor más determinante en la estadificación de riesgo de recurrencia de la enfermedad, tomando también relevancia en la indicación de terapia complementaria con yodo radioactivo1,2,13,51,52.
Manejo de linfonodos cervicales en cáncer papilar de tiroidesEl cáncer diferenciado de tiroides, y en especial el carcinoma papilar, que es el tipo histológico más frecuente, puede desarrollar metástasis en los linfonodos cervicales y en etapas más avanzadas y con mayor tiempo de evolución, eventualmente también metástasis a distancia, la mayoría de las veces a pulmón.
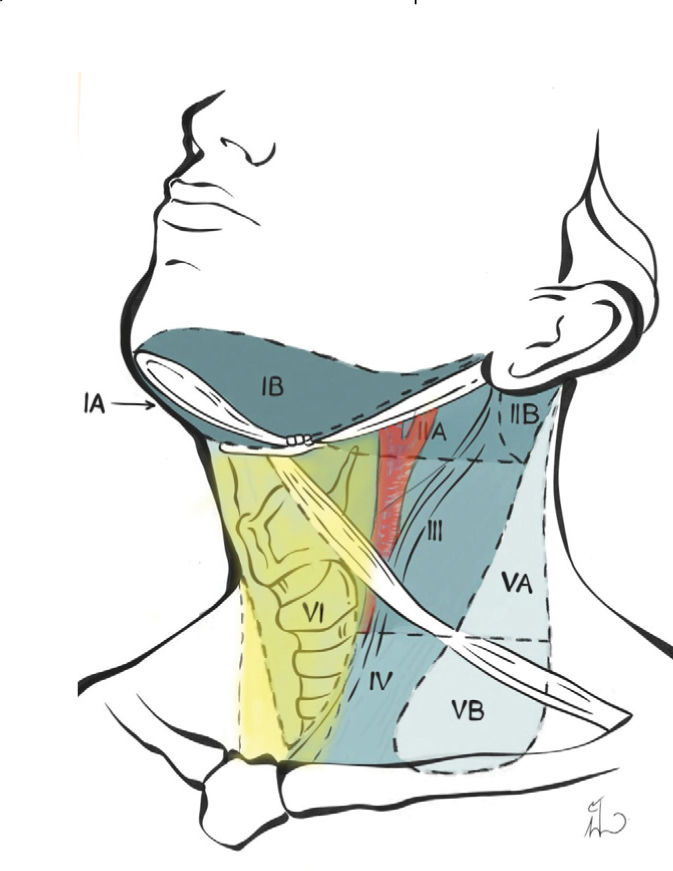
Los linfonodos cervicales siguen un patrón de drenaje conocido, lo que permite predecir en parte el posible origen de su compromiso por patología inflamatoria o neoplásica. Con fines de descripción clínica e imagenológica se les agrupa en seis niveles, permitiendo unificar criterios y nomenclatura53 (figura 11).
Es por ello que hoy, tal como se mencionó anteriormente, se recomienda realizar un estudio ecográfico dirigido; una ecografía de etapificación, hecha por radiólogos especializados y habituados a estudiar este segmento corporal. En dicha ecografía, el radiólogo realiza un barrido sistemático por los distintos niveles ganglionares, y consigna sus hallazgos en cuanto a presencia de linfonodos sospechosos, su número, ubicación, tamaño, forma, relación entre ejes, patrón de vascularización y relación con otras estructuras1,2,11–13,15.
El patrón de drenaje linfático de la glándula tiroides es relativamente predecible, siendo la primera escala de diseminación tumoral los linfonodos del compartimento central (figuras 11 y 12). Dicho compartimento está limitado entre ambas vainas carotideas por lateral, el borde inferior del hueso hioides por cefálico y el borde superior del manubrio esternal por caudal, compartimento conocido como Nivel VI de acuerdo a la Clasificación de la AHNS1,53. La disección de este compartimento, en gran parte ya queda hecha con la disección que se realiza para extirpar la glándula tiroides, debiendo poner énfasis en la extirpación de los linfonodos para traqueales y perirecurrenciales, así como del tejido en vecindad al lóbulo piramidal.
En algunos casos es necesario además vaciar el contenido del mediastino anterosuperior, (figura 13) dejando ampliamente expuesta la tráquea y la emergencia de los vasos braquiocefálicos. Este espacio es denominado compartimento del mediastino antero superior. (consignado aún en algunos textos como Nivel VII, aunque no aceptado en la nomenclatura oficial)
Si bien, en manos experimentadas el realizar la disección de este compartimento no conlleva una dificultad técnica mayor, y sólo prolonga escasamente la duración de la cirugía, el realizarlo puede ocasionar la afectación al menos parcial en la irrigación y en el drenaje venoso de las paratiroides, en especial de las inferiores, lo que se traduce en una mayor incidencia de hipoparatiroidismo postquirúrgico. Debido a ello, la conducta mayoritariamente recomendada hoy en día, es el realizar su disección sólo ante casos en que exista confirmación de compromiso ganglionar en dicho territorio, es decir una disección terapéutica1,2,54,55.
No obstante, algunos grupos realizan disección profiláctica de este compartimento. Esto avalado en la posibilidad de la existencia de enfermedad ganglionar microscópica que habitualmente es inaparente a la ecografía preoperatoria e incluso a la exploración intraoperatoria. Sin embargo, y dado que esta condición no se ha logrado asociar en una afectación de la sobrevida en estos pacientes, es que su indicación debe ser avalada por una sospecha alta de compromiso linfático o en aquellos tumores de alto riesgo de recurrencia, como T3 o superior, siempre con una discusión de cada caso en particular dentro de un comité conformado por un equipo multidisciplinario1,2,54,55.
Disección de compartimentos lateralesLa segunda escala de compromiso ganglionar en el cáncer papilar de tiroides, son los linfonodos del compartimento yugular, correspondientes a los niveles II (yugular superior), III (yugular medio) y IV (yugular inferior), cuyos límites anatómicos se grafican en la figura 11. A menos que el tumor primario se localice en los polos superiores de la glándula, en donde a veces puede encontrarse compromiso del nivel IIa, en la gran mayoría de los casos, los niveles más frecuentemente comprometidos con metástasis ganglionares a este nivel, son los niveles III y IV. El nivel V (triángulo posterior), al igual que el nivel IIb presentan una menor incidencia de metástasis en CPT, aunque pueden verse también comprometidos cuando existen metástasis múltiples en los demás niveles ganglionares1,2,56,57.
A diferencia de lo que ocurre en la porción más caudal del compartimento central, (mediastino anterosuperior), la ecografía de etapificación resulta de gran utilidad para definir la presencia de compromiso ganglionar en los niveles laterales del cuello, transformándose en una valiosa herramienta diagnóstica para una correcta planificación quirúrgica preoperatoria.
Técnica quirúrgica de disección linfáticaPara asegurar una disección completa de los distintos niveles ganglionares del cuello, es fundamental una correcta técnica quirúrgica, que permita la resección en bloque del tejido fibroadiposo y de los ganglios linfáticos que contiene, incluyendo las hojas superficial y media de la fascia cervical profunda, que recubren a los distintos grupos musculares y el paquete vasculonervioso del cuello, evitando resecciones parciales, o de muestreo, o con disrupción de tejidos, lo que puede determinar a futuro un mayor riesgo de persistencia o de recurrencia regional de la enfermedad. Si bien la mayoría de las veces sólo es necesario realizar la resección de los distintos niveles ganglionares, es decir, disecciones linfáticas selectivas, en aquellos casos en que la diseminación linfática es muy extensa o compromete estructuras no linfáticas, como la vena yugular interna, puede ser necesario la resección de ellas (disección radical modificada, explicitando las estructuras resecadas)1–3,53,56,57.
VÍAS DE ABORDAJE REMOTO PARA TIROIDECTOMÍA EN CÁNCER DE TIROIDESA pesar de que la tiroidectomía por abordaje cervical convencional sigue teniendo hoy en día altos niveles de eficacia y eficiencia del punto de vista costo-efectividad, con bajas tasas de complicaciones y excelentes resultados en cuanto al control oncológico locorregional del cáncer de tiroides, en las últimas dos décadas se han agregado otras vías de abordaje quirúrgico remoto o a distancia, tales como el abordaje transoral o el transaxilar. En todos los casos, se busca evitar la incisión y posterior cicatriz en la región anterior del cuello, que en otros países y culturas, especialmente de Asia, resulta un problema importante58.
Tiroidectomía transoral endoscópica vía vestibular: TOETVA(transoral endoscopic thyroidectomy vestibular approach)
Se trata de una técnica que se realiza bajo anestesia general, con un abordaje a través del vestíbulo de la cavidad oral, por donde se introduce una fibra óptica similar a la usada en laparoscopía, y de algunas pinzas de disección, realizando una disección de cefálico a caudal usando dispositivos de energía para disecar y sellar los vasos, seguido de la transección del istmo tiroideo, hasta lograr la extirpación del lóbulo tiroideo afectado60,61.
Acceso transaxilar:Se accede por el plano subcutáneo desde incisiones axilares disecando hacia la región anterolateral del cuello. Requiere incisiones en ambas axilas si se requiere realizar una tiroidectomía total62.
Acceso transmamario-axilar bilateral:
Acceso remoto combinado por vía axilar y periareolar bilateral62.
Acceso remoto tipo lifting:Se realiza un abordaje remoto a través de la región retroauricular del lado a intervenir.
En todas estas técnicas se pretende evitar el efecto cosmético que puede tener una cicatriz en el cuello. Sin embargo, para su ejecución, se requiere una larga curva de aprendizaje. En la mayoría de los casos se traduce en prolongar sustancialmente el tiempo operatorio y los costos asociados al uso de equipos e insumos. Por otro lado, es fundamental realizar una muy adecuada selección de aquellos pacientes que se puedan beneficiar de este tipo de abordajes, que deben ser realizados por equipos quirúrgicos con un alto volumen de cirugía tiroidea y familiarizados con este tipo de técnicas60–62.
Técnicas de ablación por radiofrecuenciaEl aumento sostenido en el diagnóstico de cáncer papilar de tiroides en muchos países del mundo, en parte originado en un mayor acceso a estudios diagnósticos como la ecotomografía, han redundado en un diagnóstico de lesiones cada vez de menor tamaño y circunscritas a la glándula. En esos casos donde se estima que la tiroidectomía total puede en muchos casos ser un tratamiento demasiado agresivo, es donde surgen conductas menos resectivas, tales como una lobectomía tiroidea o incluso la recomendación en muchos centros de una “vigilancia activa”, especialmente en aquellos casos de microcarcinomas (tumores de tamaño<1cm) y sin evidencia de diseminación linfática1,2,13.
Esa conducta, puede ser muy recomendable para pacientes de edad avanzada o que por diversos motivos no son candidatos a cirugía. Sin embargo, en otro grupo cada vez mayor de pacientes jóvenes, especialmente en nuestro medio, se hace muy complejo y difícil de implementar el mantener a un paciente con diagnóstico demostrado de un carcinoma en observación y estudio periódico de imágenes por un período muy prolongado. Es especialmente en ese grupo de pacientes donde la ablación por radiofrecuencia puede transformarse en un tratamiento eficaz, de muy bajo riesgo y con altas tasas de curación63,64.
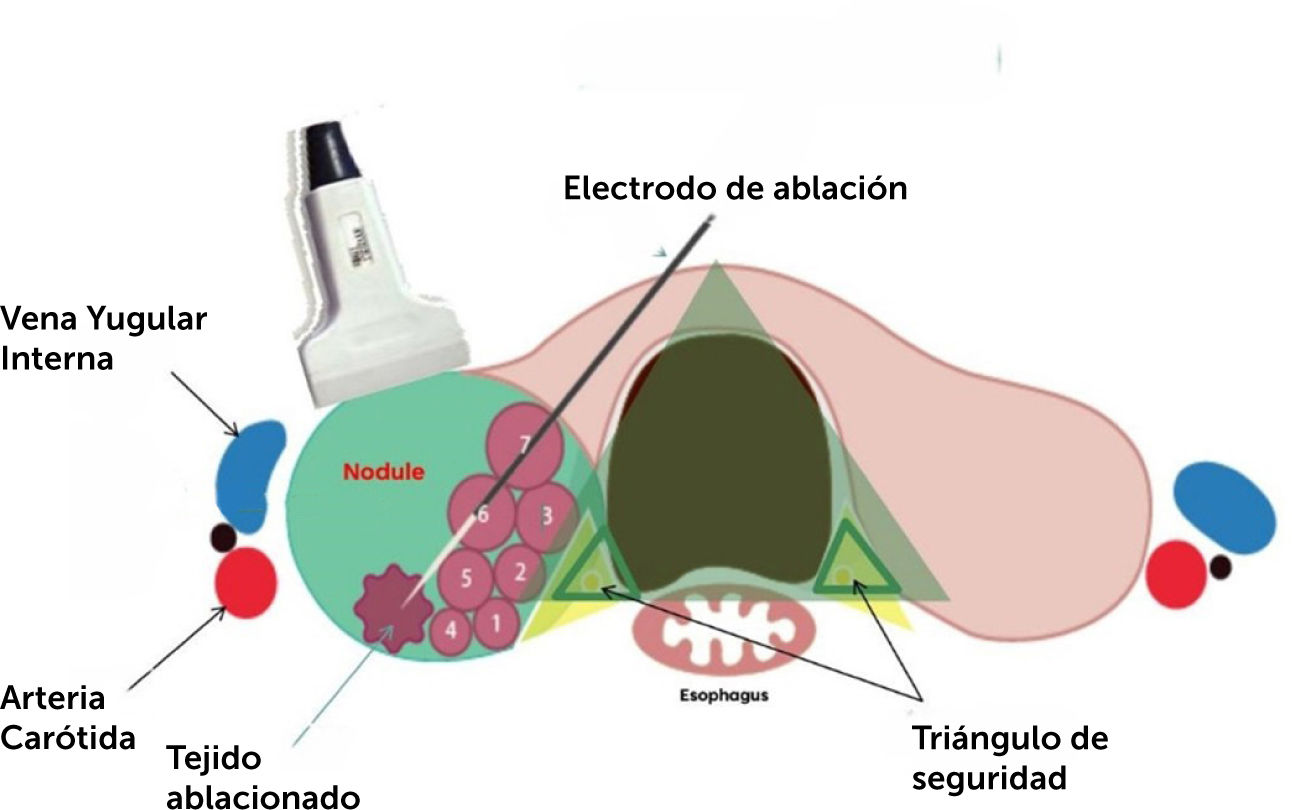
Esta técnica que partió hace ya varios años como alternativa terapéutica para pacientes portadores de nódulos benignos y nódulos de gran tamaño, ha demostrado ser eficaz en el manejo de un grupo seleccionado de pacientes con microcarcinoma de tiroides. En la ablación por radiofrecuencia se realiza una punción con aguja o electrodo guiado bajo ecografía del nódulo a tratar, y se administra energía de alta frecuencia desde una fuente de poder que produce la destrucción térmica del tejido en un área circunscrita y controlada (figura 14).
Las principales ventajas que ofrece esta técnica son el conservar la glándula tiroides y su función, no siendo necesario la administración de terapia hormonal de reemplazo con levotiroxina. Al mismo tiempo es un procedimiento que reduce aún más la morbilidad de la cirugía tradicional, por lo que habitualmente se realiza en forma ambulatoria y con un reintegro mucho más precoz a la actividad física y laboral habitual. Finalmente, y para muchos pacientes, algo no menos importante, es un procedimiento que no deja cicatrices visibles en el cuello63,64.
Esta técnica y las anteriormente mencionadas, se agregan a la cirugía tradicional de tiroidectomía total o parcial, y ofrecen hoy en día una más amplia gama de alternativas de tratamiento quirúrgico para los pacientes con diagnóstico de carcinoma papilar de tiroides, debiendo considerarse en su elección las características individuales del paciente, las características del tumor primario, su eventual extensión local y compromiso linfático cervical detectado en el estudio de etapificación pre quirúrgico, así como también la experiencia y preferencias del equipo médico multidisciplinario y del equipo quirúrgico tratante.
Conflictos de interésEl autor no declara ningún conflicto de interés.
Dra Karol Baksai (anatomopatóloga Clínica Las Condes) por imágenes de citología (figuras 2 y 3).
Dr. Alex Wash (radiólogo Clínica Las Condes) por colaboración con imagen de punción con aguja fina (figura 1).
Valeria Inzunza Navarro (licenciada en Artes, Universidad Católica de Chile) por colaboración en diseño de imágenes (figuras 6, 10, 11, 12 y 13).