El shock séptico continúa siendo una de las principales causas de mortalidad en las unidades de cuidados intensivos. Recientemente han surgido terapias de hemoadsorción como una herramienta adicional para abordar esta patología, contribuyendo a restablecer la homeostasis inmune del paciente. Sin embargo, aún existen dudas sobre la efectividad de estas intervenciones y es necesario mejorar el conocimiento sobre su aplicación en la práctica clínica.
ObjetivoEvaluar el impacto de la combinación de terapia hemoadsorptiva y hemofiltración de alto volumen en el tratamiento del shock séptico refractario en una cohorte no concurrente de pacientes, analizando parámetros clínicos y de laboratorio.
MétodosSe realizó una revisión no concurrente de pacientes ingresados en la unidad de cuidados intensivos con shock séptico refractario que recibieron terapia hemoadsorptiva asociado a hemofiltración de alto volumen (HFAV) durante un periodo de cinco años (2016-2020). Se analizaron variables clínicas, como la edad y género, puntajes APACHE II y SOFA, requerimientos de vasopresores y los parámetros de laboratorio, así como la mortalidad hospitalaria y la mortalidad a los 30 y 90 días. Se calcularon estadísticas descriptivas, y se compararon las variables pre y post terapia utilizando la prueba de Mann-Whitney.
ResultadosLa edad media de la cohorte fue de 54,57 años, y consistió en 14 pacientes. La terapia hemoadsorptiva se asoció con una reducción en los requerimientos de vasopresores, con un requerimiento inicial mediano de noradrenalina de 0,7μg/kg/min (RIC 0,45-0,8875) que disminuyó a 0,12μg/kg/min (RIC 0-0,225) después de la terapia. El requerimiento total normalizado de vasopresores a noradrenalina al inicio de la terapia fue de 0,8125μg/kg/min (RIC 0,56-1,08), y después de la terapia fue de 0,175μg/kg/min (RIC 0,01-0,29). El 100% recibió noradrenalina como agente vasopresor primario. Un 71,4% tuvo un tratamiento adicional con adrenalina, el 28,6% con vasopresina, y tan solo el 7,1% fue complementado con dobutamina.
Las puntuaciones APACHE II medianas pre y post terapia fueron de 30,5 y 20,5, respectivamente, mientras que las puntuaciones SOFA fueron de 13,5 y 11,5. Los niveles medios de lactato disminuyeron en un 60%, de 7,47 mmol/l pre-terapia a 2,97 mmol/l post terapia. Los parámetros inflamatorios, como la proteína C reactiva, disminuyeron de un promedio de 206mg/dL a 180mg/dl y la procalcitonina disminuyó de un promedio de 58 a 8,91 ng/ml. La mortalidad hospitalaria fue del 57%, aumentando a un 64% a los 90 días de seguimiento.
ConclusiónEn nuestra cohorte no concurrente de 14 pacientes, la terapia hemoadsorptiva combinado con hemofiltración de alto volumen demostró resultados alentadores en el tratamiento del shock séptico refractario, mejorando significativamente los outcomes intermedios como los requerimientos de vasopresores, niveles de lactato y parámetros inflamatorios. Sin embargo, nuestros resultados en outcomes duros, como la mortalidad, fueron similares a los reportados en casos de shock séptico refractario sin el uso de terapia hemoadsortiva. Estos datos publicados nos sirven como punto de partida para conformar una base de datos comparativa. Los resultados son prometedores y justifican la necesidad de estudios de cohorte más grandes para evaluar el impacto de la terapia hemoadsorptiva en la mortalidad a largo plazo y explorar su papel potencial como opción de tratamiento estándar para el shock séptico refractario.
Septic shock continues to be one of the main causes of mortality in intensive care units. Recently, hemoadsorption therapies have emerged as an additional tool to address this pathology, contributing to reestablishing the patient's immune homeostasis. However, there are still doubts about the effectiveness of these interventions and it is necessary to improve knowledge about their application in clinical practice.
ObjectiveAssess the impact of combined hemoadsorptive therapy and high-volume hemofiltration in the treatment of refractory septic shock in a non-concurrent patient cohort, analyzing clinical and laboratory parameters.
MethodsA non-concurrent review of patients admitted to the intensive care unit with refractory septic shock who received hemoadsorptive associated with high-volume hemofiltration therapy over a period of five years (2016-2020) was conducted. Clinical variables, including age and gender, APACHE II and SOFA scores, vasopressor requirements, laboratory parameters, as well as in-hospital mortality and mortality at 30 and 90 days, were analyzed. Descriptive statistics were calculated, and pre- and post-therapy variables were compared using the Mann-Whitney test.
ResultsThe mean age of the cohort was 54.57 years and consisted of 14 patients. Hemoadsorptive therapy was associated with a reduction in vasopressor requirements, with a median initial requirement of noradrenaline of 0.7μg/kg/min (IQR 0.45-0.8875) that decreased to 0.12μg/kg/min (IQR 0-0.225) after therapy. The total normalized vasopressor requirement to noradrenaline at the start of therapy was 0.8125μg/kg/min (IQR 0.56-1.08), and after therapy, it was 0.175μg/kg/min (IQR 0.01-0.29). All patients received norepinephrine as the primary vasopressor agent. 71.4% had additional treatment with adrenaline, 28.6% with vasopressin, and only 7.1% were supplemented with dobutamine.
The median APACHE II scores pre- and post-therapy were 30.5 and 20.5, respectively, while the SOFA scores were 13.5 and 11.5. Mean lactate levels decreased by 60%, from 7.47mmol/l pre-therapy to 2.97 mmol/l post-therapy. Inflammatory parameters, such as C-reactive protein, mean procalcitonin levels decreased from 206mg/dl to 180mg/dl, mean level of procalcitonin decreased from 58 to 8.91ng/ml. Hospital mortality was 57%, increasing to 64% at 90-day follow-up.
ConclusionIn our non-concurrent cohort of 14 patients, hemoadsorptive therapy combined with high-volume hemofiltration demonstrated encouraging results in the treatment of refractory septic shock, significantly improving intermediate outcomes such as vasopressor requirements, lactate levels, and inflammatory parameters. However, our results in hard outcomes, such as mortality, were similar to those reported in cases of refractory septic shock without the use of this therapy, which allows us to consider them as a historical control group. These results are promising and justify the need for larger cohort studies to evaluate the impact of hemoadsorptive therapy on long-term mortality and explore its potential role as a standard treatment option for refractory septic shock.
El shock séptico continúa siendo una de las principales causas de mortalidad en las unidades de cuidados intensivos (UCI), con tasas de mortalidad que oscilan entre el 30 y 40% según diversas series1. Esto se mantiene a pesar de los avances en el conocimiento y manejo de esta patología. La compleja interacción entre el huésped y el agente infeccioso, particularmente en lo que respecta a la producción desregulada de citoquinas, con niveles elevados de mediadores plasmáticos proinflamatorios (interleuquina (IL)-1β y factor de necrosis tumoral (TNF) α y antiinflamatorios (IL-6, IL-8, IL-10)2, contribuye a que ciertos pacientes (6-7%) presenten un shock séptico refractario, definido como un shock hiperdinámico persistente a pesar de una reanimación adecuada con líquidos y altas dosis de norepinefrina (a menudo ≥1μg/kg/min). La mortalidad puede superar el 90%3.
Hasta hace poco, las opciones terapéuticas para mitigar esta cascada de citoquinas eran limitadas, e incluían la hemofiltración de alto volumen HFAV4,5 y la administración de corticoides6,7. Sin embargo, en años recientes han surgido terapias de hemoadsorción como una herramienta adicional para abordar esta patología, contribuyendo a restablecer la homeostasis inmune8. Se han desarrollado también tratamientos dirigidos específicamente a la neutralización de citoquinas como IL-6 y IL-1, mediante anticuerpos monoclonales e inhibidores de sus receptores, que han mostrado potencial en el manejo del shock séptico9,10.
Los filtros de hemoadsorción utilizados en esta terapia se conectan al circuito extracorpóreo y contienen perlas absorbentes de polímero poroso biocompatible y hemocompatible en su interior. Estas perlas tienen una capacidad de unión extremadamente alta para moléculas de entre 5 a 60 kDa, como citoquinas, exotoxinas bacterianas, mioglobina, hemoglobina libre, bilirrubina, complemento activado, patrones moleculares asociados a daño y patógenos (DAMPs y PAMPs por sus siglas en inglés, respectivamente), así como otros agentes inflamatorios que pueden llevar al síndrome de respuesta inflamatoria sistémica (SIRS)11. Las moléculas susceptibles de ser removidas varían en su peso molecular y es relevante considerar que todas las moléculas estudiadas en este estudio; específicamente el lactato, proteína C reactiva (PCR) y procalcitonina, tienen pesos moleculares que no exceden los 23 kDa, siendo PCR la más grande de ellas. Por lo tanto, se debe tener en cuenta que la mejoría en las mediciones de estas moléculas podría estar influenciada no sólo por una reducción en su producción, sino también por su remoción directa a través de la terapia.
Por otro lado, la HFAV no solo tiene la capacidad de remover estas moléculas de bajo peso molecular. Se ha documentado que también contribuye a la reducción en los requerimientos de drogas vasoactivas, lo que resalta la importancia de considerar ambas terapias en conjunto cuando se analizan los resultados obtenidos en este estudio.
Debido a estas características, esta terapia ha ganado relevancia e interés en diferentes áreas de la medicina más allá de la UCI, como, por ejemplo, en el campo de la cirugía cardíaca. Esto ha llevado a la realización de diversos estudios, algunos ya publicados y otros en proceso de reclutamiento. Entre los estudios multicéntricos aleatorizados recientemente publicados se encuentran los estudios REMOVE12 y PACIFIC13. Estos estudios evidenciaron que la terapia de hemoadsorción podría ser efectiva en la prevención de la disfunción de órganos en pacientes con endocarditis infecciosa que requieren cirugía cardíaca y que, en casos de pancreatitis aguda, mejora los parámetros hemodinámicos, lo que sugiere su potencial como herramienta terapéutica.
Un estudio piloto aleatorizado controlado realizado por Monard et al., evaluó la eliminación de citoquinas en pacientes durante las primeras 24 horas después de sobrevivir un paro cardíaco durante las primeras 24 horas. El estudio encontró que la terapia de hemoadsorción es factible y segura, reduciendo los niveles de citoquinas en plasma, aunque sin alcanzar significación estadística. Este hallazgo abre un nuevo campo de investigación en esta área14.
Además de los estudios previamente mencionados, existen varios estudios observacionales15–17 y series de casos18 a nivel mundial que reportan resultados positivos en el uso de terapias hemoadsortivas en el tratamiento del shock séptico. Se ha observado una reducción del 50% en los requerimientos de drogas catecolaminérgicas dentro de las primeras 24 horas de su uso, así como una disminución en la mortalidad a los 28 días19, destacando la seguridad en la aplicación de estas terapias15.
El estudio realizado por Rathkamp et al en Chile, describe su experiencia en un número reducido de pacientes con shock séptico refractario en los que se aplicó terapia de hemoadsorción y se observó una reducción progresiva en las dosis de vasopresores, efecto que comenzó a las nueve horas de iniciada la terapia y se mantuvo hasta su retiro a las 26 horas20.
En este estudio, se analizó una cohorte no concurrente de pacientes tratados con terapias hemoadsortivas combinadas con HFAV en el contexto de shock séptico refractario, con el objetivo de evaluar la efectividad de estas intervenciones y mejorar el conocimiento sobre su aplicación en la práctica clínica.
2MetodologíaSe llevó a cabo un estudio de cohorte no concurrente retrospectivo observacional de pacientes hospitalizados en la UCI de una institución de salud privada, que recibieron tratamiento hemoadsortivo durante su hospitalización como parte de la terapia de un shock séptico durante el periodo de 5 años comprendido entre el 2016 y el 2020.
Se realizó un seguimiento de los pacientes por 90 días desde su ingreso a la UCI.
Dentro de los criterios utilizados para el inicio de terapia hemoadsortiva en los pacientes de nuestra cohorte se incluyen: persistencia de lactato mayor a 2,5 mmol/l a pesar de una adecuada reanimación con fluidos, requerimiento de vasopresores a dosis consideradas por el médico a cargo como altas o necesidad de inicio de un segundo vasopresor y uso de corticoides para mantener metas de presión arterial media (PAM) ≥ 65mmHg. Se excluyeron pacientes con enfermedades autoinmunitarias, neoplasias activas o aquellos que fallecieron antes de completar 12 horas de tratamiento.
La estadística descriptiva se calculó en relación con los datos clínicos de los pacientes durante el seguimiento, registrando edad, sexo, diagnóstico, requerimiento de vasoactivos, como también el comportamiento de puntajes predictivos APACHE II (Acute Physiology and Chronic Health Evaluation II) que evalúa severidad y SOFA (The Sequential Organ Failure Assessment) que predicen mortalidad en la UCI. Asimismo, se registraron los exámenes de laboratorio (PCR, procalcitonina, lactato entre otros) y mortalidad intrahospitalaria, a 30 y 90 días. Para valores continuos, se presentaron mediana y rango intercuartil, y para los discretos, frecuencia y valor relativo.
Para estandarizar las dosis de vasopresores, empleamos la calculadora de equivalencia de noradrenalina (NEE)21.
El análisis estadístico se llevó a cabo con pruebas de Wilcoxon para muestras pareadas, comparando el uso y la necesidad normalizada de noradrenalina pre y post terapia, así como el análisis de puntajes pronósticos. Todos los cálculos y análisis se efectuaron utilizando Microsoft Excel 365 (Microsoft, USA) complementado con XLSTAT 2023.1 (Addinsoft, Francia). Se adoptó un valor de p<0,05 como criterio para determinar significación estadística.
La información presentada en este estudio proviene de datos previamente recopilados y no se realizaron intervenciones específicas para este trabajo de investigación.
Todos los datos se presentan de forma agregada, y no es posible identificar a ningún paciente individualmente basándose en la información proporcionada.
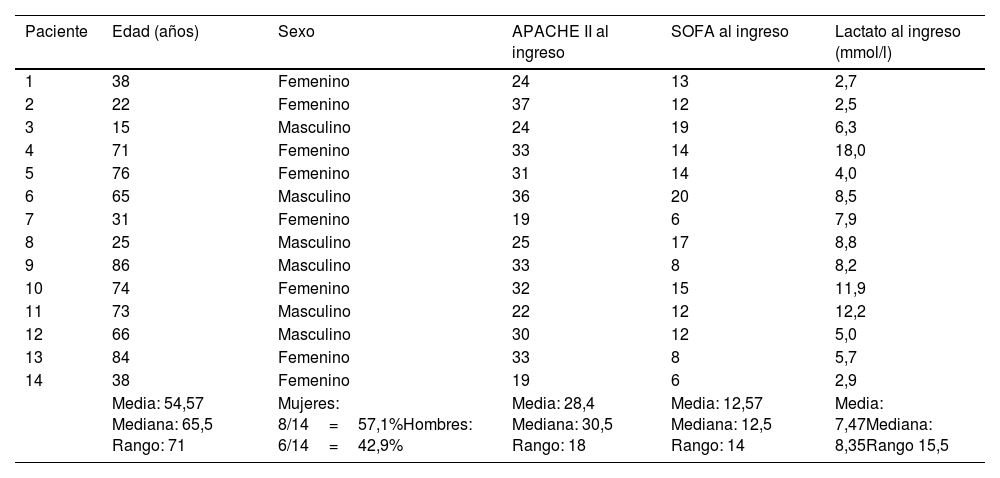
3ResultadosEn la tabla 1, se detalla la información clínica y demográfica de los 14 pacientes de la cohorte, de los cuales 8 eran mujeres. La mediana de edad fue de 65,5 años, con un rango intercuartil (RIC) de 32,75 a 73,75. Todos los pacientes recibieron terapia hemoadsortiva en conjunto con hemofiltración de alto volumen. Adicionalmente, en esta tabla se consignan los puntajes APACHE II y SOFA, con el propósito de reflejar la gravedad clínica de los pacientes previo a la terapia.
Característica clínicas y demográficas de los pacientes previo al inicio de la terapia
| Paciente | Edad (años) | Sexo | APACHE II al ingreso | SOFA al ingreso | Lactato al ingreso (mmol/l) |
|---|---|---|---|---|---|
| 1 | 38 | Femenino | 24 | 13 | 2,7 |
| 2 | 22 | Femenino | 37 | 12 | 2,5 |
| 3 | 15 | Masculino | 24 | 19 | 6,3 |
| 4 | 71 | Femenino | 33 | 14 | 18,0 |
| 5 | 76 | Femenino | 31 | 14 | 4,0 |
| 6 | 65 | Masculino | 36 | 20 | 8,5 |
| 7 | 31 | Femenino | 19 | 6 | 7,9 |
| 8 | 25 | Masculino | 25 | 17 | 8,8 |
| 9 | 86 | Masculino | 33 | 8 | 8,2 |
| 10 | 74 | Femenino | 32 | 15 | 11,9 |
| 11 | 73 | Masculino | 22 | 12 | 12,2 |
| 12 | 66 | Masculino | 30 | 12 | 5,0 |
| 13 | 84 | Femenino | 33 | 8 | 5,7 |
| 14 | 38 | Femenino | 19 | 6 | 2,9 |
| Media: 54,57 Mediana: 65,5 Rango: 71 | Mujeres: 8/14=57,1%Hombres: 6/14=42,9% | Media: 28,4 Mediana: 30,5 Rango: 18 | Media: 12,57 Mediana: 12,5 Rango: 14 | Media: 7,47Mediana: 8,35Rango 15,5 |
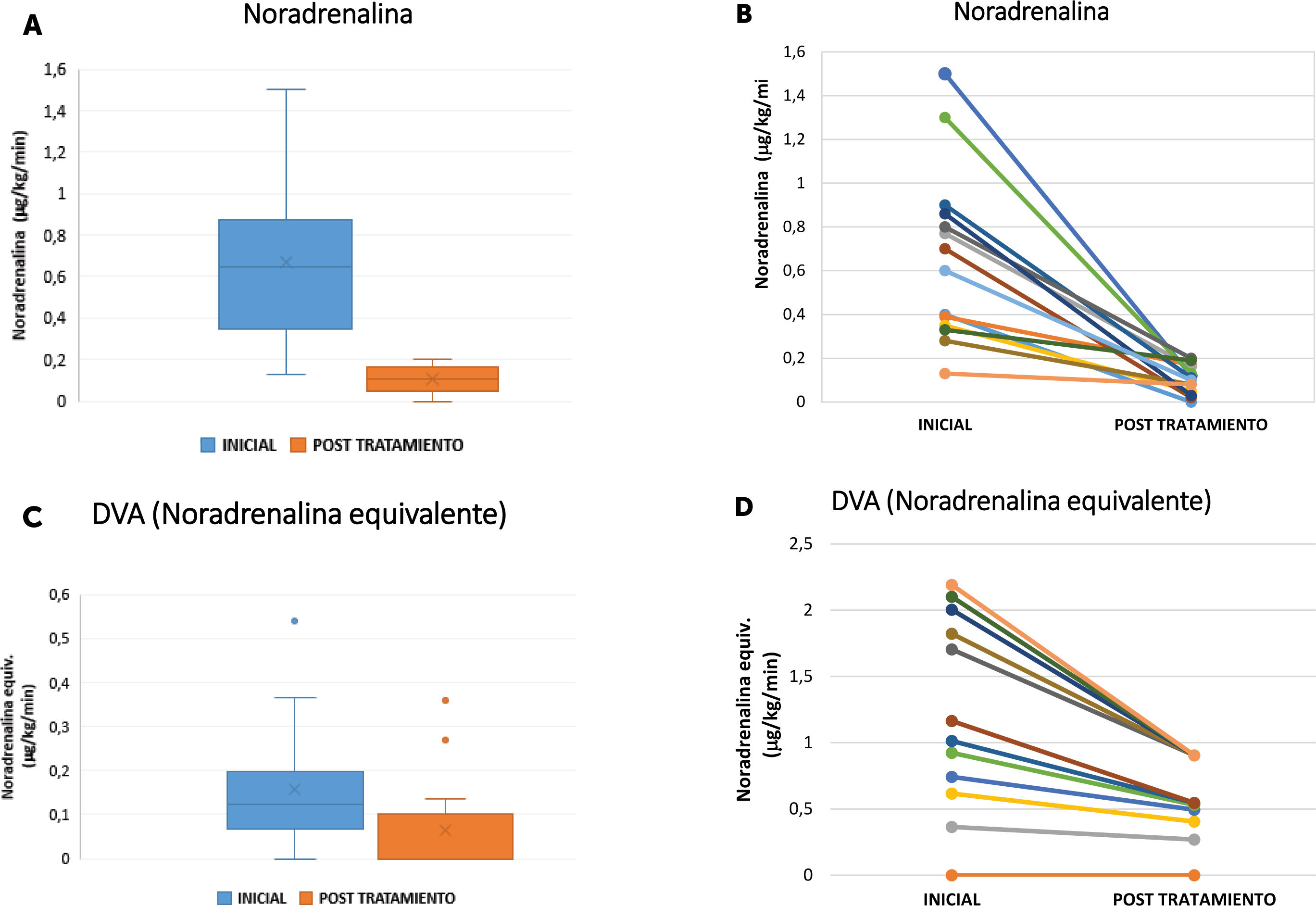
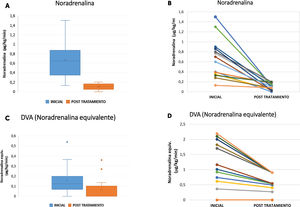
La mediana del requerimiento inicial de terapia vasoconstrictora con noradrenalina fue de 0,7μg/kg/min (RIC 0,45-0,8875), y después de la terapia, de 0,12 (RIC 0-0,225), con una diferencia significativa (p=0,001). La terapia vasoconstrictora total normalizada al inicio fue de 0,8125 (RIC 0,56-1,08) y después de la terapia, de 0,175 (RIC 0,01-0,29), diferencia significativa (p=0,001) (trayectorias individuales presentadas en la figura 1). De la cohorte compuesta por 14 pacientes, el 100% recibió noradrenalina como agente vasopresor primario. De ellos, solamente el 21,4% (3/14) recibió noradrenalina como único agente. Un 71,4% (10/14) tuvo un tratamiento adicional con adrenalina, el 28,6% (4/14) con vasopresina, y tan solo el 7,1% (1/14) fue complementado con dobutamina.
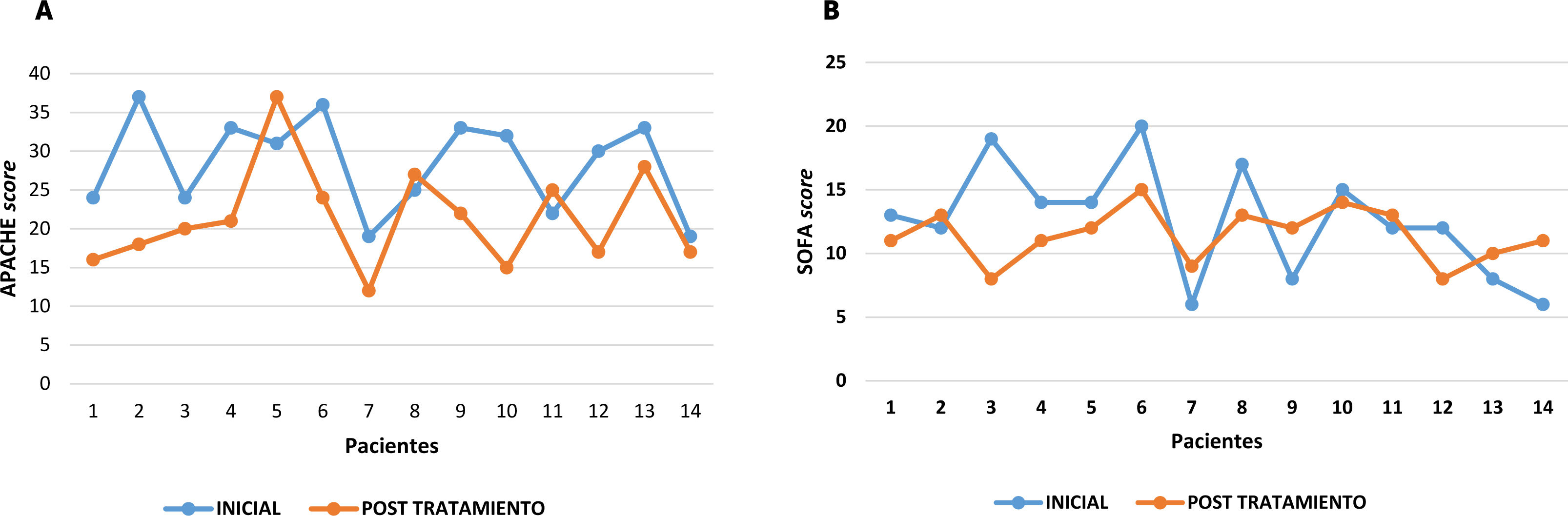
Antes de la terapia, la mediana del puntaje APACHE II era de 30,5, correspondiente a una mortalidad estimada del 75%. Tras la intervención, esta mediana disminuyó a 20,5, lo que representa una mortalidad estimada del 40%, con una diferencia significativa (p=0,012). En contraste, el puntaje SOFA que es una herramienta ampliamente reconocida para evaluar la función y fallo de múltiples sistemas, presentó una mediana preterapéutica de 13,5 que se redujo a 11,5 después de la terapia. Sin embargo, esta variación no fue estadísticamente significativa (p=0,124). Las evoluciones individuales de estos puntajes se ilustran en la figura 2.
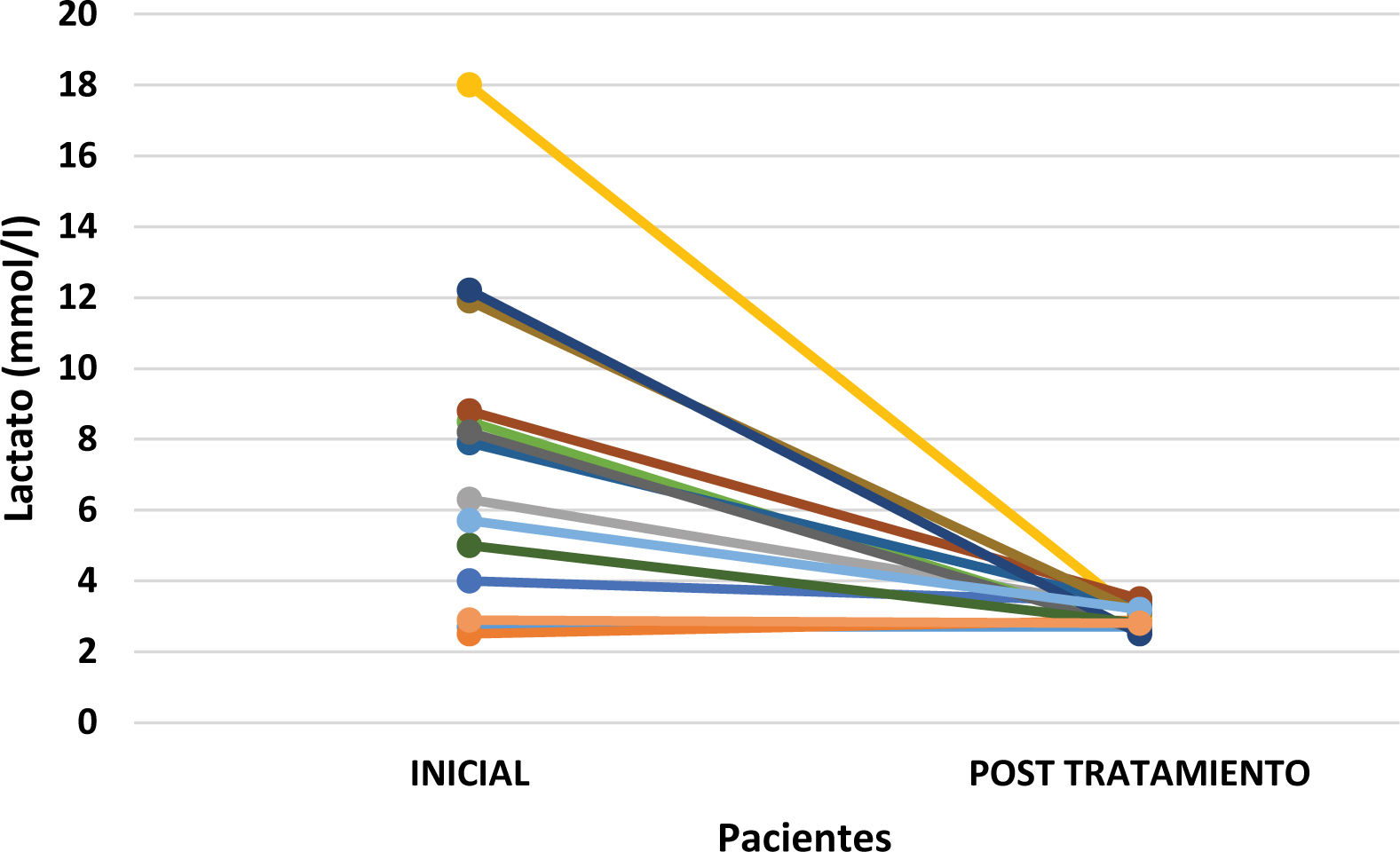
El análisis de parámetros de laboratorio mediante métodos enzimáticos, mostró una mediana de lactato preterapia de 7,47 mmol/l y post terapia de 2,97 mmol/l (valores normales; 0,5 a 2,2 mmol/l) con una disminución del 60%. Además, se observó una disminución en los parámetros inflamatorios, tanto en la PCR, que disminuyó desde un promedio de 206 a 180mg/dl (valores normales; < 10mg/dl), como en la procalcitonina (PCT), que disminuyó de un promedio de 58 a 8,91 ng/ml (valores normales < 0,1 ng/ml), lo que equivale a una reducción porcentual del 84,64%.
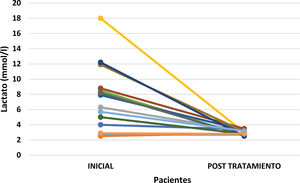
La figura 3 ilustra el cambio en los niveles individuales de lactato pre y post terapia.
Dentro del grupo de estudio, se observó que 8 de ellos no sobrevivieron a su período de hospitalización. Incluso, cuando se extendió el período de observación a un total de 90 días, un paciente adicional también falleció. En términos porcentuales, esto significa que el 64% de los pacientes del estudio fallecieron dentro de este período.
4DiscusiónLa terapia hemoadsortiva emerge como una valiosa estrategia en el tratamiento del shock séptico refractario. A lo largo de este artículo hemos referenciado múltiples investigaciones que sugieren que esta terapia, al disminuir las citoquinas circulantes, podría favorecer la mejora de la función orgánica. De esta manera, se propiciaría la restauración de la homeostasis inmune, lo que podría traducirse en una potencial reducción de la mortalidad.
Nuestros registros están en consonancia con estos hallazgos. Observamos una significativa reducción en la administración de drogas vasoactivas y una disminución en los indicadores de hipoperfusión, como el nivel de lactato. Estos datos sugieren una notable mejora en la evolución del shock séptico refractario, validando la terapia hemoadsortiva como un recurso terapéutico esencial en nuestro centro.
Uno de los cuestionamientos que emerge es si iniciar esta terapia antes de que los pacientes alcancen el estado de shock refractario alteraría sus resultados clínicos. Aunque tal interrogante excede los límites de nuestro estudio, plantea un interesante camino para futuras investigaciones.
Es importante mencionar que, más allá del shock séptico, la terapia ha mostrado resultados prometedores en áreas como la cirugía cardíaca y el paro cardio-respiratorio. Sin embargo, es esencial encarar estos descubrimientos con prudencia, dada la naturaleza preliminar de la literatura en estos subcampos.
En cuanto a las limitaciones de nuestra investigación, es importante señalar que el inicio de la terapia no se ajustó a un protocolo riguroso, sino que se basó en decisiones individuales, lo que podría sesgar los resultados. Distinguir la influencia exacta de la hemofiltración de alto volumen es, asimismo, un desafío.
Además, la exclusión de aquellos pacientes que fallecieron en las primeras 12 horas plantea otro punto, el grupo con intención de tratar. Este grupo, al ser excluido, introduce un sesgo de selección, cuya interpretación metodológica resulta compleja.
Habría sido enriquecedor analizar este grupo separadamente, para identificar posibles predictores de mortalidad a corto plazo y considerar la conveniencia de iniciar o no la terapia.
5ConclusiónEn nuestra cohorte retrospectiva de 14 pacientes, la terapia combinada de hemoadsorción y hemofiltración de alto volumen mostró resultados alentadores en el tratamiento del shock séptico refractario. Observamos una mejoría significativa en parámetros intermedios como los requerimientos de vasopresores, niveles de lactato y marcadores inflamatorios.
Sin embargo, la mortalidad fue similar a la reportada previamente en la literatura en casos de shock séptico refractario manejados sin hemoadsorción. Estos datos publicados nos sirven como punto de partida para conformar una base de datos comparativa.
Estos hallazgos son prometedores y resaltan la necesidad de realizar estudios de cohortes más grandes para evaluar rigurosamente el impacto de la terapia de hemoadsorción en resultados críticos como la mortalidad a largo plazo. Así se podría explorar su potencial papel como una opción de tratamiento estándar para el manejo de shock séptico refractario.
Se comparan dosis de noradrenalina previo al inicio de la terapia posterior al uso de la terapia, así como el uso de otras drogas vasoactivas (DVA) cuando se estandariza su uso a noradrenalina. En A se compara medianas de dosis de noradrenalina mediante el uso de gráfico de cajas, previo al inicio de la terapia y posterior a ella. En B se evalúa mediante el gráfico de muestras pareadas la trayectoria de las dosis de noradrenalina previo y posterior a la terapia En C se compara medianas de dosis de DVA normalizadas a noradrenalina mediante el uso de gráfico de cajas, previo al inicio de la terapia y posterior a ella. En D se evalúa mediante el gráfico de muestras pareadas la trayectoria de las dosis de DVA normalizadas a noradrenalina previo y posterior a la terapia.
Se ha empleado un gráfico de muestras pareadas diseñado específicamente para evaluar las fluctuaciones en los niveles de lactato. Este gráfico ha sido concebido para proporcionar una visualización de los niveles de lactato previos a la intervención terapéutica y después de haber aplicado el tratamiento. La naturaleza comparativa de este método gráfico facilita la identificación de alteraciones significativas en dichos niveles.
Se evalúa mediante el gráfico de muestras pareadas la variación de los scores de severidad utilizado en este estudio observacional. En la sección A del gráfico, se exponen los valores correspondientes al puntaje de APACHE antes y después de la intervención terapéutica. Por otro lado, en la sección B, se despliegan los valores relacionados con el puntaje SOFA, tanto previos como posteriores a la terapia.
Consideraciones éticasEl diseño y la metodología del estudio han sido revisados y aprobados por el comité de ética correspondiente.
Declaración de conflictos de interesesLos autores declaran no tener conflictos de intereses.
Referencia no citada[12].