El campo de la cirugía fetal es de reciente comienzo y rápida evolución. Con el avance en las herramientas de diagnóstico antenatal, la capacidad de diagnóstico de condiciones fetales susceptibles de ser tratadas in utero ha dado paso a una serie de procedimientos destinados a dar solución a situaciones que, de no ser por estas intervenciones, terminarían en un resultado adverso perinatal. Las técnicas descritas para la terapia fetal incluyen procedimientos percutáneos guiados por ultrasonido, cirugía fetal abierta y cirugía mínimamente invasiva. En este artículo se presentan las diversas condiciones fetales tributarias de cirugía fetal y se discuten las opciones terapéuticas actuales para cada una.
The field of fetal surgery has recently emerged and evolved with incredible speed. With the antenatal diagnostic tools breakthrough, our ability to diagnose treatable fetal conditions in utero has given birth to a wide variety of procedures that have made possible the survival of situations that otherwise would end in adverse perinatal outcome. Ultrasound guided percutaneous procedures, open fetal surgery and minimally invasive surgery are some of the techniques used for this purpose. In this article we present fetal diseases treatable by fetal therapy and the therapeutical options discussed for each case.
La capacidad de observar, diagnosticar y tratar al feto es una disciplina de reciente desarrollo. El concepto de cirugía fetal, de realizar procedimientos invasivos en la madre y en el feto, evolucionó rápidamente desde la década de los 60 gracias a la utilización de nuevas herramientas que han permitido pesquisar diversas condiciones fetales. En la mayoría de los casos estas condiciones pueden esperar para recibir tratamiento oportuno luego del nacimiento. Sin embargo, existen situaciones en las que la condición fetal se deteriora progresivamente y la latencia en la instalación de terapia puede culminar en un resultado adverso. De esta manera la terapia fetal surge como una respuesta lógica al avance del área del diagnóstico antenatal. Previo a la era del ultrasonido las intervenciones fueron realizadas con técnicas percutáneas a ciegas, como la primera transfusión intrauterina realizada por Lileyen 1961 o con útero abierto, como las exanguíneo transfusiones realizadas por Adamson en 1966 (1). No obstante, estas intervenciones fueron abandonadas debido a resultados poco consistentes. Con el posterior advenimiento de la ultrasonografía se abrió la posibilidad de realizar procedimientos guiados por ecografía y de esta forma, abarcar una amplia gama de terapias para diversas condiciones fetales. En 1982 se realizó la primera cirugía fetal abierta a cargo del Dr. Harrison a un feto con hidroureteronefrosis bilateral, lo que se resolvió creando una vesicostomía (2). En la década de los 90 se concretó la idea de cirugía fetal mínimamente invasiva, gracias a la explosión del mercado de la cirugía laparoscópica y al desarrollo de endoscopios de mejor calidad y pequeño calibre.
Los criterios para la aplicación de las intervenciones fetales fueron creados en 1982 por Harrison y se encuentran actualmente vigentes (3). En la tabla 1 se muestran los criterios que se deben cumplir para realizar una cirugía fetal.
Criterios para la realización de cirugía fetal
| Diagnóstico preciso con exclusión de anomalías asociadas |
| La historia natural de la enfermedad está bien documentada y pronóstico establecido |
| Ausencia de terapia postnatal efectiva actual |
| El procedimiento in utero ha sido mostrado en modelos animales, con la demostración de la reversión de los efectos deletéreos de la condición |
| El procedimiento debe ser realizado en centros de terapia fetal multidisciplinarios con protocolos estrictos y consentimiento informado de los padres |
Actualmente existen múltiples condiciones que son tributarias de terapia fetal, las que pueden ser tratadas de forma percutánea, endoscópica o abierta, dependiendo de la condición específica (tabla 2). A continuación se detallará cada una de estas patologías y su manejo.
Patolo gías fetales tributarias de terapia fetal
| Lesiones intratorácicas con compresión mediastínica |
| Hernia diafragmática congénita |
| Estenosis aórtica crítica |
| Mielomeningocele |
| Obstrucción urinaria baja |
| Transfusión intravascular intrauterina para el tratamiento de anemia fetal |
| Síndrome de transfusión feto-fetal |
| Secuencia TRAP |
Las lesiones pulmonares incluyen, principalmente, las malformaciones adenomatosas quísticas, secuestros broncopulmonares o el derrame pleural aislado.
La Malformación Adenomatosa Quística (MAQ) es una lesión benigna sólido-quística, generalmente restringida a un lóbulo del pulmón. En su interior se pueden observar quistes de diversos tamaños. Histológicamente se caracteriza por un sobrecrecimiento de los bronquiolos respiratorios terminales. Su irrigación proviene del sistema pulmonar y están conectados al árbol traqueobronquial. Por otro lado, el secuestro pulmonar es una masa de tejido pulmonar no funcionante. No tiene conexión con el árbol bronquial y su nutrición proviene directamente de la aorta. Estas lesiones en general tienen un pronóstico favorable con regresión espontánea parcial o total durante la gestación. El punto de máximo crecimiento se sitúa alrededor de las 28 semanas y posteriormente tienden a disminuir de tamaño (4). En algunos casos el crecimiento de estas lesiones persiste y produce complicaciones al feto en desarrollo. La afectación fetal se genera ya sea por compresión directa del mediastino o por la producción de derrame pleural, con la consecuente producción de hidrops fetal y/o polihidroamnios.
La terapia de primera línea en el tratamiento de estas condiciones es el uso de corticoides (especialmente en las MAQ) (5,6), los que han mostrado una reducción en el tamaño de las lesiones con mejoría del hidrops. La indicación de intervención fetal está dada en fetos con hidrops secundario que no responden a la terapia corticoisteroidal. El procedimiento que se plantea depende del tipo de lesión. En lesiones predominantemente quísticas la colocación de comunicaciones toracoamnióticas o shunt toracoamniótico han reportado una sobrevida de 70%. En el caso de lesiones sólidas o microquísticas la alternativa de cirugía fetal abierta muestra resultados con sobrevida de 50% (1,7). En estos casos últimamente también se ha planteado, en los secuestros pulmonares, la posibilidad de usar agentes esclerosantes o coagulación del vaso nutricio por vía percutánea para producir disminución del tamaño de la lesión (8). En casos de embarazos sobre las 32 semanas, se puede considerar de forma excepcional la realización de una toracotomía fetal mientras el feto está conectado a circulación placentaria, lo que se denomina EXIT (7).
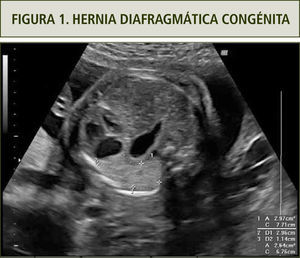
Hernia diafragmática congénita (HDC)Es la condición probablemente más estudiada dentro del ámbito de la cirugía fetal. Se trata de una solución de continuidad en el diafragma, a través de la cual ascienden órganos abdominales a la cavidad torácica, con una incidencia de 1 en 3.000 a 1 en 5.000 recién nacidos vivos (9). El problema de la hernia diafragmática radica en la hipoplasia pulmonar fetal por la compresión de las vísceras que ascienden a través del diafragma. El 40% de las HDC se asocian a cromosomopatías (Trisomía 18 y 13), otras alteraciones estructurales (espina bífida y malformaciones cardíacas) o a síndromes genéticos (9).
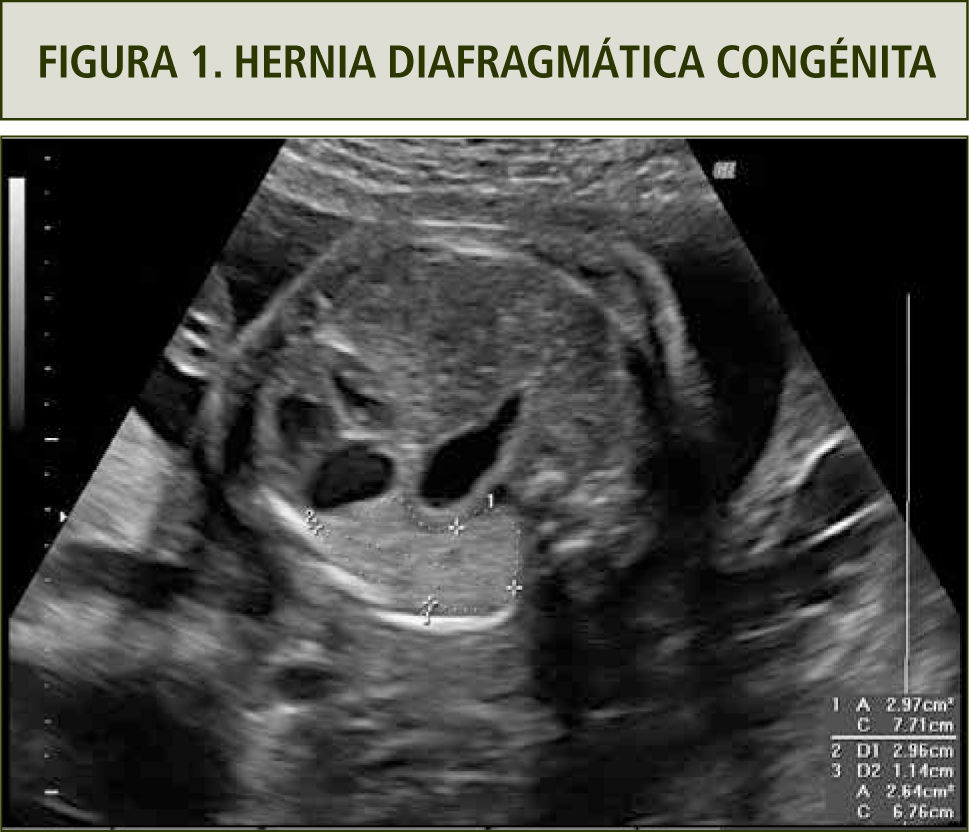
El diagnóstico de la hernia diafragmática se basa en la visualización de órganos abdominales en el tórax, los que a su vez desplazan al corazón. La ubicación más frecuente del defecto diafragmático es hacia el lado izquierdo (90%). Es, por ende, característico ver el corazón en dextro posición y el estómago más asas intestinales en hemitórax izquierdo en un corte de cuatro cámaras (figura 1). El diagnóstico de la HDC derecha es más difícil por la ecogenicidad similar del hígado con el pulmón. La HDC derecha se asocia en un 50% con la presencia del hígado en el tórax. La resonancia nuclear permite precisar si hay ascenso del hígado y también permite calcular el volumen pulmonar residual.
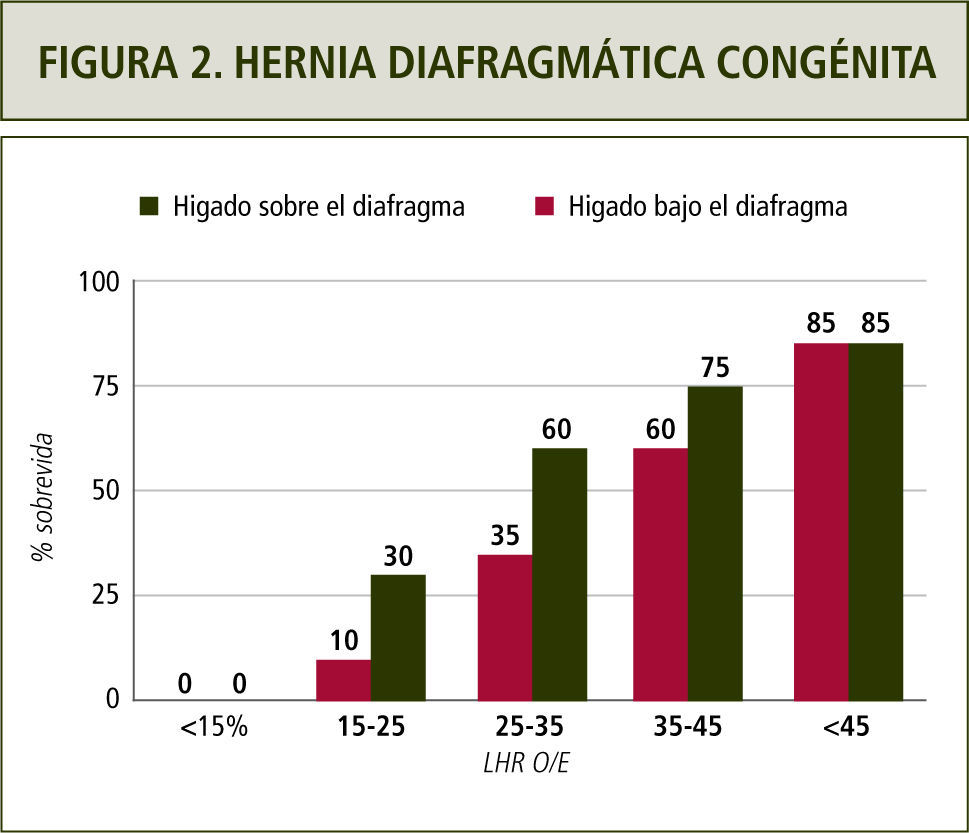
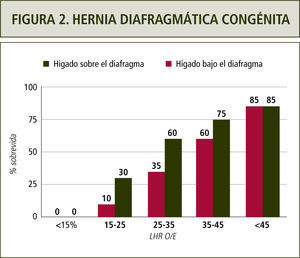
El pronóstico de esta condición se establece mediante un índice que relaciona la circunferencia craneana con el área de pulmón residual contralateral. El LHR o Lung to Head Ratio es la razón entre ambas estructuras. Inicialmente se utilizaban valores absolutos para designar un pronóstico con respecto a la sobrevida fetal. Actualmente, esta razón se correlaciona con la esperada para la edad gestacional y sumado a la presencia o ausencia de hígado en el tórax se establece el pronóstico de sobrevida fetal y, consecuentemente, la necesidad de terapia fetal (1,9). En la figura 2 se muestra la sobrevida en relación a la razón LHR y a la situación del hígado fetal.
La terapia fetal por cirugía abierta fue abandonada por morbilidad excesiva y por el desarrollo de centros neonatales de alta complejidad, que permitieron mejorara la sobrevida de estos pacientes previo a la corrección definitiva postnatal. En los 90 se redescubrió un fenómeno que permitió plantear un abordaje mínimamente invasivo en esta condición. La oclusión traqueal produce una acumulación de fluido pulmonar en los espacios alveolares y lleva a la expansión pulmonar. Este hecho fue utilizado por investigadores para proponer un abordaje fetoscópico que consideraba ocluir la traquea con la intención de producir expansión pulmonar y evitar la hipoplasia pulmonar. La estrategia PLUG (Plug the Lung Until it Grows: ocluir el pulmón hasta que crezca) proponía la oclusión traqueal durante un período crítico del desarrollo pulmonar fetal. De las técnicas propuestas la oclusión traqueal con balón mediente fetoscopía ha sido la más utilizada.
La colocación de balón intratraqueal endoscópico se realiza entre las 25 a 30 semanas de gestación y se retira en otro procedimiento en la semana 34 a 35. La indicación de realización del procedimiento se basa en el pronóstico de sobrevida, calculado por la razón LHR asociada a la presencia o ausencia de hígado en tórax descrita previamente. Cuando la sobrevida esperada es de menos de 60% la terapia fetal tiene indicación. Los resultados descritos por el grupo europeo FETO destacan un aumento en la sobrevida de 24 a 49% en las HDC izquierdas y de 0 a 35% en las HDC derechas (10).
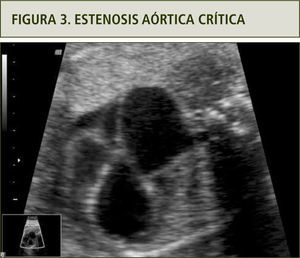
Estenosis aórtica críticaEsta malformación tiene una incidencia de 0.04 por 1.000 recién nacidos vivos. Esta patología puede llevar a la detención del crecimiento del ventrículo izquierdo, válvula aórtica y aorta ascendente, culminando en un síndrome de corazón izquierdo hipoplásico. Dependiendo del grado de severidad de la obstrucción valvular, la alteración hemodinámica asociada provoca una sobrecarga del ventrículo izquierdo y dilatación. Además produce de isquemia subendocárdica con deterioro de la función cardíaca y es responsable de la fibroelastosis subendocárdica, característica de esta lesión (11).
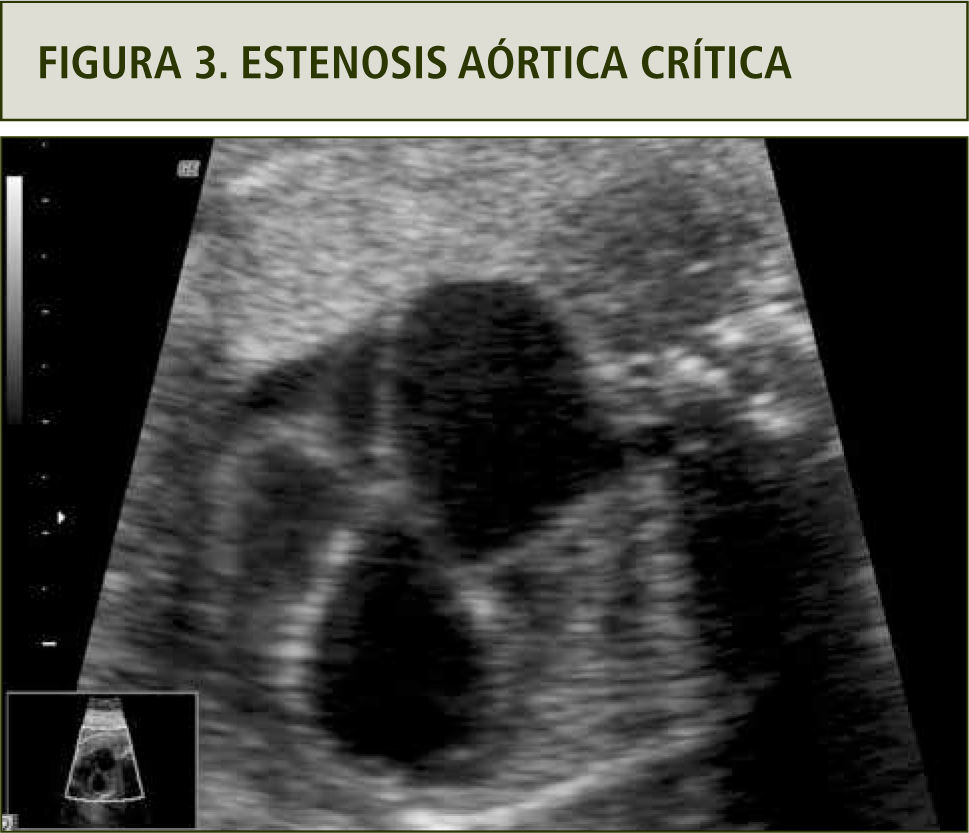
En el examen ecocardiográfico se puede observar un ventrículo izquierdo dilatado, de paredes gruesas, endocardio ecorrefringente, arteria aorta disminuida de diámetro con velocidades aumentadas y flujo turbulento, asociado a insuficiencia mitral y flujo reverso por el foramen oval (figura 3).
El propósito de la dilatación mediante valvuloplastía prenatal es mejorar la hemodinamia fetal, lo que permitirá el correcto desarrollo de las
estructuras de tal manera que se logre una circulación biventricular en la etapa postnatal. Los dos centros con mayor experiencia en dilatación aórtica percutánea (Boston, Estados Unidos y Linz, Austria) reportan éxito del procedimiento entre 66 y 74%, circulación biventricular entre 32 y 66% con muerte fetal entre 7 y 12% (11,12).
MielomeningoceleMielomeningocele es una anomalía congénita del sistema nervioso central para la cual no existe cura y cuyas consecuencias implican una morbilidad significativa y secuelas permanentes. Se trata de una protrusión de las meninges y elementos neurales, a través de una apertura de los arcos vertrebrales. Además, los fetos con este defecto desarrollan la malformación de Arnold Chiari tipo 2, que consiste en el desplazamiento caudal de las estructuras de la fosa posterior a través del foramen magnum, lo que lleva a una alteración en la circulación del líquido cefalorraquídeo y a la aparición de hidrocefalia que requiere la colocación de drenajes en el 80 a 90% de los casos. Si bien la etiología del mielomeningocele no está completamente dilucidada, la falla primaria de cierre del neuroporo inferior resulta en la exposición del tejido de la médula espinal al ambiente intrauterino. Sin la protección adecuada ocurre la destrucción del tejido neural mediada por trauma o por el líquido amniótico (13,14).
La racional detrás de la cirugía fetal en el mielomeningocele se basa en la teoría de los dos golpes. El primero, el desarrollo anormal que permite la exposición del tejido neural y el segundo, el daño producido por el trauma y líquido amniótico. La cirugía pretende reducir el daño causado por el segundo golpe, es decir, evitar la exposición del tejido a los elementos nocivos del ambiente intrauterino (figura 4).
La primera experiencia de reparación de mielomeningocele fue reportada en 1998 en el Hospital de Niños de Filadelfia, con buen resultado en la función neurológica (15). El año siguiente se realizaron 10 correcciones de MMC entre las 22 y 25 semanas, nueve de las cuales permanecieron por un promedio de 10 semanas luego del procedimiento. Seis de los casos tuvieron función motora mejor de lo esperado y sólo cuatro requirieron derivación ventriculoperitoneal (16). En 2011 se publicó un estudio multicéntrico randomizado de 153 pacientes que comparó los resultados de la corrección de MMC por cirugía fetal entre las 19 y 25 semanas versus manejo conservador. El estudio mostró una reducción significativa de la necesidad de drenajes por hidrocefalia de 82% en el grupo control a 40% en el grupo tratado. Además evidenció una importante mejoría en la función motora, con un 42% de independencia para caminar en el grupo tratado versus un 21% en grupo control. Por otro lado, también se pudo observar un aumento de complicaciones en el grupo tratado, como rotura prematura de membranas (46 vs 8%), parto prematuro (79 vs 15%) (13).
A pesar de los resultados positivos aportados por el estudio multicéntrico randomizado, la decisión de la reparación antenatal debe considerar las posibles complicaciones del procedimiento y debe ser indicado en casos en los que la reparación tendrá un impacto importante en la función motora postnatal. El desarrollo de técnicas mínimamente invasivas para la reparación de esta patología promete ser la solución a las complicaciones de la cirugía abierta, mejorando los resultados para la madre y el feto.
Obstrucción urinaria bajaLas malformaciones del tracto urinario son bastante frecuentes, afectando a 1 en 500 fetos. Las anomalías obstructivas dan cuenta de la mayoría de los casos. La obstrucción puede ocurrir a diferentes niveles y puede ser uni o bilateral. Cuando la obstrucción es bilateral o uretral, el pronóstico es sombrío debido a dos aspectos. Por un lado, la patología obstructiva produce daño renal progresivo e insuficiencia renal secundaria; y por otro, la disminución en la producción de orina repercute en el volumen de líquido amniótico, generando un oligohidramnios secundario e hipoplasia pulmonar. La mortalidad perinatal se estima en un 90%, y los sobrevivientes presentan un riesgo de 50% de requerir diálisis por daño renal (17).
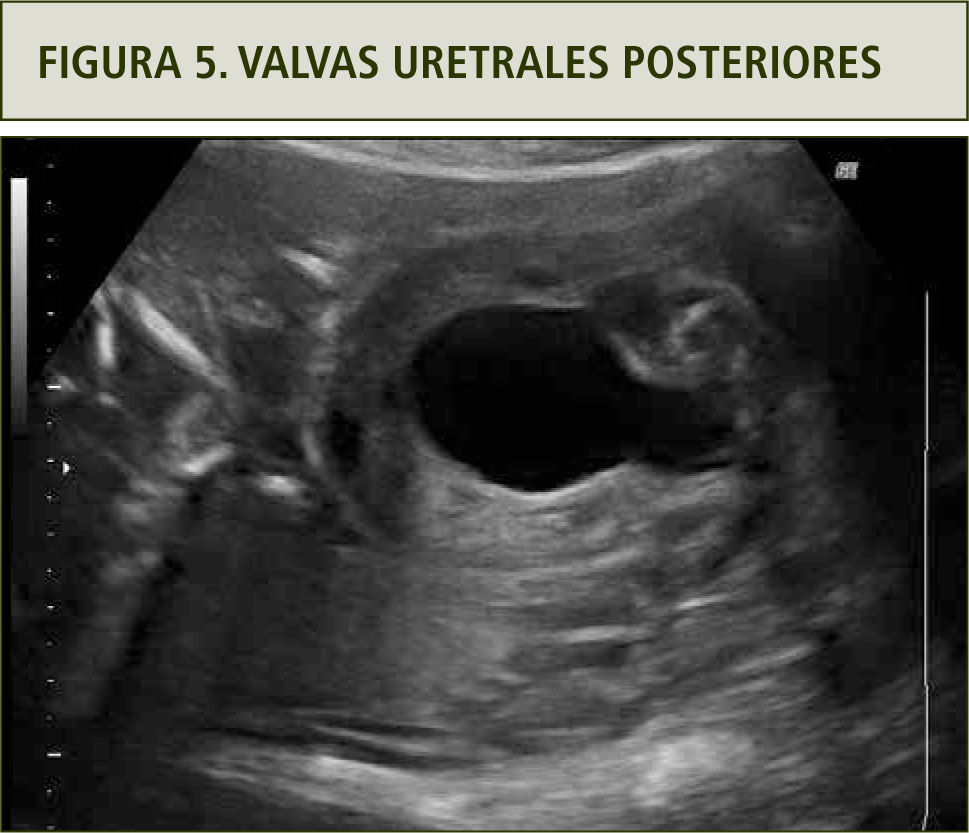
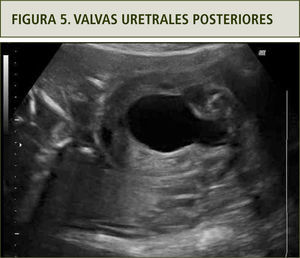
Si bien la obstrucción urinaria baja fetal puede ocurrir por diferentes causas, la más frecuente corresponde a valvas uretrales posteriores cuya frecuencia es de 1–2 por 10.000 recién nacidos y es más frecuente en fetos masculinos. El grado de severidad es variable y puede ser parcial o total, asociado a ascitis en algunos casos. El diagnóstico se efectúa por la identificación ultrasonográfica de una megavejiga a comienzos del 2o trimestre con el característico signo de la cerradura (figura 5) (17).
La terapia pretende restaurar la continuidad del tracto urinario previniendo las complicaciones renales y pulmonares. Los criterios de selección de los candidatos a terapia fetal deben considerar un examen de orina, que no muestre alteración de la función renal, oligoamnios, ausencia de otras anomalías y un cariotipo normal.
La vesicocentesis con aspiración de orina en estos casos, permite el estudio de la orina para pruebas de función renal y solucionar temporalmente la megavejiga. Sin embargo, como tratamiento definitivo requiere de punciones repetidas, lo que lleva a un aumento del riesgo de producción de infecciones, ruptura de membranas, aborto y parto prematuro. Por lo tanto, esta intervención sólo es útil durante el período de estudio de esta patología.
La terapia actualmente planteada para estos casos es la comunicación o shunt vesicoamniótico y la cistoscopía con ablación láser de la valva uretral posterior. La colocación de un shuntvesicoamniótico corresponde a la alternativa más usada para corregir esta patología y consiste en la colocación de un catéter doble J por vía percutánea, comunicando la vejiga con la cavidad amniótica. Esta técnica ha sido usada por más de 25 años y existen más de 300 casos reportados en la literatura. Los resultados muestran una sobrevida de aproximadamente 40% con un 50% de los sobrevivientes con daño renal (18). Complicaciones relacionadas con este procedimiento son la migración del catéter en un 20% y bloqueo del catéter en un 25% (17).
La cistoscopía fetal fue introducida en 1995 por Quintero y permite una observación directa de la vejiga posterior con mejor identificación de la causa, corrección anatómica y drenaje fisiológico (19). El procedimiento se realiza mediante la inserción del cistoscopio a través de la vejiga fetal bajo visión ecográfica, visualización de la uretra posterior y ablación con láser de las valvas. Existen menos de 40 casos reportados en la literatura. Los resultados muestran una sobrevida fetal de 75% con daño renal menor en comparación al shunt vesicoamniótico (17,20). Complicaciones descritas con esta técnica son escasas sin embargo, la experiencia acumulada no permite analizar este punto. Se considera que si bien esta técnica presenta resultados alentadores para el manejo de esta condición, la experiencia es todavía escasa para considerarla superior al manejo tradicional con vesicostomía percutánea.
Transfusión intrauterina intravascularDurante los años 70, el estado hematológico fetal sólo podía ser evaluado indirectamente a través de la bilirrubina en líquido amniótico. En 1973 Valenti describió el uso de una aguja 23-G, introducida a través de un laparoamnioscopio que punciona bajo visión directa, vasos de la placa coriónica, esto se conoció como la fetoscopía. Desafortunadamente su tasa de mortalidad de un 5% limitó su aplicación.
Los intentos por aproximarse al diagnóstico antenatal de diversas alteraciones fetales ha generado una serie de técnicas invasivas, entre las cuales se cuenta la obtención de muestras sanguíneas del paciente aún no nacido.
Así es como se inició la técnica que permite tratar in utero la anemia fetal, entre otras múltiples aplicaciones. En 1981 Rodeck describió la primera transfusión intrauterina guiada porfetoscopía. En 1983, Daffos describió la primera punción percutánea para tomar muestras de sangre fetal umbilical, con una aguja de 20-G, guiada por ultrasonido, con una tasa de pérdida fetal de un 1% (21).
Con la incorporación de las nuevas técnicas de ultrasonido y Doppler se ha facilitado el estudio de la situación hemodinámica fetal. Desde la década de los 90 la anemia fetal se puede evaluar mediante la medición del peak sistólico de velocidad en la arteria cerebral media. De este modo se puede seleccionar de manera más adecuada los pacientes para la realización de la punción del cordón o cordocentesis, que confirmará finalmente la anemia fetal.
Esta técnica consiste en obtener sangre fetal mediante la punción de la vena umbilical bajo visión ecográfica. Debe realizarse en condiciones estériles, usando una aguja espinal n° 20 a 25 que tiene un largo estándar: 88,9 mm.
Para realizar la punción es necesario visualizar el sitio de inserción placentaria del cordón, lo que es más fácil cuando la placenta es anterior. Si está inserta en la cara posterior, el feto puede interferir en la maniobra. El volumen de sangre a obtener depende de los exámenes solicitados y de la edad gestacional. En general no debe sobrepasar el 6 a 7% del volumen sanguíneo feto-placentario estimado para la edad gestacional que, en promedio, es de 125 ml/kg de peso fetal determinado por ultrasonografía. Se puede utilizar atracuronio o pancuronio para inmovilizar al feto, lo que no es necesario de regla. Si se va a realizar una amniocentesis, es conveniente hacerla antes de la cordocentesis para evitar una posible contaminación de la muestra con sangre fetal (21,22).
Esta técnica es de uso rutinario en la actualidad en aquellos fetos afectado por anemia, especialmente la asociada a isoinmunización por Rh. La sobrevida asociada a esta enfermedad luego de la introducción de la transfusión intravascular es de 82% en los casos asociados a hidrops y de hasta 96% en los casos no asociados a esta condición. La segunda indicación en frecuencia es el tratamiento de anemia fetal secundario a infecciones virales (21).
Síndrome de transfusión feto-fetal (STFF)Esta patología constituye actualmente la indicación más frecuente de cirugía fetal. Consiste en una distribución de sangre desbalanceada que ocurre entre dos gemelos a través de una anastomosis vascular placentaria en fetos que comparten una misma placenta. Este problema ocurre en el 15 a 20% de los fetos gemelares monocoriónicos. Cuando el desbalance es extremo se produce una hipervolemia y polihidroamnios de uno de los fetos y una hipovolemia y oligoamnios del otro. La evolución natural de síndrome produce una mortalidad, cuando ocurre en segundo trimestre cercana al 100%. De los pocos fetos que sobreviven el 30% presenta secuelas neurológicas (10).
La comunicación vascular en los fetos monocoriónicos es de prácticamente el 90% de ellos, sin embargo el Síndrome de Transfusión Feto Fetal se produce en un reducido porcentaje. Las razones por lo cual se produce en uno y no en otros permanece desconocida (23).
El tratamiento clásico del Síndrome TFF fue durante años la amnio-reducción. Sin embargo, y en base a un largo estudio randomizado europeo, la técnica de elección actualmente es la fotocoagulación con láser de las anastomosis en el lecho placentario mediante fetoscopía. Brevemente, esta técnica consiste en la visualización directa de los vasos comunicantes, que atraviesan el ecuador de la placenta, y realizar coagulación con láser de estos vasos.
El primer estudio multicéntrico randomizado fue realizado en 2004 por Senat y colaboradores, en el que comparó el resultado de ambas técnicas: amnioreducción seriada versus fotocoagulación con láser. El estudio incluyó 142 fetos y los resultados mostraron una clara ventaja del tratamiento por fetoscopía. Los autores observaron que la sobrevida de al menos un feto fue mayor en el grupo tratado con láser (76% v/s 51%) y que además, tanto la prematurez como las secuelas neurológicas, fueron significativamente menores en este mismo grupo (24). En base a este y a otros estudios, no cabe duda que la terapia fetal endoscópica constituye la herramienta de elección en las complicaciones de los embarazos gemelares monocoriales.
Síndrome de perfusión arteria reversa (TRAP)La Secuencia de Perfusión Arterial Reversa (TRAP) es una rara complicación de la gestación, presente en el 1% de los embarazos gemelares monocigóticos (1/35000 partos). Se caracteriza por la presencia de una placenta única y de una comunicación anatómica arterio-arterial, entre los dos gemelos; los fenómenos hemodinámicos secundarios a esta comunicación culminan, en etapas tempranas de la gestación, con uno de los fetos como transfusor y el otro como transfundido. La sangre sale desde la arteria umbilical del feto transfusor e ingresa, de forma reversa, a través de la arteria umbilical del feto transfundido, produciendo un aumento de presión en la arteria aorta y una perfusión reversa con sangre pobremente oxigenada en el transfundido. Este proceso produce una claudicación del corazón y una hipoperfusión en el hemicuerpo superior, lo que se traduce en una falta de desarrollo del corazón, cabeza y escaso crecimiento de la parte superior del cuerpo del feto transfundido. El hemicuerpo inferior, caudal a la llegada de la arteria umbilical, es perfundido de forma variable y también puede tener crecimiento disminuido. El feto transfundido se denomina feto acardio-acéfalo (24).
De esta forma el feto sano se ve enfrentado a una expansión de su espacio intravascular, representada por el tejido remanente del feto acardio-acéfalo, lo que se expresa desde el punto de vista funcional como una hipervolemia relativa. Esta alteración hemodinámica produce una insuficiencia cardíaca y la muerte del feto sano en un 50–75% de los casos.
Las alternativas terapéuticas propuestas para el manejo de estos casos han sido: parto selectivo del feto acardio, o la interrupción de la comunicación entre el feto sano y el espacio vascular remanente del feto acardio-acéfalo mediante técnicas mínimamente invasivas. En la primera alternativa, el parto selectivo debe realizarse por medio de una histerotomía con el riesgo posterior de parto prematuro, rotura uterina, acretismo placentario y hemorragias puerperales; y requiere además de una prolongada hospitalización materna, razón por la cual se ha dejado de lado como estrategia terapéutica (25).
Por lo tanto, existe consenso de que cuando una intervención es requerida, las técnicas mínimamente invasivas son las que presentan los mejores resultado obstétricos y los menores riesgos maternos. En este aspecto, se distinguen dos técnicas.
La primera de ellas corresponde a las técnicas de oclusión del cordón umbilical. Inicialmente fueron técnicas percutáneas ecoguiadas, en las cuales se introducían agentes trombogénicos en el cordón del feto acardio, tales como alcohol o fibrina. Posteriormente se desarrollaron las técnicas de oclusión vía endoscópica. En 1994 Quinteros y colaboradores comunicaron el primer caso exitoso de ligadura endoscópica del cordón umbilical de un feto acárdico-acéfalo en un embarazo gemelar complicado con secuencia TRAP, a las 19 semanas de gestación (26). Los resultados de este grupo mostraron un éxito terapéutico en la interrupción del flujo, con una mejoría de la sobrevida. En los últimos años se ha introducido fuertemente la oclusión fetoscópica con láser.
La segunda técnica mínimamente invasiva corresponde a la ablación vascular intrafetal. En ella, los objetivos son la interrupción del flujo sanguíneo en la aorta abdominal o en los vasos pélvicos del feto acárdico, esto mediante quimioesclerosis con alcohol, o termo coagulación monopolar, por radiofrecuencia o por láser.
En una revisión sistemática, se observa que no hubo diferencia significativa en la tasa de sobrevida del feto bomba entre las dos técnicas (84% v/s 70%) sin embargo, la tasa de éxito clínico, definido como sobrevida después de la interrupción completa del flujo sanguíneo y parto después de las 32 semanas, fue mayor en la ablación vascular intrafetal (77% v/s 50%) (25).
SíntesisLa cirugía fetal es un campo de constante cambio y desarrollo. Gracias a las herramientas diagnósticas prenatales se puede comprender de mejor manera la fisiopatología de múltiples patologías fetales, como también tener un diagnóstico confiable de malformaciones fetales. También ha permitido observar progresión de estas condiciones en el tiempo y, de esta manera, decidir el mejor momento de alguna intervención terapéutica.
Al revisar de forma crítica la historia de la terapia fetal parece razonable pensar que el futuro desarrollo de esta disciplina favorecerá los procedimientos percutáneos o mínimamente invasivos, ya que éstos presentan la mejor relación de resultados favorables versus complicaciones materno fetales.
Las terapias percutáneas y en especial la cirugía fetal representan un ícono en la obstetricia, sobre cómo una enfermedad o condición del feto, que tiene una mortalidad cercana al 100%, se puede revertir con el uso de estas técnicas. Probablemente en un futuro no lejano la terapia fetal génica o técnicas de miniaturización permitirán el tratamiento de condiciones que hoy están lejos del alcance del conocimiento.
Los autores declaran no tener conflictos de interés, en relación a este artículo.