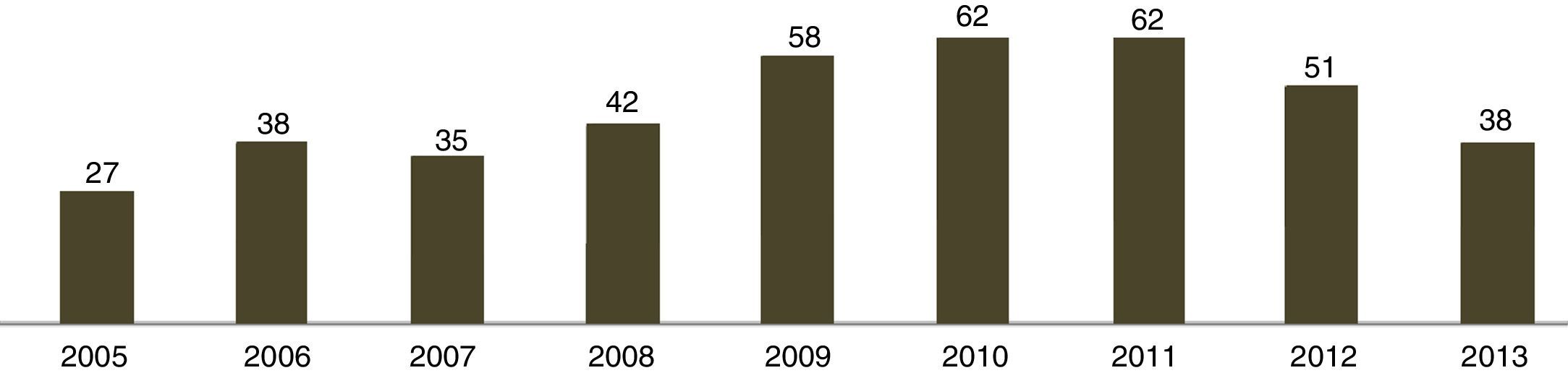La candidiasis invasora sigue siendo en la actualidad un reto para el clínico debido a su alta morbimortalidad, el progresivo aumento de su incidencia y los costes asociados. Como bien es sabido, un diagnóstico y tratamiento precoz conlleva un mejor pronóstico. Por todo ello se ha llevado a cabo una minuciosa puesta al día centrada en recientes datos epidemiológicos españoles, nuevos scores predictivos y tests microbiológicos tales como la detección del antígeno manano y de anticuerpos antimanano, anticuerpos antimicelio, (1→3)-β-D-glucano, técnicas moleculares, avances en el tratamiento antifúngico y programas educacionales en España. El objetivo de esta revisión es dotar al clínico de la mejor información disponible para mejorar el pronóstico de estos pacientes.
Invasive candidiasis in non-neutropenic critically ill patients remains a challenge for clinicians due to its association with high morbidity and mortality rates, increased incidence, and health-care costs. It is well known that early diagnosis and treatment are associated with a better prognosis. For these reasons a thorough update has been performed in this setting focused on recent Spanish epidemiology, new predictive scores and microbiological tests such as mannan antigen, mannan antibodies, Candida albicans germ-tube antibodies or (1→3)-β-D-glucan detection, molecular techniques for the detection of fungal-specific DNA, advances in antifungal treatment and educational programs in Spain. An early diagnostic and therapeutic algorithm is proposed based on the combination of scores and microbiological test. The aim of this review is to provide physicians with the best information available in order to improve the prognosis of these patients.
Los últimos hitos relacionados con la candidiasis invasora (nuevos estudios epidemiológicos publicados en nuestro país, nuevos scores basados en diferentes factores de riesgo, avances en técnicas microbiológicas no basadas en el cultivo, nuevas estrategias de tratamiento anticipado y novedades terapéuticas) hacen necesaria una revisión actualizada de la candidiasis invasora del enfermo crítico con el objeto de poder optimizar su manejo.
En esta revisión se hará una descripción actualizada de la epidemiología, se analizarán los scores vigentes y las nuevas técnicas microbiológicas no basadas en el cultivo para poder anticipar el tratamiento en estos pacientes, y se intentará describir una estrategia terapéutica global basada en los apartados anteriores y en las campañas educativas nacionales desarrolladas en los últimos tres años. En el año 2012 se publicó en la Revista Iberoamericana de Micología un monográfico donde se incluyeron revisiones completas tanto para el diagnóstico47 como para las opciones terapéuticas de la candidiasis invasora66, por lo tanto en esta revisión solo se incluirán las novedades más relevantes que se hayan producido desde entonces.
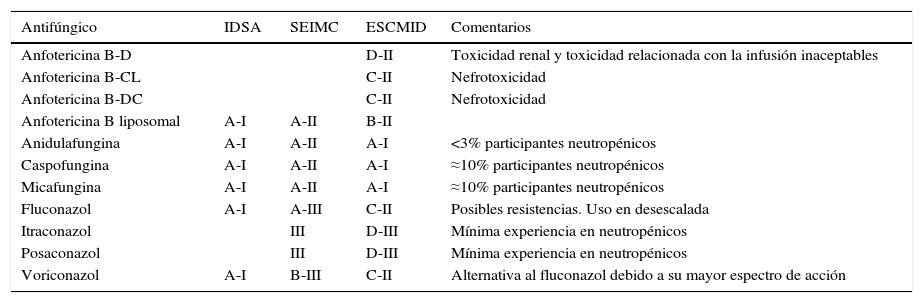
Epidemiología de la infección invasora por Candida en el paciente críticoAunque numéricamente se podría incurrir en el error de minimizar la trascendencia de la candidiasis invasora en el paciente crítico, su gran impacto pronóstico aseguraría a esta entidad un importante papel en el ámbito de la medicina intensiva. Registros nacionales e internacionales como el ENVIN o el EPIC II ponen de manifiesto que Candida es responsable del 12-20% de los eventos infecciosos que sufren los pacientes críticos59,60. El análisis detallado de los datos procedentes de ENVIN a lo largo de los últimos años muestra un incremento progresivo de la presencia de Candida en hemocultivos (desde un 5% en 2005 hasta un 10% en 2010) (fig. 1)59. Sin embargo, es destacable el descenso de las candidemias detectado en los últimos dos años (6% en 2013, 8% en 2014) (fig. 1). El incremento progresivo de la infección fúngica invasora es consecuencia de los avances en las terapias médicas y quirúrgicas, cada vez más eficaces pero también más agresivas, de modo que el paciente sobrevive a la enfermedad original pero a costa de aumentar su susceptibilidad a las infecciones oportunistas. Parece razonable suponer que el descenso observado en la incidencia de la candidemia en los últimos años pueda deberse a una mejora en las actuaciones preventivas, tanto en el campo de la prevención de las infecciones asociadas a dispositivos invasores como en las estrategias de profilaxis antifúngica.
La mortalidad atribuible a un episodio de candidemia se cifra en un 15-35% en los adultos y en un 10-15% para los neonatos43, pero existen claras diferencias si la mortalidad se evalúa a los 7 días del diagnóstico (13%) o a los 30 días (30%). Evidentemente, la mortalidad precoz depende de factores más modificables (instauración del tratamiento antifúngico apropiado o retirada del catéter intravenoso) y la tardía está afectada por factores propios del huésped, menos susceptibles de intervención externa52. Junto a estas graves consecuencias, existen importantes aspectos económicos asociados ya que el coste promedio de un episodio de candidiasis invasora en la población hospitalaria se ha calculado en 40.000 $18.
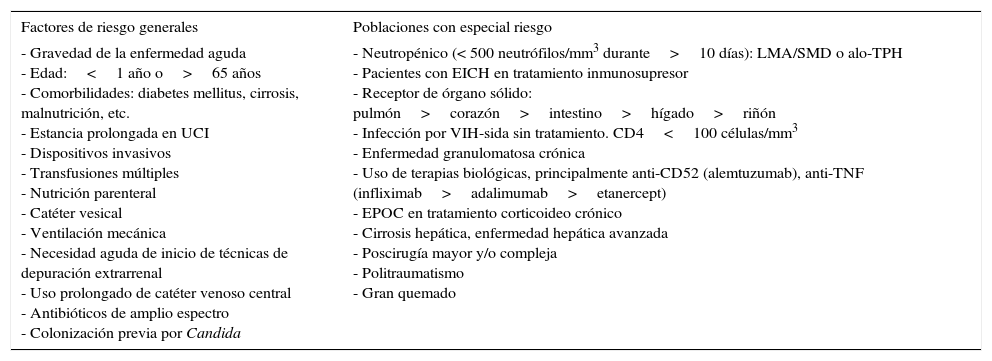
La instauración de una candidiasis invasora requiere de la presencia de factores de riesgo que permitan o favorezcan la colonización por Candida, la entrada del microorganismo y finalmente la superación de la respuesta inmune. Estas situaciones son extremadamente frecuentes en el paciente crítico. El uso de antibióticos y la consecuente disminución del inóculo bacteriano favorece la colonización fúngica, fundamentalmente en el tubo digestivo. Además, Candida puede alcanzar el torrente sanguíneo vehiculizada por la instrumentación a la que son sometidos los pacientes o por translocación intestinal (facilitada en los enfermos sometidos a cirugía digestiva o con enfermedad abdominal, p.ej. una pancreatitis necrohemorrágica). En el paciente crítico concurren con frecuencia factores inmunosupresores debidos a la enfermedad de base o su tratamiento, sin olvidar la existencia de la inmunoparálisis adquirida tras la superación del evento inflamatorio inicial. En la tabla 1 se recogen los factores de riesgo asociados a la infección por Candida. Aparte de los factores de riesgo comunes, se han descrito otros asociados con la aparición de ciertas especies: trasplante de progenitores hematopoyéticos o neutropenia con Candida tropicalis y Candida krusei; uso previo de fluconazol con Candida glabrata o C. krusei; y nutrición parenteral, catéter intravascular y paciente neonato con Candida parapsilosis32,44,50. Evidentemente la incidencia de infección fúngica en cada unidad estará vinculada al tipo de enfermos atendidos en la misma y cada paciente deberá ser evaluado individualmente en función de la presencia de los factores de riesgo conocidos.
Factores de riesgo asociados a la infección invasora por Candida en el paciente crítico
| Factores de riesgo generales | Poblaciones con especial riesgo |
|---|---|
| - Gravedad de la enfermedad aguda - Edad:<1 año o>65 años - Comorbilidades: diabetes mellitus, cirrosis, malnutrición, etc. - Estancia prolongada en UCI - Dispositivos invasivos - Transfusiones múltiples - Nutrición parenteral - Catéter vesical - Ventilación mecánica - Necesidad aguda de inicio de técnicas de depuración extrarrenal - Uso prolongado de catéter venoso central - Antibióticos de amplio espectro - Colonización previa por Candida | - Neutropénico (< 500 neutrófilos/mm3 durante>10 días): LMA/SMD o alo-TPH - Pacientes con EICH en tratamiento inmunosupresor - Receptor de órgano sólido: pulmón>corazón>intestino>hígado>riñón - Infección por VIH-sida sin tratamiento. CD4<100 células/mm3 - Enfermedad granulomatosa crónica - Uso de terapias biológicas, principalmente anti-CD52 (alemtuzumab), anti-TNF (infliximab>adalimumab>etanercept) - EPOC en tratamiento corticoideo crónico - Cirrosis hepática, enfermedad hepática avanzada - Poscirugía mayor y/o compleja - Politraumatismo - Gran quemado |
La principal fuente de Candida es endógena, pero existen estudios que demuestran una transmisión horizontal, a partir de pacientes infectados o colonizados, a través de las manos de trabajadores sanitarios7,8,16,23.
Se conocen más de cien especies distintas de Candida, pero el 95-97% de todas las infecciones invasoras están causadas por solo 5 especies: Candida albicans, C. glabrata, C. parapsilosis, C. tropicalis y C. krusei. La variabilidad geográfica en la distribución de estas especies es ampliamente reconocida, y puesto que su sensibilidad a los antifúngicos no es uniforme es muy aconsejable conocer la epidemiología del entorno. Los registros procedentes de Estados Unidos o del norte de Europa muestran una mayor prevalencia de C. glabrata (y menor de C. parapsilosis), mientras que los datos procedentes de España o Brasil indican una menor presencia de C. glabrata y una predominancia de C. parapsilosis5,6,12,13,23,45,52,58. No existe una clara explicación para esta diferente distribución pero se ha valorado la posible participación del clima, la política de uso de los antifúngicos o el manejo de los catéteres venosos.
En el estudio epidemiológico multicéntrico FUNGEMYCA realizado en España en 2009, en el que participaron 43 centros hospitalarios y se incluyeron 1.357 episodios de candidemia, C. albicans fue la especie más frecuentemente aislada (44,7%), seguida de C. parapsilosis (26,6%) y C. glabrata (11,5%)45. En 2010-2011, el estudio CANDIPOP (29 hospitales y 767 episodios de candidemia) puso en evidencia que C. albicans es la especie más frecuente en España (44,6%), seguida de C. parapsilosis (24,5%), pero detectó un claro incremento en la presencia de C. glabrata (13%)23. En ambos registros se describe una variabilidad geográfica dentro del territorio nacional. La tasa de aislamientos de C. albicans fue más baja (35%) en la Comunidad Valenciana y Andalucía; C. parapsilosis se aisló de manera más notable en la Comunidad Valenciana (40%) y C. glabrata en Cataluña (17%)45. También fue posible detectar diferencias en la distribución de especies cuando se analizaron los distintos servicios participantes en el registro. Aunque C. albicans, C. parapsilosis y C. glabrata fueron las tres especies mayoritarias en casi todas las unidades de hospitalización, C. parapsilosis fue la especie predominante en los servicios de neonatología y pediatría general, aislándose con mayor frecuencia que C. albicans (46 frente a 43% y 59 frente a 19%, respectivamente)44.
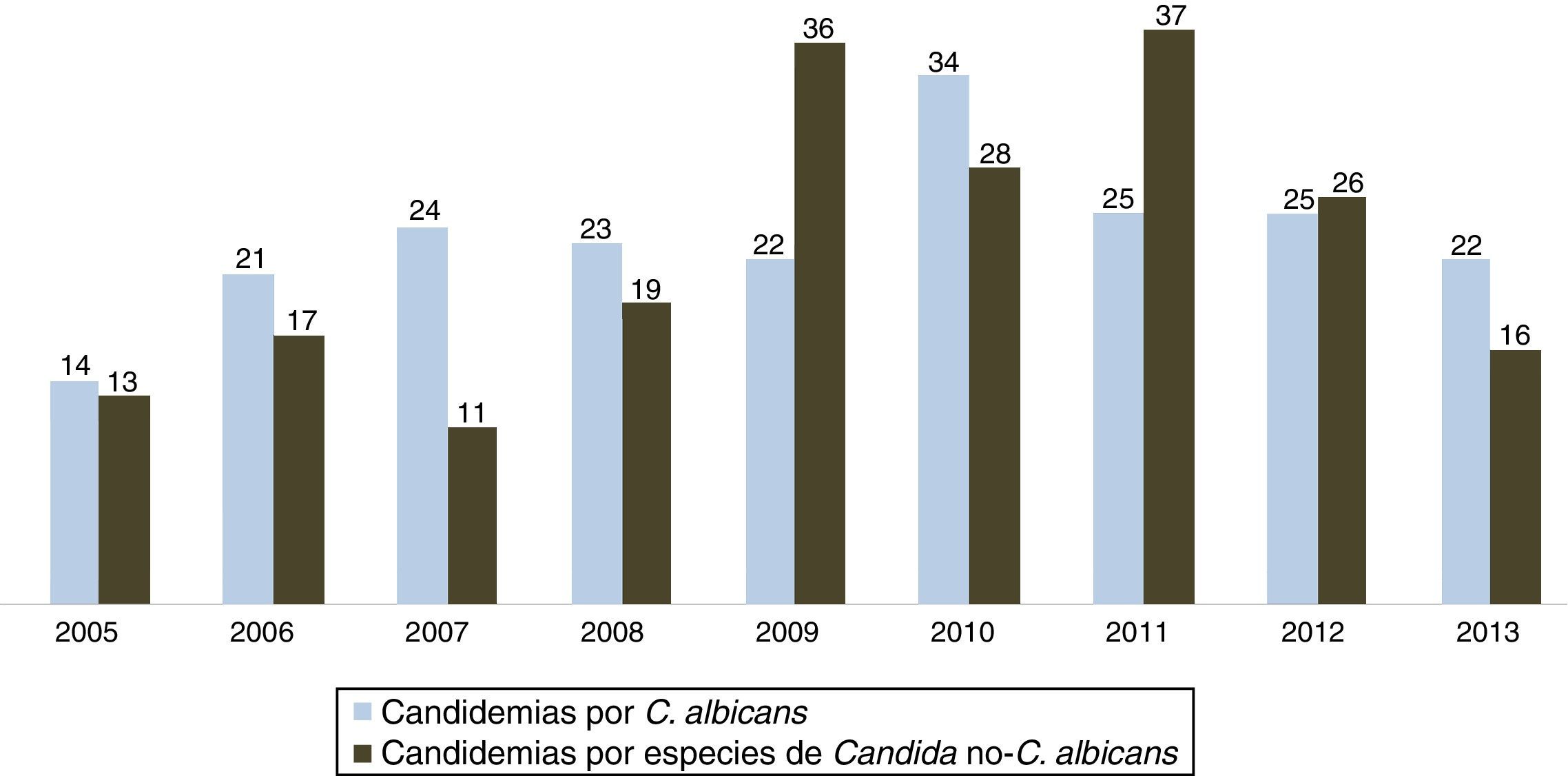
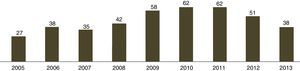
En los primeros años del siglo actual el registro ENVIN muestra una clara predominancia de C. albicans frente a otras especies del género en las candidemias del paciente crítico (fig. 2). Tras el incremento de estas últimas especies en los años coincidentes con FUNGEMYCA o CANDIPOP, en los últimos dos años se ha observado (junto al ya comentado descenso en la incidencia de la candidemia) un ascenso de C. albicans59. Este hecho puede ser debido al impacto del proyecto Bacteriemia Zero en la incidencia de candidemias relacionadas con catéteres y, por tanto, con la presencia de especies de Candida diferentes de C. albicans, sobre todo C. parapsilosis41.
El estudio CANDIPOP realizó un exhaustivo análisis de las resistencias a los antifúngicos y detectó un claro incremento del porcentaje de aislamientos resistentes o menos sensibles al fluconazol con respecto a los datos existentes de un registro catalán realizado 2 años antes (20 frente a 7%)3,23. Este dato está en consonancia con los procedentes de otras zonas geográficas11,13,21,49. Guinea et al. encontraron una asociación entre el uso previo del fluconazol y la resistencia a dicho antifúngico así como un mayor aislamiento de C. glabrata23. Solo un 2% de los aislamientos del estudio CANDIPOP fueron resistentes a las equinocandinas. A pesar de que los dos registros realizados en Cataluña con una diferencia de 9 años coincidían con la urgencia de los nuevos antifúngicos no se observó un efecto sobre la distribución de las especies de Candida, aunque existen datos que sí relacionan el uso de la caspofungina con un incremento en la presencia de C. parapsilosis, C. glabrata y C. krusei34.
Recomendaciones consensuadas por expertos españoles para el diagnóstico y tratamiento de la candidiasis invasora (proyecto EPICO)Aunque en la última década ha mejorado el manejo de la candidiasis invasora todavía persisten aspectos controvertidos en su estrategia diagnóstica y terapéutica. Ante esta realidad, hace tres años un grupo de expertos españoles de diferentes especialidades se plantearon identificar los conocimientos clínicos esenciales y formular unas recomendaciones (consensuadas mediante la técnica DELPHI) para la asistencia de pacientes críticos adultos no neutropénicos con candidiasis invasora (proyecto EPICO)63.
Para ello se preparó una encuesta de 47 preguntas que se envió de forma anónima a 25 especialistas nacionales de diferentes disciplinas médicas, expertos en infección fúngica invasora, incluidos intensivistas, anestesistas, microbiólogos, farmacólogos e infectólogos. Los objetivos educativos contemplaron cinco categorías: epidemiología, instrumentos diagnósticos, scores, estrategias terapéuticas y estrategias de desescalada. Para que una determinada acción fuera seleccionada, el grado de acuerdo alcanzado entre los expertos debía superar el 75%. Después de extraer las recomendaciones de los ítems seleccionados, se celebró una reunión presencial donde participaron más de 80 especialistas y se les solicitó la validación de las recomendaciones preseleccionadas. Finalmente se validaron las 12 recomendaciones generales que se describen en la tabla 2.
Recomendaciones finales Proyecto EPICO
| Epidemiología |
| 1. Puesto que la incidencia de candidiasis invasora en pacientes ingresados en las áreas de críticos ha aumentado en las últimas décadas, considere de forma precoz esta posibilidad en los pacientes críticos con un proceso infeccioso |
| 2. Si bien es fundamental conocer la epidemiología local, en el paciente crítico con candidiasis invasora considere la posibilidad de la existencia de especies de Candida resistentes a fluconazol en aquellos que han recibido tratamiento previo con triazoles, en los que presentan insuficiencia renal crónica y en enfermos neutropénicos |
| Scores |
| 1. Investigue la presencia de colonización candidiásica múltiple y determine el Candida score en todo paciente crítico con sospecha de candidiasis invasora como herramienta de screening |
| Diagnóstico de laboratorio |
| 1. Realice hemocultivos en el momento de sospecha de candidiasis invasora y cada 2-3 días si persiste la infección. En el caso de aislar Candida realice hemocultivos de control hasta su negatividad |
| 2. Cultive los fluidos estériles o los tejidos y realice una observación directa al microscopio siempre que sea posible |
| 3. Ante la sospecha de candidiasis invasora utilice de forma rutinaria una técnica microbiológica no basada en el cultivo, si dispone de ella en su centro |
| 4. Solicite estudio de sensibilidad antifúngica en caso de candidiasis invasora confirmada |
| Tratamiento |
| 1. Inicie el tratamiento precozmente desde el momento en que considere el diagnóstico de candidiasis invasora |
| 2. Una equinocandina debe ser el tratamiento empírico de elección en el paciente crítico e inestable |
| 3. Se recomienda al menos un estudio oftalmológico en todo paciente con candidemia. Si existe afectación ocular debe tenerse en cuenta la mala penetración de las equinocandinas |
| 4. Siempre que sea posible, se recomienda la retirada del catéter venoso central en un paciente con candidemia |
| Desescalada terapéutica |
| 1. En el paciente crítico con candidiasis invasora confirmada por un aislamiento de Candida sensible al fluconazol que está recibiendo tratamiento empírico con una equinocandina, considere desescalar a fluconazol tras 2 o 3 días de estabilidad clínica |
Un año más tarde se realizó una segunda edición del proyecto con la misma metodología DELPHI, esta vez centrada en aspectos terapéuticos más concretos de la candidiasis invasora en el paciente crítico: candidiasis peritoneal, pacientes inmunodeprimidos, situaciones especiales y fracaso orgánico (Proyecto EPICO 2.0)62. Después de la reunión presencial con 60 especialistas, 13 recomendaciones fueron validadas (tabla 3).
Recomendaciones finales EPICO 2.0
| Candidiasis peritoneal |
| 1. Debido al mal pronóstico de la peritonitis candidiásica, se recomienda un adecuado control del foco infeccioso junto a un tratamiento antifúngico precoz y apropiado |
| 2. Se recomienda iniciar un tratamiento antifúngico empírico en pacientes con peritonitis secundaria nosocomial y con factores de riesgo de colonización por Candida o en aquellos pacientes con peritonitis terciaria |
| 3. En la peritonitis candidiásica se recomienda utilizar una equinocandina en los pacientes inestables, en aquellos que han recibido previamente azoles o en los que el aislamiento de Candida es resistente al fluconazol |
| Paciente inmunodeprimido y trasplantado |
| 1. En el tratamiento de la candidiasis invasora con azoles en un paciente con trasplante de órgano sólido deben considerarse sus interacciones y hepatotoxicidad |
| 2. En el paciente neutropénico, la duración del tratamiento de la candidemia debe ser de 14 días desde el primer cultivo negativo y hasta la normalización de la cifra de neutrófilos |
| 3. En un paciente neutropénico con candidemia, la caspofungina es la equinocandina con más respaldo científico |
| 4. La caspofungina es la equinocandina de elección en la neutropenia febril con sospecha de candidemia |
| 5. En un paciente neutropénico inestable con candidemia y catéter venoso central de fácil recambio es aconsejable la retirada del mismo |
| Tratamiento antifúngico en situaciones especiales |
| 1. En el tratamiento de la candidiasis invasora en pacientes con disfunción hepática moderada (Child B) se recomienda utilizar equinocandinas (preferentemente anidulafungina o caspofungina con ajuste de la dosis) y se debe evitar el uso de azoles |
| 2. Aunque las interacciones farmacológicas de las equinocandinas son pocas se recomienda revisar la medicación concomitante y, en caso de posible interacción, utilizar preferentemente la anidulafungina |
| Tratamiento antifúngico en presencia de fracasos orgánicos |
| 1. En lo que a seguridad se refiere las equinocandinas son la familia de antifúngicos de primera elección |
| 2. El uso del fluconazol precisa ajuste de la dosis que hace reconsiderar su uso en el paciente en tratamiento con técnica continua o intermitente de depuración extrarrenal |
| 3. Todas las equinocandinas son aceptadas y pueden considerarse similares para el tratamiento de los pacientes que necesitan técnicas de depuración extrarrenal, continuas o intermitentes, y no precisan ajuste de la dosis |
Si bien el proyecto EPICO63 recomienda el uso del Candida score por su fácil aplicabilidad27, es cierto que fue una de las recomendaciones que menos consenso obtuvo. Todos los scores predictivos publicados hasta el momento (Candida score, regla de Ostrosky-Zeichner40, Playford51, Nebraska score y Paphitou25) se caracterizan por presentar un alto valor predictivo negativo (95-97%) y valores predictivos positivos muy bajos que no alcanzan el 20% en el mejor de los casos47, no superando ninguno de ellos el área bajo la curva de 0,77 descrito para el Candida score30. Esta realidad y su sencillez hacen que siga siendo el más utilizado. Un estudio realizado por un grupo francés en 94 pacientes críticos en situación de shock séptico evaluó el Candida score, y llegó a la conclusión de que, en esta situación clínica, un valor de 4 puntos se asociaba a una incidencia de candidiasis invasora del 17%, mientras que un valor de 5 puntos se asociaba a una incidencia del 100%31.
Recientemente se ha desarrollado un nuevo score predictivo mediante un estudio con pacientes con sepsis grave o shock séptico y hemocultivos positivos, donde un 10,2% de ellos (266 pacientes) presentaron candidemia22. Los factores de riesgo obtenidos y su ponderación fueron los siguientes: antibioterapia previa, 2 puntos; catéter venoso central, 2 puntos; ingreso desde un centro de asistidos, 2 puntos; ingreso desde otro hospital, 1 punto (puntuaciones dicotómicas); nutrición parenteral total, 2 puntos; ventilación mecánica, 1 punto; y foco respiratorio, 6 puntos. Al establecer el punto de corte en 3 puntos los autores determinaron para el desarrollo de una candidemia una sensibilidad del 87,6%, una especificidad del 55,9%, un área bajo la curva de 0,72, valor predictivo negativo del 97,5% y valor predictivo positivo del 18,5%.
Técnicas microbiológicas no basadas en el cultivoLas últimas guías europeas recomiendan, para el diagnóstico de la candidemia, la detección de manano y anticuerpos antimanano, y de β-glucano14; ambas pruebas diagnósticas se han descrito ampliamente en revisiones ya publicadas47,48. Aunque la detección de anticuerpos antimicelio, técnica con resultados esperanzadores evaluados por nuestro grupo46,64,65, no se recomienda en las guías, esta técnica ha sido recientemente evaluada por un grupo español, que ha observado una mayor rentabilidad diagnóstica en los casos de candidiasis invasora profunda frente a los de origen superficial (candidemias asociadas a catéter)35.
Gracias a su elevado valor predictivo negativo, la detección de β-glucano también ha sido valorada en 64 pacientes críticos que recibieron tratamiento antifúngico anticipado o empírico, y se observó una sensibilidad del 100%, una especificidad del 75%, un valor predictivo positivo del 30% y un valor predictivo negativo del 100%, para un punto de corte de 80pg/ml24. Además, la técnica sirvió para la monitorización del tratamiento, en este caso con anidulafungina, lo que llevó a poder reducir significativamente su concentración. Un estudio español que utilizó un punto de corte mayor (259pg/ml) ha demostrado la utilidad de la combinación de esta técnica con la detección de anticuerpos antimicelio en 115 pacientes críticos poscirugía abdominal29.
Recientemente un estudio multicéntrico prospectivo que utiliza una nueva herramienta de nanodiagnóstico que combina PCR con resonancia magnética T2 en muestras de 2ml de sangre completa, ha descrito para esta técnica una especificidad del 99,1% y una sensibilidad del 98,9% en 1.801 pacientes con sospecha de candidiasis invasora, todo ello en menos de 5 h desde la extracción de la sangre y de forma totalmente automatizada38. Si se confirman estos resultados en próximos estudios, este nuevo tipo de diagnóstico molecular supondrá un gran adelanto en el diagnóstico de la candidiasis invasora.
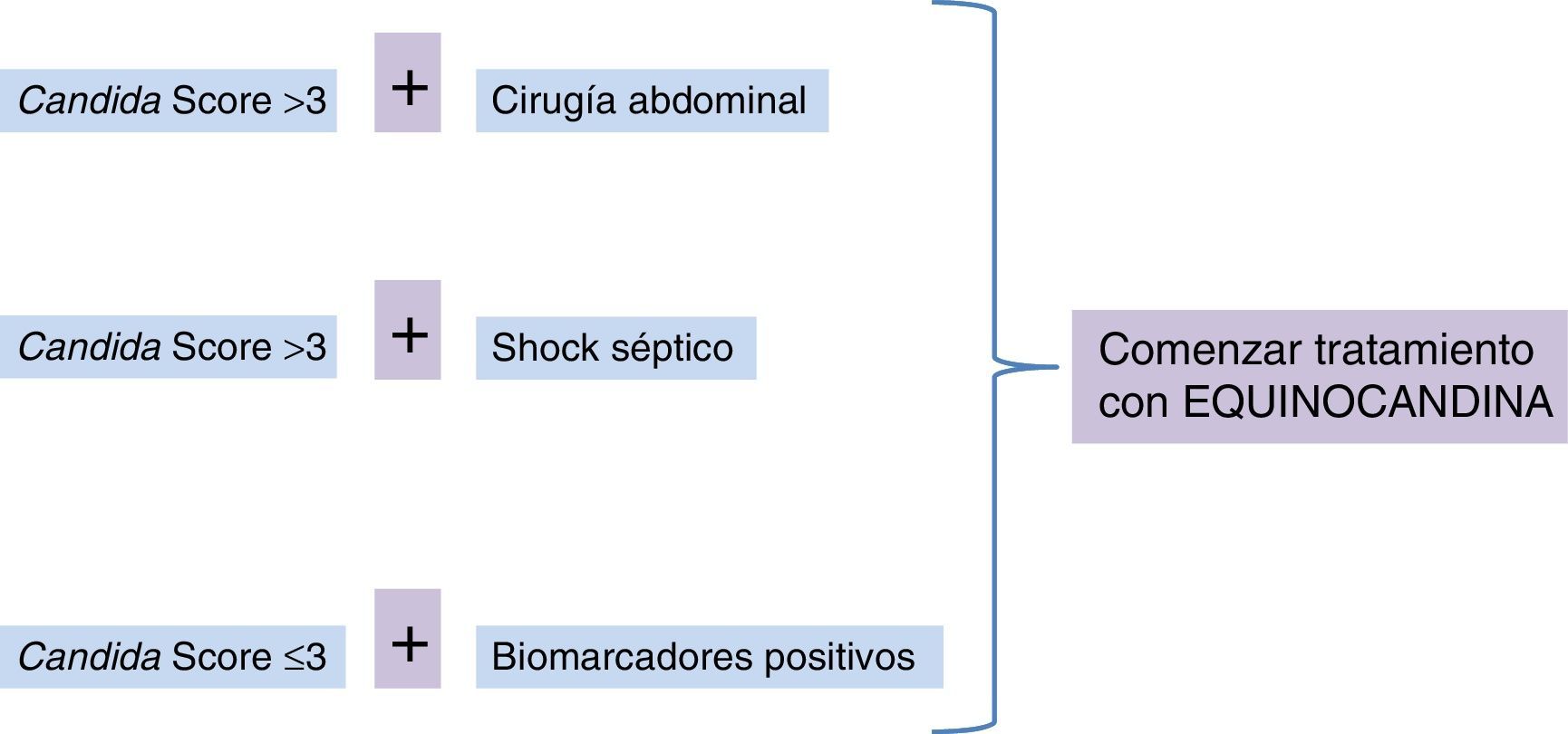
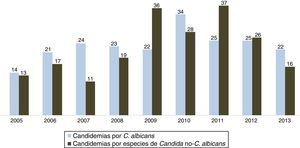
Uso combinado de técnicas y scoresHasta que exista un nuevo gold standard para el diagnóstico de la candidiasis invasora, una estrategia basada en la combinación de scores de predicción clínicos junto con el uso de técnicas microbiológicas independientes del cultivo podría ser una adecuada aproximación28,48. En esta línea, un reciente editorial basa la estrategia de un tratamiento precoz en la combinación de la situación clínica, cirugía previa y test de β-glucano para comenzar un tratamiento empírico o anticipado9. Nuestro grupo, tras analizar lo anteriormente expuesto, propone un sencillo algoritmo para el inicio de un tratamiento precoz de la candidiasis invasora en pacientes críticos (fig. 3).
Optimización del tratamientoDonde más inciden las recomendaciones de los proyectos EPICO y EPICO 2.0 es en el tratamiento62,63. En términos generales, sus recomendaciones pueden dividirse en dos grandes grupos: las relacionadas con estrategias asociadas y aquellas propias de los fármacos antifúngicos y su elección. Seguidamente se revisarán estas recomendaciones analizándolas bajo la luz de los últimos estudios publicados.
Estrategias terapéuticas globales asociadasLa administración precoz del tratamiento antifúngico y la retirada del catéter central (o el control del foco infeccioso) son dos de las estrategias que tuvieron más consenso en el proyecto EPICO63. Estas recomendaciones tenían su evidencia en trabajos previos26, y en los pacientes donde no se cumplieron ninguna de las dos recomendaciones (control del foco y/o inicio precoz del tratamiento antifúngico) la mortalidad fue del 100%. Aunque el control del foco abdominal no es discutido en la literatura, la retirada del catéter ha sido cuestionada por Garnacho et al. cuando el foco de la infección tiene un claro origen abdominal en un trabajo con un diseño impecable realizado con 188 pacientes con candidemia y portadores de catéter19. El estudio CANDIPOP, tanto en su serie general publicada52 como en la cohorte de enfermos críticos53, resuelve la controversia y encuentra como factores asociados a mayor mortalidad precoz (aquella que se produce en los 7 primeros días tras el diagnóstico) la no retirada del catéter y la instauración de un tratamiento antifúngico tras más de 48 h, independientemente del foco de la candidemia. Un estudio multicéntrico europeo, publicado casi simultáneamente a CANDIPOP, en pacientes con shock séptico secundario a candidemia, corroboró nuevamente la necesidad de un adecuado control del foco y el tratamiento antifúngico precoz10, por lo que dichas estrategias deberían ser de obligado cumplimiento en estos pacientes.
Tratamiento antifúngicoEl proyecto EPICO considera las equinocandinas como el tratamiento empírico de elección en el paciente crítico e inestable63. Nuestra revisión previa67 y las últimas guías europeas publicadas14 comparten dicha recomendación, apoyadas en múltiples evidencias de la literatura entre las que cabe destacar el metaanálisis publicado por Andes et al.4 en el que se incluyen 1.915 pacientes de los siete últimos ensayos clínicos en los que una equinocandina fue utilizada en uno de los brazos; en este análisis, el tratamiento con equinocandinas se asocia con un mejor pronóstico. En un trabajo previo ya se obtuvieron similares resultados39, al igual que en el ensayo pivotal de la anidulafungina frente al fluconazol donde, a pesar de tener un diseño de no inferioridad, se puso en evidencia la superioridad de la equinocandina frente al azol55, incluso en candidemias por C. albicans56. Por esta razón, entre otras, las recientes guías europeas rebajan el nivel de recomendación del fluconazol a CI14. En la tabla 4 se describen comparativamente los niveles de recomendación de las últimas guías de la IDSA42, SEIMC1 y ESCMID14. A todas las equinocandinas se les otorga el mismo nivel de recomendación, si bien las diferencias entre ellas pueden tener implicación en su elección y en la posible individualización del tratamiento en función del tipo de paciente y su situación clínica. Estas particularidades también fueron analizadas e incluidas en las recomendaciones del proyecto EPICO 2.062.
Recomendaciones actuales de las diferentes sociedades científicas para el tratamiento farmacológico de la candidiasis invasora en el paciente adulto no neutropénico
| Antifúngico | IDSA | SEIMC | ESCMID | Comentarios |
|---|---|---|---|---|
| Anfotericina B-D | D-II | Toxicidad renal y toxicidad relacionada con la infusión inaceptables | ||
| Anfotericina B-CL | C-II | Nefrotoxicidad | ||
| Anfotericina B-DC | C-II | Nefrotoxicidad | ||
| Anfotericina B liposomal | A-I | A-II | B-II | |
| Anidulafungina | A-I | A-II | A-I | <3% participantes neutropénicos |
| Caspofungina | A-I | A-II | A-I | ≈10% participantes neutropénicos |
| Micafungina | A-I | A-II | A-I | ≈10% participantes neutropénicos |
| Fluconazol | A-I | A-III | C-II | Posibles resistencias. Uso en desescalada |
| Itraconazol | III | D-III | Mínima experiencia en neutropénicos | |
| Posaconazol | III | D-III | Mínima experiencia en neutropénicos | |
| Voriconazol | A-I | B-III | C-II | Alternativa al fluconazol debido a su mayor espectro de acción |
CL: complejo lipídico; D: desoxicolato; DC: dispersión coloidal.
La aparición de candidemias de brecha causadas por C. parapsilosis en el estudio pivotal de caspofungina37 sembró la duda sobre el uso de las equinocandinas para esta especie. Pero ese temor se ha disipado con el uso de las mismas en la práctica diaria y con estudios, como el análisis extraído del estudio CANDIPOP, en el que el uso empírico de equinocandinas en candidemias por C. parapsilosis no se asociaba a una mala evolución de los pacientes17.
En pacientes tratados con técnica continua o intermitente de depuración extrarrenal la necesidad de ajustar las dosis de fluconazol muchas veces hace replantearse su uso, a diferencia de las equinocandinas, que pueden considerarse similares para el tratamiento de estos pacientes. Recientemente se han publicado diferentes estudios para cada una de ellas, y se ha validado su uso en pacientes con técnicas de depuración extrarrenal2,36,61, por lo que no precisan ajuste de la dosis. Seguidamente se describen las posibles ventajas de cada una de las equinocandinas en determinadas situaciones clínicas o escenarios terapéuticos.
CaspofunginaEn el paciente neutropénico con candidemia la caspofungina es la equinocandina con más respaldo científico, además de ser de elección en la neutropenia febril con sospecha de candidemia62.
AnidulafunginaEn el tratamiento de la candidiasis invasora en pacientes con insuficiencia hepática grave es el antifúngico de elección debido a la ausencia de metabolización hepática. Aunque las interacciones farmacológicas de las equinocandinas son escasas, se recomienda revisar la medicación concomitante y, en caso de posible interacción, utilizar preferentemente la anidulafungina ya que es la que menos interacciones presenta, lo que facilita especialmente el manejo de pacientes inmunodeprimidos y trasplantados que reciben inmunosupresores. El estudio ICE permitió conocer los buenos resultados que en pacientes críticos presenta este fármaco en diferentes situaciones clínicas y fracasos orgánicos57, incluidos pacientes ancianos15. Estos buenos resultados podrían estar justificados por la excelente farmacocinética del fármaco demostrada en pacientes críticos y su buena penetración tisular33. Además, también ha sido validada para su uso en diálisis con albúmina (MARS)2. Diversos estudios farmaeconómicos también consideran la anidulafungina coste-efectiva, incluso en pacientes críticos20,54, por lo que su uso en estos pacientes está sobradamente justificado.
MicafunginaEl uso de esta equinocandina comporta una leve ventaja económica al no ser necesaria una dosis de carga al inicio del tratamiento62.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.