Los linfomas son los tumores no epiteliales malignos más frecuente en la cavidad oral y región maxilofacial. El riesgo de los pacientes con VIH de presentar esta enfermedad es 200 veces mayor en comparación con la población general. El linfoma plasmablástico es una neoplasia agresiva poco frecuente. La clasificación del 2008 de la OMS lo define como una proliferación difusa de células grandes neoplásicas semejantes a inmunoblastos B con inmunofenotipo de células plasmáticas, con la mayoría de los casos asociados a pacientes con VIH. El propósito de este artículo es presentar una revisión sistemática de esta enfermedad junto a un caso clínico de difícil diagnóstico por su expresión clínica, en el que el estudio histopatológico fue determinante.
Lynphomas are the most common malignant non-epithelial tumours in the oral cavity and maxilofacial región. The risk of HIV patients presenting with this condition is 200 times more compared to the general population. Plasmablastic lymphoma is a rare aggresive neoplasm. The WHO 2008 classification defines it as a diffuse proliferation of large neoplastic cells, such as B immunoblasts with plasma inmunophenotype cells, with most cases being associated with HIV patients. The purpose of this article is to present a systematic review of this pathology together with a case of difficult diagnosis due to its clinical expression, and in which the histopathology study was decisive.
Los linfomas son los tumores no epiteliales malignos más frecuente en la cavidad oral y región maxilofacial. Representan el tercer grupo más común de lesiones malignas de esta área después del carcinoma de células escamosas y de las neoplasias de las glándulas salivales1. El riesgo de los pacientes con virus de la inmunodeficiencia humana (VIH) de presentar esta enfermedad es 200 veces mayor en comparación con la población general2.
Los linfomas más observados en pacientes con VIH son predominantemente de estirpe B, incluidos: linfoma difuso de células grandes, linfoma de Burkitt, linfoma primario de serosas y linfoma plasmablástico3(LPB).
El LPB, además de presentarse con mayor frecuencia en pacientes con VIH, tiene una predilección por la cavidad oral, características que no se observan en otras neoplasias linfoides.
En este trabajo se realiza una revisión sistemática sobre el LPB de localización intraoral en pacientes con VIH. Se analiza el comportamiento clínico, la metodología para su diagnóstico y el tipo de tratamiento aplicado. Se documenta un caso de un LPB intraoral en paciente con VIH tratado en nuestro centro hospitalario.
Materiales y métodosLa búsqueda bibliográfica se ha realizado electrónicamente a través de la bases de datos y motores de bu¿squeda Medline (PubMed). Se han empleado los siguientes términos claves: «oral plasmablastic lymphoma», «lymphoma intraoral» y «lymphoma in HIV». Se han seleccionado los artículos que presentaban esta enfermedad en localización intraoral en pacientes con VIH. De los artículos seleccionados se analizaron variables de edad, tamaño tumoral, tratamiento y resultados. Se excluyeron los artículos que no aportaban datos concretos de los casos tratados y los artículos no relacionados con el VIH.
ResultadosLa expresión «oral plasmablastic lymphoma» identificó 169 artículos, de los cuales se excluyeron 90, ya que el linfoma era extraoral o no se documentaba la información objeto del estudio; 34 fueron excluidos ya que eran artículos enfocados en pacientes sin VIH; 7 artículos se excluyeron porque no pudieron ser localizados, por razones de antigüedad o accesibilidad; un artículo se excluyó por estar escrito en francés y 2 por estar en mandarín. Así mismo, otro artículo fue excluido por retracción de este. La muestra final incluyó 34 artículos, sobre los que se procedió al análisis de las variables (tabla 1).
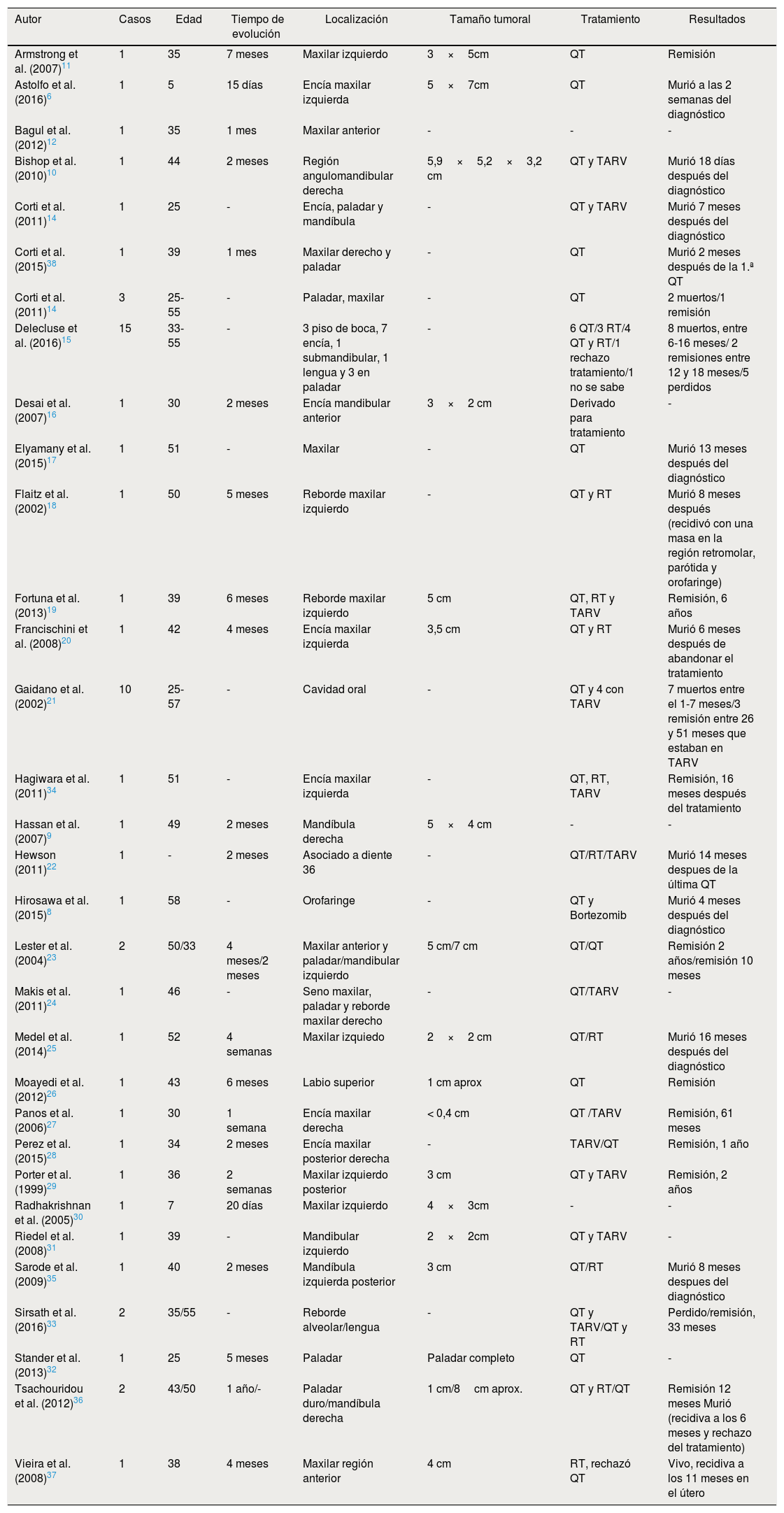
Casos documentados en la literatura sobre linfoma plasmablástico intraoral en pacientes con VIH
| Autor | Casos | Edad | Tiempo de evolución | Localización | Tamaño tumoral | Tratamiento | Resultados |
|---|---|---|---|---|---|---|---|
| Armstrong et al. (2007)11 | 1 | 35 | 7 meses | Maxilar izquierdo | 3×5cm | QT | Remisión |
| Astolfo et al. (2016)6 | 1 | 5 | 15 días | Encía maxilar izquierda | 5×7cm | QT | Murió a las 2 semanas del diagnóstico |
| Bagul et al. (2012)12 | 1 | 35 | 1 mes | Maxilar anterior | - | - | - |
| Bishop et al. (2010)10 | 1 | 44 | 2 meses | Región angulomandibular derecha | 5,9×5,2×3,2 cm | QT y TARV | Murió 18 días después del diagnóstico |
| Corti et al. (2011)14 | 1 | 25 | - | Encía, paladar y mandíbula | - | QT y TARV | Murió 7 meses después del diagnóstico |
| Corti et al. (2015)38 | 1 | 39 | 1 mes | Maxilar derecho y paladar | - | QT | Murió 2 meses después de la 1.ª QT |
| Corti et al. (2011)14 | 3 | 25-55 | - | Paladar, maxilar | - | QT | 2 muertos/1 remisión |
| Delecluse et al. (2016)15 | 15 | 33-55 | - | 3 piso de boca, 7 encía, 1 submandibular, 1 lengua y 3 en paladar | - | 6 QT/3 RT/4 QT y RT/1 rechazo tratamiento/1 no se sabe | 8 muertos, entre 6-16 meses/ 2 remisiones entre 12 y 18 meses/5 perdidos |
| Desai et al. (2007)16 | 1 | 30 | 2 meses | Encía mandibular anterior | 3×2 cm | Derivado para tratamiento | - |
| Elyamany et al. (2015)17 | 1 | 51 | - | Maxilar | - | QT | Murió 13 meses después del diagnóstico |
| Flaitz et al. (2002)18 | 1 | 50 | 5 meses | Reborde maxilar izquierdo | - | QT y RT | Murió 8 meses después (recidivó con una masa en la región retromolar, parótida y orofaringe) |
| Fortuna et al. (2013)19 | 1 | 39 | 6 meses | Reborde maxilar izquierdo | 5 cm | QT, RT y TARV | Remisión, 6 años |
| Francischini et al. (2008)20 | 1 | 42 | 4 meses | Encía maxilar izquierda | 3,5 cm | QT y RT | Murió 6 meses después de abandonar el tratamiento |
| Gaidano et al. (2002)21 | 10 | 25-57 | - | Cavidad oral | - | QT y 4 con TARV | 7 muertos entre el 1-7 meses/3 remisión entre 26 y 51 meses que estaban en TARV |
| Hagiwara et al. (2011)34 | 1 | 51 | - | Encía maxilar izquierda | - | QT, RT, TARV | Remisión, 16 meses después del tratamiento |
| Hassan et al. (2007)9 | 1 | 49 | 2 meses | Mandíbula derecha | 5×4 cm | - | - |
| Hewson (2011)22 | 1 | - | 2 meses | Asociado a diente 36 | - | QT/RT/TARV | Murió 14 meses despues de la última QT |
| Hirosawa et al. (2015)8 | 1 | 58 | - | Orofaringe | - | QT y Bortezomib | Murió 4 meses después del diagnóstico |
| Lester et al. (2004)23 | 2 | 50/33 | 4 meses/2 meses | Maxilar anterior y paladar/mandibular izquierdo | 5 cm/7 cm | QT/QT | Remisión 2 años/remisión 10 meses |
| Makis et al. (2011)24 | 1 | 46 | - | Seno maxilar, paladar y reborde maxilar derecho | - | QT/TARV | - |
| Medel et al. (2014)25 | 1 | 52 | 4 semanas | Maxilar izquiedo | 2×2 cm | QT/RT | Murió 16 meses después del diagnóstico |
| Moayedi et al. (2012)26 | 1 | 43 | 6 meses | Labio superior | 1 cm aprox | QT | Remisión |
| Panos et al. (2006)27 | 1 | 30 | 1 semana | Encía maxilar derecha | < 0,4 cm | QT /TARV | Remisión, 61 meses |
| Perez et al. (2015)28 | 1 | 34 | 2 meses | Encía maxilar posterior derecha | - | TARV/QT | Remisión, 1 año |
| Porter et al. (1999)29 | 1 | 36 | 2 semanas | Maxilar izquierdo posterior | 3 cm | QT y TARV | Remisión, 2 años |
| Radhakrishnan et al. (2005)30 | 1 | 7 | 20 días | Maxilar izquierdo | 4×3cm | - | - |
| Riedel et al. (2008)31 | 1 | 39 | - | Mandibular izquierdo | 2×2cm | QT y TARV | - |
| Sarode et al. (2009)35 | 1 | 40 | 2 meses | Mandíbula izquierda posterior | 3 cm | QT/RT | Murió 8 meses despues del diagnóstico |
| Sirsath et al. (2016)33 | 2 | 35/55 | - | Reborde alveolar/lengua | - | QT y TARV/QT y RT | Perdido/remisión, 33 meses |
| Stander et al. (2013)32 | 1 | 25 | 5 meses | Paladar | Paladar completo | QT | - |
| Tsachouridou et al. (2012)36 | 2 | 43/50 | 1 año/- | Paladar duro/mandíbula derecha | 1 cm/8cm aprox. | QT y RT/QT | Remisión 12 meses Murió (recidiva a los 6 meses y rechazo del tratamiento) |
| Vieira et al. (2008)37 | 1 | 38 | 4 meses | Maxilar región anterior | 4 cm | RT, rechazó QT | Vivo, recidiva a los 11 meses en el útero |
QT: quimioterapia; RT: radioterapia; TARV: terapia antirretroviral.
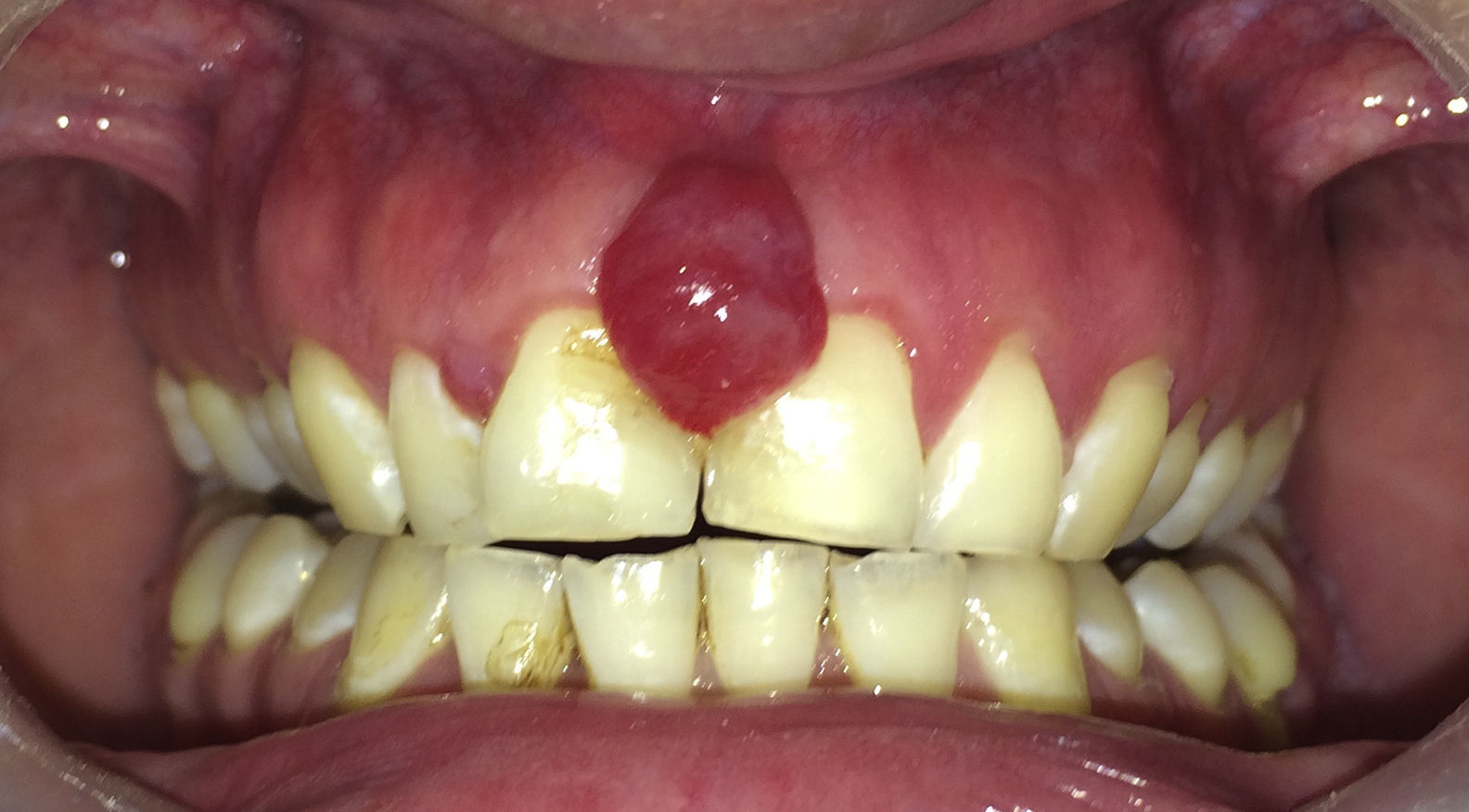
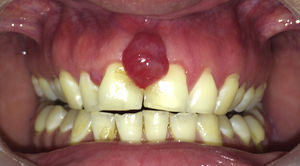
Paciente de 30 años de edad, sexo masculino, con antecedente de inmunodeficiencia adquirida, en tratamiento antirretroviral, con un recuento de linfocitos T CD4 de 198 cel/mm3, derivado al Servicio de Cirugía Maxilofacial por aumento de volumen intraoral, localizado entre dientes centrales maxilares, de 15 días de evolución, doloroso a estímulos mecánicos. Al examen, presentaba un aumento del volumen interincisal en encía marginal de 8mm de diámetro, eritematoso y sangrante al contacto (fig. 1).
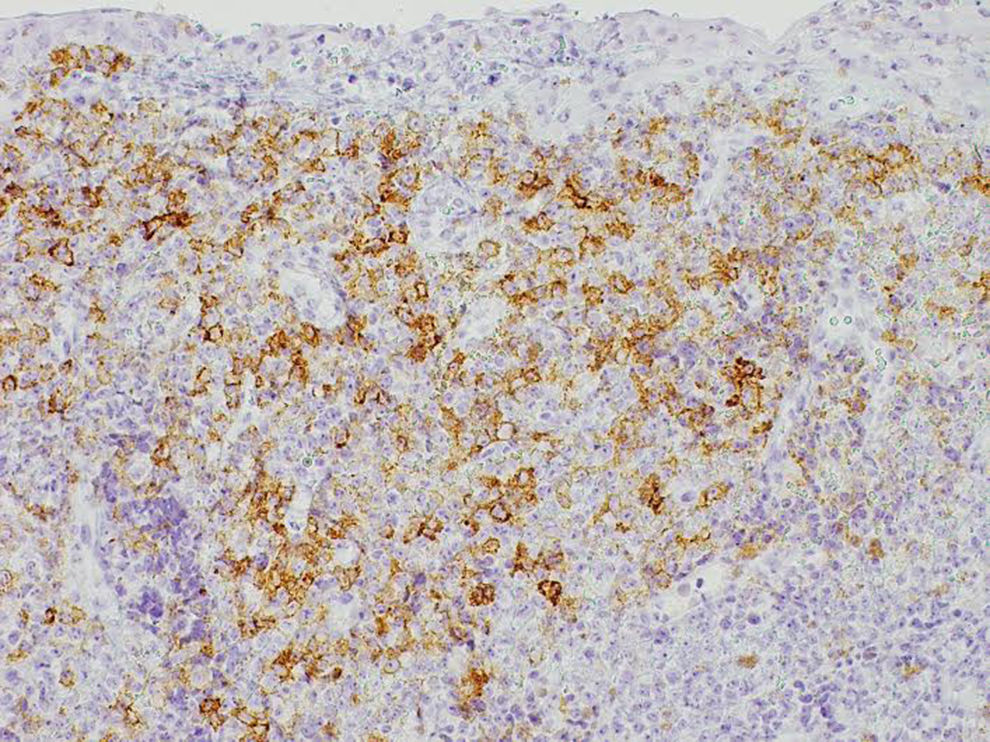
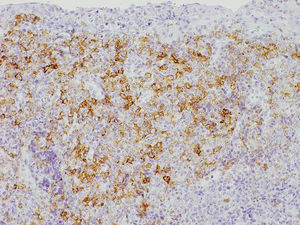
Se realizó una biopsia escisional y se indicó controlar la placa bacteriana, con el diagnóstico presuntivo de granuloma piogénico. El resultado de la biopsia indicó lesión con infiltrado inflamatorio inespecífico. Un mes más tarde, presentó lesión recidiva en el mismo sitio anatómico, sin embargo, esta vez tenía de un diámetro mayor (1,2cm) y era transfixiante hacia palatino. Se repitió la biopsia escisional, que permitió determinar al examen macroscópico una lesión de 0,9×0,6cm; el estudio inmunohistoquímico reveló mucosa oral con extenso infiltrado de células linfoides, plasmocitoides atípicas de tamaño grande. Presentaba expresión positiva para CD30, CD45 y EMA (fig. 2). Fue negativo para CD3, CD20 y CD79a. El Ki67 fue cercano al 100%, con una alto rango de proliferación. Con el diagnóstico definitivo de LPB, se realizó la derivación a Hematooncología, quienes descartaron metástasis y se comenzó quimioterapia de 4 ciclos cada 3 semanas con vincristina (2mg), ciclofosmamida (1.300mg), doxorrubicina (87mg) y prednisona (70mg).
El paciente se presentó asintomático hasta 9 meses después de finalizado el último ciclo de quimioterapia, cuando cursó con una lesión de similares características clínicas entre el incisivo lateral y central maxilar de 0,3cm de diámetro mayor. La biopsia escisional indicaba proceso linfoproliferativo de alto grado; sin embargo, el estudio inmunohistoquímico, debido al tamaño de la lesión, no fue concluyente. Dados los antecedentes del paciente, se inició el ciclo de quimioterapia de rescate: se mantiene sin recidivas hasta la fecha.
DiscusiónEl LPB es un subtipo de linfoma no Hodgkin (LNH), originalmente descrito como una variante de linfoma de células grandes B diagnosticado en la mucosa oral en pacientes con infección de VIH1.
En origen fue descrito como una entidad que se presentaba específicamente en la cavidad oral de pacientes con inmunodeficiencia, pero una serie de casos han sido descritos en otras localizaciones extraorales como linfonodos, nasofaringe, estómago, intestino delgado, ano, pulmones, tejido óseo y otros2,3. A su vez, también han sido reportados algunos casos en pacientes inmunocompetentes4.
En el caso descrito, nuestro paciente es de sexo masculino, de 30 años de edad con antecedentes de VIH, con un recuento de linfocitos CD4 de 198 cel/mm3, por lo que se encontraba más propenso a infecciones y enfermedades oportunistas. El LPB representa un 2,6% de todos los LNH asociados a VIH5, y se presenta en un 90% de los casos en pacientes con VIH, sin predilección significativa por sexo ni edad2. Sin embargo, también se ha reportado que presenta una predilección por el sexo masculino6, con una relación de hombre: mujer de 5,7:1 en su presentación intraoral y de 4:1 en su presentación extraoral2.
Los LNH en la cavidad oral que se describen en la literatura pueden presentar aumento de volumen o masa exofítica, ulceración, retraso en la cicatrización en sitios de extracción y neuropatía trigeminal. Es importante distinguir este tipo de linfoma confinado a la mucosa gingival de otras lesiones, ya que el LPB puede asemejarse a lesiones benignas/reactivas como el granuloma telangectásico o el granuloma periférico de células gigantes7. La presentación clínica del LPB intraoral es descrita como una masa localizada, dolorosa y de rápido crecimiento, lo que se explica por su alto índice mitótico8, y que puede infiltrar hueso adyacente, por lo que es un cuadro clínico que se puede confundir con el sarcoma de Kaposi2. Además, se debe diferenciar el LPB de otros subtipos de LNH de células B, como el linfoma difuso de células B grandes y el linfoma de Burkitt9. En el presente caso, las características de la lesión concuerdan con lo descrito previamente, al ser un aumento de volumen que se localizaba en la encía marginal interincisal de los centrales maxilares, de una rápida evolución (15 días), lesión que era eritematosa y sangrante a la exploración.
El estudio histopatológico de la lesión reveló un extenso infiltrado de células linfoides, plasmocitoides y atípicas de gran tamaño, mientras que el estudio inmunohistoquímico presentó expresión positiva para CD30, CD45 y EMA, y negativa para CD3, CD20 y CD79a. Además, su Ki67 fue cercano al 100%. Con relación a las características histopatológicas del LPB, se describe la proliferación de un gran número de células linfoides de gran tamaño y dispuestas en un patrón de sábanas. Las células tumorales muestran, o una mínima expresión, o una expresión negativa de antígenos de células B y de antígeno leucocitario común como el CD20, CD79a y PAX-510, una expresión débil para CD4511 y una alta expresión de antígenos como CD38, CD138, VS38c y MUM15,12,13. También presenta positividad variable para CD30 y marcadores epiteliales y endoteliales como el EMA y el CD31, con lo que puede generar dificultades diagnósticas para distinguirlo de tumores sólidos poco diferenciados14. La ausencia de antígenos CD20 permite diferenciarlo de otros tumores agresivos de células B en los cuales este es fuertemente positivo2. La expresión aberrante de marcadores de células T, como el CD3 y el CD4, también han sido descritas15–17. Finalmente la expresión de Ki67 se describe superior al 70%18.
Con relación al tratamiento de esta entidad, no se encuentra establecido un protocolo de tratamiento definido, dada su baja incidencia10. Hasta ahora los pacientes han sido tratados de forma heterogénea y, dentro de las alternativas terapéuticas se describe el uso de quimioterapia usando CHOP o regímenes similares, radioterapia, radioterapia/quimioterapia y también la escisión quirúrgica de la lesión, sumada a las terapias mencionadas anteriormente19,20. El pronóstico de la lesión se describe como pobre a pesar del tratamiento, independientemente del sitio de presentación y del escenario clínico (VIH positivo o inmunocompetente)2,19. También se ha descrito el uso de terapia antirretroviral altamente activa como una alternativa terapéutica adicional21, aunque hay otros estudios que, con regímenes más intensos que el CHOP, no se asociaron a una mejor sobrevida9. El pronóstico del LPB es desfavorable, independientemente del tratamiento. Presenta una sobrevida descrita de 1-24 meses y una mortalidad promedio de 6 meses19,22.
ConclusiónEn general, es un desafío diagnóstico: tanto sus características clínicas como histológicas son ambiguas, lo que reduce la capacidad de un diagnóstico certero y rápido. Esta enfermedad necesita un tratamiento intensivo, centrado en la quimioterapia. Aunque tiene mal pronóstico, este dependerá del estadio del linfoma, de la edad, de la gravedad de la inmunodeficiencia y del estado funcional del paciente.
Conflicto de interesesLos autores del presente artículo no tenemos conflicto de interés con ninguno de los aspectos presentados en este caso clínico o relacionados con él.
Por la consideración por nuestro trabajo, al Hospital San Juan de Dios, campo clínico de la Universidad de Chile, junto a sus colaboradores.