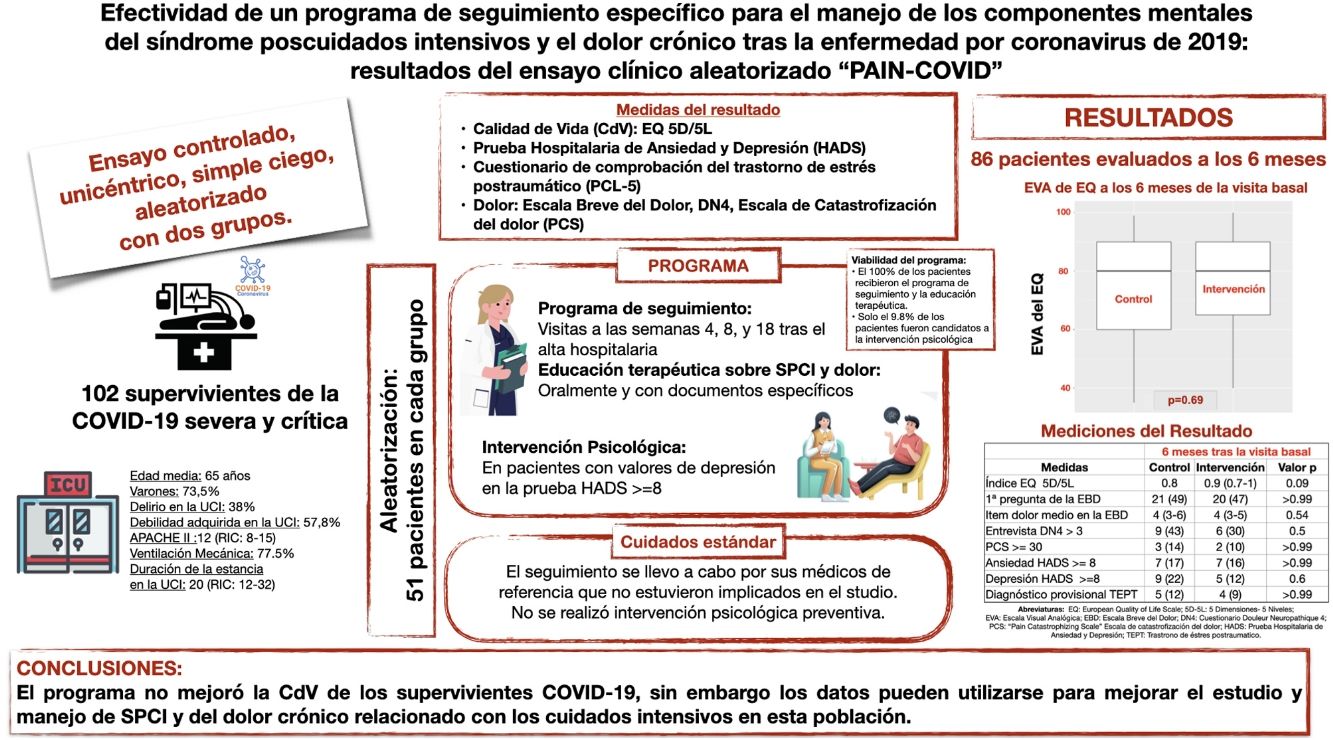
Los supervivientes de la COVID-19 crítica tienen riesgo de desarrollar síndrome poscuidados intensivos (SPCI) y dolor crónico relacionado con la UCI (CIRP). Nuestro objetivo fue comparar si los cuidados específicos mejoran la calidad de vida (CdV) de los pacientes con riesgo de desarrollar SPCI y CIRP tras la COVID-19.
MétodosEl DOLOR-COVID se trató de un ensayo controlado aleatorizado de grupo paralelo, unicéntrico y uniciego. La intervención consistió en un programa de seguimiento, educación al paciente sobre SPCI y dolor, y una intervención psicológica basada en el modelo de autocontrol de Rehm en pacientes con puntuación de depresión anormales (≥8 de la Hospital Anxiety and Depression Scale [HADS]) en la visita basal. La CdV fue evaluada mediante EQ 5D de 5 niveles (EQ 5D 5L), los trastornos del ánimo con HADS, el trastorno de estrés postraumático (TEPT) con la lista de comprobación PCL-5 y el dolor con el formulario abreviado Brief Pain Inventory (BPI), el cuestionario Douleur Neuropathique 4 (DN4) y Pain Catastrophizing Scale (PCS). El resultado primario fue determinar si el programa era superior al estándar de cuidados en la escala visual analógica (EVA) de EQ transcurridos 6 meses de la visita basal. Los resultados secundarios fueron EVA de EQ transcurridos 3 meses y el índice EQ, la incidencia y las características de CIRP, así como ansiedad, depresión y TEPT transcurridos 6 meses de las visitas basales.
ConclusionesEste programa no fue superior a los cuidados estándar para mejorar la CdV en los supervivientes de COVID-19 crítica, según la medición EVA de EQ. Sin embargo, nuestros datos pueden ayudar a establecer mejores estrategias para el estudio y manejo de SPCI y CIRP en esta población.
Registro del ensayo: # NCT04394169; registrado el 19 de mayo de 2020.
Critical COVID-19 survivors are at risk of developing Post-intensive Care Syndrome (PICS) and Chronic ICU-Related Pain (CIRP). We determined whether a specific care program improves the quality of life (QoL) of patients at risk of developing PICS and CIRP after COVID-19 disease.
MethodsThe PAIN-COVID trial was a parallel-group, single-centre, single-blinded, randomized controlled trial. The intervention consisted of a follow up program, patient education on PICS and pain, and a psychological intervention based on Rehm's self-control model in patients with abnormal depression scores (>=8) in the Hospital Anxiety and Depression Scale (HADS) at the baseline visit. QoL was evaluated with the 5-level EQ 5D (EQ 5D 5L), mood disorders with the HADS, post-traumatic stress disorder (PTSD) with the PCL-5 checklist, and pain with the Brief Pain Inventory short form, the Douleur Neuropathique 4 questionnaire, and the Pain Catastrophizing Scale. The primary outcome was to determine if the program was superior to standard-of-care on the EQ visual analogue scale (VAS) at 6 months after the baseline visit. The secondary outcomes were EQ VAS at 3 months, and EQ index, CIRP incidence and characteristics, and anxiety, depression, and PTSD at 3 and 6 months after baseline visits.
ConclusionsThis program was not superior to standard care in improving QoL in critical COVID-19 survivors as measured by the EQ VAS. However, our data can help establish better strategies for the study and management of PICS and CIRP in this population.
Trial registration: # NCT04394169, registered on 5/19/2020.
La pandemia de SARS-CoV-2ha incrementado considerablemente el número de pacientes hospitalizados y, en particular, aquellos ingresados en la unidad de cuidados intensivos (UCI). Es bien sabido que los supervivientes de UCI pueden experimentar un deterioro significativo de su salud mental y física, así como de su calidad de vida (CdV)1. En 2012 La Sociedad de cuidados críticos definió el síndrome poscuidados intensivos (SPCI) mediante un término para referirse a la nueva aparición de problemas físicos o mentales a largo plazo en los pacientes críticos tras recibir el alta de la UCI2. Recientemente, se ha reportado que los supervivientes de COVID-19 crítica refirieron con frecuencia síntomas físicos, mentales y cognitivos durante el plazo de un año desde el ingreso en la UCI3. También se ha observado una alta prevalencia de dolor crónico de moderado a extremo en los supervivientes de enfermedades críticas4, habiéndose sugerido la expresión «dolor crónico relacionado con la UCI» (CIRP) para describir el dolor que persiste durante al menos 3 meses tras el alta de la UCI4. Dichos problemas tienen una relación recíproca, habiendo sido asociados a un peor pronóstico5.
A pesar de la gran población susceptible de desarrollar SPCI y CIRP en los pacientes de COVID-19, con un alto impacto asociado en términos de CdV y costes económicos, a nuestro saber hay pocos estudios6,7 que hayan evaluado la eficacia de una intervención preventiva para mejorar el bienestar tras el alta en los pacientes de COVID-19.
Por tanto, conjeturamos que un programa de seguimiento específico que incluya educación terapéutica e intervención psicológica puede mejorar la CdV de los pacientes de COVID-19 con riesgo de desarrollar SPCI y CIRP. El resultado primario del estudio fue determinar si el programa específico es superior a los cuidados estándar para mejorar la CdV, según la medición de la EVA de EQ, transcurridos 6 meses de la visita inicial. Los resultados secundarios incluyen la evaluación de la influencia del programa de intervención con EVA de EQ transcurridos 3 meses, el índice EQ, la incidencia y características de CIRP, así como las incidencias de ansiedad, depresión y TEPT transcurridos 3 y 6 meses de las visitas basales.
Material y métodosDiseño del estudioEl ensayo PAIN-COVID es un ensayo ciego, aleatorizado, controlado y de superioridad de 2 grupos paralelos, realizado en el Hospital Clinic de Barcelona, España. Fue aprobado por el Comité Ético de Investigación Clínica del Hospital Clinic de Barcelona (HCB/2020/0549) y registrado el 9 de mayo de 2020 en http://www.clinicaltrials.gov. (NCT04394169). El protocolo del estudio ha sido previamente descrito8.
Pacientes elegiblesFueron elegibles para participar los supervivientes adultos de la enfermedad por COVID-19 severa y crítica, confirmada mediante pruebas basadas en la reacción en cadena de la polimerasa con al menos uno de los siguientes criterios de inclusión: 1) puntuación Acute Physiology and Chronic Health Evaluation II superior a 14; 2) estancia en la UCI superior a 10 días; 3) debilidad adquirida en la UCI (definición del suplemento D1); y 4) delirio durante el ingreso en la UCI (definición del suplemento D2). Dichos criterios coincidieron con los previamente recomendados para el programa de monitorización y rehabilitación de pacientes críticos9. Se añadió el delirio, ya que ha sido asociado a peores resultados en múltiples estudios10.
Los criterios de exclusión fueron: 1) enfermedades degenerativas del sistema nervioso central (definición del suplemento D3); 2) estado terminal (definición del suplemento D4); 3) comprensión insuficiente del idioma español; 4) dificultad para completar el seguimiento (distancia al domicilio>50km desde el hospital); y 5) no aportación de consentimiento informado.
AleatorizaciónSe asignó a los pacientes a los grupos control o intervención en proporción 1:1, de acuerdo con un listado de números aleatorios generados informáticamente. Los datos para el cribado se obtuvieron de las historias clínicas.
Protocolo del estudioSe comparó el programa de intervención con la práctica clínica del estándar de cuidados. La intervención incluyó un programa de seguimiento, educación terapéutica acerca de SPCI y dolor, y una intervención psicológica en los pacientes con valores anormales de depresión (≥8) de la Hospital Anxiety and Depression Scale (HADS) en la visita basal (cuestionario del suplemento Q1).
CegamientoLas visitas fueron realizadas por un investigador con formación adecuada en términos de administración de cuestionarios, que no participó en la intervención o la evaluación de los resultados. El programa de seguimiento y educación terapéutica fueron realizados por un facultativo, con conocimiento sobre SPCI y CIRP (AO) y la intervención psicológica fue realizada por 2 psicólogos (MMSR y ACC). Dichos investigadores no participaron en el cuestionario ni en la recopilación de los datos basales. A los investigadores que analizaron los resultados se les ocultó el brazo de las aleatorizaciones.
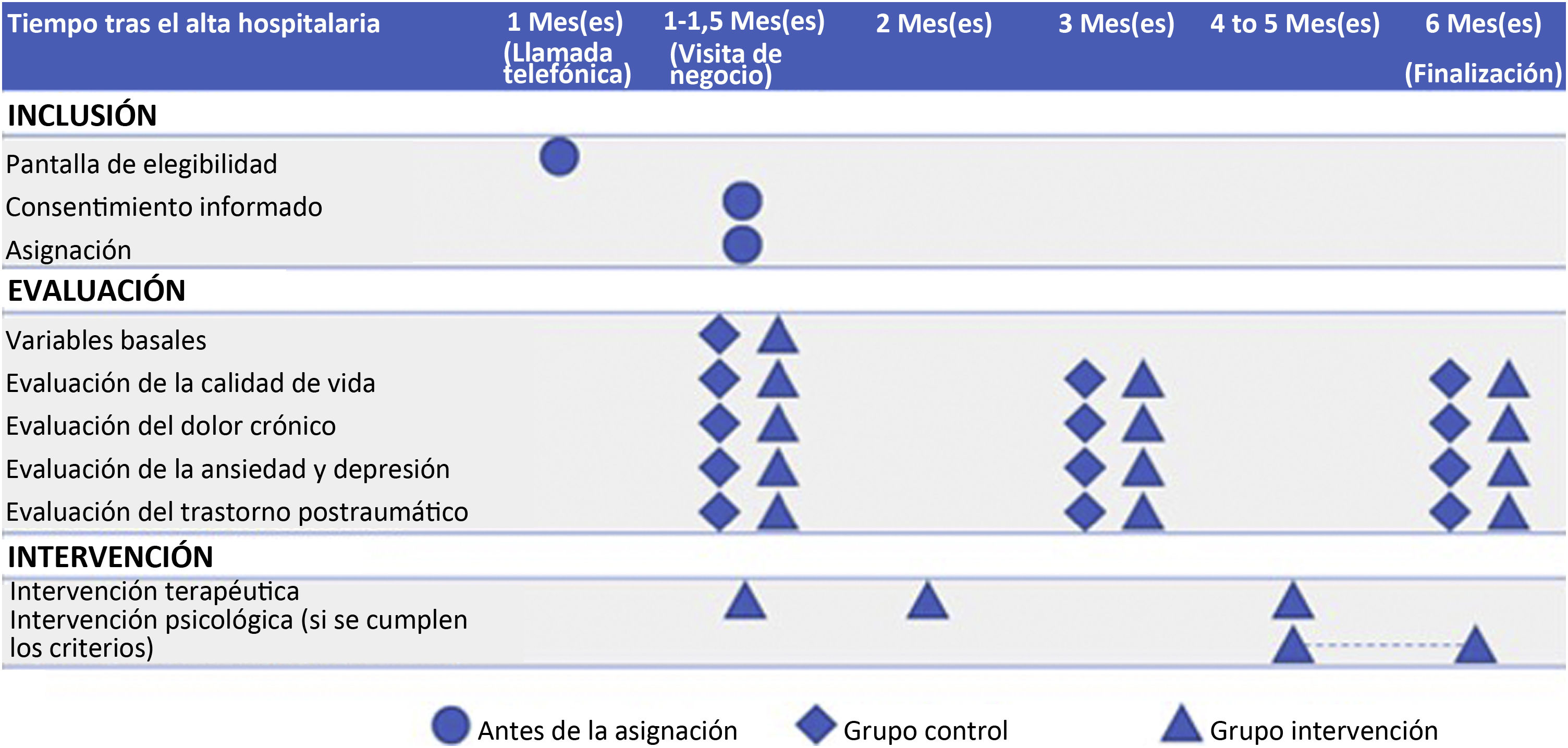
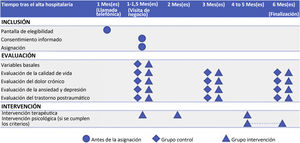
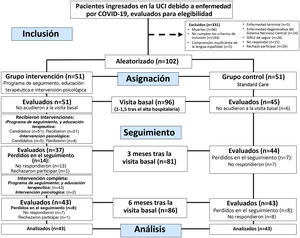
Selección de los participantes y calendarioTodos los pacientes que recibieron el alta de la UCI fueron identificados utilizando la base de datos clínicos del sitio. Aquellos que fueron elegibles fueron contactados transcurrido un mes del alta hospitalaria, para determinar su interés en participar en el estudio, obteniéndose su consentimiento informado. Una vez obtenido este se aleatorizó a los pacientes. La figura 1 muestra el calendario de los participantes en el estudio.
Visita basal (V1): a todos los pacientes se les programó una visita presencial basal durante la cual se recopilaron las variables referentes a datos demográficos, historia médica, UCI y hospitalización. Las definiciones de dichas variables pueden encontrarse en el material suplementario. Para evaluar la CdV, ansiedad, depresión, TEPT y características del dolor de los pacientes se administraron diferentes escalas, incluyendo EQ 5D/5L, HADS, cuestionario PCL-5, cuestionario Brief Pain Questionnarie (BPI), cuestionario de entrevista Dolour Neuropathique 4 (DN4) y Pain Catastrophizing Scale (PCS). Pueden encontrarse explicaciones detalladas de cada prueba en la sección de medidas del resultado y el material suplementario. Previamente a la respuesta a los cuestionarios se realizó la prueba Mini-Mental State Exam (MMSE), que es ampliamente utilizada para evaluar la función cognitiva entre los mayores, que analiza la orientación, atención, memoria, lenguaje y habilidades visuales-espaciales.
Visitas de seguimiento (V2, V3): dichas visitas fueron realizadas telefónicamente transcurridos 3 y 6 meses (visita final) de la visita basal. Durante dichas visitas los participantes completaron la prueba de medida de los resultados: EQ 5D/5L, HADS, PCL-5, BPI-SF, cuestionario de entrevista DN4 y PCS.
Grupo intervenciónPrograma de seguimiento específico y educación terapéuticaConsistió en 3 sesiones presenciales (tabla 1 del material suplementario):
Sesión 1: programada transcurridas 4 semanas del alta, de acuerdo con las recomendaciones publicadas9. La sesión tuvo una duración de 60minutos y consistió en una entrevista estandarizada y un examen físico para evaluar la situación del paciente. Sobre la base de los hallazgos se aconsejó a los pacientes que solicitaran seguimiento especializado. Además, dicha sesión marcó el inicio de la educación terapéutica sobre SPCI y dolor, que se explicará con detalle en las secciones siguientes.
Sesiones 2 y 3: dichas sesiones fueron programadas transcurridas 8 y 18 semanas del alta, respectivamente. Tuvieron una duración de 30minutos e incluyeron una entrevista estandarizada para evaluar cualquier síntoma nuevo relacionado con SPCI y el dolor crónico. Se aconsejó a los pacientes que solicitaran ayuda de un especialista si presentaban nuevos hallazgos, o si no habían sido evaluados por el especialista adecuado. En dicha sesión también se evaluó si el paciente había leído y completado el manual de rehabilitación entregado11. Si el paciente reportaba dolor, se proporcionó educación terapéutica específica sobre la gestión del mismo.
Se proporcionó educación terapéutica sobre SPCI de forma oral y mediante documentos específicos, que incluyeron una hoja descriptiva desarrollada por los investigadores («Otros documentos 1» del material suplementario) y un manual de rehabilitación desarrollado por el grupo Jones del Hospital Universitario St. Helens and Knowsley del Reino Unido, que fue recomendado por el Comité de rehabilitación y seguimiento de la Sociedad Argentina de Cuidados Intensivos. Dicho manual de rehabilitación consiste en 3 secciones: la primera de ellas contiene un programa de rehabilitación de 6 semanas, la segunda aporta recomendaciones e información acerca de los problemas comunes que pueden surgir tras los cuidados intensivos y la tercera sección destaca el programa de ejercicios que deberá seguirse durante el proceso de rehabilitación11. A los sujetos se les solicitó que leyeran detenidamente los documentos y completaran el manual de rehabilitación en casa.
Se proporcionó oralmente a todos los sujetos el Programa de educación terapéutica sobre el dolor (tabla 2 del material suplementario). Se les proporcionó información sobre el objetivo del dolor agudo y las diferencias entre dolor agudo y crónico. Además, se les explicó que el dolor sirve como mecanismo de protección en lugar de ser únicamente un síntoma del daño. A los sujetos que reportaron una nueva aparición del dolor se les proporcionó información adicional, que incluyó el modo en el que el dolor puede convertirse en crónico, la importancia del diagnóstico y tratamiento adecuados del dolor neuropático, el uso racional de los analgésicos prescritos, las estrategias para mantener las actividades diarias a la vez que se experimenta dolor, la importancia del manejo preventivo del dolor para una rehabilitación adecuada, la sensibilización central y sus causas y la relación entre estrés, emociones y dolor crónico. Las sesiones fueron diseñadas para animar a las preguntas y comentarios de los pacientes, enfatizando la información individualizada. Las materias cubiertas en este programa se basaron en la educación sobre neurociencia del dolor, que tiene evidencia científica sólida para mejorar los resultados de diversos síndromes crónicos del dolor12.
Intervención psicológicaEl protocolo de intervención consistió en 7 sesiones semanales de una hora y media cada una (tabla 3 del material suplementario). La intervención de depresión se basa en el modelo de Rehm de intervenciones psicológicas de autocontrol. Las intervenciones psicológicas pueden causar episodios adversos que originen un empeoramiento del curso clínico de los pacientes (sobredosis, autolesión e intentos de autolesión). Por tanto, los investigadores monitorizaron cualquier síntoma relacionado, lo reportaron como episodio adverso y derivaron al paciente para tratamiento en una unidad especializada.
Se consideró que el paciente había completado la intervención si había asistido al menos al 66% de las visitas presenciales programadas (2 de 3 para el programa de seguimiento y visitas de educación terapéutica y 5 de 7 visitas de intervención psicológica).
Grupo controlLos pacientes del estudio a quienes se proporcionaron cuidados locales estándar, que incluyeron citas de seguimiento rutinarias con sus médicos de referencia (atención primaria o especialistas) no estuvieron directamente implicados en el estudio. El estudio no interfirió en los cuidados médicos habituales o planes terapéuticos de los pacientes. No se administró intervención psicológica preventiva a los pacientes como parte del estudio. Por tanto, cualquier asesoramiento psicológico o terapia recibidos por los pacientes formaron parte de sus cuidados regulares, no siendo un componente del estudio.
Medidas del resultadoEl impacto del programa de intervención sobre la CdV fue evaluado mediante EQ 5D/5L (Cuestionario Q2 del material suplementario). Dicho cuestionario evalúa 5 dominios de la CdV: movilidad, autocuidado, actividades normales, dolor/malestar, ansiedad/depresión, puntuados sobre una escala de 1 (ausencia de problemas) a 5 (indicativo de problemas extremos), que genera un código de 5 dígitos correspondiente a la CdV. También se evaluó la escala visual analógica de la misma prueba (de 0 —peor salud imaginable— a 100 —mejor salud imaginable—).
Para evaluar el dolor (presencia e intensidad) se utilizó el cuestionario BPI (Cuestionario Q3 del material suplementario). Se trata de un cuestionario multidimensional que evalúa la intensidad del dolor en las últimas 24horas (peor, mejor y medio) y actual (ahora). De acuerdo con las recomendaciones IMMPACT se define el dolor clínicamente significativo cuando la media del ítem de dolor de BPI es superior o igual a 313. La definición de nueva aparición de dolor fue una respuesta afirmativa a la primera pregunta del cuestionario BPI-SF. De ser positiva la respuesta el investigador confirmó que no existía dolor antes del ingreso en la UCI o antes de la infección por COVID-19. Se indicó a los pacientes que no consideraran los síntomas agudos de la COVID cuando les preguntaran si habían tenido dolor antes del ingreso en la UCI. De ser BPI positivo para el dolor se evaluaron la catastrofización y el dolor neuropático (DN) mediante PCS (Cuestionario Q4 del material suplementario) y la entrevista de la prueba DN4 (entrevista DN4) (Cuestionario Q5 del material suplementario), respectivamente. Una puntuación PCS superior o igual a 30 se consideró un nivel clínicamente relevante de catastrofización. Se consideró la presencia de DN cuando la puntuación de la entrevista DN4 fue superior o igual a 3.
El impacto del programa de intervención en la incidencia de ansiedad o depresión se evaluó mediante la prueba HADS (Cuestionario Q1 del material suplementario). Se utilizó un punto de corte igual o superior a 8 para valores anormales de ansiedad o depresión14. Por último, la incidencia de TEPT se evaluó mediante el cuestionario de comprobación de TEPT (Cuestionario Q6 del material suplementario) (PCL-5).
Métodos estadísticosTamaño de la muestraSe presentaron el protocolo del estudio y el plan de análisis estadístico antes de la inclusión8. El tamaño muestral se calculó suponiendo una media de 50 puntos en la EVA de EQ en el grupo control y una diferencia clínicamente relevante entre los grupos del 20%. Para la distribución de una cola con error de tipo i de 0,05 y potencia del 80%, calculamos un tamaño muestral de 84 pacientes, 42 para cada brazo. Calculando una pérdida en el seguimiento del 20% necesitaríamos un tamaño muestral de 102 pacientes (51 en cada grupo).
Análisis de los datosLas variables cualitativas se presentaron como proporciones, mientras que para las variables cuantitativas se presentaron media (desviación estándar) o mediana (rango intercuartílico), tras revisar la normalidad utilizando la prueba de Shapiro-Wilk. Para comparar las variables entre los grupos se realizaron pruebas «t» de Student o U de Mann-Whitney para los datos continuos, y Chi cuadrado para las variables categóricas. Antes de realizar la prueba de hipótesis paramétrica se estudió la igualdad de las varianzas utilizando la prueba de Levene y, de no cumplirse los supuestos, se realizaron contrastes mediante la prueba de Welch. Se siguió el enfoque de intención de tratar. Se presentaron valores P bilaterales y un nivel de significación de 0,05. Para los resultados secundarios se realizó un ajuste con el procedimiento de Benjamini-Hochberg. Se realizó un subanálisis del efecto del tratamiento en los cumplidores para el resultado principal, definiéndose los cumplidores como aquellos sujetos que, siendo aleatorizados para la intervención, completaron al menos 2 de 3 visitas médicas y al menos 5 de 7 intervenciones psicológicas. Para el análisis estadístico se realizó un análisis de la variable instrumental. El análisis estadístico se realizó utilizando el software estadístico R.
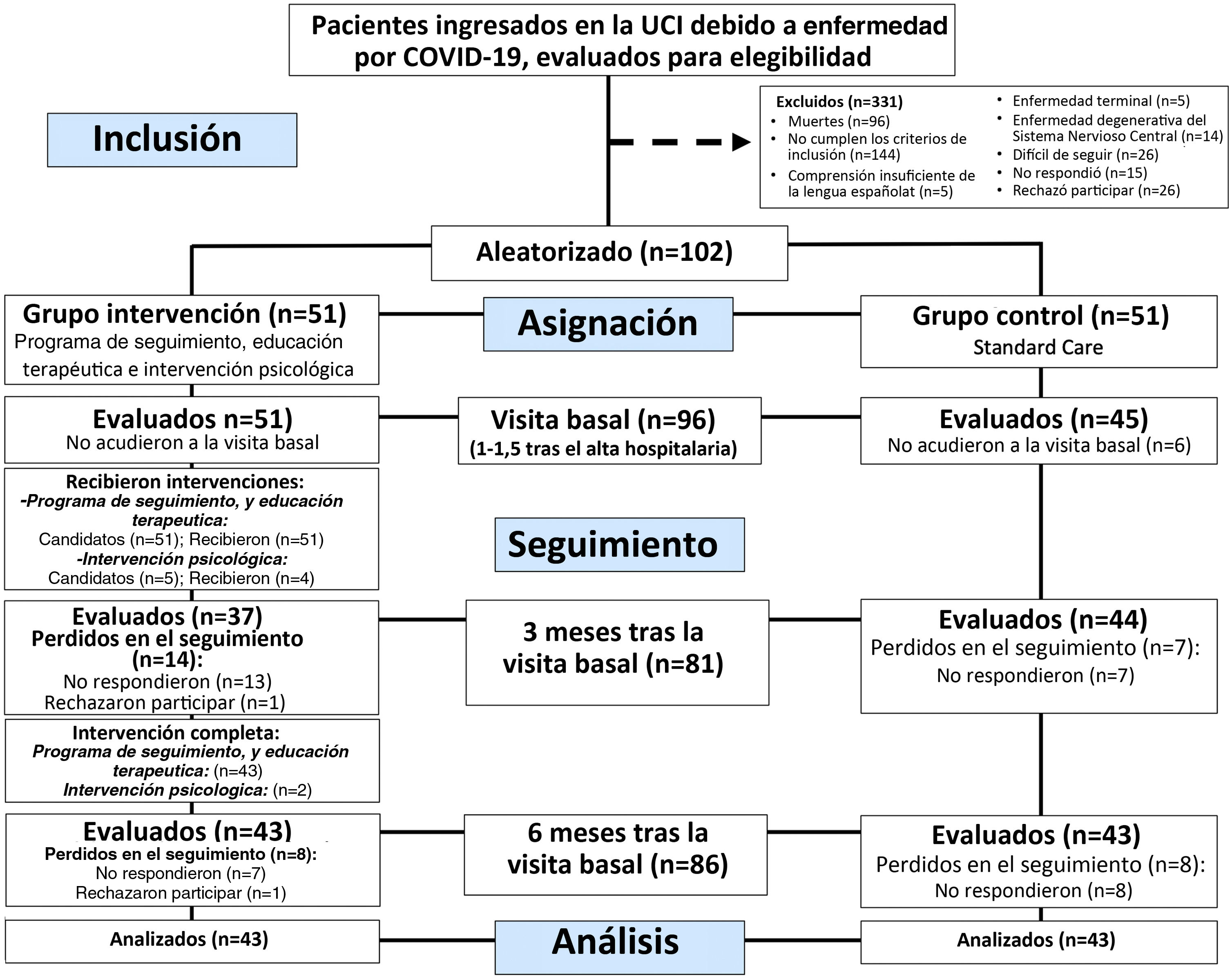
ResultadosParticipantesLa selección se inició el 27 de mayo de 2020 y finalizó el 26 de febrero de 2021, una vez logrado el tamaño muestral. Se evaluaron consecutivamente 433 pacientes para elegibilidad, de los cuales 144 no cumplieron los criterios de inclusión, excluyéndose 187 sobre la base de los criterios de exclusión. Finalmente, 102 pacientes accedieron a participar en el estudio y fueron aleatorizados, de los cuales 96 fueron evaluados en la primera visita (grupo intervención, n=51), 81 a los 3 meses (grupo intervención, n=37) y 86 a los 6 meses (grupo intervención, n=43) (fig. 2). La tasa de pérdida en el seguimiento a los 3 meses fue del 13,7% en el grupo control y del 27,5% (p=0,14) en el grupo intervención, a los 6 meses, teniendo ambos grupos la misma tasa de pérdida en el seguimiento (15,7%, p>0,99).
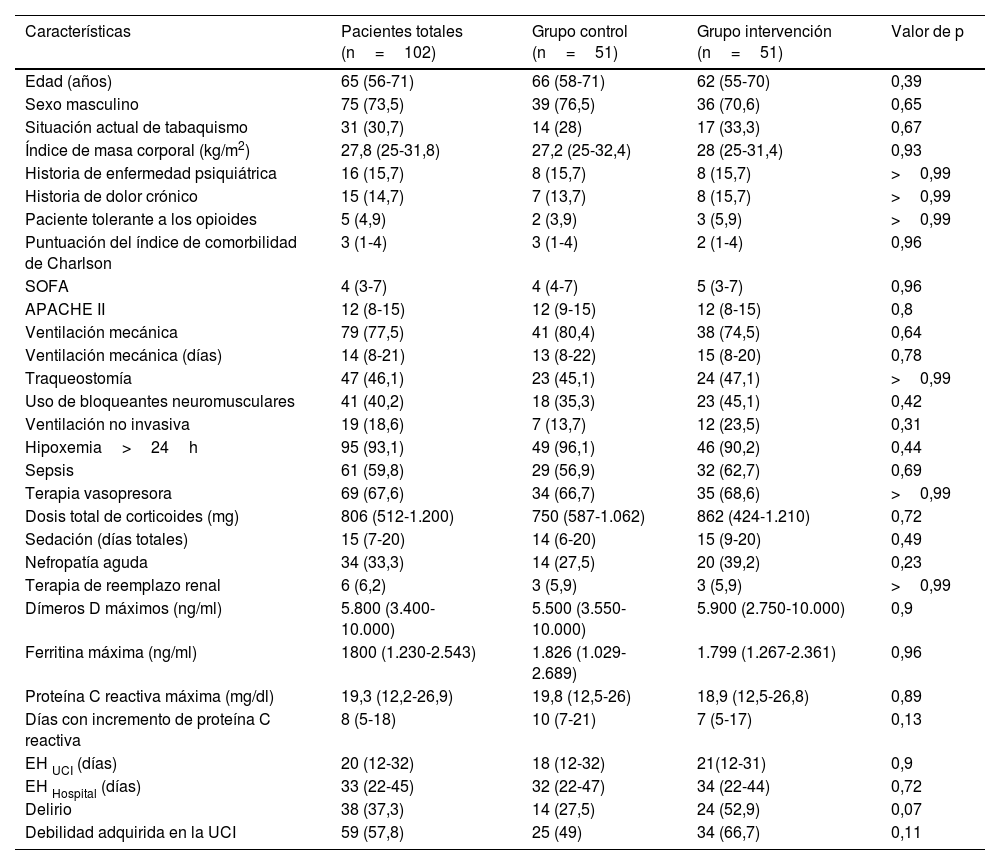
La tabla 1 recoge un resumen de las características basales de todos los pacientes seleccionados y la tabla 4 del material suplementario contiene un resumen de las características basales de todos los pacientes. Las características basales de todos los pacientes seleccionados y analizados fueron similares en ambos grupos.
Resumen de los datos demográficos y características de todos los pacientes incluidos
| Características | Pacientes totales (n=102) | Grupo control (n=51) | Grupo intervención (n=51) | Valor de p |
|---|---|---|---|---|
| Edad (años) | 65 (56-71) | 66 (58-71) | 62 (55-70) | 0,39 |
| Sexo masculino | 75 (73,5) | 39 (76,5) | 36 (70,6) | 0,65 |
| Situación actual de tabaquismo | 31 (30,7) | 14 (28) | 17 (33,3) | 0,67 |
| Índice de masa corporal (kg/m2) | 27,8 (25-31,8) | 27,2 (25-32,4) | 28 (25-31,4) | 0,93 |
| Historia de enfermedad psiquiátrica | 16 (15,7) | 8 (15,7) | 8 (15,7) | >0,99 |
| Historia de dolor crónico | 15 (14,7) | 7 (13,7) | 8 (15,7) | >0,99 |
| Paciente tolerante a los opioides | 5 (4,9) | 2 (3,9) | 3 (5,9) | >0,99 |
| Puntuación del índice de comorbilidad de Charlson | 3 (1-4) | 3 (1-4) | 2 (1-4) | 0,96 |
| SOFA | 4 (3-7) | 4 (4-7) | 5 (3-7) | 0,96 |
| APACHE II | 12 (8-15) | 12 (9-15) | 12 (8-15) | 0,8 |
| Ventilación mecánica | 79 (77,5) | 41 (80,4) | 38 (74,5) | 0,64 |
| Ventilación mecánica (días) | 14 (8-21) | 13 (8-22) | 15 (8-20) | 0,78 |
| Traqueostomía | 47 (46,1) | 23 (45,1) | 24 (47,1) | >0,99 |
| Uso de bloqueantes neuromusculares | 41 (40,2) | 18 (35,3) | 23 (45,1) | 0,42 |
| Ventilación no invasiva | 19 (18,6) | 7 (13,7) | 12 (23,5) | 0,31 |
| Hipoxemia>24h | 95 (93,1) | 49 (96,1) | 46 (90,2) | 0,44 |
| Sepsis | 61 (59,8) | 29 (56,9) | 32 (62,7) | 0,69 |
| Terapia vasopresora | 69 (67,6) | 34 (66,7) | 35 (68,6) | >0,99 |
| Dosis total de corticoides (mg) | 806 (512-1.200) | 750 (587-1.062) | 862 (424-1.210) | 0,72 |
| Sedación (días totales) | 15 (7-20) | 14 (6-20) | 15 (9-20) | 0,49 |
| Nefropatía aguda | 34 (33,3) | 14 (27,5) | 20 (39,2) | 0,23 |
| Terapia de reemplazo renal | 6 (6,2) | 3 (5,9) | 3 (5,9) | >0,99 |
| Dímeros D máximos (ng/ml) | 5.800 (3.400-10.000) | 5.500 (3.550-10.000) | 5.900 (2.750-10.000) | 0,9 |
| Ferritina máxima (ng/ml) | 1800 (1.230-2.543) | 1.826 (1.029-2.689) | 1.799 (1.267-2.361) | 0,96 |
| Proteína C reactiva máxima (mg/dl) | 19,3 (12,2-26,9) | 19,8 (12,5-26) | 18,9 (12,5-26,8) | 0,89 |
| Días con incremento de proteína C reactiva | 8 (5-18) | 10 (7-21) | 7 (5-17) | 0,13 |
| EH UCI (días) | 20 (12-32) | 18 (12-32) | 21(12-31) | 0,9 |
| EH Hospital (días) | 33 (22-45) | 32 (22-47) | 34 (22-44) | 0,72 |
| Delirio | 38 (37,3) | 14 (27,5) | 24 (52,9) | 0,07 |
| Debilidad adquirida en la UCI | 59 (57,8) | 25 (49) | 34 (66,7) | 0,11 |
Datos expresados en números y proporciones (%) para las variables categóricas y mediana y rango intercuartílico (RIC) para las variables continuas. APACHE II: evaluación de la salud fisiológica crónica y aguda ii; EH: duración de la estancia; SOFA: puntuación de evaluación de fallo orgánico secuencial; ventilación no invasiva: pacientes sin intubación a lo largo del proceso; p: el valor hace referencia a la comparación estadística entre los pacientes del “grupo intervención” y el “grupo control.
Todos los pacientes asignados al grupo intervención recibieron el programa de seguimiento y educación terapéutica. Ocho pacientes fueron considerados no cumplidores (solo acudieron a una visita médica), de los cuales 6 pacientes reportaron no tener tiempo para acudir a las visitas, un paciente refirió no querer asistir a las visitas y otro fue hospitalizado en el momento de las visitas médicas.
Intervención psicológicaSolo 5 pacientes fueron candidatos para recibir intervención psicológica específica, dado que la escala de depresión HADS era igual o superior a 8 en la evaluación basal. De dichos sujetos uno ya seguía tratamiento psicológico por trastorno de uso de sustancias. De los 4 pacientes restantes solo 2 acudieron a más de 5 visitas.
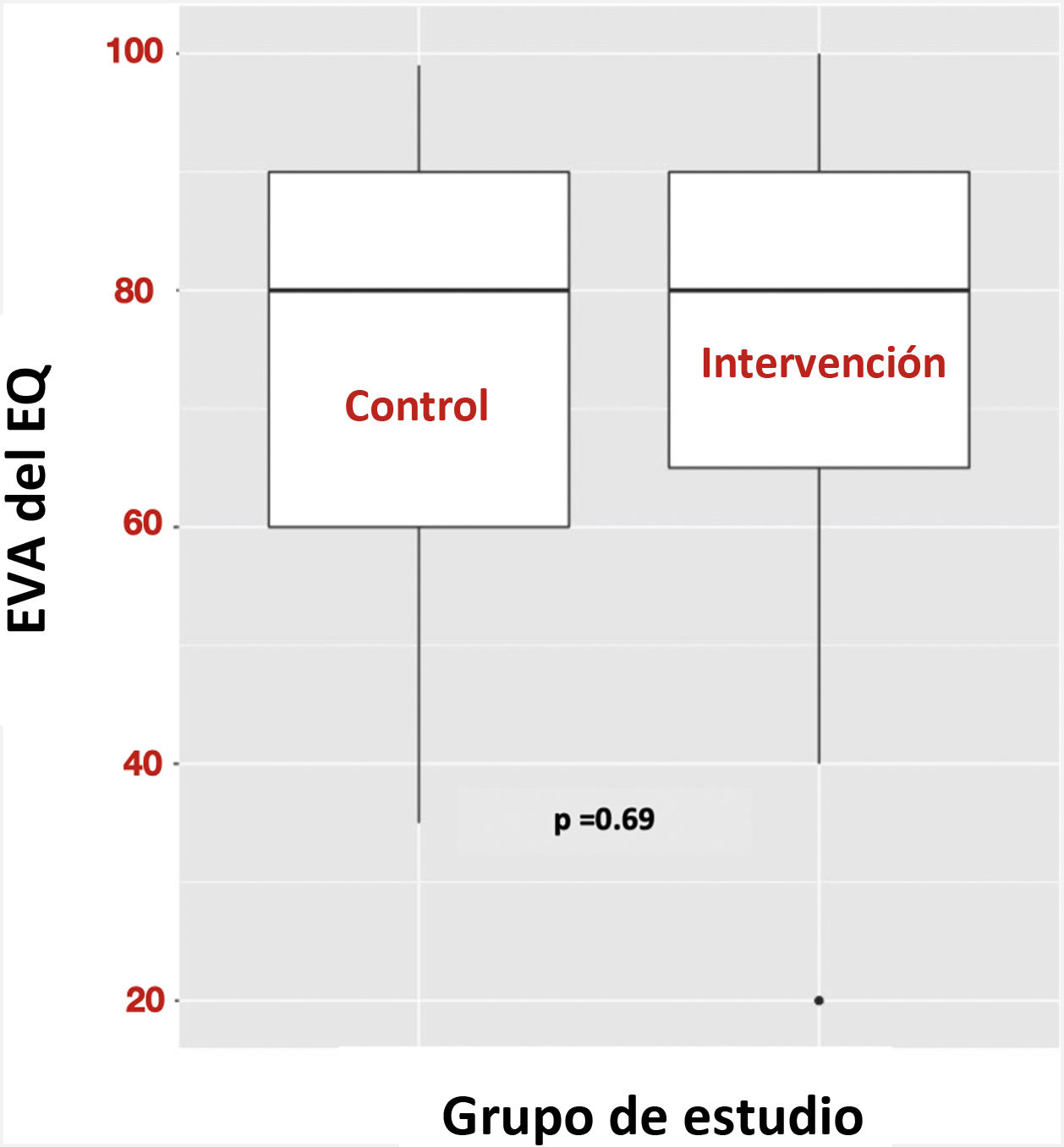
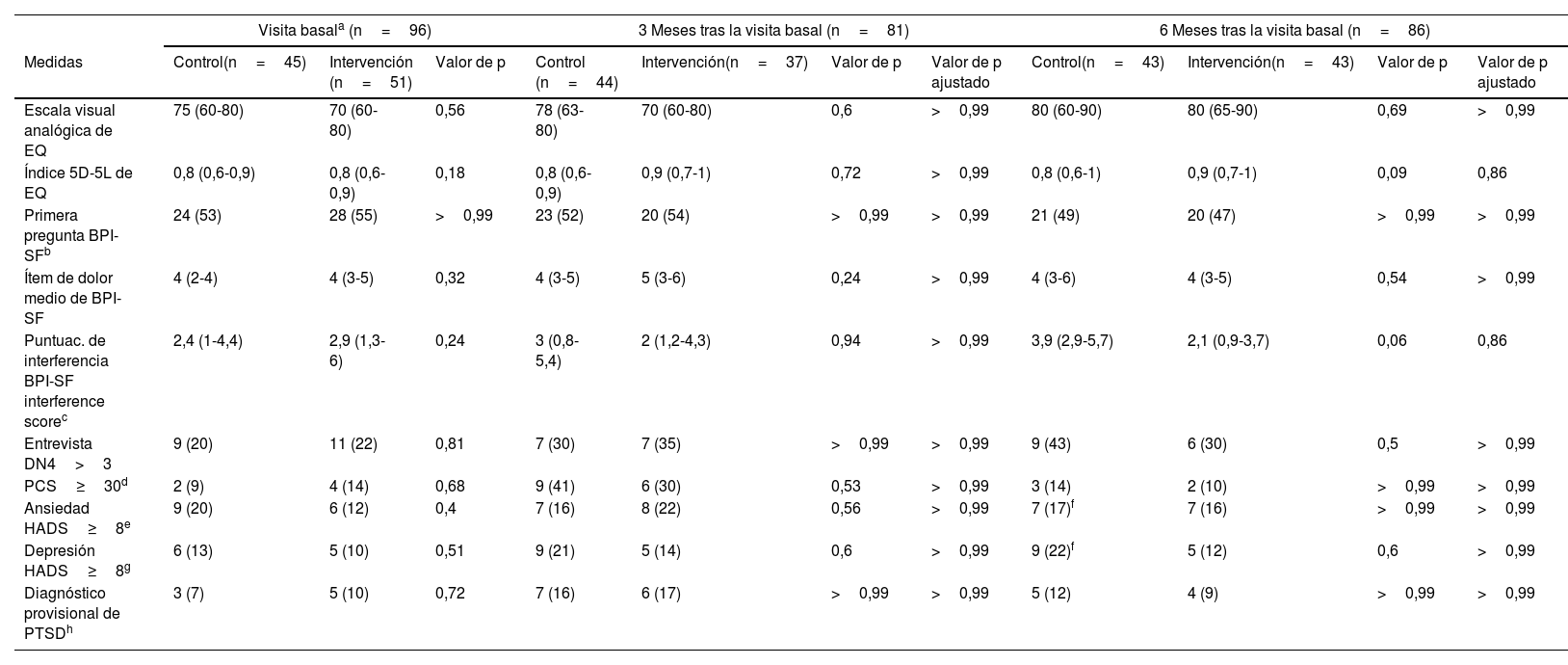
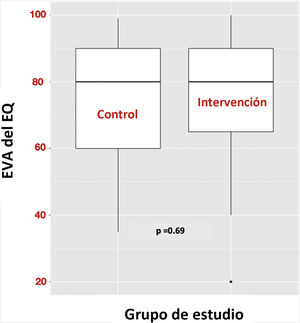
ResultadosEn la población de supervivientes de COVID-19 crítica no existieron diferencias estadísticamente significativas en cuanto a CdV en términos de EVA de EQ a los 6 meses de la visita basal, comparando los sujetos de los grupos intervención y control (EVA de EQ: 80 [65-90] frente a 80 [60-90]; p=0,69) (fig. 3). Tampoco existieron diferencias estadísticamente significativas al comparar los resultados secundarios (tabla 2). Además, el cumplimiento de los programas de seguimiento y educación terapéutica no guardó relación con la respuesta a la intervención para el resultado primario.
Medidas del resultado
| Visita basala (n=96) | 3 Meses tras la visita basal (n=81) | 6 Meses tras la visita basal (n=86) | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| Medidas | Control(n=45) | Intervención (n=51) | Valor de p | Control (n=44) | Intervención(n=37) | Valor de p | Valor de p ajustado | Control(n=43) | Intervención(n=43) | Valor de p | Valor de p ajustado |
| Escala visual analógica de EQ | 75 (60-80) | 70 (60-80) | 0,56 | 78 (63-80) | 70 (60-80) | 0,6 | >0,99 | 80 (60-90) | 80 (65-90) | 0,69 | >0,99 |
| Índice 5D-5L de EQ | 0,8 (0,6-0,9) | 0,8 (0,6-0,9) | 0,18 | 0,8 (0,6-0,9) | 0,9 (0,7-1) | 0,72 | >0,99 | 0,8 (0,6-1) | 0,9 (0,7-1) | 0,09 | 0,86 |
| Primera pregunta BPI-SFb | 24 (53) | 28 (55) | >0,99 | 23 (52) | 20 (54) | >0,99 | >0,99 | 21 (49) | 20 (47) | >0,99 | >0,99 |
| Ítem de dolor medio de BPI-SF | 4 (2-4) | 4 (3-5) | 0,32 | 4 (3-5) | 5 (3-6) | 0,24 | >0,99 | 4 (3-6) | 4 (3-5) | 0,54 | >0,99 |
| Puntuac. de interferencia BPI-SF interference scorec | 2,4 (1-4,4) | 2,9 (1,3-6) | 0,24 | 3 (0,8-5,4) | 2 (1,2-4,3) | 0,94 | >0,99 | 3,9 (2,9-5,7) | 2,1 (0,9-3,7) | 0,06 | 0,86 |
| Entrevista DN4>3 | 9 (20) | 11 (22) | 0,81 | 7 (30) | 7 (35) | >0,99 | >0,99 | 9 (43) | 6 (30) | 0,5 | >0,99 |
| PCS≥30d | 2 (9) | 4 (14) | 0,68 | 9 (41) | 6 (30) | 0,53 | >0,99 | 3 (14) | 2 (10) | >0,99 | >0,99 |
| Ansiedad HADS≥8e | 9 (20) | 6 (12) | 0,4 | 7 (16) | 8 (22) | 0,56 | >0,99 | 7 (17)f | 7 (16) | >0,99 | >0,99 |
| Depresión HADS≥8g | 6 (13) | 5 (10) | 0,51 | 9 (21) | 5 (14) | 0,6 | >0,99 | 9 (22)f | 5 (12) | 0,6 | >0,99 |
| Diagnóstico provisional de PTSDh | 3 (7) | 5 (10) | 0,72 | 7 (16) | 6 (17) | >0,99 | >0,99 | 5 (12) | 4 (9) | >0,99 | >0,99 |
Los datos se expresan como números y proporciones (%) para las variables categóricas, y mediana y rango intercuartílico (RIC) para las variables continuas. Los valores de p se ajustaron por la tasa de descubrimiento de falsos mediante el método de Benjamini–Hochberg.
BPI-SF: Brief Pain Inventory Short Form; 5D-5L: 5 dimensiones-5 niveles; DN4: Cuestionario Douleur Neuropathique 4; EQ: European Quality of Life Scale; HADS: Hospital Anxiety and Depression Scale; PCS: Pain Catastrophizing Scale; PTSD: Post Traumatic Stress Disorder.
Primera pregunta del cuestionario BPI: «A lo largo de nuestras vidas muchos de nosotros hemos tenido dolor ocasional (cefaleas menores, esguinces y dolor de muelas). ¿Ha tenido Vd. un dolor diferente a estos tipos de dolor de cada día?».
Hasta donde sabemos, este es el primer ensayo clínico aleatorizado que evalúa la eficacia de un programa de seguimiento específico para el manejo de los componentes mentales de SPCI y dolor crónico en los supervivientes de COVID-19 crítica. En comparación con los cuidados estándar, el programa de intervención no reflejó cambios significativos en cuanto a los resultados evaluados. Sin embargo, más allá de estos resultados, encontramos una serie de hallazgos que aportaron información valiosa para la investigación futura en esta población. También hemos propuesto algunas hipótesis que podrían explicar dichos hallazgos.
Los cuidados post-UCI se encuentran actualmente en fase de desarrollo, siendo objeto de debate a la hora de elegir el resultado adecuado para evaluar el impacto de una intervención1. Sobre la base de recomendaciones previas9, decidimos utilizar la EVA de EQ como resultado primario. El valor de EVA de EQ de la población de nuestro estudio tras la visita basal fue de 80 (RIC 60-90), lo cual es similar a lo reportado en la población general de España (77,53; DE 18,6)15. Nuestros hallazgos son similares a los de un estudio longitudinal previo16, en el que los valores de la EVA de EQ fueron similares a los de la población general y prácticamente no cambiaron con el tiempo (tabla 2). Sin embargo, el valor EVA de EQ comparable a la población general que no se modifica con el tiempo impide evaluar el impacto de una intervención en la CdV de los sujetos estudiados. Podrían existir diferentes motivos que explicaran el desajuste entre los síntomas y las deficiencias que puede tener un superviviente de una enfermedad crítica con respecto al modo en que dicha persona percibe su salud, siendo alguna de estas razones el crecimiento postraumático17, la resiliencia18, otros fenómenos psicológicos tales como el optimismo ciego19 y la comparación social20, en los que las personas responden a los estados de salud en comparación a sus grupos de referencia. Recientemente, Turnbull et al. describieron un término para definir la diferencia entre la salud percibida de un individuo y la percepción de la salud esperada entre pares con autorreportes similares. Dicho término fue denominado desviación perspectiva, siendo definida como la diferencia entre la percepción de la salud de una persona y la media de la percepción de la salud esperada, dadas las medidas autorreportadas de funcionamiento físico, emocional y social tras un periodo en un nuevo estado de salud. En su análisis de los resultados de 2 cohortes longitudinales, ellos reportaron una correlación moderada entre la percepción de la salud predicha y real, y aproximadamente la mitad de los supervivientes reportan una percepción que difiere de las predicciones en mayor medida que las diferencias clínicamente importantes mínimas para EVA de EQ-5D21. Es importante destacar que el uso de EVA de EQ y el índice EQ como medidas del resultado para las intervenciones centradas en los componentes mentales SPCI está limitado por su capacidad de evaluar el aspecto físico de la CdV del paciente. Esto es particularmente relevante para pacientes de COVID-19 post-UCI, que a menudo experimentan síntomas que afectan principalmente al dominio físico de la escala EQ5D, tales como disnea y debilidad muscular22,23. Por tanto, para evaluar ampliamente el impacto de un programa de EQ5D es necesario evaluar también la debilidad muscular y la disfunción respiratoria. Es importante destacar que en nuestro estudio no evaluamos específicamente dichos aspectos, lo cual podría haber afectado a la evaluación general de la CdV de los pacientes.
Otra limitación de nuestro estudio es que los criterios para acceder al programa psicológico de la intervención (HADS D≥8 en la evaluación basal) limitaron el número de candidatos a recibir esta intervención, y solo 4 pacientes fueron derivados a este tratamiento. Por dicho motivo no pudo realizarse el análisis comparativo para probar la efectividad de las intervenciones psicológicas. Además, la ratio de síntomas depresivos se incrementó en el seguimiento, pero no se incluyó en el tratamiento psicológico. El porcentaje incrementado de pacientes con síntomas depresivos (del 5,2% a nivel basal al 16,3% en V3) sugiere que los síntomas psicológicos pueden incrementarse transcurridos algunos meses del alta hospitalaria. Dicho fenómeno ha sido observado también en otras situaciones adversas24. También encontramos cuestiones prácticas y organizativas en el logro de la implementación completa de la intervención psicológica. Como se ha reflejado en otras series, muchos de los pacientes tenían limitaciones físicas significativas22,23. Por tanto, algunas opciones a considerar incluyen la coordinación de los programas de intervención psicológica y rehabilitación física en el hospital, o introducir un tratamiento online para mejorar el acceso.
En contraste con otros estudios25, nuestra muestra tuvo tasas bajas de síntomas depresivos basales, debido potencialmente al sesgo de selección en el distrito de nuestro hospital, en el que los participantes tendieron a tener estatus socioeconómico y sociocultural altos. Ambos son factores protectores de psicopatología, amortiguando el efecto negativo de los factores de estrés en la salud mental26.
Tras tratar a los pacientes post-UCI, nos cuestionamos si la terapia de autocontrol era adecuada, ya que estaba diseñada para trastornos depresivos mayores, y nuestra población se enfrentaba a cuestiones mentales, emocionales y físicas con relación a SPCI y la crisis de COVID-1922, las cuales condicionaban la implementación de intervenciones conductuales. Deberán diseñarse intervenciones psicológicas considerando la especificidad de esta población, con una intervención amplia que incluya no solo los síntomas depresivos, sino también otros síntomas psicológicos, tales como ansiedad o síntomas postraumáticos, y el tratamiento neuropsicológico de una posible disfunción cognitiva.
Es importante destacar que casi la mitad de la población de nuestro estudio reportó experimentar dolor de nueva aparición durante los 3 periodos de evaluación (V1: 54%, V2: 53% y V3: 48%). Además, la incidencia de DN en estos pacientes se incrementó con el tiempo (V1: 21%, V2: 33% y V3: 37%). La alta incidencia de dolor crónico de nueva aparición, que es alarmantemente superior a la previamente reportada en otros estudios27, podría ser una secuela post-COVID a largo plazo28. Nuestra intervención no fue efectiva para reducir la incidencia de este problema, lo cual subraya la necesidad de desarrollar programas de intervención multidisciplinares y multimodales.
Aunque no es estadísticamente significativa, es necesario destacar la mayor incidencia clínicamente relevante de delirio y debilidad adquirida en la UCI del grupo intervención, lo cual podría haber contribuido a la falta de diferencias significativas en los resultados observados entre los grupos.
Nuestro estudio tiene otras limitaciones que cabe mencionar. En primer lugar, existe un sesgo de selección potencial, ya que los pacientes con limitaciones de movilidad severa, que cumplieron los criterios de inclusión, pueden haber sido incapaces de acudir a las visitas del ensayo. En segundo lugar, nuestro estudio fue realizado en un único centro, lo cual puede haber restringido la generalizabilidad de nuestros hallazgos. Además, reconocemos que las evaluaciones telefónicas realizadas durante el seguimiento a 3 y 6 meses podrían ser menos ideales que las evaluaciones presenciales con una entrevista estructurada, lo cual ha sido criticado previamente. Los estudios futuros deberán abordar dichas limitaciones, para garantizar la evaluación precisa y amplia de los resultados de los pacientes.
Por último, dada la urgencia sanitaria causada por la primera ola de la pandemia de COVID-19, nuestra capacidad para ofrecer un programa más amplio fue limitada. Es esencial enfatizar la importancia de prevenir SPCI y CIRP mediante la focalización de los factores de riesgo modificables con rehabilitación física, estimulación cognitiva e intervenciones psicológicas. Además, son esenciales los cuidados tras el alta de la UCI durante la hospitalización. Un análisis preliminar de los datos de un programa de intervención previo en 47 pacientes de no COVID reflejó mejoras en cuanto a los componentes de la salud mental, la capacidad de los pacientes para realizar las actividades básicas de la vida diaria y las reducciones en cuanto a la carga percibida del cuidador desde el alta de la UCI al alta hospitalaria29.
Estos hallazgos requieren confirmación mediante estudios de mayor tamaño, aleatorizados y multicéntricos, específicamente centrados en la evaluación del impacto a largo plazo de los programas de intervención en la calidad de vida de los pacientes, utilizando medidas del resultado diseñadas y recomendadas para esta población30.
ConclusionesEste programa específico no fue superior a los cuidados estándar para mejorar la CdV de los supervivientes de COVID-19 crítica, según la medición mediante EVA de EQ, pero hemos mostrado hallazgos que pueden ayudar a mejorar los estudios futuros en los supervivientes de la UCI.
FinanciaciónLos autores no han recibido respaldo financiero para la financiación. El pago por el copyright y el uso de todos los cuestionarios fue realizado con recursos propios.
Podrá disponerse de los datos que respaldan los hallazgos de este estudio en www.clinicaltrials.gov o mediante solicitud razonable al autor para correspondencia (Dr. Ojeda).
Conflicto de interesesLos autores declaran la ausencia de conflicto de intereses.
AutoríaTodos los autores han contribuido a la concepción y diseño del estudio. El diseño fue realizado por A. Ojeda. La preparación, la selección de pacientes y la recopilación de los datos fueron realizadas por A. Calvo, T. Cuñat, O. Comino-Trinidad, J. Aliaga y M. Arias. El primer borrador del documento fue redactado por A. Ojeda y todos los autores comentaron las versiones previas del documento. La intervención fue realizada por A. Ojeda, A. Costas-Carrera y M. M. Sánchez. El análisis de los datos fue realizado por R. Mellado-Artigas. C. Dürsteler, G. Martinez-Palli y C. Ferrando, quienes revisaron las diferentes contribuciones de todos los autores y colaboraron con la estructura del documento. Todos los autores leyeron y aprobaron el documento final.
Los autores quieren expresar su agradecimiento al personal de la unidad del dolor y la unidad de cuidados intensivos quirúrgicos, así como a todos los pacientes que han hecho posible este estudio.