La implementación de los programas Patient Blood Management (PBM) es variable en Europa, incluso en centros en los que estos programas están bien establecidos, donde existe variabilidad en cuanto a prácticas transfusionales.
Objetivos y métodosRealizamos una encuesta para valorar la práctica actual sobre PBM perioperatoria en pacientes programados para artroplastia total de cadera y rodilla, entre los investigadores involucrados en el Estudio POWER.2 en España (estudio observacional prospectivo que evaluaba las vías de recuperación intensificada en cirugía ortopédica).
ResultadosSe obtuvo un total de 322 respuestas (37,8%). El 50% de los respondedores revisaban los niveles de hemoglobina, al menos 4 semanas antes de la cirugía; el 35% trataba a todos los pacientes anémicos, aunque el 99,7% consideraba que la detección y tratamiento de la anemia preoperatoria podrían influir en los resultados postoperatorios. La falta de infraestructuras (76%) y la falta de tiempo (51%) fueron los principales motivos para no tratar a los pacientes anémicos. El estatus del hierro es revisado antes de la cirugía por el 19% de manera rutinaria, y el 36% lo evalúa únicamente en pacientes anémicos. Hb<9,9g/dl es el valor umbral para demorar la cirugía para el 61% de los clínicos, y el 22% consideraría transfundir preoperatoriamente a los pacientes clínicamente estables sin sangrado activo. El valor umbral para transfundir a los pacientes sin enfermedad cardiovascular es 8g/dl para el 43% y 7g/dl para el 34% de los respondedores; el 75% de los facultativos considera que utiliza «umbrales restrictivos», y el 90% sigue la política transfusional uno a uno (single unit).
ConclusionesLos resultados de nuestra encuesta muestran la variabilidad en la práctica clínica en PBM en cirugía ortopédica mayor, a pesar de ser el tipo de cirugía con más tradición en estos programas.
Implementation of Patient Blood Management programs remain variable in Europe, and even in centres with well-established PBM programs variability exists in transfusion practices.
Objectives and methodsWe conducted a survey in order to assess current practice in perioperative Patient Blood Management in patients undergoing total hip and knee replacement among researchers involved in POWER.2 Study in Spain (an observational prospective study evaluating enhanced recovery pathways in orthopaedic surgery).
ResultsA total of 322 responses were obtained (37.8%). Half of responders check Haemoglobin levels in patients at least 4 weeks before surgery; 35% treat all anaemic patients, although 99.7% consider detection and treatment of preoperative anaemia could influence the postoperative outcomes. Lack of infrastructure (76%) and lack of time (51%) are the main stated reasons not to treat anaemic patients. Iron status is routinely checked by 19% before surgery, and 36% evaluate it solely in the anaemic patient. Hb<9.9 g/dl is the threshold to delay surgery for 61% of clinicians, and 22% would consider transfusing preoperatively clinically stable patients without active bleeding. The threshold to transfuse patients without cardiovascular disease is 8 g/dl for 43%, and 7 g/dl for 34% of the responders; 75% of clinicians consider they use “restrictive thresholds”, and 90% follow the single unit transfusion policy.
ConclusionsThe results of our survey show variability in clinical practice in Patient Blood Management in major orthopaedic surgery, despite being the surgery with the greatest tradition in these programs.
La anemia preoperatoria está asociada al incremento de la morbilidad1,2 y la mortalidad3 tras cirugía ortopédica, y a la exposición a las transfusiones de sangre alogénica4 (TSA). Patient Blood Management (PBM) aplica enfoques médicos y quirúrgicos basados en la evidencia, para manejar la anemia, optimizar la hemostasia y minimizar la hemorragia y la transfusión sanguínea, a fin de mejorar los resultados de los pacientes5. La implementación de un PBM multidisciplinario y multimodal reduce la TSA6,7, y ha sido asociada a una disminución de lesión renal aguda, tasa de infección, estancia hospitalaria (EH), mortalidad7 y costes8.
Aunque los protocolos PBM han sido adoptados por instituciones a nivel mundial, y que en 2010 la Organización Mundial de la Salud (OMS) urgió a los estados el establecimiento de estos programas9, su implementación sigue siendo variable en Europa10. Además, existe variabilidad en cuanto a conocimiento de los principios PBM11 y prácticas transfusionales12 entre los facultativos e instituciones europeas, incluso en centros con programas PBM bien establecidos13. La transfusión innecesaria de sangre es común a nivel mundial14,15, y ha sido descrita como uno de los procedimientos más excesivamente utilizados en los EE. UU.16. Existen ciertas barreras para la implementación de un PBM. La necesidad de recursos, la formación y los equipos multidisciplinares17 requieren el respaldo de los administradores sanitarios, y el compromiso por parte de los diferentes departamentos hospitalarios.
Realizamos una encuesta para evaluar la práctica actual en cuanto a PBM perioperatorio en pacientes programados para artroplastia total de cadera y rodilla, entre los investigadores involucrados en el Estudio POWER.2 en España18.
Materiales y métodosLos grupos Perioperative Audit and Research Network España (REDGERM) y Anaemia Working Group España (AWGE) avalaron la encuesta, tras la aprobación de sus comités científicos y de investigación.
La población diana de este estudio fueron los facultativos participantes en el Estudio POWER.2, un estudio prospectivo, multicéntrico y observacional, de cohorte en pacientes programados para artroplastia total de cadera (ATC) y artroplastia total de rodilla (ATR) electivas, que tuvo lugar en España durante un periodo de 2 meses consecutivos en 201818. El tamaño estimado de la población diana de nuestra encuesta fue de cerca de 850 investigadores. Utilizando una calculadora del tamaño de la muestra de estudio (población total de 850, 95% de intervalo de confianza), se calculó un tamaño muestral total de 265 personas.
Invitamos a los investigadores de POWER.2 de 130 centros participantes a cumplimentar voluntariamente un cuestionario abierto en Internet, a través de una carta de invitación que incluía el enlace a la encuesta. El estudio no fue anunciado, pero el acceso al cuestionario por parte de personas no invitadas era improbable. Se recopilaron las respuestas de los participantes al final del estudio, en cada centro participante, utilizando survio.com. El consentimiento informado de los participantes era implícito a la cumplimentación y envío electrónico del cuestionario.
Dicho cuestionario era un formulario estructurado, basado en web, con respuestas únicas y múltiples. Todas las preguntas eran obligatorias. También registramos el tiempo empleado en cumplimentar el cuestionario. Para impedir respuestas múltiples de un investigador, se solicitaban el nombre y el correo electrónico. Antes de realizar el análisis se eliminaron las entradas en la base de datos con un mismo usuario.
Se desarrolló una encuesta con 50 preguntas, para examinar la práctica clínica habitual en PBM perioperatorio. Se solicitó a los participantes que respondieran a las preguntas con arreglo a su práctica clínica personal actual. Las preguntas se basaron en las directrices, las recomendaciones y las sugerencias de ESA19 y NATA20, categorizándose en características de los médicos participantes, valoración preoperatoria y tratamiento de la anemia, medidas para minimizar la hemorragia, optimización de la tolerancia a la anemia, y riesgos transfusionales. La validez aparente y del contenido del cuestionario fueron establecidos y probados durante la fase de desarrollo por parte de un panel de expertos de AWGE (JAGE y EB) y REDGERM (JRM y AAM). Los datos fueron expresados como frecuencia (proporción), analizándose con arreglo al número de respuestas obtenidas para cada pregunta. El estudio fue descrito en concordancia con las directrices Checklist for Reporting Results of Internet E-Surveys (CHERRIES)21.
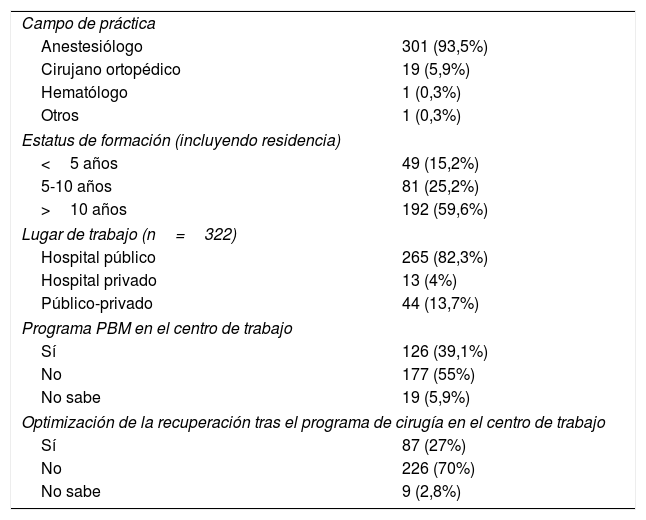
ResultadosLa encuesta fue enviada a 850 investigadores, de los cuales 599 (70,5%) abrieron la misma. De ellos, 322 cumplimentaron la encuesta, con una tasa de cumplimentación del 53,8%, y una tasa de respuesta del 37,8%. Como se refleja en la tabla 1, la mayoría de los respondedores eran anestesiólogos (93,5%), con más de 10 años de experiencia (59,6%), que trabajaban en hospitales públicos (82,3%). Más de la mitad de los respondedores (55%) declararon que su hospital no contaba con un protocolo PBM establecido.
Características de los respondedores (n=322)
| Campo de práctica | |
| Anestesiólogo | 301 (93,5%) |
| Cirujano ortopédico | 19 (5,9%) |
| Hematólogo | 1 (0,3%) |
| Otros | 1 (0,3%) |
| Estatus de formación (incluyendo residencia) | |
| <5 años | 49 (15,2%) |
| 5-10 años | 81 (25,2%) |
| >10 años | 192 (59,6%) |
| Lugar de trabajo (n=322) | |
| Hospital público | 265 (82,3%) |
| Hospital privado | 13 (4%) |
| Público-privado | 44 (13,7%) |
| Programa PBM en el centro de trabajo | |
| Sí | 126 (39,1%) |
| No | 177 (55%) |
| No sabe | 19 (5,9%) |
| Optimización de la recuperación tras el programa de cirugía en el centro de trabajo | |
| Sí | 87 (27%) |
| No | 226 (70%) |
| No sabe | 9 (2,8%) |
Hb: hemoglobina; PBM: Patient Blood Management’.
Valores expresados en cifras (proporción).
En cuanto a la detección de la anemia preoperatoria, el 90% de los respondedores valoran rutinariamente la hemoglobina (Hb) en el periodo preoperatorio: el 51% al menos 4 semanas antes de la cirugía electiva, y el 39% menos de 4 semanas antes. Hasta un 10% no mide rutinariamente la Hb, aunque el 99,7% de los respondedores consideran que la detección y tratamiento de la anemia preoperatoria podría influir en los resultados postoperatorios de los pacientes sometidos a ATC y/o ATR.
El déficit de hierro (DH) es considerado la causa más probable de anemia por el 50% de los respondedores, mientras que el 36% considera que es la anemia de trastornos crónicos. El estatus del hierro es revisado rutinariamente por el 19% antes de la cirugía, y el 36% lo evalúa únicamente en el paciente anémico. Sin embargo, el 90,1% considera que la detección y tratamiento de DH sin anemia podría influir en los resultados de los pacientes sometidos a ATR y/o ATC.
Tratamiento preoperatorio de la anemia y/o déficit de hierroCon respecto al tratamiento de la anemia preoperatoria, el 35% de los facultativos declara que tratan a todos los pacientes anémicos antes de la cirugía, el 26% trata únicamente a los pacientes anémicos o con DH y una cirugía con una hemorragia estimada superior a 500ml; el 22% trata a los pacientes con DH, con o sin anemia, y el 7% de los facultativos no trataría a ninguno de estos pacientes.
Los motivos alegados por los que los médicos no tratan preoperatoriamente a los pacientes anémicos son: «la falta de infraestructuras» (76%), «la falta de tiempo» (51%), «los costes» (15%) y «la falta de conocimiento del beneficio» (2%). La tabla 2 muestra los umbrales de Hb para tratar la anemia preoperatoria, y el umbral de Hb que haría que los médicos demoraran la cirugía para tratar a los pacientes con anemia preoperatoria.
Umbral de tratamiento de la anemia preoperatoria y de demora de la cirugía
| Umbral de hemoglobina para tratar la anemia preoperatoria (n=322) | |
| Hb<12g/dl en mujeres y Hb<13g/dl en varones | 168 (52,2%) |
| Hb<13g/dl | 62 (19,3%) |
| Hb<10g/dl | 86 (26,7%) |
| Hb<7g/dl | 6 (1,9%) |
| Umbral de hemoglobina para demorar la cirugía en caso de anemia preoperatoria (n=322) | |
| Hb10-12g/dl | 101 (31,4%) |
| Hb<9.9g/dl | 198 (61,5%) |
| No demoraría nunca la cirugía | 23 (7,1%) |
Hb: hemoglobina.
Valores expresados en cifras (proporción).
Preguntados acerca del umbral para tratar el DH, el 20% de los respondedores mide rutinariamente los niveles de ferritina, y la mayoría de ellos (79%) declara que trata a los pacientes con ferritina <50ng/ml. En cuanto a los valores de Hb que harían que los respondedores trataran el DH, el 35% utiliza los criterios sobre anemia de la OMS (mujeres con Hb<12g/dl y varones con Hb<13g/dl), el 23% trataría a las mujeres y a los varones con Hb<13g/dl, el 25% a los pacientes con Hb<10g/dl y el 15% no trataría nunca el DH. La mayoría de los facultativos declara: «la falta de infraestructuras» (74%) como uno de los motivos para no tratar a los pacientes con DH preoperatorio, seguido de «la falta de tiempo» (49%), «los costes» (15%) y «la falta de conocimiento del beneficio» (6,6%).
En cuanto a la formulación del hierro elegida para tratar a los pacientes con DH: el 37% elegiría hierro intravenoso, el 33% hierro oral y el 30% elegiría ambas formas. Para el tratamiento con hierro intravenoso, el 56% elige hierro carboximaltosa, y el 36% hierro sacarosa. En cuanto a los agentes estimulantes de eritropoyetina, el 43% de los respondedores disponía de ellos para el tratamiento preoperatorio de la anemia.
Preguntados por la valoración del tratamiento con hierro, el 83% de los facultativos mide la Hb tras el tratamiento con hierro antes de la cirugía, y el 45% no demoraría la cirugía en caso de persistir la anemia del paciente. Hasta el 22% de los médicos considera transfundir preoperatoriamente a los pacientes clínicamente estables y sin hemorragia activa.
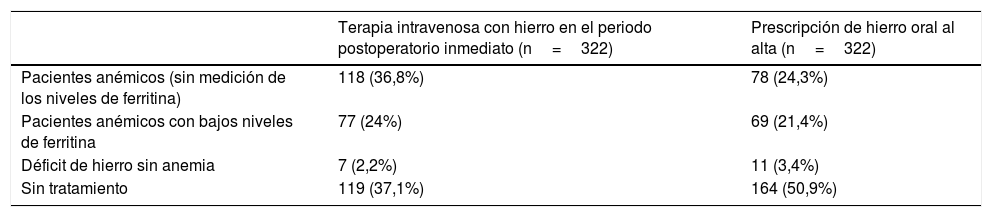
Tratamiento postoperatorio para la anemiaLa tabla 3 muestra las respuestas correspondientes a la terapia con hierro intravenoso en el periodo postoperatorio inmediato, y a la terapia con hierro oral al alta. Preguntados acerca de la formulación de hierro elegida, el 44% de los respondedores utilizan hierro carboximaltosa, el 40% hierro sacarosa y el 16% otro tipo de formulación.
Terapia con hierro postoperatoria
| Terapia intravenosa con hierro en el periodo postoperatorio inmediato (n=322) | Prescripción de hierro oral al alta (n=322) | |
|---|---|---|
| Pacientes anémicos (sin medición de los niveles de ferritina) | 118 (36,8%) | 78 (24,3%) |
| Pacientes anémicos con bajos niveles de ferritina | 77 (24%) | 69 (21,4%) |
| Déficit de hierro sin anemia | 7 (2,2%) | 11 (3,4%) |
| Sin tratamiento | 119 (37,1%) | 164 (50,9%) |
Valores expresados en cifras (proporción).
Los agentes antifibrinolíticos, como el ácido tranexámico son administrados rutinariamente por el 97,8% de los participantes para minimizar la hemorragia. En cuanto a la sangre autóloga, el 27% de los respondedores manifiestan que en sus centros se realiza donación de sangre preoperatoria en algunos casos, mientras que el 16% de los respondedores realizan hemodilución normovolémica. La recuperación de sangre autóloga intraoperatoria es utilizada por el 31% de los médicos en pacientes con contraindicaciones para el uso de ácido tranexámico, mientras el 8% de los respondedores utilizan siempre recuperadores. En cuanto al uso postoperatorio de recuperadores, la mayoría (54%) de los facultativos no la utilizan nunca; el 32% únicamente en pacientes con contraindicación para el uso de ácido tranexámico, mientras que es siempre utilizada por el 11% de los respondedores. La mayoría de facultativos utilizan alguna medida para mantener la normotermia: el 33% mantas térmicas, el 8% calentadores de fluidos y el 57% ambos.
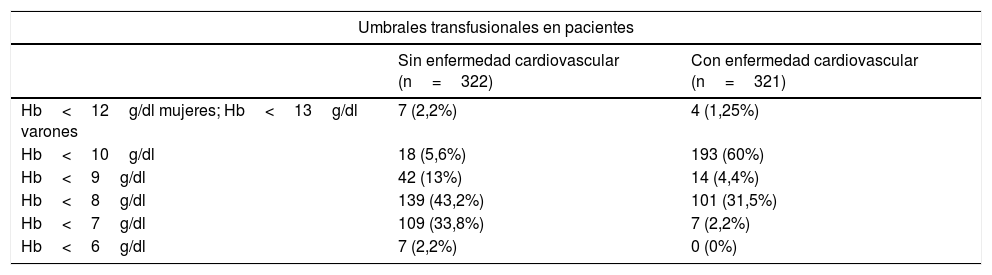
Pilar 3: Mejorar la tolerancia a la anemia y criterios transfusionalesLos facultativos fueron preguntados acerca del umbral transfusional para pacientes con y sin enfermedad cardiovascular (se refleja en la tabla 4); el 75% de los facultativos considera que utilizan «umbrales restrictivos». En cuanto a las políticas transfusionales institucionales, el 59% de los respondedores manifiestan que su centro cuenta con una. Hasta el 10% de los médicos declara la falta de conocimiento acerca de esta cuestión. Una mayoría de clínicos (90%) transfunde los concentrados de hematíes de uno en uno, mientras que el 10% de ellos transfunde 2 unidades. Además de los niveles de Hb, en una pregunta con opción a múltiples respuestas, el 87% de los clínicos tiene en cuenta la hipotensión arterial, el 81% la taquicardia, el 53% los cambios electrocardiográficos, el 47% la oliguria y el 46% la elevación de lactato. Se preguntó a los médicos acerca de los riesgos transfusionales relativos a la transfusión de sangre alogénica, pudiendo aportarse respuestas múltiples (tabla 5).
Pilar 3: Umbrales transfusionales
| Umbrales transfusionales en pacientes | ||
|---|---|---|
| Sin enfermedad cardiovascular (n=322) | Con enfermedad cardiovascular (n=321) | |
| Hb<12g/dl mujeres; Hb<13g/dl varones | 7 (2,2%) | 4 (1,25%) |
| Hb<10g/dl | 18 (5,6%) | 193 (60%) |
| Hb<9g/dl | 42 (13%) | 14 (4,4%) |
| Hb<8g/dl | 139 (43,2%) | 101 (31,5%) |
| Hb<7g/dl | 109 (33,8%) | 7 (2,2%) |
| Hb<6g/dl | 7 (2,2%) | 0 (0%) |
Hb: hemoglobina.
Valores expresados en cifras (proporción).
Riesgos relacionados con la transfusión de sangre alogénica (respuestas múltiples)
| Infección | 251 (78%) |
| TRALI (lesión pulmonar relacionada con la transfusión) | 229 (71%) |
| Hemólisis/inmune | 228 (70,8%) |
| Transmisión de enfermedades infecciosas | 214 (66,5%) |
| Muerte | 172 (53%) |
| TACO (sobrecarga circulatoria asociada a la transfusión) | 146 (45,3%) |
La reserva funcional es valorada rutinariamente por el 56% de los respondedores utilizando METS u otros métodos, mientras que el 44% no la valora nunca. La mayoría de los clínicos (54%) utiliza monitorización del gasto cardiaco para optimizar la tolerancia a la anemia únicamente en pacientes de muy alto riesgo, el 23% a veces y el 21% nunca utiliza monitorización del gasto cardiaco. De manera similar, el 53% de los clínicos declara utilizar Terapia guiada por objetivos basándose en la monitorización del gasto cardiaco, solo en pacientes de muy alto riesgo.
DiscusiónEsta encuesta valoró la práctica actual de PBM entre los investigadores de 130 hospitales españoles, que participaron en el Estudio POWER.2, en su mayoría anestesiólogos, independientemente de si trabajaban o no en un centro con un programa PBM establecido. La encuesta muestra variabilidad entre los respondedores en cuanto al manejo de la transfusión en pacientes sometidos a ATC y ATR.
Aun cuando existe suficiente evidencia acerca de que la anemia preoperatoria está asociada a una tasa de transfusión más alta4,22,23, así como a peores resultados en la cirugía ortopédica mayor24,25, solo el 35% de los participantes declara tratar a todos los pacientes con anemia preoperatoria. Esta situación puede encontrarse en el 26% de los pacientes programados para cirugía ortopédica mayor26, y la mayoría de sociedades científicas recomienda la evaluación preoperatoria de Hb al menos 4 semanas antes de la cirugía ortopédica programada, para disponer de más tiempo para tratar dicha anemia19. En nuestra encuesta, solo la mitad de los respondedores declara disponer de un valor de Hb con un mes de antelación. Paradójicamente, casi el 100% cree que la detección y el tratamiento de la anemia preoperatoria podrían influir en los resultados postoperatorios, y el 90% piensa lo mismo en cuanto al tratamiento del DH en pacientes no anémicos. Las directrices de consenso internacional recomiendan la suplementación preoperatoria con hierro a los pacientes no anémicos con bajas reservas de hierro programados para cirugía mayor, con pérdida de sangre estimada >500ml y/o riesgo transfusional >10%27, con el fin de acelerar la recuperación de Hb tras la hemorragia quirúrgica28. Sin embargo, existen pocos estudios, y la evidencia es débil en cuanto a la mejora de los resultados en cirugía no cardiaca. Se ha relacionado el DH sin anemia con un incremento de TSA en cirugía cardiaca29, sin diferencia en cuanto a morbimortalidad, aunque otros estudios no han encontrado diferencia en cuanto a las necesidades de TSA, aunque sí una tendencia a incrementar la EH entre los pacientes con déficit de hierro30. Waters et al. no encontraron ninguna asociación entre DH y complicaciones postoperatorias en una cohorte de 100 pacientes sometidos a cirugía ortopédica31. Miles et al. publicaron recientemente un estudio retrospectivo exploratorio en una cohorte de 141 pacientes programados para cirugía colorrectal, que sugiere un incremento de la tasa de reingreso a los 90 días de seguimiento en pacientes con DH, en comparación con los pacientes sin DH. Son necesarios más estudios con poder estadístico adecuado, para confirmar esta asociación32.
Los principales motivos aducidos para no tratar la anemia preoperatoria en nuestra muestra son la falta de infraestructuras y la falta de tiempo, lo cual coincide con la encuesta realizada por Manzini et al.11. A pesar de la creciente evidencia que respalda los protocolos PBM7,33,34, y las recomendaciones para elaborar programas nacionales sobre PBM en Europa35, la variabilidad persiste en cuanto a prácticas transfusionales36 y la implementación de PBM10. Una de las principales dificultades para establecer un PBM radica en el manejo de la anemia preoperatoria. Establecer un protocolo para poder valorar a los pacientes con tiempo suficiente, que implique que la cirugía deba posponerse para tratar la anemia, requiere el respaldo de todas las especialidades médicas, las autoridades hospitalarias y los servicios sanitarios implicados.
Con la adopción de umbrales transfusionales más bajos, los pacientes reciben el alta con menores niveles de Hb de los que previamente era habitual37. Además, la implementación de vías de recuperación intensificada ha disminuido la EH en 3 días en cuanto a ATR y ATC en grandes series de pacientes38,39, coincidiendo con el nivel de Hb nadir37. Estos procedimientos se realizan incluso como cirugías ambulatorias en pacientes seleccionados40. Existe escasa evidencia y resultados conflictivos acerca de la asociación entre anemia postoperatoria y deficiencia de recuperación funcional. La anemia postoperatoria ha sido asociada a una menor fuerza en los cuádriceps en pacientes sometidos a ATC41, mientras que Jans et al. encontraron que la anemia moderada tenía un impacto clínico irrelevante en la recuperación funcional temprana en un estudio prospectivo en pacientes sometidos a ATC en un programa de recuperación acelerada («fast-track»)42, aunque los pacientes incluidos eran pacientes sanos. Por tanto, este resultado podría no ser aplicable a pacientes con comorbilidades, que podrían ser menos tolerantes a la anemia. Las directrices de consenso recomiendan la terapia intravenosa y temprana con hierro para corregir la anemia o DH postoperatorio moderado y grave, en lugar de la terapia oral, debido a su efecto limitado en presencia de estatus inflamatorio y baja adherencia al tratamiento a causa de sus efectos secundarios19,37. Sin embargo, hasta el 37% de los participantes en nuestra encuesta nunca administra terapia intravenosa con hierro a los pacientes con anemia postoperatoria, y casi la mitad de los respondedores tratan a los pacientes anémicos con hierro oral al alta.
A pesar de la recomendación de no realizar donación preoperatoria de sangre autóloga, y hemodilución normovolémica, del Documento Sevilla sobre alternativas a la trasfusión de sangre alogénica43, el 27 y el 16% de los respondedores, respectivamente, la utilizan aún en ciertos tipos de pacientes en ATC y ATR. Por otro lado, el uso de ácido tranexámico parece ser la norma en nuestra muestra. Aunque teniendo en cuenta que existen contraindicaciones para su administración, en un estudio observacional europeo publicado en 2016, el ácido tranexámico se utilizó en el 39 y 43% de los pacientes sometidos a ATC y ATR10.
La mayoría de los médicos participantes consideró que utilizaban umbrales transfusionales «restrictivos». Sin embargo, hasta el 22% consideraría transfundir preoperatoriamente sangre a los pacientes clínicamente estables sin hemorragia activa, a pesar de las recomendaciones contra esta práctica por parte de las Sociedades Españolas de Anestesiología y Hematología43–45. Además, los altos umbrales transfusionales y/o el manejo inadecuado de la anemia previo a la cirugía podrían originar más TSA intra y postoperatorias. En nuestra encuesta, el 61% de los respondedores demoraría la cirugía para tratar a los pacientes con Hb<10g/dl, y el 7% no pospondría nunca la cirugía. Considerando que el 43% trasfundiría a pacientes sin enfermedad cardiovascular con Hb<8g/dl, y que el 20% tienen umbrales incluso más altos, la falta de optimización de los pacientes anémicos podría conducir a tasas de TSA evitables. Las recomendaciones actuales sugieren la adopción de un umbral restrictivo de Hb de 7-8g/dl, dependiendo de las comorbilidades del paciente27,31,32. Además, las mujeres tienen mayor riesgo de recibir TSA que los varones. La OMS define la anemia como una concentración de Hb de <13g/dl para varones y de <12g/dl para mujeres no embarazadas44. Sin embargo, las mujeres tienen menor superficie corporal y volumen circulatorio en comparación con los varones, aunque sufrirán hemorragias similares a los varones al ser sometidas a los mismos procedimientos. Por tanto, la pérdida de sangre es proporcionalmente más alta en mujeres, con tasas transfusionales más elevadas26. Por ello, se ha establecido un nuevo término para la población quirúrgica, la concentración preoperatoria de Hb sub-óptima, en el que los pacientes con Hb<13g/dl son considerados anémicos, independientemente de su sexo45, debiendo considerarse el mismo objetivo para la optimización preoperatoria en ambos sexos.
Los resultados de encuesta nuestra sugieren que los principios PBM que son relevantes para la práctica clínica no están extendidos, y que existen ciertos puntos reveladores que exigen programas educacionales que requieren la implicación de los servicios sanitarios, autoridades hospitalarias, sociedades científicas y centros de transfusión: más de la mitad de los respondedores trabajan en centros sin un programa PBM establecido, el 39% no mide los niveles de Hb al menos 4 semanas antes de la cirugía, e incluso el 10% no mide la Hb rutinariamente; el 65% no trata a todos los pacientes anémicos, el 22% consideraría transfundir preoperatoriamente a un paciente anémico y sin sangrado activo, el 55% no es consciente de la sobrecarga circulatoria asociada a la transfusión (TACO), a pesar de estar hoy en día entre los efectos adversos más frecuentes asociados a la TSA46; el 49% trata la anemia postoperatoria con hierro oral, y el 41% declara que su centro no tiene una política transfusional, o carece de conocimiento acerca de esta cuestión.
Un punto fuerte de nuestra encuesta es la alta tasa de respuesta (37,8%) en comparación con las encuestas recientemente publicadas por Baron et al. (7,6%)47 y Manzini et al. (15,9%)11 que evalúan PBM entre especialistas europeos. Uno de los motivos podría ser que los médicos invitados a participar en la encuesta fueron investigadores del Estudio POWER.2, con mayor probabilidad de desear participar en la investigación. En una encuesta reciente entre médicos españoles de centros involucrados en el proyecto Maturity Assessment Model in Patient Blood Management (MAPBM), el conocimiento de los protocolos locales de PBM fue menor entre los cirujanos y otros especialistas médicos, en comparación con los anestesiólogos13 y, por tanto, es esencial la implicación de diferentes especialidades médicas en la implementación del programa PBM. La amplia mayoría de los participantes en nuestra encuesta eran anestesiólogos, quienes podrían estar más concienciados acerca de los riesgos transfusionales, y conocer los protocolos locales sobre transfusión, con el consiguiente riesgo de sesgo del respondedor. Además, deberían considerarse con precaución los resultados relacionados con la terapia con hierro en el periodo postoperatorio, ya que solo el 6% de los respondedores eran cirujanos ortopédicos, quienes son normalmente responsables del tratamiento de la anemia postoperatoria en nuestro entorno.
ConclusionesLos resultados de nuestra encuesta reflejan la variabilidad en cuanto a la práctica clínica de PBM en cirugía ortopédica mayor, a pesar de ser el tipo de cirugía con mayor tradición de este programa, así como la alta preocupación reflejada por nuestra muestra acerca de los riesgos de la anemia preoperatoria en los resultados postoperatorios. Deberían introducirse estrategias para mejorar el Primer Pilar del PBM, y en especial el tratamiento de la anemia preoperatoria y el déficit de hierro. Además, considerando la necesidad de divulgar las cuestiones relevantes para la práctica clínica, que implican a diversas especialidades médicas y quirúrgicas, las autoridades sanitarias y las sociedades científicas nacionales deberían tomar la iniciativa para desarrollar programas educacionales a nivel nacional.
FinanciaciónLos autores declaran no haber recibido ninguna financiación para la realización de este trabajo.
Conflicto de interesesCJ recibió honorarios por conferencias/asesorías de Vifor Pharma España SL, Bial, y Zambon, pero no por la realización de este trabajo. MB recibió honoraros por asistencia a congresos/asesorías de Vifor Pharma España SL, pero no por la realización de este trabajo. JAGE reportó honorarios personales de Amgen, Jansen, Sandoz, honorarios personales de Vifor Pharma, Zambon, y respaldo no financiero de Vifor Pharma no relacionado con el trabajo presentado. AAM, JRM, CA, MCO, RNP y EB han declarado la ausencia de conflicto de intereses.
Los autores quisieran mostrar su agradecimiento por la cumplimentación de la encuesta a los investigadores del Estudio POWER.2.