Diseñar un procedimiento de validación de 4 magnitudes bioquímicas en un gasómetro frente a un analizador acreditado que sea sencillo, consistente y aceptable según la Norma ISO 15189:2007 y que pueda servir como método de acreditación flexible.
MétodosMedición secuencial en los analizadores Dimension RxL y GEM 4000 de glucosa, sodio (Na+), potasio (K+) y lactato en 91 muestras de plasma (heparina de litio) de pacientes entre marzo y junio de 2009 (EP-9). Se chequearon outliers y error sistemático. Los pares de resultados se estudiaron mediante análisis de regresión lineal y gráficos de Bland-Altman.
El criterio de aceptación fue obtener un error sistemático inferior a las especificaciones de calidad definidas en el laboratorio acreditado.
Resultados y discusiónLos resultados de glucosa y K+ fueron aceptables según el procedimiento 6.1 de la guía EP-9, mientras que Na+ fue aceptable según el procedimiento 6.2. En cuanto a lactato, se detectó un error sistemático superior a la especificación del laboratorio.
ConclusionesSe han validado los métodos de determinación de glucosa, Na+ y K+ en un gasómetro GEM 4000 mediante la aplicación de la norma EP-9 con respecto a los del Dimension RxL (métodos de referencia). El lactato no se pudo validar porque el error sistemático superó la especificación del laboratorio.
Este procedimiento se propone como herramienta de validación de métodos para laboratorios acreditados con alcance flexible según la Norma UNE EN ISO 15189.
Designing a 4 biochemical parameters validation procedure in a gasometer versus an accredited analyzer. This procedure is simple, robust and acceptable according to the standard ISO 15189: 2007 and that can serve as flexible accreditation method.
MethodsSequential measurement in Dimension RxL and GEM 4000 analysers of glucose, Na+, K+ and lactate in 91 patients plasma samples (Lithium heparin) between March and June 2009 (EP-9). Checked outliers and bias results pairs were studied using linear regression analysis and Bland-Altman graphics.
The acceptance criterion was to get a bias lower than quality specifications defined in the accredited laboratory.
Results and discussionThe results of glucose and K+ were acceptable, following the procedure 6.1 of EP9 guideline, while for Na+ it was acceptable by the procedure 6.2. For lactate, a superior to the specification of the lab bias was detected.
ConclusionsMeasuring methods of glucose, sodium and potassium in a GEM 4000 gasometer applying standard EP9 versus Dimension RxL as reference methods have been validated. Lactate could not be validated because the bias exceeded the specification of the laboratory.
This procedure is intended as validation tool of methods for laboratories accredited with flexible scope according to UNE EN ISO 15189 standard.
Desde hace unos años el sistema de gestión de la calidad por implantar en los laboratorios clínicos es una cuestión recurrente1. Hay defensores de la certificación por la Norma UNE EN ISO 9001, hay defensores de la acreditación por la Norma UNE EN ISO 15189 y hay quienes defienden que cada laboratorio debe utilizar un sistema de gestión de calidad acorde a sus necesidades y a los requerimientos por parte de sus clientes2.
Muy recientemente tuvo lugar la 2009 Convocation of experts on Laboratory Quality. Uno de los grupos de trabajo debatió sobre la situación de los diferentes países europeos respecto a que con sus leyes se obligara a los laboratorios clínicos a acreditarse (Pan European Medical Laboratory Accreditation: Pros and cons [conclusiones pendientes de publicación]).
No es fácil llegar a una situación de consenso entre las diferentes opciones enfrentadas3. Sin embargo, desde la óptica de un laboratorio con un alcance acreditado, sí resulta muy útil llegar a incluir en este la opción de «alcance flexible»4–6, mediante el cual el laboratorio acreditado puede ampliar el alcance a nuevos parámetros con la tecnología ya acreditada para otros sin tener que comunicarlo previamente a la Entidad Nacional de Acreditación (ENAC).
Llegar a conseguir la «confianza» de la ENAC exige la definición, la aplicación y la revisión constante de procedimientos de validación estrictos por parte del laboratorio.
En este artículo proponemos: 1) un procedimiento de validación de 4 magnitudes bioquímicas en un gasómetro frente a un analizador acreditado, que sea sencillo, consistente y aceptable según la Norma ISO 15189:2007, y 2) que este procedimiento pueda aplicarse como herramienta de validación en los laboratorios acreditados con alcance flexible.
Material y métodosSe han seguido las recomendaciones de la guía de consenso CLSI para comparación de métodos mediante la utilización de muestras de pacientes, conocida como guía EP-9-A27. Se denomina Y al método que se está probando (GEM 4000, Instrumentation Laboratory) y X al método de comparación o de referencia (Dimension RxL, Siemens).
MuestrasSe han empleado muestras de sangre de 91 pacientes que acudieron al servicio de urgencias del hospital, recogidas entre los meses de marzo y junio de 2009. Las muestras se recogieron en jeringas de gasometría con heparina de litio y se procesaron inmediatamente a su llegada en el analizador de gases GEM 4000. A continuación se centrifugaron a 3.500 rpm y se procesaron en el analizador Dimension RxL. Los parámetros estudiados fueron glucosa, lactato, sodio (Na+) y potasio (K+). La tecnología empleada en las determinaciones del Dimension RxL para glucosa y lactato fue espectrofotometría y para Na+ y K+ potenciometría indirecta, mientras que en GEM 4000 para glucosa y lactato se empleó amperometría y para Na+ y K+ potenciometría directa. Todos los resultados obtenidos se encontraban dentro del rango de linealidad de los citados parámetros.
Las muestras se analizaron por duplicado en ambos analizadores. El tiempo transcurrido entre el procesamiento en un analizador y el otro no superó los 20min.
Análisis de los resultados- 1.
Detección de valores extremos o outliers. El procedimiento seguido es el indicado en los puntos 4.1 y 4.4 de la EP-97. Se comparan las diferencias absolutas entre los duplicados de cada método8. Estas diferencias no deben superar el valor de 4 veces la media de las diferencias absolutas. Si se encuentra algún valor que exceda este límite, se comprueba que las diferencias normalizadas (punto 4.1 de la EP-9) de los duplicados no superen el valor de 4 veces la media normalizada de las diferencias de cada método.
- 2.
Relación lineal entre valores de ambos métodos. Se realizan 4 diagramas de dispersión mediante la utilización de escalas iguales: 1) entre los valores medios de ambos métodos; 2) entre los valores individuales de Y frente a los valores medios de X; 3) entre las diferencias entre la media de Y y la media de X para cada método frente a la suma de los valores medios de Y y de X dividida por 2, y 4) por último, un diagrama entre la diferencia entre cada valor individual de Y y de X frente a la misma suma del diagrama tercero.
De acuerdo con la EP-9 (punto 4.2)7, se valora la relación lineal mediante inspección visual.
- 3.
Coeficiente de correlación (r). Se calcula el r, y si es mayor o igual a 0,975 (o coeficiente de determinación mayor o igual a 0,95), se considera aceptable el rango de X, es decir, que el error de X está compensado por el rango de los datos, y posibilita la utilización del análisis de regresión simple para estimar la pendiente y la ordenada en el origen9.
- 4.
Estimación de la dispersión. El punto 5.2 de la EP-97 recomienda la inspección visual de la dispersión constante, tras lo que se realiza un análisis de regresión según los puntos 6.1 o 6.2 de la citada guía.
- 5.
Estimación del error sistemático predicho y sus intervalos de confianza (IC). La diferencia entre cada valor puntual de Y y la recta de regresión es lo que se denomina el residuo para ese punto. La desviación estándar de esos residuos es una medida de la dispersión de los puntos alrededor de la recta de regresión.
Interpretación. Se calculó el error del residual (error sistemático del residual según la guía EP-9 punto 6.1) y sus IC (de acuerdo con el error estándar de los residuales según el punto 6.1 de la EP-9). Si el error aceptable es superior al límite superior del IC del error residual, se asume que el método evaluado tiene condiciones metrológicas aceptables (punto 7 de la EP-9).
El análisis estadístico se ha realizado con la ayuda del paquete MedCalc para Windows versión 10.3.2.0 (MedCalc Software, Mariakerke, Bélgica).
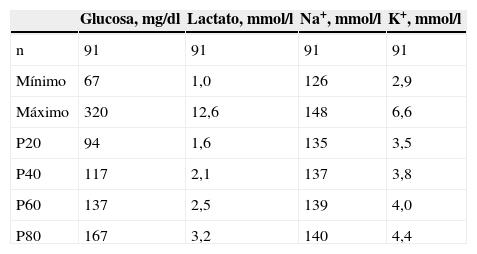
ResultadosEn la tabla 1 se muestran los resultados de los distintos parámetros analizados según la distribución de sus valores respectivos, agrupados por quintiles.
Detección de outliers. En los parámetros glucosa, lactato y K+ no se encontraron valores outliers, mientras que en el Na+ se encontró un valor (el 0,9% del total) que superaba los límites establecidos, por lo que se eliminó del análisis.
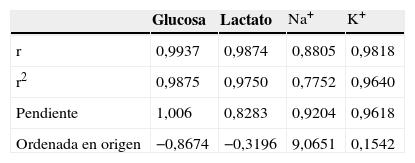
Linealidad y dispersión constante. Se comprobó que la glucosa, el lactato y el K+ seguían una relación lineal (r>0,975; coeficiente de determinación >0,95) con dispersión constante, por lo que se aplicó el procedimiento 6.1 de la guía EP-97 (tabla 2).
Resultados del análisis de regresión lineal
| Glucosa | Lactato | Na+ | K+ | |
| r | 0,9937 | 0,9874 | 0,8805 | 0,9818 |
| r2 | 0,9875 | 0,9750 | 0,7752 | 0,9640 |
| Pendiente | 1,006 | 0,8283 | 0,9204 | 0,9618 |
| Ordenada en origen | −0,8674 | −0,3196 | 9,0651 | 0,1542 |
K+: potasio; Na+: sodio; r: coeficiente de correlación; r2: coeficiente de determinación.
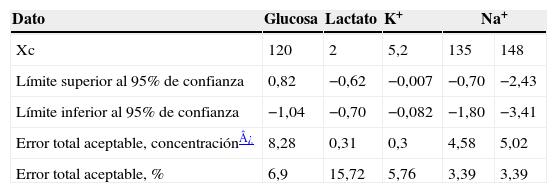
En el caso del Na+ el valor de r fue de 0,88, con lo que no es aplicable el procedimiento 6.1 de la guía EP-97. En estos casos la citada guía recomienda con antelación aumentar el número de muestras por encima de 40. Dado que el número de muestras de este estudio ya era superior al recomendado por la guía EP-9 (n=91), se procedió a aplicar el procedimiento 6.2. En la tabla 3 se muestran los valores de los errores predichos calculados en distintos niveles críticos de decisión clínica.
Error total aceptable en los niveles críticos de decisión clínica
| Dato | Glucosa | Lactato | K+ | Na+ | |
| Xc | 120 | 2 | 5,2 | 135 | 148 |
| Límite superior al 95% de confianza | 0,82 | −0,62 | −0,007 | −0,70 | −2,43 |
| Límite inferior al 95% de confianza | −1,04 | −0,70 | −0,082 | −1,80 | −3,41 |
| Error total aceptable, concentración¿ | 8,28 | 0,31 | 0,3 | 4,58 | 5,02 |
| Error total aceptable, % | 6,9 | 15,72 | 5,76 | 3,39 | 3,39 |
K+: potasio; Na+: sodio; Xc: nivel crítico de decisión.
Asimismo, se realizó un análisis gráfico mediante gráficos tipo Bland-Altman para verificar que no existían diferencias significativas entre pares de puntos entre los 2 equipos comparados (no mostrados). Se pudo corroborar que menos del 3% de los datos excedía las 2 desviaciones típicas; sin embargo, en el caso del lactato se observaba una deriva que evidenciaba que los valores del GEM 4000 eran inferiores a los del Dimension RxL, es decir, no se pueden superponer los datos de lactato de ambos analizadores.
DiscusiónEl Laboratorio de Urgencias del Hospital Universitario Príncipe de Asturias está acreditado por la ENAC según la Norma ISO 15189:2007 con el número 630/LE1377. Su alcance10 incluye 42 parámetros con diferentes técnicas, como espectrofotometría, potenciometría, inmunoanálisis, crioscopia, amperometría, dispersión de la luz, etc.
Hay ocasiones en que los analizadores de bioquímica, a pesar de estar duplicados, se averían simultáneamente, y en ese momento un gasómetro puede resultar vital para suplir a los analizadores convencionales, ya que por su naturaleza el laboratorio de urgencias ha de responder a las demandas de resultados en plazos muy cortos durante las 24h del día los 365 días del año. No obstante, para que el resultado sea fiable, el método o el analizador deben estar validados.
Se han validado los métodos de determinación de Na+ y K+ (potenciometría directa) y glucosa (amperometría) en un gasómetro GEM 4000 mediante la aplicación de la norma EP-97, y se han utilizado como referencia los métodos espectrofotométricos (glucosa) y la potenciometría indirecta (Na+ y K+) ya acreditados para el analizador Dimension RxL. Como limitaciones del estudio, cabe citar que no se ha realizado la secuencia inversa en la medición de los replicados, como recomienda la EP-9, si bien este hecho probablemente no reporta ningún factor favorable al estudio. Tanto es así que no ha sido posible la validación del lactato, porque los resultados en GEM 4000 fueron significativamente distintos a los de Dimension RxL. No obstante, puesto que tanto la imprecisión calculada (datos no aportados) como los datos de correlación con respecto al método de referencia resultaron excelentes, aun cuando la guía no contempla explícitamente la ortodoxia de la utilización de una ecuación de regresión para conseguir la superposición deseada, desde nuestro punto de vista su uso es conceptualmente correcto, por lo que se propone utilizar una ecuación del tipo citado y que la entidad de acreditación correspondiente avale esta práctica. Merece también comentarse el hecho de que la validación del Na+ haya requerido el procedimiento 6.2 (más complicado). Se ha tenido que recurrir a este procedimiento alternativo debido a que este parámetro no reunía todos los criterios de linealidad, requisitos que se pueden resumir en el r de 0,8. La causa más probable de esta moderada correlación es que el rango de valores obtenidos para este catión es estrecho9, circunstancia que, por otra parte, es difícil de obviar en la práctica clínica habitual.
De esta manera, queda cubierto el primer objetivo de nuestro trabajo, que era validar estas magnitudes en el gasómetro GEM 4000 para que ante una situación de urgencia pudieran llevarse a cabo las determinaciones en un analizador consistente y de tratamiento sencillo. Como valor añadido se obtiene la posibilidad de utilizar únicamente el espécimen sangre heparinizada sin necesidad de centrifugar para las determinaciones referidas, lo que llevaría consigo un ahorro tanto de muestra como de tiempo. Cabe destacar que a pesar del efecto matriz, los resultados obtenidos en los diferentes parámetros en el gasómetro, con excepción del lactato, permiten la superponibilidad de éstos con los del Dimension RxL, ya que los errores observados en este estudio son inferiores a las especificaciones analíticas establecidas en nuestro laboratorio.
Para la validación de métodos hemos empleado la guía EP-97. El uso de la guía, si bien a priori puede parecer tedioso, una vez utilizada es fácil de estandarizar. Resulta llamativa la escasez de artículos que refieren la utilización de esta norma (16 referencias) para la cuantificación del error sistemático en la bibliografía consultada, aunque sí aparecen referencias de utilización de otras guías, como la EP-5 y la EP-10, para el cálculo de la imprecisión. En cualquier caso tan sólo aparece en la bibliografía un artículo publicado11 sobre validación de magnitudes bioquímicas en un gasómetro comparado con un analizador bioquímico, aunque sí existen resultados de validación de los parámetros clásicos y específicos de gasómetros, concretamente pH y calcio iónico12, y de analizadores bioquímicos13.
A pesar de que los procedimientos de la guía EP-9 no se corresponden con las recomendaciones sobre métodos estadísticos clásicos en cuanto a fiabilidad al comparar métodos14, la enorme utilidad de disponer y aplicar esta guía y su efectividad como instrumento de validación nos lleva a proponerla como herramienta de validación de métodos para laboratorios acreditados con alcance flexible según la Norma UNE EN ISO 15189, al igual que para validación de métodos en laboratorios que aspiran a acreditarse.
Los requisitos para la implantación de alcance flexible han sido objeto de normativas en diferentes normas y sociedades europeas5,6; sin embargo, la ENAC aún no ha marcado directrices sobre la implementación de alcance flexible para la ISO 15189, por lo que creemos que este procedimiento podría incluirse en la futura nota técnica al respecto de la ENAC.
Queremos manifestar nuestro agradecimiento a todo el personal del Servicio de Análisis Clínicos del Hospital Universitario Príncipe de Asturias, sin cuya colaboración no hubiera sido posible la acreditación ni la realización de este trabajo.