La fistula gastropericárdica es una patología infrecuente y extremadamente grave que pone en riesgo la vida del paciente. Su etiología más frecuente es la secundaria a una lesión iatrogénica tras una cirugía gástrica. La clínica puede ser inespecífica con dolor precordial, simulando un síndrome coronario agudo, y acompañarse de alteraciones en el electrocardiograma. El diagnóstico se realiza mediante tomografía computarizada (TC) toracoabdominal con contraste oral e intravenoso. El tratamiento es quirúrgico y consiste en la reparación de la comunicación anómala. Se presenta un caso de un paciente de 81años con fístula gastropericárdica intervenido, con el objetivo de revisar el diagnóstico y la estrategia terapéutica apropiados.
Gastropericardial fistula is a rare, extremely serious and life-threatening condition. Its most common etiology is secondary to iatrogenic injury following gastric surgery. Clinical manifestations may be non-specific with precordial pain, simulating an acute coronary syndrome, and may be accompanied by electrocardiogram abnormalities. Diagnosis is made by thoracoabdominal computed tomography (CT) with oral and intravenous contrast. Treatment is surgical and consists of repair of the anomalous communication. We present the case of an 81-year-old male patient with gastropericardial fistula who underwent surgery, with the aim of reviewing the diagnosis and the appropriate therapeutic strategy.
La fistula gastropericárdica es una comunicación anómala entre el estómago y el pericardio1. Es una patología infrecuente que puede ser extremadamente grave por el riesgo de desencadenar situaciones críticas como taponamiento cardiaco, sepsis e inestabilidad hemodinámica, con la consecuente amenaza para la vida del paciente2. Su etiología es múltiple, y la más frecuente es la secundaria a una lesión iatrogénica tras una cirugía gastroesofágica (técnicas antirreflujo, cirugía bariátrica o resecciones oncológicas) o tras un procedimiento intervencionista (técnicas endoscópicas), quedando el trauma abierto o cerrado, procesos infecciosos o la ingesta de cáusticos como causas menos comunes3,4. La clínica es inespecífica, con dolor precordial y epigástrico, fiebre, disnea y alteraciones en el electrocardiograma3. El diagnóstico se realiza mediante tomografía computarizada (TC) toracoabdominal con contraste intravenoso (CIV). El contraste oral también puede emplearse, aunque con cautela debido a sus posibles efectos adversos sobre el pericardio3. El tratamiento es quirúrgico y consiste en la reparación de la comunicación anómala3,4. Se presenta un caso de un paciente de 81años con fístula gastropericárdica que recibió cirugía precoz de manera exitosa con el objetivo de remarcar la importancia de un abordaje multidisciplinar de esta patología y revisar el diagnóstico y la estrategia terapéutica realizada.
Presentación del casoVarón de 81años, exfumador, obeso y dislipémico. Había sido intervenido de un quiste hidatídico del lóbulo hepático izquierdo en 1969 y de ulcus duodenal en 1979 a través de laparotomía media, con posterior eventración reparada en varias ocasiones mediante eventrorrafia y colocación de mallas supraponeuróticas (malla de Vicryl® y malla de politetrafluoretileno expandido [ePTFE]). Acude a urgencias por dolor torácico de horas de evolución, con irradiación a la mandíbula. El dolor empeora con la inspiración y con la postura y mejora con Cafinitrina® y paracetamol. Coincidiendo con el dolor, el electrocardiograma presenta una elevación del intervalo ST en la cara inferior. Ingresa a cargo de cardiología con el diagnóstico de síndrome coronario agudo.
Se realizó una placa de tórax, en la que se observa neumopericardio, que pasó inadvertido inicialmente (fig. 1A). Se activó el protocolo «código corazón», definido en nuestro centro como un dolor torácico de media hora de evolución refractario a tratamiento médico con elevación del ST en más de dos derivaciones contiguas, y desde el servicio de cardiología se realizó una coronariografía en la que no se encontraron lesiones coronarias significativas y se observó un derrame pericárdico, atribuyéndose los cambios del electrocardiograma a una pericarditis. Además, durante el procedimiento se detectó un artefacto adyacente a las cámaras cardiacas derechas. Una vez finalizado el procedimiento, se revisó la radiografía de tórax y se contactó con el servicio de radiodiagnóstico para confirmar que se trataba de un neumopericardio, y se decidió hacer una TC para una mejor valoración.
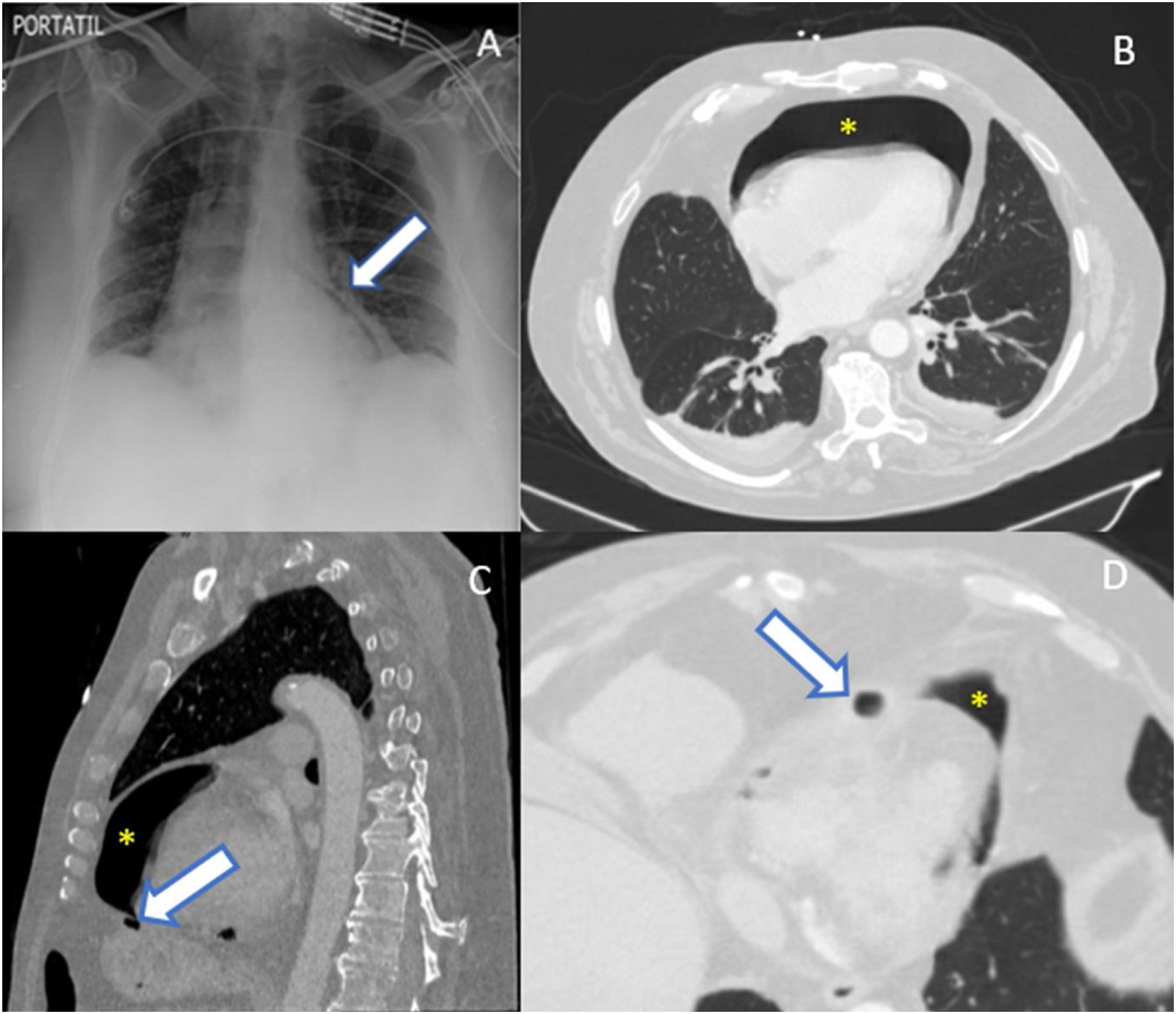
A) Radiografía de tórax. Línea radiolúcida que rodea parcialmente el ventrículo izquierdo compatible con neumopericardio leve (flecha).
B-D)TC de tórax con CIV con ventana de pulmón, planos axiales (B y D) y sagital (C). B-D)Contenido aéreo con morfología en semiluna que rodea la cara anterior, ambas caras laterales y la cara inferior del corazón con un espesor máximo de aproximadamente 35mm en relación con neumopericardio (asterisco amarillo). C y D)En las capas externas de la pared del estómago, en la región del cuerpo en la curvatura mayor, hay una imagen de burbuja aérea que podría tratarse de un divertículo, en íntimo contacto con la pared anterior y medial del diafragma. Aunque no se objetiva una clara solución de continuidad, es la zona de mayor proximidad al neumopericardio (flechas).
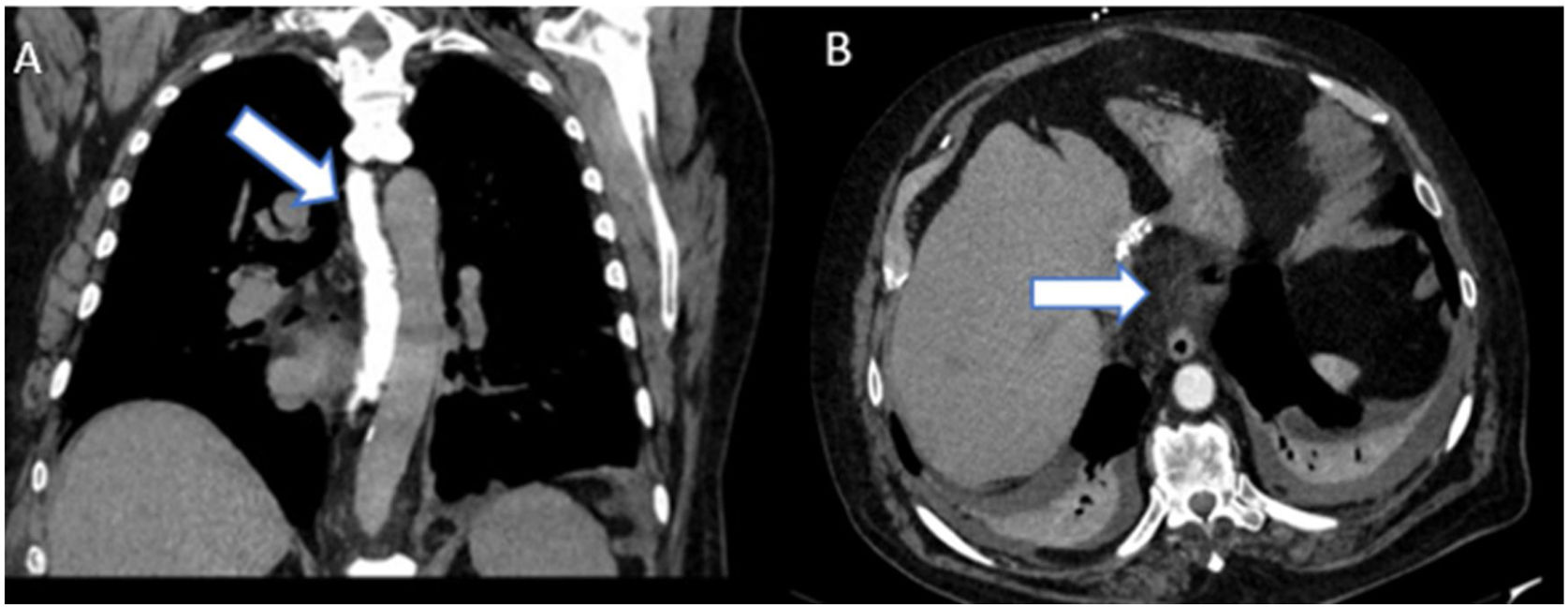
Se realizó una TC toracoabdominal con CIV, que mostró contenido aéreo con morfología en semiluna que se extiendía por la cara anterior, por ambas caras laterales y por la cara inferior del corazón con un espesor máximo de aproximadamente 35mm, en relación con neumopericardio (fig. 1B-D). También se vieron pequeñas burbujas aéreas en los recesos pericárdicos derechos, de predominio en el receso aórtico, que también presentaba una pequeña cantidad de líquido. En las capas externas de la pared del estómago, en la región del cuerpo en la curvatura mayor, había una imagen de burbuja aérea, que podría tratarse de un divertículo, en íntimo contacto con la pared anterior y medial del diafragma, que, aunque no se objetivaba una clara solución de continuidad, es la zona de mayor proximidad al neumopericardio (fig. 1C,D). No había evidencia de claras fístulas traqueales o bronquiales. Se administró contraste oral (diatrizoato de meglumina y sodio, Gastrografin®) sin objetivar extravasación de contraste a nivel del esófago (fig. 2A) ni a nivel del estómago, aunque este último no presentaba repleción completa de contraste. Además, se identificaba una estriación de la grasa adyacente a la unión esofagogástrica (fig. 2B).
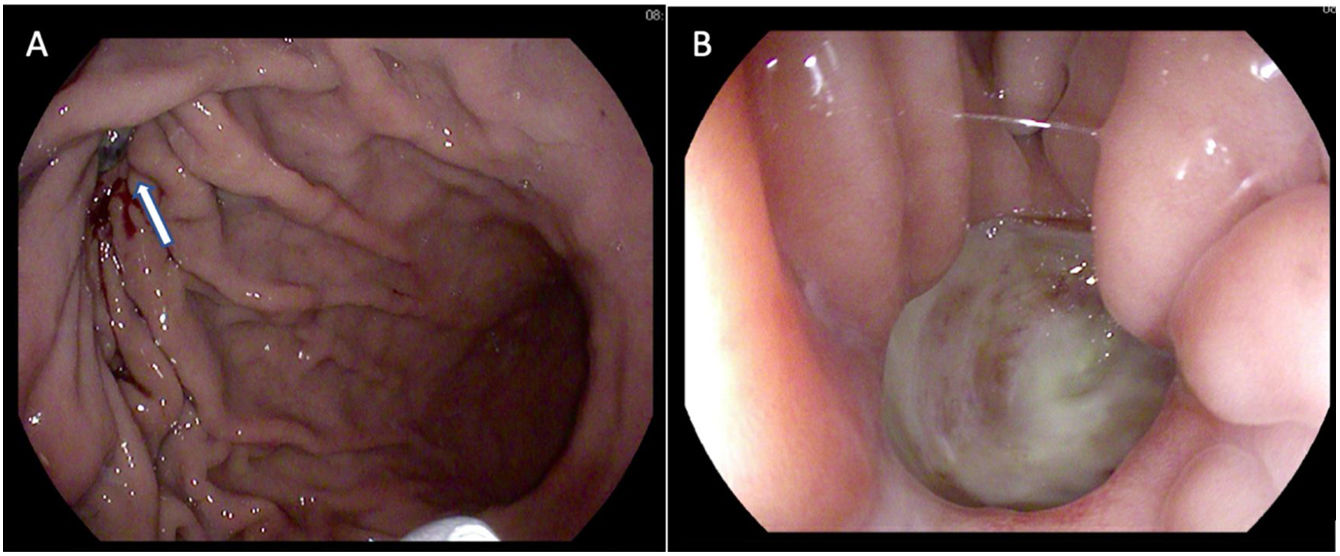
Dados los hallazgos, se realizó una gastroscopia, que mostró en la curvatura mayor del cuerpo gástrico, hacia la cara anterior, un probable divertículo de 8mm, sin eritema circundante, con fondo de fibrina simulando una úlcera (fig. 3A). En la zona central se veía un poro puntiforme, sugestivo de una fístula (fig. 3B). Con el diagnóstico de fístula gastropericárdica se decide intervención quirúrgica por vía abierta debido a las cirugías previas. En la cirugía se identificó, en la curvatura mayor del estómago, un orificio fistuloso de 1cm de diámetro. El orificio pericárdico es milimétrico y se amplió mediante tijera, creando una ventana pericárdica, para vaciar el derrame pericárdico de aspecto seroso (<50cc). Se realizó una resección segmentaria de la curvatura mayor gástrica, incluyendo el orificio fistuloso, con endograpadora y se reforzó la línea de grapado con sutura monofilamento reabsorbible. El orificio diafragmático se reparó con una sutura no reabsorbible. El paciente evolucionó de manera favorable y fue dado de alta al 5.° día postoperatorio. En la revisión ambulatoria a los 3meses está asintomático tanto a nivel gástrico como a nivel cardíaco. La anatomía patológica solo mostró cambios inflamatorios en la pared gástrica.
Imágenes de gastroscopia. A)En la curvatura mayor del cuerpo gástrico se ve una imagen redondeada de unos 8mm de bordes bien delimitados (flecha) que parece corresponder con un divertículo con fondo de fibrina. B)En la zona central se visualiza un poro puntiforme/imagen de burbujeo que podría ser sugestivo de un divertículo complicado por fistulización. La supuración por la fístula cubriría las paredes del divertículo simulando la apariencia de una úlcera.
La fístula gastropericárdica es una patología que puede ser letal por producir taponamiento cardíaco. La causa más frecuente es la iatrogénica tras cirugía gastroesofágica (funduplicatura de Nissen, resecciones tumorales, cirugía por úlcera péptica), y suele presentarse transcurridos años desde la cirugía, o tras procesos intervencionistas (broncoscopia, endoscopia, toracocentesis)4,5. Otras causas menos frecuentes son los traumatismos abiertos o cerrados, las úlceras gástricas refractarias, la ingesta de cuerpos extraños o de agentes cáusticos, las neoplasias o las infecciones por gérmenes productores de gas3,6,7.
Estos pacientes suelen presentar dolor torácico penetrante y disnea, siendo característica la irradiación del dolor al hombro izquierdo por irritación pericárdica en el momento del diagnóstico. No obstante, algunos pacientes refieren otros síntomas, como dolor abdominal, sangrado digestivo o alteraciones en la deglución, como disfagia o vómitos, de años de evolución antes del diagnóstico definitivo3,6.
El diagnóstico es fundamentalmente radiológico. En la radiografía de tórax puede aparecer una banda radiotransparente rodeando parcial o totalmente a la silueta cardiaca que corresponde a gas en el pericardio, que podría acompañarse también de líquido (hidroneumopericardio), aumentando así la sospecha de fístula gastropericárdica4. La TC toracoabdominal con CIV es la prueba más sensible para el diagnóstico de esta patología. Puede identificarse hidroneumopericardio y un engrosamiento y una hipercaptación pericárdicos. En pocas ocasiones podremos visualizar claramente el trayecto fistuloso. El contraste oral tiende a usarse con cautela, debido a que se desconocen sus posibles efectos adversos sobre el pericardio. La reconstrucción de las imágenes en los tres planos del espacio permite la visualización correcta de la fístula y la planificación de la cirugía4-6. No obstante, si los estudios radiológicos no son concluyentes, la realización de una gastroscopia para esclarecer el diagnóstico ha demostrado ser útil sin aumentar el riesgo de taponamiento cardiaco8.
El tratamiento de la fístula pericárdica es quirúrgico y debe realizarse de manera precoz, con cobertura antibiótica y antifúngica3,8. El abordaje puede ser laparoscópico o mediante laparotomía, dependiendo de las características del paciente y de la experiencia del cirujano9. En el caso presentado se decidió laparotomía media debido al antecedente de múltiples cirugías abdominales junto a la existencia de una infección crónica de la prótesis parietal, colocada en el pasado durante la cirugía de la eventroplastia en posición supraponeurótica, que se extirpó durante la intervención. Independientemente del abordaje, todas las estrategias deben incluir drenaje del pericardio, resección del trayecto fistuloso, reparación del diafragma, reparación gástrica y tratamiento adicional de patología de base en función de los hallazgos intraoperatorios10. En el caso expuesto la etiología de la fístula probablemente esté asociada al antecedente de cirugías previas, motivo por el cual el cuerpo gástrico ha quedado adherido al diafragma, erosionándolo y generando finalmente la fístula hacia el pericardio subyacente.
ConclusiónLa fístula gastropericárdica es una entidad infrecuente pero que amenaza la vida del paciente. Es difícil de diagnosticar, ya que es muy complicada de sospechar clínicamente, dado que la sintomatología es típica de un síndrome coronario agudo. El antecedente de cirugía esofágica o gástrica, así como la historia de úlcera péptica, son las causas más frecuentes sin una relación temporal determinada. El abordaje multidisciplinar de estos pacientes es esencial para un diagnóstico correcto y una cirugía precoz para garantizar un tratamiento exitoso.
Contribucion de los autoresResponsable de la integridad del estudio: B. Carrasco Aguilera.
Concepción del estudio: B. Carrasco Aguilera, M. Martínez-Cachero García, L. Sanz Álvarez.
Diseno del estudio: B. Carrasco Aguilera, M. Martínez-Cachero García.
Obtención de los datos: B. Carrasco Aguilera, M. Martínez-Cachero García, F. Cadenas Fernández.
Busqueda bibliográfica: B. Carrasco Aguilera, P del Val Ruiz, L. Sanz Álvarez.
Revisión crítica del manuscrito con aportaciones intelectualmente relevantes: B. Carrasco Aguilera, M. Martínez-Cachero García, L. Sanz Álvarez.
Aprobación de la versión final: todos los autores.
FinanciaciónEl estudio no ha requerido financiación externa para su realización.
Conflicto de interesesNinguno de los autores presenta ningún tipo de conflicto de intereses ni con el material y el método usados en el estudio ni con los hallazgos descritos en el mismo.