Los síndromes autoinflamatorios (SAI) son entidades recientemente descritas1. Comprenden, entre otros, el síndrome PAPA (artritis piogénica, pioderma gangrenoso y acné), PASH (pioderma gangrenoso, acné e hidradenitis supurativa [HS]), y PAPASH (artritis piogénica, acné, pioderma gangrenoso e HS). Su fisiopatología incluye una activación aberrante del sistema inmunitario innato. Se manifiestan a nivel dermatológico como lesiones en el espectro de las dermatosis neutrofílicas. Desde el punto de vista de la genética, se han descrito mutaciones que tienen como consecuencia una disfunción de proteínas del complejo del inflamasoma. En la literatura está documentada la amiloidosis renal secundaria a la HS2.
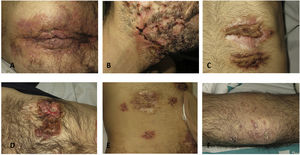
Caso clínicoUn paciente varón de 48 años fue ingresado en nuestro hospital en enero de 2020 a causa de un fracaso renal agudo. Sus antecedentes personales reflejaban una distocia social grave atribuible en parte al impacto personal y social de su enfermedad. Había pasado temporadas sin techo, medios de sostenimiento vital, ni contacto con su familia (una mujer fallecida por sobredosis de drogas y 2 hijos tutelados por los servicios sociales). Era fumador de 2 paquetes de tabaco al día. No explicaba antecedentes familiares conocidos de su enfermedad. Presentaba desde la adolescencia una HS afectando la totalidad del área glútea y perianal (fig. 1A), acné conglobata (fig. 1B) y pioderma gangrenoso múltiple (figs. 1C y D). Desde 2014, había padecido episodios de osteítis amicrobiana de la región sacra y coccígea. Una colonoscopia había descartado la enfermedad inflamatoria intestinal. Diversas biopsias de las lesiones perianales pusieron de manifiesto un proceso inflamatorio crónico y descartaron un carcinoma escamoso. El paciente había recibido antibióticos orales en tandas largas (3-6 meses) y antibióticos y corticoides intravenosos en varios ingresos hospitalarios motivados por la osteítis y los brotes inflamatorios de las lesiones cutáneas. Se inició tratamiento biológico con adalimumab para su HS, con un cumplimiento irregular y escasa eficacia, que motivaron un cambio a infliximab en pauta intensificada (10 mg/kg cada 8 semanas) en 2019. Valorado por un comité disciplinario medicoquirúrgico, había sido intervenido en varias ocasiones para el destechado de tractos fistulosos en la cara y la zona glútea. Se decidió una colostomía laparoscópica de descarga temporal como fase previa a una cirugía radical de la zona glútea y perianal. Como resultado, el fenómeno de patergia provocado por las incisiones quirúrgicas desencadenó nuevas lesiones de pioderma gangrenoso (fig. 1E). El paciente continuó fallando a las visitas de control, y abandonando las infusiones de infliximab, hasta que una analítica realizada en Atención Primaria en enero de 2020 puso de manifiesto una alteración grave de la función renal que motivó su ingreso hospitalario.
Imágenes clínicas del paciente. A) Hidradenitis supurativa fistulizante en el área glútea y perianal. B) Lesiones de acné conglobata. C) Lesiones de pioderma gangrenoso en el abdomen. D) Lesiones agudas de pioderma gangrenoso en el pecho. E) Patergia provocada por las incisiones de la cirugía laparoscópica. F) Lesiones de psoriasis en los codos.
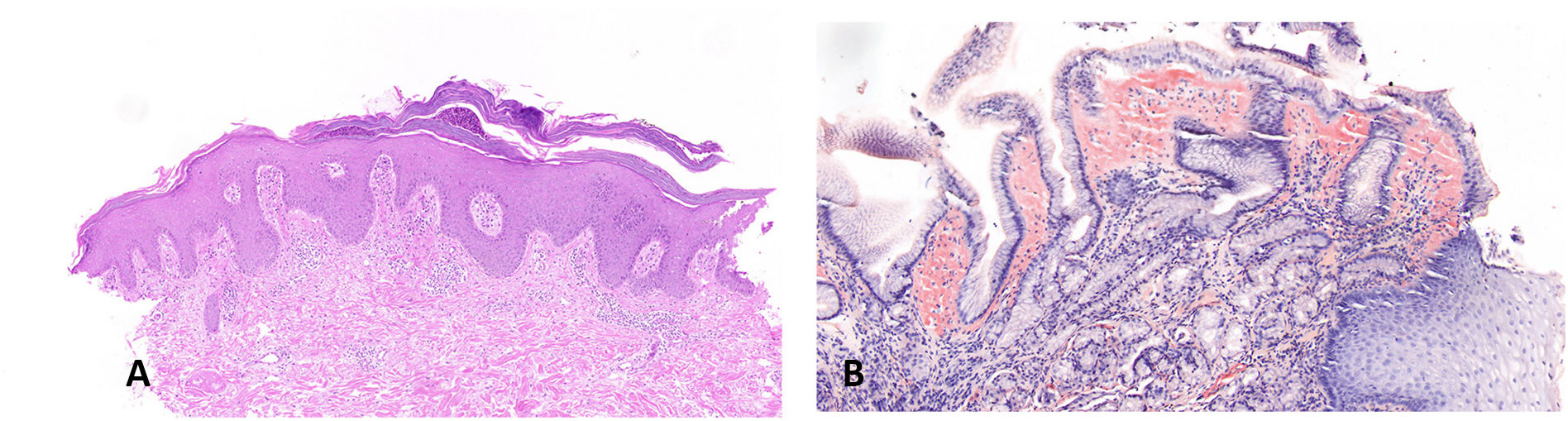
Al ingreso, los valores de laboratorio más destacados fueron una creatinina plasmática de 5,35 mg/dl, y una urea de 97 mg/dl, una proteinuria en el rango nefrótico, anemia y elevación de reactantes de fase aguda. La diuresis estaba inicialmente preservada. Durante el ingreso, se observó la aparición de lesiones en placas eritematosas y descamativas generalizadas (fig. 1F), y el estudio histopatológico de una biopsia punch confirmó la impresión clínica de psoriasis (fig. 2A). El paciente explicaba dolor epigástrico y vómitos. Por ello, recibió una fibrogastroscopia, y la toma de biopsias de unas lesiones nodulares visualizadas en la mucosa gástrica puso de manifiesto depósitos de amiloide (fig. 2B). El mismo diagnóstico fue confirmado por una biopsia de la grasa abdominal. La afinidad por el Rojo Congo se perdía tras la incubación con permanganato potásico, confirmándose una amiloidosis secundaria. El paciente manifestó palpitaciones, y el estudio mediante Holter reveló una taquicardia paroxística supraventricular. La ecocardiografía confirmó una hipertrofia ventricular izquierda indicativa de amiloidosis cardíaca. Fue tratado con ivabradina, consiguiendo un buen control de los episodios de taquicardia. Se desestimó la práctica de una biopsia renal puesto que la amiloidosis había sido ya confirmada mediante las biopsias gástrica y cutánea, y la situación de colapso hospitalario provocada por la pandemia de COVID-19 en España durante ese periodo limitaba más procedimientos invasivos.
A) Biopsia punch de la lesión del codo, evidenciando acantosis, elongación de papilas, paraqueratosis focal con microabscesos de Munro y un infiltrado mixto inflamatorio dérmico, hallazgos demostrativos de psoriasis (HE 10×). B) Biopsia gástrica mostrando depósito de amiloide (rojo Congo 10×).
Un estudio genético, incluyendo un panel de NGS (next generation sequence) diseñado para enfermedades autoinflamatorias, puso de manifiesto una mutación heterocigótica en el gen MEFV (c.442G > C), actualmente clasificada como variante de significado incierto por el American College of Clinical Genetics and Genomics. No se detectaron mutaciones en los genes PSTPIP1, PSENEN, PSEN1 o NSCT.
Se estableció el diagnóstico de una amiloidosis secundaria a un síndrome PsPAPASH (psoriasis, artritis piogénica, acné, pioderma gangrenoso e HS). Se inició tratamiento con tocilizumab intravenoso (8 mg/kg/mes), con mejoría de los reactantes de fase aguda, pero no del deterioro de la función renal, que requirió iniciar la hemodiálisis en abril de 2020. En ese momento, en el pico de la pandemia por COVID-19 en España, y con la práctica totalidad del hospital dedicado a atender enfermos con la infección por coronavirus, el paciente comenzó a manifestar síntomas compatibles con neumonía por SARS-CoV-2 (tos, disnea y fiebre), que fue confirmada mediante PCR y radiografía de tórax. Sus elevados requerimientos de FiO2 motivaron el tratamiento, según protocolo, con azitromicina, hidroxicloroquina, y pulsos de metilprednisolona. Al no manifestar mejoría, se decidió adelantar la segunda dosis de tocilizumab, administrado inicialmente para la amiloidosis, consiguiendo una mejoría rápida de la función respiratoria. El paciente pudo ser dado de alta en mayo, y en la actualidad sigue tratamiento con hemodiálisis y tocilizumab semanal subcutáneo a dosis de 162 mg.
ComentarioLos SAI con manifestaciones en el espectro de las dermatosis neutrofílicas comprenden un espectro clínico-patológico mal definido4. Más que entidades individuales, constituyen manifestaciones de una disfunción de la inmunidad innata causante de lesiones cutáneas y/o articulares que pueden combinarse de diferente manera en cada paciente: acné, HS, osteítis, pioderma gangrenoso, o psoriasis son las principales. Su base inmunogenética no está completamente aclarada, y no siempre están ligados a mutaciones del complejo gamma-secretasa, como se ha descrito en ciertas formas familiares de HS. Se han descrito previamente mutaciones en el gen de la fiebre mediterránea familiar (MEFV) en la HS3. Dicho gen regula la pirina, una proteína con una función capital en la respuesta inflamatoria. Su disfunción podría llevar a una inflamación inadecuada o prolongada en el tiempo, tal y como ocurre en el síndrome PsPAPASH. La mutación encontrada en nuestro paciente puede ser frecuente en la población mediterránea sana, y no puede ligarse con la patogenia de su enfermedad en el momento actual.
La amiloidosis secundaria es debida al daño de órganos internos ocasionado por el depósito de fibrillas originadas de fragmentos proteolíticos de amiloide A sérico, producidos por el hígado en el contexto de una enfermedad inflamatoria crónica. El objetivo primordial del tratamiento consiste en el control riguroso de la inflamación asociada a la enfermedad de base, aunque una vez se ha producido el daño renal por depósito, el pronóstico de recuperación de la función renal es sombrío.
El tratamiento óptimo de los SAI no está bien definido. Los inmunosupresores y antagonistas del factor de necrosis tumoral, la IL-1 o la IL-6 son los tratamientos más habitualmente empleados5. Nuestra opción terapéutica fue tocilizumab, un antagonista de la IL-6, debido sobre todo a la falta de efecto de los antagonistas del TNF, motivada en parte por el mal cumplimiento terapéutico por parte del paciente. Tocilizumab se ha empleado tanto para la amiloidosis secundaria6 como para la neumonía grave por COVID-197,8, ya que es uno de los fármacos que puede controlar la tormenta de citoquinas que causa el daño pulmonar y el fracaso ventilatorio. En la actualidad el paciente sigue en hemodiálisis, y las lesiones cutáneas están controladas en su vertiente inflamatoria. Sigue pendiente una cirugía radical seguida de reversión de la colostomía, y la posibilidad remota de un trasplante renal.
Conflicto de interesesLos autores no manifiestan ningún conflicto de interés.