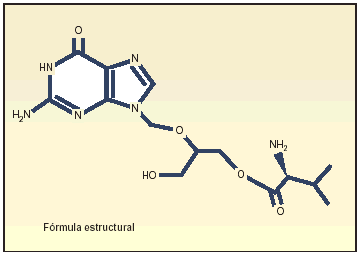
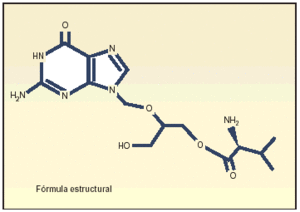
Valganciclovir es un profármaco de ganciclovir con una biodisponibilidad del 60%, diez veces mayor que la de ganciclovir oral. Es el primer tratamiento sistémico oral disponible para el tratamiento, tanto de inducción como de mantenimiento, de la retinitis por citomegalovirus.
El citomegalovirus (CMV) es la causa más común de las infecciones oculares y una de las causas más comunes de muerte de personas afectadas por VIH.
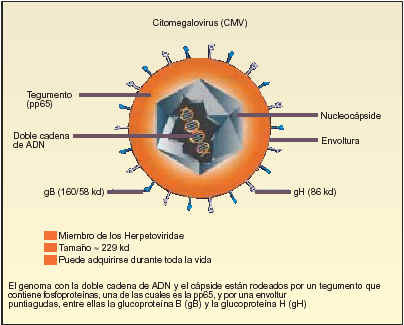
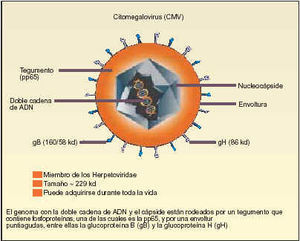
El CMV pertenece a la familia del virus del herpes y es, esencialmente, una enfermedad transmisible sexualmente, a través de transfusiones de sangre, de madre a hijo o por vía de trasplante de órganos.
La incidencia de la infección aumenta con la edad. Casi la mitad de la población adulta, en países desarrollados, está infectada por el virus. La tasa de infección del CMV es mucho más alta en los grupos de alto riesgo de infección por VIH (casi la totalidad de los varones homosexuales) de los que entre el 25 y el 40% desarrollan el CMV.
El riesgo de contraer CMV es directamente proporcional a la disminución del recuento de las células CD4+.
Se cree que la enfermedad por CMV es causada por la reactivación del virus inactivo en las personas con un sistema inmunológico deprimido. Las infecciones por CMV no causan enfermedades graves ni amenazan la vida a menos que el sistema inmunológico esté gravemente deprimido.
Tras la introducción del TARGA (tratamiento antirretroviral de gran actividad) la disminución de la incidencia de retinitis por CMV ha sido espectacular y ha puesto de manifiesto claramente la importancia de la función inmunitaria en el desarrollo de la enfermedad. No obstante, la retinitis por CMV sigue siendo motivo de preocupación, ya que algunos pacientes responden mal al tratamiento antirretroviral y su función inmunitaria no se restaura de modo apropiado. Además, el CMV es una amenaza para los pacientes que inicialmente responden al TARGA y luego desarrollan resistencia y desciende, por consiguiente, su función inmunitaria.
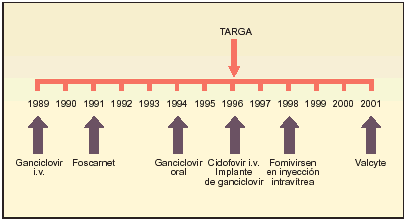
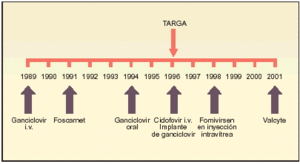
Con anterioridad a 1989 no se disponía de ningún tratamiento contra el CMV. Ganciclovir, por vía intravenosa (i.v.), fue el primer tratamiento utilizado en la retinitis por CMV. Más adelante aparecieron tratamientos sistémicos intravenosos y se desarrollaron tratamientos locales (implantes e inyecciones oculares). En 1994 se dispuso de ganciclovir oral y también de foscarnet y cidofovir.
Debido a las dificultades que supone el uso prolongado de tratamiento i.v. y al carácter invasivo de los implantes y las inyecciones intraoculares, el desarrollo de tratamientos en los últimos años se ha basado en obtener medicamentos vía oral eficaces para la retinitis por CMV.
Valganciclovir, un profármaco de ganciclovir, se ha desarrollado y ha demostrado su eficacia vía oral. Su biodisponibilidad del 60% es diez veces superior a la de ganciclovir oral y da lugar a concentraciones plasmáticas similares a las obtenidas con ganciclovir i.v.
Mecanismo de acción
Tras la administración oral de valganciclovir, las esterasas intestinales y hepáticas lo convierten rápidamente en ganciclovir.
Ganciclovir inhibe la replicación del CMV al inhibir de forma selectiva la ADN-polimerasa del virus. La ADN-polimerasa de la célula huésped es mucho menos sensible a la inhibición por ganciclovir.
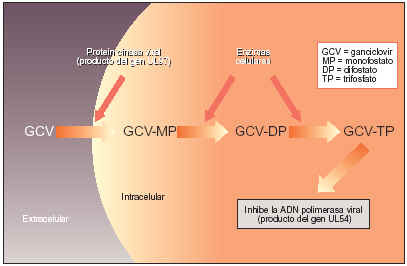
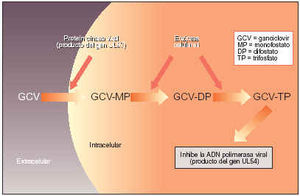
Para que ganciclovir sea activo debe fosforilarse y convertirse en la forma trifosfato (TP). Tras entrar en una célula infectada, una cinasa codificada por el virus convierte ganciclovir en su monofosfato. Después, las cinasas de la célula añaden dos grupos fosfato para formar el TP activo.
Ganciclovir-TP inhibe la replicación viral al competir con desoxiguanosina-TP como substrato de la ADN-polimerasa del virus. La ralentización o la interrupción de la extensión de la cadena de ADN inhibe la replicación viral, debido a la menor incorporación de dGTP y a la incorporación de ganciclovir-TP. La prolongada vida media intracelular de ganciclovir-TP en las células infectadas por el CMV potencia la eficacia de ganciclovir frente al CMV. Una vez formado, ganciclovir-TP es bastante estable y se mantiene durante días en la célula infectada, lo que hace que la actividad viral sea prolongada. Ganciclovir-TP también inhibe la ADN-polimerasa microcelular, pero para ello, su concentración debe ser de siete a doce veces mayor que la que inhibe la ADN-polimerasa viral.
Farmacocinética
Valganciclovir es un profármaco de ganciclovir con una biodisponibilidad alta que se absorbe bien en el tracto gastrointestinal y se metaboliza rápidamente a ganciclovir en la pared intestinal y en el hígado.
Estructura del virión del CMV
La biodisponibilidad absoluta de ganciclovir administrado con alimentos es del 60%, alrededor de diez veces mayor que la de ganciclovir administrada por vía oral.
La exposición sistémica al profármaco, valganciclovir, es transitoria y baja. Los valores del área bajo la curva durante 24 horas y los de la concentración sérica máxima de valganciclovir son aproximadamente el 1% y el 3% de los de ganciclovir respectivamente.
Es recomendable que valganciclovir se administre con alimentos, ya que la proporcionalidad entre la dosis y el área bajo la curva de ganciclovir se mantiene sólo si el fármaco se administra con alimentos, según estudios abiertos realizados.
Debido a la rápida conversión de valganciclovir en ganciclovir, la unión a las proteínas plasmáticas de valganciclovir no se ha determinado. La unión a las proteínas plasmáticas de ganciclovir es del 1 al 2%. No es necesario ajustar la dosis según el peso corporal.
Cronología del desarrollo de los tratamientos para la retinitis por el CMV
Valganciclovir se hidroliza rápidamente a ganciclovir y no se han detectado otros metabolitos. Ningún metabolito de ganciclovir marcado radiactivamente administrado por vía oral, representó más del 2% de la radiactividad recuperada en las heces o en la orina.
Valganciclovir se elimina principalmente por excreción renal en forma de ganciclovir mediante filtración glomerular y secreción tubular activa.
Seguridad y tolerabilidad
Es de esperar que muchos de los efectos asociados al uso de ganciclovir se produzcan también con valganciclovir debido a la rápida conversión tras su administración oral.
Valganciclovir está aprobado para el tratamiento de la retinitis por CMV como tratamiento de inducción y de mantenimiento
Los acontecimientos adversos presentados con mayor frecuencia fueron: diarrea, neutropenia, náuseas, cefalea, anemia e infecciones relacionadas con catéteres.
En la actualidad se están realizando otros estudios para evaluar la seguridad y tolerabilidad a largo plazo. El aumento de la supervivencia de los pacientes, debido a los efectos del TARGA, ha permitido que la seguridad de valganciclovir se pueda evaluar durante períodos más prolongados.
Precauciones especiales
Valganciclovir no debe administrarse, si el recuento absoluto de neutrófilos es menor de 500 células/µl, el recuento de plaquetas es menor de 25.000/µl o la hemoglobina es menor de 8 g/dl.
Mecanismo de acción de ganciclovir
En los pacientes tratados con valganciclovir y con ganciclovir se ha observado leucopenia, neutropenia, anemia, trombocitopenia, pancitopenia, depresión de la médula ósea y anemia aplásica intensas. Por todo ello, el fármaco debe administrarse con precaución a los pacientes con citopenias preexistentes o a los que han recibido o están recibiendo fármacos o radioterapia mielosupresores. Puede producirse citopenia en cualquier momento del tratamiento y puede aumentar con el tratamiento continuado. Los recuentos celulares habituales empiezan a recuperarse entre 3 y 7 días después de la suspensión del tratamiento.
Valganciclovir puede producir alteración de la fertilidad y posee potencial mutágeno y teratógeno, por lo que, durante el tratamiento, deben adoptarse medidas anticonceptivas eficaces.
Es esencial cumplir estrictamente las recomendaciones posológicas para evitar sobredosis.
Si la función renal está alterada, debe ajustarse la dosis y, en todo momento, debe realizarse un control del paciente.
Conclusión
La retinitis por CRV que puede dañar gravemente la visión, sigue siendo una preocupación para los pacientes con inmunosupresión intensa y sostenida, a pesar de que la incidencia de infecciones oportunistas en los pacientes con sida ha disminuido considerablemente desde la introducción del TARGA. Incluso los pacientes cuya función inmunitaria se ha restaurado tras presentar una respuesta favorable al TARGA corren un cierto riesgo, ya que se han empezado a publicar casos clínicos de pacientes con retinitis recurrentes, a pesar de que sus recuentos de CD4+ habían aumentado.
En los pacientes con retinitis activa diagnosticada es necesario administrar un tratamiento de inducción durante 21 días y luego un tratamiento de mantenimiento. Antes sólo se disponía de tratamiento i.v, pero en la actualidad se dispone de otra alternativa, valganciclovir vía oral, un profármaco de ganciclovir que da lugar a concentraciones sistémicas de ganciclovir similares a las obtenidas con la dosis recomendada de ganciclovir i.v.
Valganciclovir está aprobado para el tratamiento de la retinitis por CMV como tratamiento de inducción y de mantenimiento en dosis de 900 mg (2 comprimidos de 450 mg) dos veces al día (inducción) o una vez al día (mantenimiento).