La condición imprescindible para que las conclusiones de un estudio sean aplicables a una generalidad es que esté dotado de validez interna y externa. Un error común consiste en aplicar el estudio a una muestra incorrecta, lo que puede anular parcial o totalmente su validez. En el presente artículo se indican las características esenciales de que dispondrá la muestra, determinante fundamental de la validez del estudio.
El primer determinante de la validez de un estudio es la muestra en la que se ensayará el procedimiento a evaluar. Sólo si ese procedimiento (un nuevo fármaco, una tecnología sanitaria, un programa de atención farmacéutica, etc.) se implementa en un subgrupo de pacientes que tenga análogas características a las del total de la población, se podrá extraer conclusiones que pueden extrapolarse al total de los pacientes.
La inobservancia de esta regla elemental ofrecerá unos resultados que no gozarán de la validez externa suficiente como para considerar que los obtenidos en el subgrupo evaluado pueden ser aplicables al grupo.
Para dotar a un estudio de validez, la muestra subconjunto de la población a estudio ha de ser representativa de la población o conjunto de todos los elementos que cumplen ciertas condiciones.
Con el fin de ver claros los conceptos que se manejan, así como la repercusión de su falta de observancia, analizaremos un ejemplo de un estudio ficticio de la implementación de un programa de atención farmacéutica (PAF) de hipertensión arterial (HTA).
Muestra de estudio
En el ejemplo que se incluye, se plantea la siguiente cuestión: ¿la implementación del programa de atención farmacéutica en hipertensos mejora el control de su presión arterial?
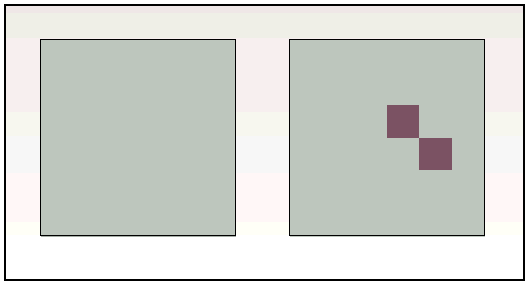
Para responder de un modo contundente a la pregunta planteada sólo se pueden realizar dos acciones (fig. 1):
Fig. 1. En la parte izquierda se representa el conjunto de la población de pacientes con HTA. En la derecha, se representa sólo una subpoblación representativa del universo de hipertensos: la muestra.
Implementar el mencionado PAF en todos los hipertensos existentes, analizando posteriormente la fracción que ha alcanzado un adecuado control.
Realizar el PAF sobre un grupo de hipertensos, analizar a continuación cuántos de ellos han logrado el objetivo del control de su HTA y extrapolar el resultado al conjunto de hipertensos.
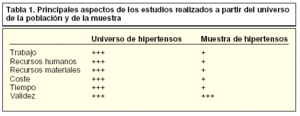
Por supuesto, el resultado más exacto lo ofrece la primera alternativa. Ahora bien, ello plantea dificultades obvias de toda índole (tabla 1), por lo que la respuesta más práctica es la segunda: escoger un subconjunto del conjunto de individuos que presentan HTA, implementar en él el programa y estimar posteriormente el grado de efectividad del PAF en el conjunto de la sociedad.
Elección de los pacientes
Si hemos desechado estudiar el programa sobre todos los pacientes que tengan HTA, se deberá aplicar sobre algunos de ellos. Pero, ¿a quiénes elegimos? La respuesta a tal cuestión es obvia, se elegirá a aquellos que formen un grupo que represente exactamente al formado por todos los hipertensos y que responda al objetivo del estudio, que tiene que haber sido definido previamente con exactitud y rigor.
El primer paso consiste en definir a los sujetos que pueden ser «elegibles» para el estudio; en nuestro caso podrían ser individuos con HTA primaria que se hallen en tratamiento antihipertensivo.
Si el estudio evalúa exclusivamente la HTA primaria será preciso imponer unas reglas para definir, de quienes presenten HTA, cuáles son incluibles (p. ej., que tengan diagnóstico médico de la enfermedad, que sean mayores de edad, que no presenten ciertas comorbilidades, etc.).
Finalmente, habrá que definir unas reglas que harán que ciertos pacientes, aún siendo elegibles y haber sido incluidos en un principio, no puedan evaluarse finalmente, por lo que son excluibles del estudio. En estos criterios se pueden citar, por ejemplo, los pacientes que lleven menos de un tiempo con el tratamiento, que no acudan regularmente a la misma oficina de farmacia para la obtención de sus fármacos antihipertensivos, que no quieran firmar el consentimiento de participación, etc.
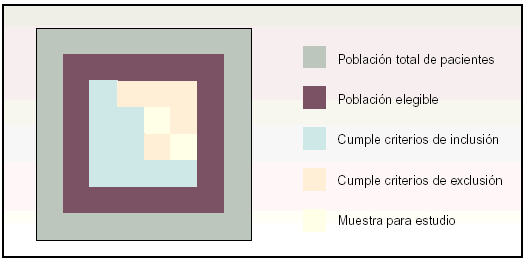
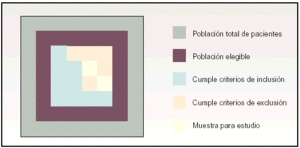
Como se ha visto, del universo de la población española se han definido unos criterios de elegibilidad para escoger solamente a los individuos susceptibles para el estudio. A continuación se definen unos criterios de inclusión y de exclusión con el fin de seleccionar sólo los que, pudiendo ser elegibles, cumplan con determinadas características que los hagan representativos de la población a análisis (fig. 2).
Fig. 2. De la población total del esquema de la izquierda se pasa a los elementos que compondrán la muestra del esquema de la derecha, después de haber superado los criterios de elegibilidad, inclusión y exclusión.
¿Se estudia igual a todos los incluidos?
Para poder concluir que un determinado programa de atención farmacéutica ha sido efectivo o no en una población concreta, hay que establecer unos escenarios que sean capaces de demostrar que el efecto observado está directa e inexorablemente relacionado con una causa; en nuestro caso, el PAF. El programa implementado varía la respuesta en el control de la enfermedad sólo si existe una relación causa/efecto entre ambos.
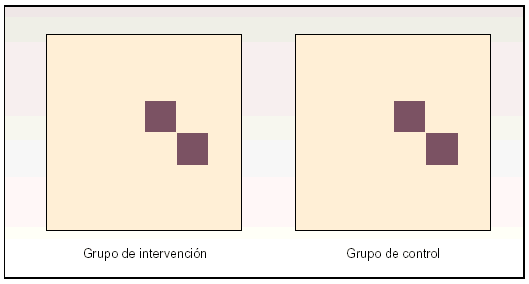
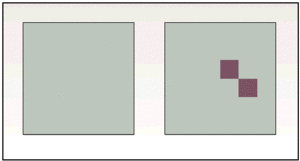
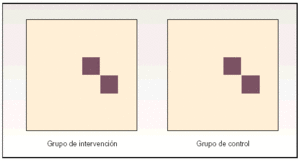
La única forma de poder llevar a cabo lo expuesto es la distribución del estudio en dos grupos homogéneos. La homogeneidad es un factor imprescindible para que el investigador pueda variar de forma voluntaria una única variable, dejando el resto idéntico en ambos grupos. De esta forma, la variación en los resultados obtenidos se deberá exclusivamente al cambio de la variable modificada por el investigador; es decir, se producirá una relación causa/efecto entre el PAF implementado y el resultado conseguido. Los dos grupos de estudio que se han aludido son el grupo de intervención y el grupo de control (fig. 3).
Fig. 3. El estudio debe realizarse sobre dos subpoblaciones de características homogéneas. En una de ellas, que se tomará como control, no se implementará la acción a estudio, mientras que en la otra subpoblación se ejercerá la intervención investigada. De otra manera no se podrá asignar una relación causa/efecto inequívoca.
En el grupo de intervención se aplicará sobre unos individuos el programa de atención farmacéutica, tal y como se haya definido con anterioridad. En el grupo control, se aplicará sobre otros individuos diferentes pero homogéneos con los anteriores, otro tipo de actuación, como puede ser el cuidado tradicional. En ambos grupos se realizarán las medidas oportunas de las variables primarias y secundarias establecidas en el protocolo del estudio.
El motivo de realizar un estudio controlado no es otro que asegurar que la respuesta ofrecida se debe únicamente a la acción implementada, eliminando otro tipo de respuestas, como la producida por el efecto placebo o por el efecto Hawthorne.
¿Quién va a cada grupo?
El azar es el elemento distorsionador más potente con que cuenta cualquier estudio. Ello quiere decir que, por mucho cuidado que se haya puesto en el diseño de las muestras, el azar ha podido incluir con mayor proporción en un grupo que en otro cualquier elemento de confusión que altere el resultado, pero no como consecuencia de la implementación del PAF, sino debido a la existencia de la diferente proporción de tales elementos.
La única forma de luchar contra el azar, que puede dar al traste con nuestro estudio, es contar con él; esto es, distribuyendo de forma aleatoria la muestra para estudio en los dos grupos citados. Así, el azar podrá distribuirse homogéneamente entre ambos grupos, ofreciendo dos subgrupos de características similares entre ambos y respecto a la población de la que son origen.
Este proceso, conocido como aleatorización, se consigue mediante diversas técnicas que deben ser seguidas rigurosamente. No valdrían, pues, medidas de seudoaleatorización basadas en metodologías sistemáticas, como la de incluir el primer sujeto que acuda a la oficina de farmacia, pues ello podría conllevar un sesgo oculto, como es el hecho de que fueran los jóvenes quienes acudieran en mayor proporción a primera hora, antes de ir al trabajo, dejando a los jubilados, que tienen una edad mucho más avanzada y, por tanto, una mayor prevalencia de HTA, fuera del estudio.
Número de pacientes a estudiar
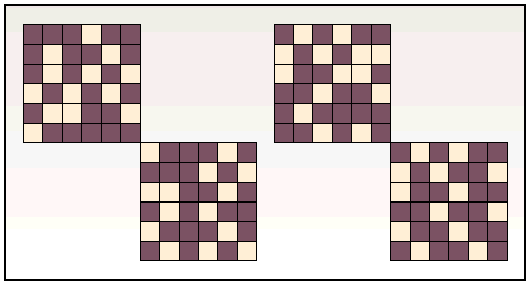
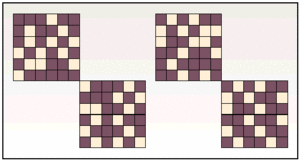
Un punto clave, olvidado en muchos más casos de lo que sería recomendable, es el del número de elementos que conforman el subgrupo muestra. Debe cumplir dos requisitos contrapuestos: que sea lo más grande posible para acercarse al tamaño de la población en estudio y ser más fiables sus resultados, y que sea lo más pequeño posible con el fin de ahorrar tiempo, recursos y esfuerzos en el estudio (fig. 4).
Fig. 4. Los pacientes que son elegibles y pasan los criterios de inclusión y exclusión son distribuidos aleatoriamente en los grupos de intervención y control en un número mínimo y calculado previamente, en función del objetivo del estudio. Los cuadrados grises oscuros cumplen con los criterios; los grises claros son aquellos que componen la muestra. El tamaño de ambos grupos será igual o muy aproximado.
Por otra parte, el número dependerá de los errores máximos que estemos dispuestos a asumir. Estos errores son de tipo I y II. Los de tipo I consisten en rechazar la hipótesis nula siendo ésta verdadera, es decir, estimar que hay diferencias entre los resultados del PAF y el cuidado estándar, cuando en realidad no existen. Los errores de tipo II aceptan una hipótesis nula cuando es falsa, es decir, manifiestan que los resultados entre las dos intervenciones realizadas en la HTA son iguales, cuando en realidad existe una diferencia entre ambas actuaciones.
La probabilidad de cometer un error de tipo I (la llamaremos α) y la de cometer uno de tipo II (la llamaremos β) deben ser definidas para estimar el tamaño de la muestra. Usualmente estos valores son 0,05 y 0,20, respectivamente.
Un dato esencial que influye poderosamente en la magnitud de nuestra muestra es el tamaño del resultado final que se evalúa en cada grupo. Cuanto mayor sea la diferencia buscada entre ambos será preciso un menor tamaño de muestra. Es obvio que si queremos demostrar que existe una diferencia en el porcentaje de pacientes con su presión arterial controlada debido a la actuación farmacéutica de sólo un 5%, precisaremos de mayor número de pacientes en estudio que si buscáramos un incremento del 50% por la aplicación del PAF.
Por último, la dispersión de los resultados producidos en los pacientes ofrece una tendencia para la estimación del tamaño de la muestra. Si el conjunto de pacientes presenta unos valores muy diferentes de sus presiones arteriales, es decir, una mayor dispersión, el tamaño final será notablemente mayor que si los valores están muy agrupados frente a un valor medio, es decir, con una dispersión pequeña.
A partir de lo expuesto, el tamaño de muestra es una función compleja de las variables de las que depende, pudiendo describirse como: N = f (α, β, (Ei Ec), s2. Siendo N el tamaño de la muestra a estudio; α, la probabilidad de error tipo I; β, la probabilidad de tipo II; Ei y Ec, los efectos obtenidos en el grupo de intervención y control, y s2, la desviación típica.
Análisis de homogeneidad de la muestra
Es de todos sabido que la presión arterial aumenta de forma progresiva con la edad. Asimismo, hay evidencias de que la prevalencia de HTA en diabéticos es superior a la estimada en la población no diabética. También se sabe que cuanto mayor tasa de hipertensos no controlados haya, mejor resultado se puede obtener. Por último, se ha comprobado que la proporción de sujetos con HTA es variable con el sexo, predominando entre los varones. Todo ello quiere decir que se habrá de analizar con rigor si existen diferencias o no en cuanto a las tasas de elementos de confusión entre las muestras del grupo control y el de intervención.
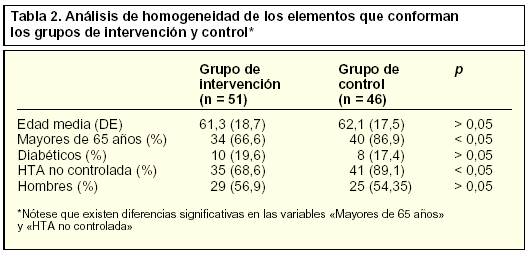
Siguiendo con nuestro ejemplo, imaginemos que en la muestra analizada se hallan distribuidas las variables edad, diabetes, HTA no controlada y sexo, tal como se indica en la tabla 2. Es preciso, entonces, determinar la homogeneidad entre los grupos al inicio del estudio aplicando las pruebas estadísticas correspondientes. Así, se observa que en el grupo de intervención existe una proporción menor y estadísticamente significativa de pacientes mayores de 65 años y de hipertensos no controlados. Estos resultados pueden desvirtuar las conclusiones finales ya que, como se dijo anteriormente, una mayor tasa inicial de HTA descontrolada puede ofrecer un mejor resultado, que no podría ser nunca aplicable al programa de intervención implementado, sino a la variable de confusión.
A la vista de lo expuesto, se observa la extraordinaria importancia de realizar el estudio de intervención farmacéutica sobre una muestra perfectamente extraída de la población total, ya que la falta de seguimiento de las razones indicadas puede anular parcial o incluso totalmente las conclusiones del estudio.
Bibliografía general
Carrasco J. Bioestadística básica. 1.ª ed. Madrid: Cibest, 1990-1991.
Cobo E. Estadística para no estadísticos. 1.ª ed. Barcelona: Gestión 2000, 1993.
Laporte J. Principios básicos de la investigación clínica. 2.ª ed. Barcelona: Comunicación en Ciencias de la Salud. División de Biomedical Systems Group, 2001.
Matos L (editor). Farmacoepidemiología. 1.ª ed. Santiago de Compostela: Xunta de Galicia, 1995.
Pérez-Llantada M. Evaluación de programas de salud y servicios sociales: Metodología y ejemplos. 1.ª ed. Madrid: Dykinson, 1999.
Rebagliato M, Ruiz I, Arranz M. Metodología de investigación en epidemiología. 1.ª ed. Madrid: Díaz de Santos, 1996.
Sanz A. Atención farmacéutica y la evaluación farmacoeconómica. Acófar 2000;383:9-11.
Sanz A. Diseño de un estudio farmacoeconómico. Offarm 2000:19(10):164-7.
Sanz A. Farmacoeconomía aplicada en atención farmacéutica. El Farmacéutico 2000:243:71-7.