El accidente cerebrovascular (ACV) es una de las principales causas de discapacidad y mortalidad a nivel mundial, generando un importante impacto en el sistema de salud. Es una emergencia tiempo-dependiente y las acciones rápidas e integradas inciden en los resultados.
ObjetivoDescribir cómo los servicios de emergencia prehospitalaria adquieren una importancia crítica, destacándose como agentes fundamentales para lograr resultados óptimos, dado que la activación de un protocolo de ACV desde el medio prehospitalario implica una mayor posibilidad de recibir un tratamiento de recanalización.
DesarrolloEn esta revisión narrativa se detallan los principales aspectos actuales del abordaje de los pacientes con ACV desde la etapa prehospitalaria, con énfasis en la integración del enfoque en un protocolo de ACV que incluya todos los eslabones que interactúan durante la fase hiperaguda.
ConclusionesLa mejoría de la asistencia en este período, por medio de la capacitación y la implementación de protocolos, es un recurso fundamental para la optimización del diagnóstico y el tratamiento de estos pacientes.
Stroke is one of the main causes of disability and mortality worldwide, with a significant impact on the health system. It is a time-dependent emergency and quick and integrated actions affect the results.
ObjectiveTo describe prehospital emergency services critical importance, standing out as fundamental agents to achieve optimal results, since the activation of a stroke protocol from a prehospital setting implies a greater possibility of receiving a recanalization treatment.
Main textIn this narrative review, main current aspects of approaching stroke patients from the prehospital setting are detailed, with emphasis on integrating the approach into a stroke protocol that includes all the stages that interact during the hyperacute phase.
ConclusionsImprovement of medical assistance in this period, through training and implementation of protocols, is a fundamental resource for optimizing the diagnosis and treatment of these patients.
El accidente cerebrovascular (ACV) se caracteriza por su gran impacto en el sistema de salud1,2 y ha provocado 1 de cada 4 muertes en adultos en 2010. El 87% de esas muertes ocurrieron en países de bajos recursos3. América Latina ha experimentado cambios demográficos, con aumento de la prevalencia de los factores de riesgo y de la morbimortalidad asociada al ACV3. En Argentina, se atribuyen a las enfermedades del sistema circulatorio (incluido el ACV) el 28% de las muertes y la mortalidad por ACV ocupa el cuarto lugar entre todas las causas4. Al ser la primera causa global de discapacidad5, el impacto personal y socioeconómico es enorme. Se advierte su importancia como un problema de salud pública que requiere abordaje integral, desde la prevención hasta las intervenciones de terapia óptima. Sin embargo, en nuestro medio, la tasa de administración de activador tisular del plasminógeno recombinante (rtPA) y de otras modalidades de recanalización aún son bajas (1,2% en hospitales privados6, alrededor del 1% en una extrapolación combinada de datos públicos y privados de la Ciudad de Buenos Aires7).
ObjetivoDescribir la importancia de los servicios de emergencia médica prehospitalaria (SEM) en el manejo del ACV, como agentes fundamentales para un resultado óptimo.
DesarrolloUna emergencia tiempo-dependienteEl ACV se caracteriza por un déficit neurológico focal súbito debido a la interrupción del flujo sanguíneo en un área del sistema nervioso central8. Los ACV se clasifican en isquémicos y hemorrágicos; los primeros son mucho más frecuentes (87%)9. El ACV isquémico ocurre por la oclusión de un vaso, produciendo un núcleo de infarto y una zona isquémica periférica de penumbra, que, si bien es disfuncionante, se mantiene viable al inicio merced a la limitada irrigación colateral de vasos permeables10 (fig. 1). La homeostasis de la neurona se mantiene por el aporte constante de oxígeno y nutrientes; al disminuirse dicho aporte, su viabilidad es muy limitada11. Esta consideración justifica la importancia de recanalizar rápidamente el vaso afectado para promover la reperfusión (sobre todo de la zona de penumbra), limitar el área infartada y devolver el mejor estado funcional posible. La recanalización puede lograrse más frecuentemente a través de la terapia fibrinolítica intravenosa (iv) sistémica (rtPA) y/o una intervención endovascular.
La administración de rtPA dentro de la ventana terapéutica es la piedra basal del tratamiento de recanalización y reduce de forma consistente la discapacidad. La naturaleza tiempo-dependiente del ACV isquémico determina que la probabilidad de un mejor estado funcional es mayor cuanto más precoz sea la administración12: el tiempo es cerebro.
La trombectomía mecánica permite extraer el material trombótico mediante un catéter. Se indica ante la obstrucción de un gran vaso proximal, en la que la monoterapia con trombolíticos tiene menor eficacia13. Esta técnica disminuye las secuelas14, pero no está disponible de forma masiva y no todos los pacientes son candidatos. Si el paciente se encuentra en la ventana de 4,5h, se administra un trombolítico mientras se prepara la intervención. Pasada la ventana o ante contraindicación para rtPA, se realiza solo la trombectomía primaria.
Por otra parte, el accidente isquémico transitorio (AIT) es un episodio breve de disfunción aguda neurológica o retiniana, clásicamente de duración menor a 24h. Las actuales técnicas de diagnóstico por imágenes permiten evidenciar un infarto en hasta un tercio de los casos15, por lo que se prefiere definir al AIT como una disfunción breve sin infarto documentado16. El AIT es parte del continuo del síndrome cerebrovascular agudo y un importante factor predictivo para ACV, en especial en los primeros 90 días17. Desde la perspectiva prehospitalaria, el AIT es un diagnóstico retrospectivo: el profesional nunca debe «esperar a comprobar si revierte» para activar el código de ACV y, aún revertido, debe considerar el traslado a un centro en todos los casos para continuar la evaluación e iniciar estrategias preventivas15.
Fase hiperaguda y recanalizaciónEl ACV demanda respuestas rápidas e integradas del SEM y los efectores posteriores implicados en el manejo inicial. Dada la ventana estrecha para el tratamiento y las condiciones para administrarlo, el SEM es clave para lograr buenos resultados18: un paciente que ingresa a través de un código de ACV desde la etapa prehospitalaria tiene más probabilidad de acceso a la terapia y que esta ocurra más rápidamente19–21.
El período para administrar rtPA es de hasta 3h desde el inicio de los síntomas/última vez que el paciente fue visto normal/asintomático (ventana convencional) o hasta 4,5h desde el inicio de los síntomas (ventana extendida) para un grupo seleccionado10,20. Para el tratamiento endovascular, la ventana es de hasta 6h desde el inicio de síntomas en la mayoría de los casos, administrando rtPA mientras se prepara la intervención si el paciente ingresa antes de las 3 a 4,5h de inicio de los síntomas. El período puede extenderse hasta 24h en casos muy seleccionados con recursos especiales de diagnóstico por imágenes20,22,23, como los estudios de perfusión por tomografía computada (TC) y resonancia magnética que formaron parte de los criterios del estudio DEFUSE 324. Así, se ha informado que la trombectomía efectuada incluso hasta 24h puede mejorar el pronóstico a 90 días de pacientes específicos con ACV25.
Se reconoce la posibilidad de indicar rtPA en casos con tiempo de evolución incierto, como los que se despertaron con los síntomas (wake-up stroke). Esta conducta requiere una adecuada selección de los pacientes y estudios por imágenes de mayor complejidad. En casos correctos, se pueden obtener un mejor resultado funcional con fibrinolíticos, a expensas de una mayor tasa de sangrado intracraneal26–28.
Rol de los servicios de emergencia médicaEl ACV es una emergencia tiempo-dependiente. El papel del SEM prehospitalario es fundamental para un enfoque apropiado29. El abordaje se sistematiza en la guía de la American Heart Association (AHA)18 y el Consenso Argentino10. La iniciativa ANGELS, impulsada por la European Stroke Organization (ESO), tiene por objetivo mejorar la atención del ACV, fortalecer una red de centros preparados y ofrecer recursos para el equipo prehospitalario. Dentro de esos recursos se destacan: reconocer el ACV; elegir el centro receptor adecuado; prenotificar a dicho centro, activar el código de ACV y trasladar al paciente de forma expedita; realizar las intervenciones necesarias para estabilizar al paciente sin prolongar el tiempo de traslado30. Parece recomendable que cada SEM cuente con una lista actualizada y revisada frecuentemente de los centros receptores adecuados para estos pacientes.
Reconocer el accidente cerebrovascularEl manejo prehospitalario comienza con el contacto de un testigo al número local de emergencias. El operador del SEM es un personal con entrenamiento específico para el triage telefónico, despacho de la unidad de emergencias y para dar instrucciones antes de la llegada de la ambulancia (prearribo). Al inicio de la llamada, se obtienen los datos de contacto (para restablecer la comunicación en caso de interrupción), la filiación del paciente y se geolocaliza la emergencia. El operador realiza preguntas pertinentes para reconocer emergencias tiempo-dependientes. Si sospecha un ACV, activa el protocolo cuando el interrogatorio brinde datos como trastorno súbito del habla, pérdida súbita de fuerza en uno o más miembros, desviación de la comisura labial, pérdida súbita de la visión, trastornos de la sensibilidad, cefalea intensa, deterioro súbito de la conciencia, etc. Dado que la capacidad para reconocer el ACV telefónicamente es un desafío y la sensibilidad diagnóstica puede no ser óptima aún aplicando escalas estandarizadas31, es recomendable un alto índice de sospecha a la hora de activar el código de ACV. Los pacientes en los que se sospecha un ACV desde la recepción del llamado muestran mejores tiempos puerta-TC y puerta-aguja32. Durante el trayecto, el operador del SEM se mantiene al teléfono obteniendo más datos, brindando instrucciones de prearribo e instruyendo la preparación para la llegada del móvil con acciones simples para ahorrar tiempo valioso (quitar las llaves de la puerta, aguardar con el ascensor en la planta baja, despejar la entrada). La comunicación solo finaliza cuando el operador indica hacerlo. Ante una comunicación no fluida porque es el paciente con trastornos del habla quien llama, se requieren todos los recursos técnicos del SEM para obtener la localización y brindar ayuda, sin desestimar un llamado por una comunicación poco satisfactoria. Como parámetro de calidad, el SEM debe brindar respuesta telefónica en menos de 90seg y, en caso de una emergencia tiempo-dependiente, apuntar a un tiempo de arribo<8min.
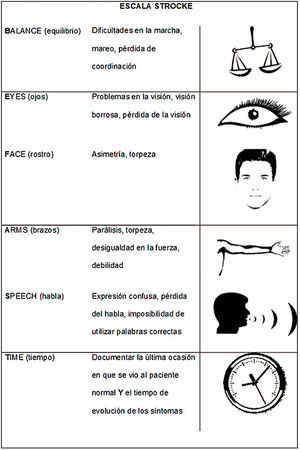
Cuando el equipo de emergencias toma contacto con el paciente, se procede a la evaluación inicial, asegurando una vía aérea permeable, buena ventilación y oxigenación y un correcto estado hemodinámico; luego, se procede a una breve evaluación neurológica. Se determina el estado de conciencia y se procede a reconocer el ACV con escalas para estandarizar el proceso. La mayoría de las escalas prehospitalarias pueden completarse en menos de 1min y las escalas de Cincinatti (CPSS) (tabla 1) y FAST (fig. 2) pueden ser aplicadas por un profesional no médico. El entrenamiento en su uso mejora la sensibilidad profesional para reconocer el ACV33. La CPSS es una de las más difundidas, se encuentra ampliamente validada34 y fue la preferida para uso en terreno en una revisión Cochrane35. La escala FAST evalúa los mismos componentes, con una sistemática diferente36; en una adaptación37,38 se modificó el acrónimo, reemplazando la T por «tiempo» (de evolución de los síntomas) y/o «teléfono» (prenotificar), aunque esos componentes no forman parte de la descripción original.
Escala prehospitalaria para accidente cerebrovascular de Cincinatti (CPSS)
| Se valora la presencia de uno o varios de los siguientes síntomas: asimetría facial, pérdida de fuerza en los brazos y afasia/disartria.• Asimetría facial: solicitar al paciente que muestre los dientes o sonría.∘ Respuesta normal: ambos lados de la cara se mueven de la misma forma.• Descenso del brazo: solicitar al paciente que cierre los ojos y extienda los brazos, manteniéndolos elevados con las palmas hacia arriba, durante 10seg.∘ Respuesta normal: los brazos se mantienen en la posición inicial, o se mueven de igual modo. También pueden ser útiles otros hallazgos, como evaluar la fuerza en la prensión de manos.• Habla anormal: solicitar al paciente que diga alguna frase o trabalenguas.∘ Respuesta normal: utiliza las palabras correctas sin arrastrarlas. |
| Especificidad(%) | Sensibilidad(%) | |
|---|---|---|
| Un ítem positivo | 87 | 66 |
| Dos ítems positivos | 95 | 26 |
| Tres ítems positivos | 99 | 11 |
| Kothari RU, Pancioli A, Liu T, Brott T, Broderick J. Cincinnati Prehospital Stroke Scale: Reproducibility and validity. Ann Emerg Med. 1999; 33:373-8 | ||
Adaptada de Pigretti et al.10.
FAST (Face, Arm, Speech Test). Adaptada y modificada de Harbison et al.36.
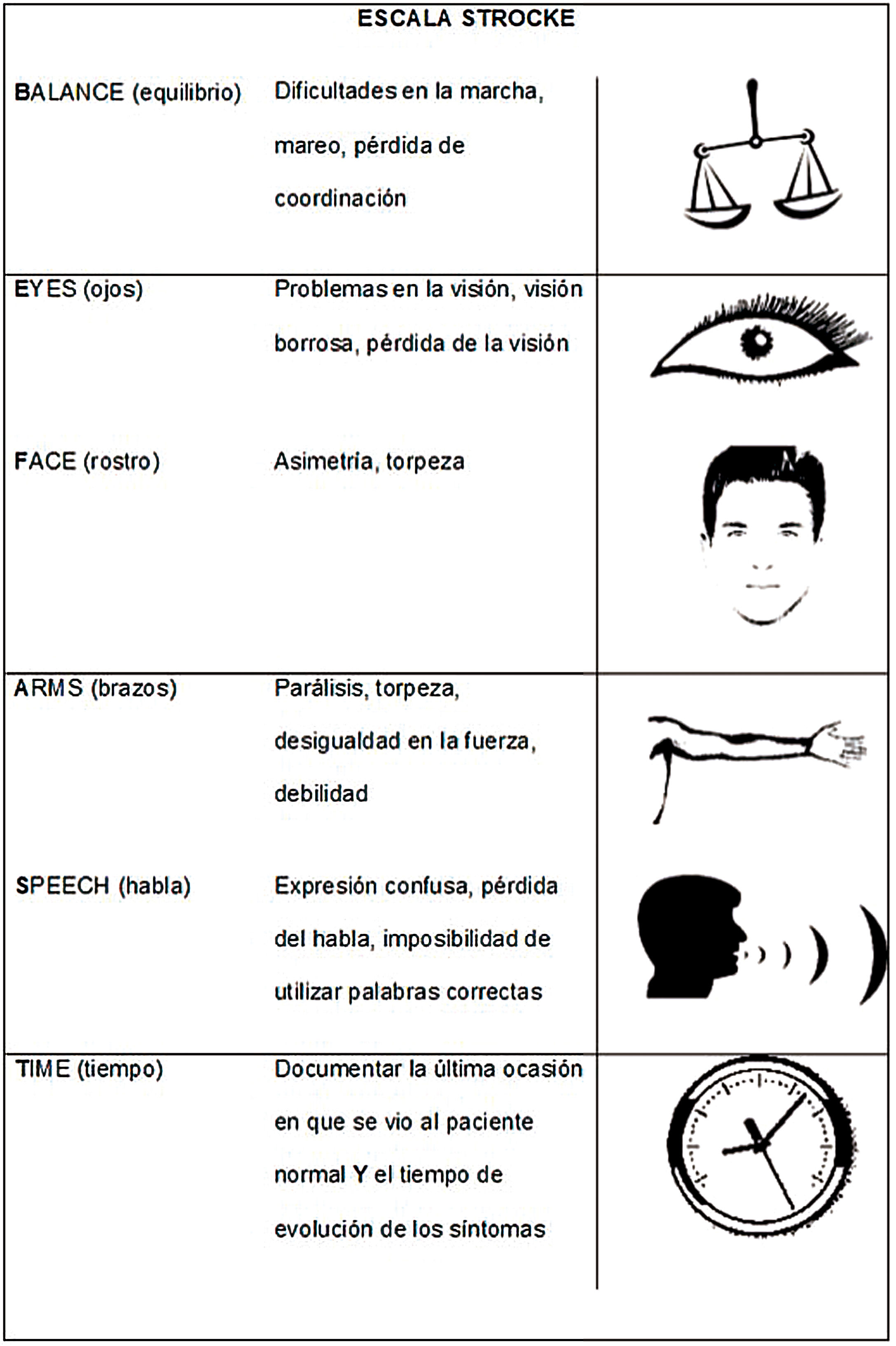
Existen otras escalas, como LAPSS, MASS y BE-FAST (fig. 3)39–41. Las escalas CPSS y FAST evalúan sobre todo síntomas de la circulación anterior y podrían pasar por alto un ACV de la circulación posterior42. Por este motivo se desarrollaron escalas como BE-FAST, que incluyen síntomas de la circulación posterior y podrían tener mayor sensibilidad, aunque son menos difundidas y resta determinar si generan una diferencia sustancial en el número de pacientes que acceden al tratamiento43. La sensibilidad de esta escala para reconocer un ACV ha sido comprobada en pacientes con episodios intrahospitalarios, incluyendo aquellos candidatos a la terapia de reperfusión44. En nuestro medio, solo el 32,3% de los profesionales de los servicios de emergencias conoce las escalas, pero los médicos no especialistas son quienes las consideran más útiles45.
BE-FAST (Balance, Eyes, Face, Arm, Speech, Time). Adaptada y modificada de Aroor et al.41.
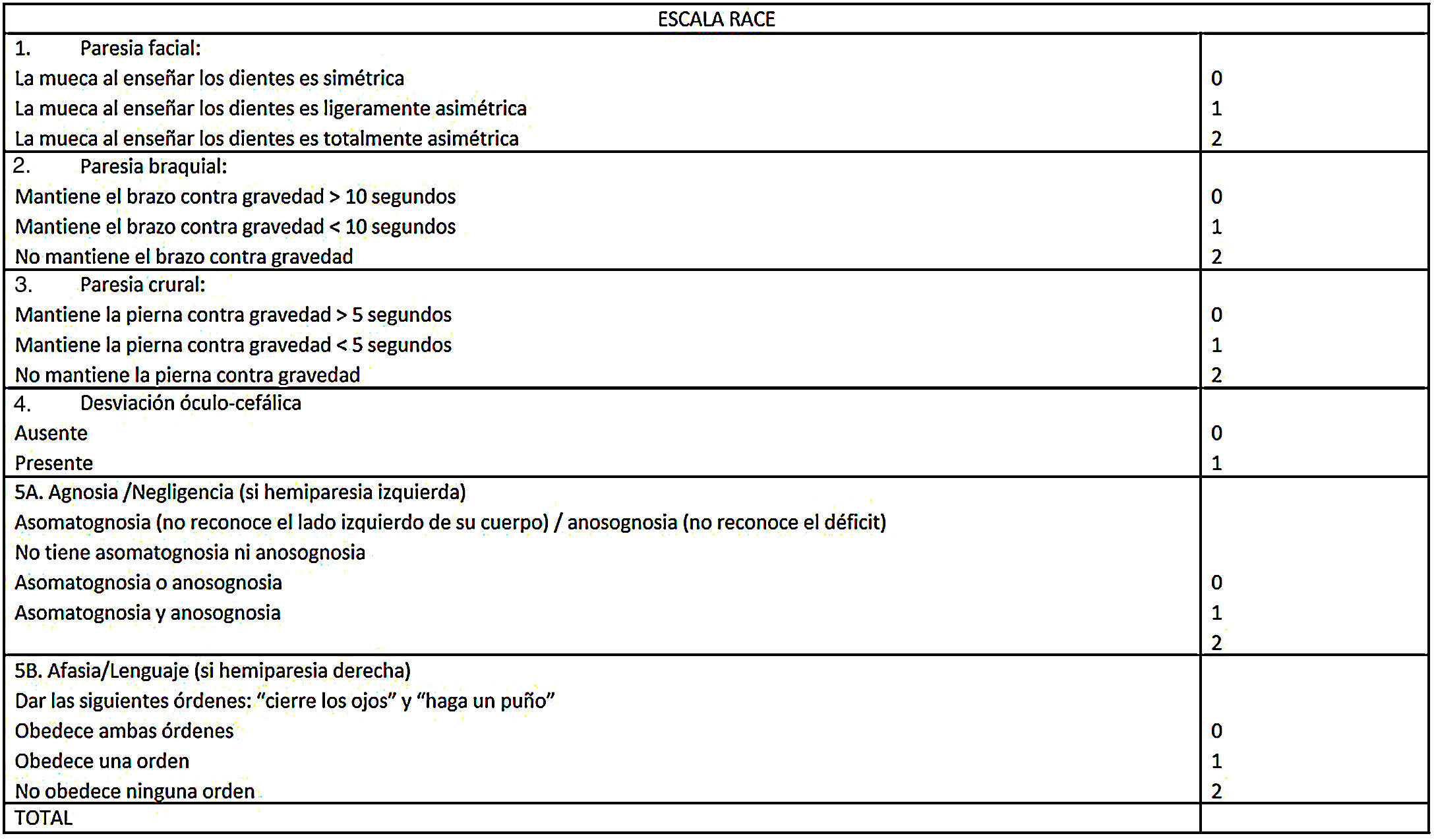
Actualmente, algunos pacientes podrían beneficiarse con el traslado directo a un centro con capacidad de trombectomía mecánica. Existen escalas que intentan predecir qué pacientes podrían tener una obstrucción de un gran vaso proximal. La más difundida es RACE (fig. 4), que se correlaciona con la escala NIHSS (National Institute of Health Stroke Scale) y parece promisoria46, aunque se aguarda su validación definitiva, ya que se han visto resultados diferentes a los del estudio original en otros contextos47.
Es difícil recomendar una escala sobre otra, pero se debe sistematizar y entrenar al personal en una de ellas, eligiendo la de mayor facilidad de aplicación y cuya sensibilidad y especificidad esté dentro de los márgenes de la capacidad operativa y de las expectativas.
Elegir el centro adecuadoLa sospecha de ACV por parte del SEM implica la necesidad de continuar el cuidado en un centro adecuado. No todos los centros pueden brindar una respuesta adecuada, por lo que es función del SEM elegir el centro más apropiado. Un centro sin capacidad de efectuar imágenes de urgencia, sin protocolo de ACV ni capacidad de administrar rtPA no debe ser considerado para la recepción de pacientes con sospecha de ACV agudo. Idealmente, el sitio debe contar con una unidad de ACV (no necesariamente como unidad física; en muchos casos existe como unidad funcional), la cual reduce la tasa de mortalidad y discapacidad, minimiza el tiempo de hospitalización y es costo-efectiva10,48. El SEM debe estabilizar y trasladar al paciente al centro adecuado para la continuidad del cuidado49. Una vez seleccionado el centro receptor, este debe ser prenotificado para ofrecer todos los servicios necesarios. Los centros para el manejo del ACV se clasifican como:
- 1.
Primario: cuenta con neuroimágenes, laboratorio y equipo de ACV con capacidad de administrar rtPA.
- 2.
Integral: cuenta con equipos interdisciplinarios de ACV y ofrece trombólisis iv y procedimientos endovasculares. Se está trabajando en escalas que permitan reconocer desde la fase prehospitalaria al paciente que, por la probabilidad de obstrucción de un gran vaso, podría ser derivado directamente a un centro integral sin pasar por un centro primario (mecanismo mothership). La estrategia más utilizada hoy es drip and ship, es decir, el paciente inicia la terapia con rtPA en un centro primario y se deriva de forma expedita a un centro integral para tratamiento endovascular. Una reciente revisión sistemática indica que la estrategia mothership podría ser superior a la drip and ship. Aún así, las recomendaciones actuales enfatizan que el paciente sea trasladado al centro apropiado más cercano (sin diferenciar la estrategia, siempre que pueda administrarse al menos rtPA); se requiere más investigación para arribar a una conclusión y eventualmente reconsiderar el enfoque50.
Una vez seleccionado el centro, el equipo prehospitalario notifica los datos filiatorios, el síntoma principal/resultado de la escala utilizada, el tiempo de evolución de los síntomas/última vez que fue visto normal, si recibe tratamiento anticoagulante, la glucemia y el tiempo estimado de arribo. Esta información mínima permite al equipo hospitalario preparar la recepción y alertar a los servicios de imágenes y laboratorio. La prenotificación es decisiva y efectiva para disminuir los tiempos puerta-TC y puerta-aguja51–53 y su utilidad depende de la gestión del receptor con los datos aportados. Si la prenotificación no activa un proceso hospitalario interno, probablemente no sea útil.
Realizar intervenciones necesarias en la escena y aprovechar el trasladoCon el diagnóstico presuntivo de ACV, el equipo prehospitalario debe minimizar el tiempo en la escena, sin exceder 15min salvo que se requieran medidas complejas de reanimación o de traslado. Para lograr un rápido proceso, es necesario aplicar protocolos estructurados que puedan estar a disposición en papel o un soporte informático. Estos protocolos mejoran la seguridad y calidad de las intervenciones en medicina crítica54, acortan los tiempos y disminuyen la morbimortalidad asociada a un procedimiento55. Los profesionales deben ser adherentes a estas herramientas, que deben aportar un claro beneficio a la dinámica. De lo contrario, el efecto difícilmente sea decisivo56. En este sentido, las aplicaciones para teléfonos inteligentes facilitan la identificación del ACV, la activación inmediata de un código de urgencia y la localización del centro receptor apropiado más cercano, como ya se ha demostrado en América Latina57. En un estudio reciente con participación de SEM privados, un protocolo prehospitalario de ACV basado en una aplicación de diseño propio redujo significativamente el tiempo prehospitalario total, a expensas de un menor tiempo en la escena58.
La figura 5 reproduce una lista de verificación (checklist) prehospitalaria, propuesta por la iniciativa ANGELS31. Dadas las características específicas de cada servicio, puede ser necesaria su adaptación a la realidad local.
Otras acciones prehospitalarias fundamentales incluyen59:
- •
Luego de la escala de evaluación del ACV, obtener el tiempo de inicio de los síntomas. Si el paciente se encontraba acompañado se puede establecer por el testimonio del acompañante; de lo contrario, se toma como tiempo de inicio la última vez en que fue visto normal
- •
Obtener antecedentes relevantes (ACV previos, cirugías y traumatismos recientes; historia de diabetes, convulsiones, consumo de tóxicos, terapia anticoagulante) y nivel de actividad previo (paciente independiente, limitado o postrado)
- •
Es recomendable trasladar junto al paciente su medicación habitual, para contar con información completa
- •
La evaluación primaria completa incluye un adecuado manejo de la vía aérea y administrar oxígeno solo si es necesario para lograr una saturación de O2 (SpO2)>94%60. Es frecuente la hipertensión arterial en estos pacientes; en este caso, se registra el valor sin intervenir con fármacos de forma rutinaria; la ansiedad, el dolor y la retención urinaria pueden aumentar la presión arterial. Se conecta al paciente a monitorizaciín continua si está disponible (ritmo cardíaco, presión arterial no invasiva, SpO2). No es necesario un electrocardiograma rutinario de 12 derivaciones en el entorno prehospitalario, salvo que se considere que cambiará la conducta (dolor torácico, sospecha de arritmia con inestabilidad hemodinámica). En otros casos, el electrocardiograma se realiza en el centro receptor
- •
Obtener uno o preferentemente 2 accesos venosos cortos y gruesos, por encima de la muñeca, en el miembro no afectado (colocar un acceso venoso del lado afectado puede interferir el examen neurológico). Dado que los accesos son para utilizar casi exclusivamente en el hospital, si luego de 2 intentos no se logra obtenerlos, es apropiado no demorar el traslado y derivar al paciente. Se coloca solución fisiológica a 7 gotas/min o se utiliza como vía intermitente. No se usan soluciones con glucosa salvo que el paciente presente hipoglucemia
- •
Una glucemia capilar<60mg/dl debe ser tratada de inmediato con glucosa hipertónica iv en bolo y/o glucagón de estar disponible. La hipoglucemia con foco neurológico agudo, deterioro del sensorio y/o convulsiones es una emergencia y un potencial simulador de ACV
Al arribar al hospital, el equipo de ACV debe estar esperando al paciente. Tras confirmar identidad, presencia de síntomas y tiempo de evolución, se traslada al paciente con la misma camilla y monitor a la sala de TC, se revisa la historia clínica y el tiempo de evolución, se completa el checklist (criterios de inclusión/exclusión para administrar rtPA), se revisan nuevamente los signos vitales, se obtiene en lo posible el consentimiento para la terapia de recanalización y, al acostar al paciente en el tomógrafo, se completa el examen físico, la escala de NIHSS y se obtiene el peso para calcular la dosis de rtPA. Se realizan las imágenes; tras excluir contraindicaciones (sangrado, lesión ocupante), se puede administrar el bolo inicial en la sala de TC. Si está disponible, se efectúa un estudio rápido del árbol vascular para determinar la necesidad de tratamiento endovascular y de inmediato, en una sala adyacente monitorizada, se completa la infusión de rtPA durante 60min con monitorización estricta de signos vitales y estado neurológico durante y luego de la infusión. Si el centro tiene camas destinadas a la infusión, esta se realiza idealmente en dicho sector.
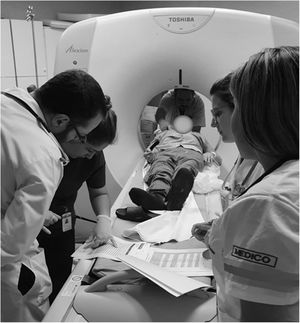
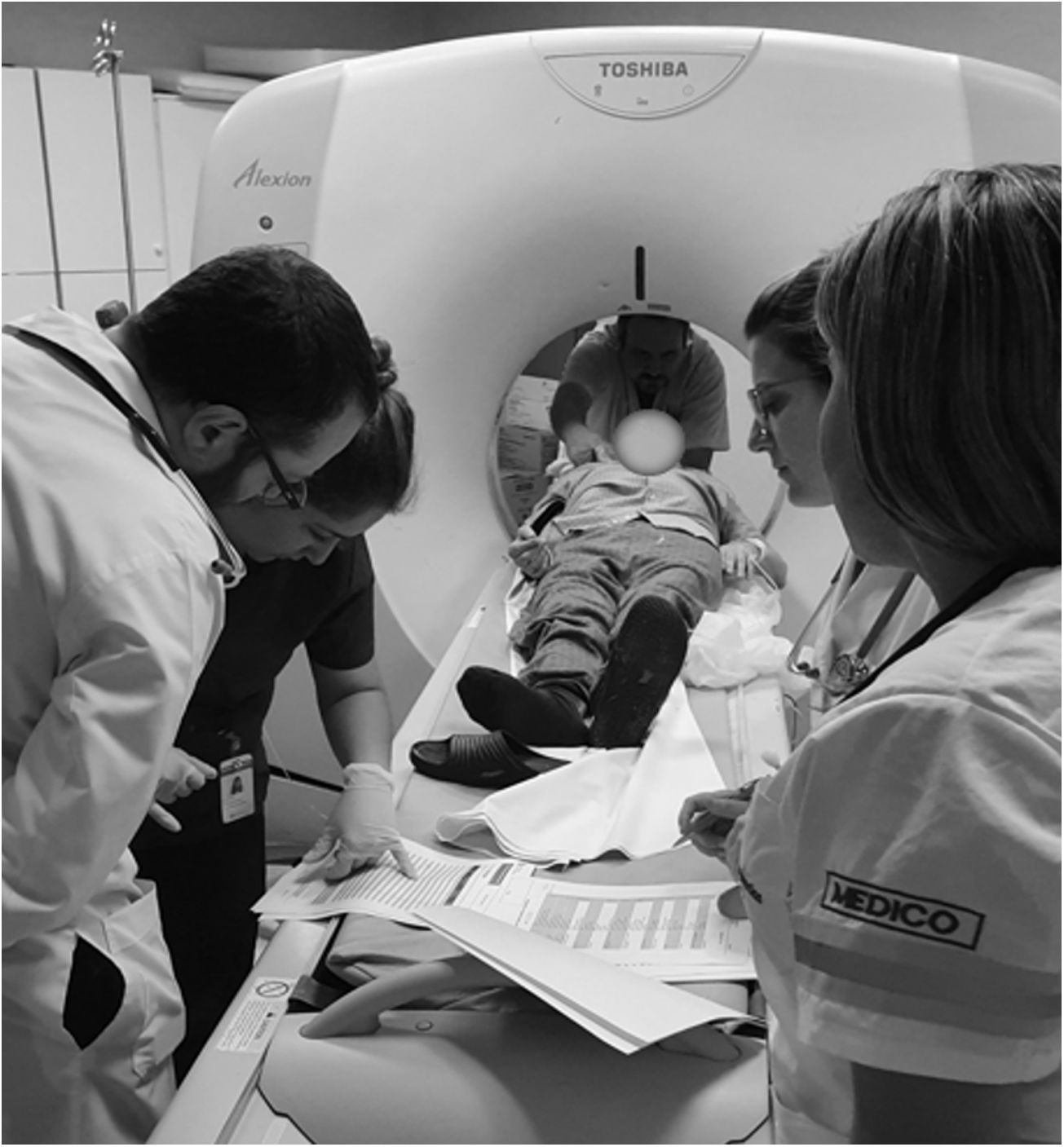
Así, los equipos prehospitalario e intrahospitalario se fusionan en un único equipo de ACV, como una expresión de cuidados continuos e integrados con el mismo objetivo desde el lugar de la emergencia hasta el centro receptor (fig. 6).
Enfoque integrado del paciente. En la cabecera, el técnico en imágenes ayuda a lograr la mejor posición para el estudio. A la izquierda, la enfermera y el médico a cargo del equipo repasan dosis de rtPA en un checklist. A la derecha, las médicas del SEM y del equipo hospitalario registran tiempos y completan la transferencia de información.
Las unidades móviles (UM) tienen presencia en Europa, Estados Unidos y existe una en Argentina. La UM combina recursos humanos entrenados para la fase hiperaguda, acceso a telemedicina en contacto con un centro avanzado de ACV, acceso a TC transportable, laboratorio básico y posibilidad de administrar fibrinolíticos en la escena.
En el estudio PHANTOM-S, las UM mejoraron el tiempo de tratamiento sin aumentar los eventos adversos, aunque aún no está clara la costo/efectividad61. El paciente que ingresa al protocolo de ACV a través de la UM tiene mejor tiempo «puerta-ingle» en caso de requerir trombectomía62. Incluso podrían ser una herramienta decisiva para definir a los pacientes con obstrucción de vaso proximal desde la fase prehospitalaria y plantear la derivación a un centro integral, evitando los centros primarios (la misma UM iniciaría la fibrinólisis). Un estudio reciente ha mostrado la superioridad de la UM versus las escalas tradicionales para este objetivo de triage63. El estudio B_Proud presentado en 2020 ha sido el primero en demostrar mejores resultados funcionales medidos por la Escala Rankin a los 3 meses en pacientes atendidos por las UM, en comparación con el tratamiento estándar64. Si bien los resultados son promisorios, se requiere de más investigación; aunque la UM podría ofrecer aumento del acceso al tratamiento65, reducción de los tiempos y eventual mejoría de los resultados funcionales, debe demostrarse que también resulta costo/efectiva.
ConclusiónLa frase «el tiempo es cerebro» es una expresión de la importancia de las acciones de emergencia durante el ACV. Asimismo, los avances en el diagnóstico por imágenes permiten reconocer la existencia de tejido cerebral viable merced a circulación colateral. En un ACV no lacunar mueren 1,9 millones de neuronas/minuto66; si bien existe variabilidad individual67, la cifra es impactante y obliga a un rápido accionar. El SEM es protagonista de la fase hiperaguda, ejecutando las acciones para estabilizar al paciente, reconocer el ACV, prenotificar, derivar al centro adecuado y aprovechar el tiempo de traslado. En el centro receptor, el SEM se integra al personal en un único equipo de ACV, merced a un protocolo coordinado que reduce de forma marcada el tiempo puerta-aguja68,69. La ESO y el registro Res-Q70, entre otros, patrocinan la campaña Stroke 2020, cuyo objetivo es que se aplique fibrinólisis al menos al 20% de los pacientes y que el tiempo puerta-aguja sea≤20min71. Este ambicioso objetivo solo se podrá alcanzar mediante un intenso esfuerzo de capacitación del personal, la aplicación de protocolos estandarizados y una comunicación eficiente, como se resume en la figura 7. El desafío es cambiar la historia de los pacientes con ACV con una oportunidad de vivir más y mejor.
Conflicto de interesesNinguno.





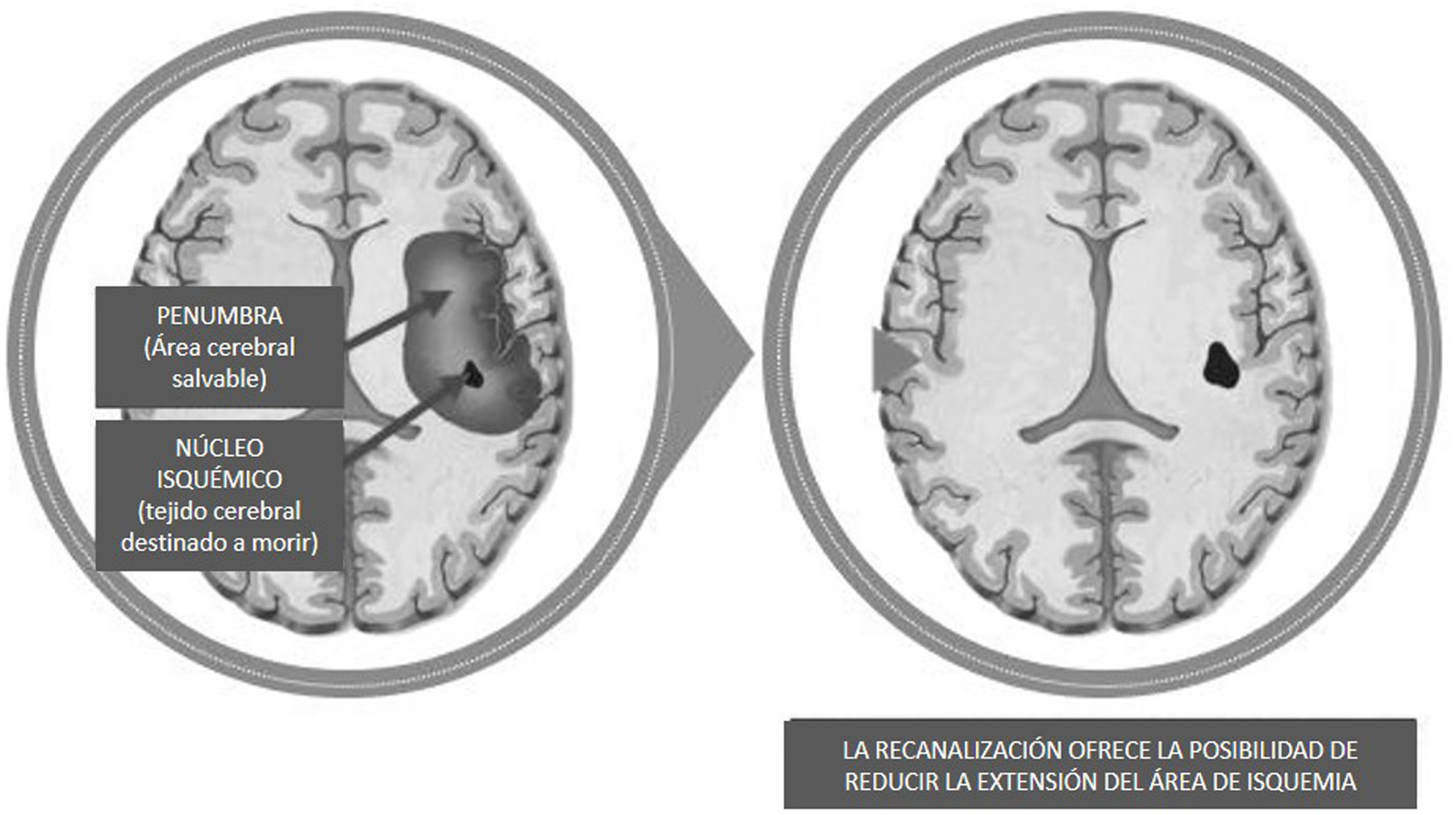




![Zona de infarto y penumbra.Adaptada y modificada de: https://bit.ly/3eFk85U [acceso 1 Ene 2020]. Zona de infarto y penumbra.Adaptada y modificada de: https://bit.ly/3eFk85U [acceso 1 Ene 2020].](https://static.elsevier.es/multimedia/18530028/0000001200000004/v1_202012180841/S1853002820300677/v1_202012180841/es/main.assets/thumbnail/gr1.jpeg?xkr=ue/ImdikoIMrsJoerZ+w96p5LBcBpyJTqfwgorxm+Ow=)

![RACE (Rapid Arterial oCclusion Evaluation). Adaptada y modificada de: https://bit.ly/2xv1Eod [acceso 10 Feb 2020]. RACE (Rapid Arterial oCclusion Evaluation). Adaptada y modificada de: https://bit.ly/2xv1Eod [acceso 10 Feb 2020].](https://static.elsevier.es/multimedia/18530028/0000001200000004/v1_202012180841/S1853002820300677/v1_202012180841/es/main.assets/thumbnail/gr4.jpeg?xkr=ue/ImdikoIMrsJoerZ+w96p5LBcBpyJTqfwgorxm+Ow=)