El control de los factores de riesgo cardiovascular (CV) en la prevención secundaria tras un ictus isquémico es bajo, en parte debido a la falta de adherencia terapéutica. La polipíldora CV puede contribuir a la buena cumplimentación del adecuado tratamiento para la prevención cerebrovascular. El objetivo fue establecer cómo y en qué casos se debería administrar.
MétodosUn grupo de 8neurólogos redactaron recomendaciones consensuadas mediante una técnica de brainstorming estructurado, basándose en su experiencia y en una revisión bibliográfica.
ResultadosLos resultados atienden a la opinión de los expertos. El uso de la polipíldora CV tiene ventajas para pacientes, profesionales sanitarios y para el sistema de salud. Las situaciones clínicas más adecuadas para su uso son el ictus aterotrombótico, el lacunar, el asociado a deterioro cognitivo, el criptogénico con factores de riesgo CV y la enfermedad cerebrovascular silente. Su uso preferente incluye la sospecha de mal cumplimiento, a los pacientes polimedicados, ancianos, polivasculares o con alta carga aterotrombótica, jóvenes activos laboralmente y pacientes con preferencias por la polipíldora CV. Las opciones de administración incluyen el paso de fármacos individuales a la polipíldora CV, el inicio directo desde la fase aguda en casos particulares, a los pacientes con otra estatina o con un antagonista del receptor de la angiotensina ii, o de novo si hubiera sospecha de mala adherencia. No obstante, su uso implica realizar seguimiento del cumplimiento de los objetivos terapéuticos para ajustar la dosis.
ConclusionesEste documento es el primero en establecer recomendaciones de uso de la polipíldora CV en enfermedad cerebrovascular, aparte de sus ventajas sobre la adherencia.
There is little control of cardiovascular (CV) risk factors in secondary prevention after an ischaemic stroke, in part due to a lack of adherence to treatment. The CV polypill may contribute to proper treatment adherence, which is necessary for CV disease prevention. This study aimed to establish how and in what cases the CV polypill should be administered.
MethodsA group of 8 neurologists drafted consensus recommendations using structured brainstorming and based on their experience and a literature review.
ResultsThese recommendations are based on the opinion of the participating experts. The use of the CV polypill is beneficial for patients, healthcare professionals, and the health system. Its use is most appropriate for atherothrombotic stroke, lacunar stroke, stroke associated with cognitive impairment, cryptogenic stroke with CV risk factors, and silent cerebrovascular disease. It is the preferred treatment in cases of suspected poor adherence, polymedicated patients, elderly people, patients with polyvascular disease or severe atherothrombosis, young patients in active work, and patients who express a preference for the CV polypill. Administration options include switching from individual drugs to the CV polypill, starting treatment with the CV polypill in the acute phase in particular cases, use in patients receiving another statin or an angiotensin ii receptor antagonist, or de novo use if there is suspicion of poor adherence. Nevertheless, use of the CV polypill requires follow-up on the achievement of the therapeutic objectives to make dose adjustments.
ConclusionsThis document is the first to establish recommendations for the use of the CV polypill in cerebrovascular disease, beyond its advantages in terms of treatment adherence.
El ictus isquémico es una de las primeras causas de muerte en todo el mundo1. Según cifras de la OMS, en 2012 se calcula que murieron 6,7 millones de personas por esta causa2. Los pacientes que han sufrido un ictus tienen un mayor riesgo de presentar un nuevo episodio cerebrovascular. La repetición de eventos cerebrales isquémicos conlleva, además, un mayor riesgo de demencia de origen vascular.
Se ha postulado que una de las barreras más importantes en la prevención secundaria de la enfermedad vascular es la falta de adherencia terapéutica3. Los factores que podrían contribuir a un bajo cumplimiento del tratamiento serían el carácter crónico y, en ocasiones, poco sintomático de la enfermedad cardiovascular (ECV), el copago de medicamentos, los esquemas terapéuticos complejos y la ausencia de programas educativos dirigidos a profesionales y a pacientes4. La consecuencia de la escasa adherencia terapéutica sería un incremento de las complicaciones cardiovasculares (CV) mayores, incluidos los ictus, con el consiguiente incremento de la mortalidad, la reducción de la calidad de vida de los pacientes supervivientes, una mayor carga asistencial y un incremento de los costes sanitarios derivados de las complicaciones y los ingresos hospitalarios5.
La reducción del copago, los recordatorios automáticos, las farmacias de pedidos por correo, el asesoramiento de un profesional de la salud y las terapias de combinación de dosis fija son medidas que han demostrado mejorar el cumplimiento terapéutico. La simplificación de los regímenes terapéuticos en terapias de combinación fija es una estrategia complementaria para mejorar la adherencia al tratamiento de muchos tipos de enfermedades y cuentan, además, con la percepción favorable de los pacientes. Las combinaciones fijas también permiten reducir los costes de producción y distribución, con lo que mejora la asequibilidad del tratamiento4.
La polipíldora CV, primer tratamiento combinado aprobado en Europa para la prevención CV secundaria, contiene ácido acetilsalicílico (AAS), atorvastatina y ramipril en una única cápsula, 3principios activos que han demostrado disminuir la mortalidad en pacientes con enfermedad vascular establecida6-9.
Actualmente, las dosis de los fármacos de las polipíldoras CV comercializadas son AAS (100 mg), atorvastatina (20 o 40 mg) y ramipril (2,5, 5 o 10 mg).
El objetivo de este trabajo fue elaborar un documento que recogiera las implicaciones del empleo de la polipíldora CV y estableciera las situaciones clínicas y los perfiles de pacientes más idóneos para su uso, así como los que no serían candidatos, y unas recomendaciones sobre el manejo general de esta combinación, en el ámbito de la prevención secundaria de infartos cerebrales.
Materiales y métodosSe mantuvo una reunión de trabajo con 8especialistas en neurología, para definir la estructura y los contenidos del documento. Para la moderación de la sesión, se usó una técnica de brainstorming estructurado, en la que un moderador externo facilitó el debate, la ordenación de las ideas y la participación equitativa. Se consensuaron los bloques y contenidos que desarrollar para el uso de la polipíldora CV en la prevención de la enfermedad cerebrovascular: implicaciones del uso para diferentes colectivos, situaciones clínicas de utilización y no utilización, pacientes con indicación preferente y recomendaciones para el uso y el manejo. Posteriormente, cada especialista redactó una parte del documento, con base en una revisión bibliográfica y en su experiencia clínica. El documento final fue revisado y validado por todos los expertos mediante correo electrónico.
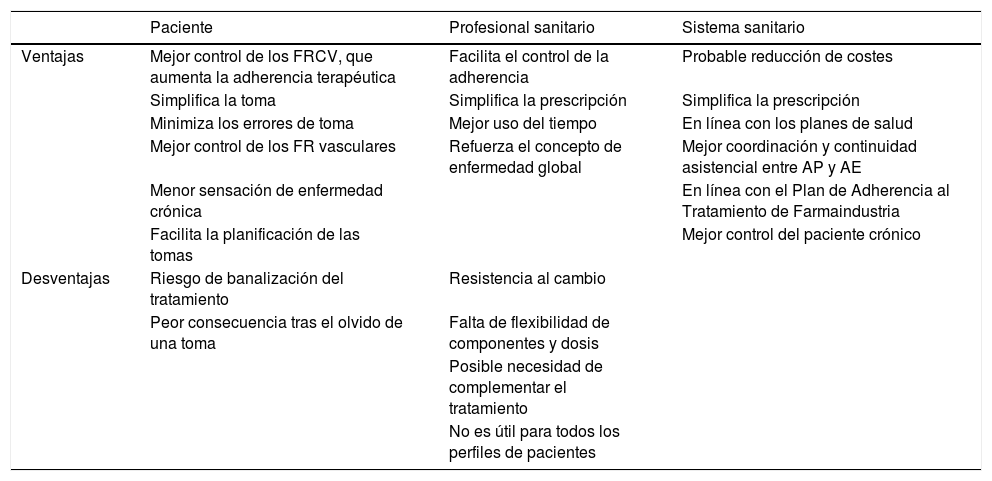
ResultadosImplicaciones del uso de la polipíldora cardiovascular en la prevención de la enfermedad cerebrovascularLa introducción de la polipíldora CV en el arsenal terapéutico para la prevención secundaria de la enfermedad cerebrovascular tiene importantes implicaciones para el paciente, el profesional sanitario y el sistema sanitario (tabla 1).
Implicaciones del uso de la polipíldora CV en la prevención de la enfermedad cerebrovascular
| Paciente | Profesional sanitario | Sistema sanitario | |
|---|---|---|---|
| Ventajas | Mejor control de los FRCV, que aumenta la adherencia terapéutica | Facilita el control de la adherencia | Probable reducción de costes |
| Simplifica la toma | Simplifica la prescripción | Simplifica la prescripción | |
| Minimiza los errores de toma | Mejor uso del tiempo | En línea con los planes de salud | |
| Mejor control de los FR vasculares | Refuerza el concepto de enfermedad global | Mejor coordinación y continuidad asistencial entre AP y AE | |
| Menor sensación de enfermedad crónica | En línea con el Plan de Adherencia al Tratamiento de Farmaindustria | ||
| Facilita la planificación de las tomas | Mejor control del paciente crónico | ||
| Desventajas | Riesgo de banalización del tratamiento | Resistencia al cambio | |
| Peor consecuencia tras el olvido de una toma | Falta de flexibilidad de componentes y dosis | ||
| Posible necesidad de complementar el tratamiento | |||
| No es útil para todos los perfiles de pacientes |
AP: atención primaria; AE: atención especializada; FR: factores de riesgo; FRCV: factores de riesgo cardiovascular.
La principal ventaja para el paciente es facilitar el tratamiento para el control de los factores de riesgo cardiovascular (FRCV) y aumentar su adherencia. La complejidad de un régimen terapéutico se correlaciona de forma inversa con el grado de cumplimiento10. Existe evidencia sólida para afirmar que el uso de tratamientos en combinación fija mejora la adherencia respecto al uso aislado de los distintos componentes11-13. Esto se debe a un menor riesgo de errores en la toma de varios fármacos y a la simplificación del tratamiento. Una mejor adherencia se asociaría a un mejor control de los factores de riesgo (FR) vascular. Sin embargo, aunque los monocomponentes han demostrado efecto sobre los FR por separado, es necesaria más evidencia que demuestre una reducción de los eventos cerebrovasculares. La polipíldora CV permite al profesional sanitario optimizar el proceso de prescripción y control del tratamiento, lo que facilita un control de los FR vasculares y permite focalizar el tiempo invertido en consulta en fomentar hábitos saludables. Aunque en ocasiones puede ser necesario complementar la polipíldora CV con medicaciones adicionales14, la estrategia de combinación fija es compatible con un enfoque personalizado de la prevención secundaria.
Finalmente, el tratamiento en combinación fija ha demostrado ser coste-efectivo en prevención primaria y secundaria15,16. Aunque es necesario realizar más estudios en prevención secundaria, es probable que la mejora en la adherencia conduzca a una reducción de costes si se traduce en un mejor control de la progresión y recurrencia clínica de la enfermedad cerebrovascular no cardioembólica.
Situaciones clínicas de utilización y no utilización de la polipíldora cardiovascular en la prevención de la enfermedad cerebrovascularLas situaciones clínicas de uso y de no uso de la polipíldora CV se definen en la tabla 2, aunque en el documento se desarrollan en mayor profundidad las primeras.
Situaciones clínicas de uso y no uso de la polipíldora CV en la prevención de la enfermedad cerebrovascular
| Situaciones clínicas de uso | Situaciones clínicas de no uso |
|---|---|
| Ictus aterotrombótico | Pacientes con ictus cardioembólico |
| Ictus lacunar | Pacientes con ictus sin hipertensión arterial ni dislipidemiaa |
| Ictus criptogénico con FRCV | Pacientes intolerantes o con contraindicación a alguno de los monocomponentes de la polipíldora |
FRCV: factores de riesgo cardiovascular.
Según algunas guías, el paciente que ha presentado un ictus aterotrombótico debe recibir tratamiento con fármacos antiagregantes, estatinas y antihipertensivos17-20. El AAS a dosis de 75-325 mg/día es el antiagregante de elección, tanto en estenosis extra- como intracraneal. Los pacientes con estenosis extra- o intracraneal, crítica o no, con ictus recurrente o curso progresivo, podrían tratarse con AAS a la dosis mencionada, clopidogrel (75 mg/día) o la combinación de AAS más dipiridamol de liberación retardada (25 y 200 mg, 2 veces/día, respectivamente), que es preferible a la combinación de AAS y clopidogrel.
Las estatinas son recomendables en pacientes asintomáticos, a dosis que permitan alcanzar el objetivo de cifras de colesterol asociado a lipoproteínas de baja densidad (cLDL) <100 mg/dl21. En pacientes con ictus aterotrombótico, el objetivo terapéutico es LDL <70mg/dl17,21. Las pruebas procedentes de ensayos clínicos con estatinas en pacientes con cardiopatía isquémica, así como un metaanálisis de estos estudios y los resultados del estudio SPARCL en pacientes con ictus isquémico aterotrombótico, muestran una reducción significativa del riesgo ictal, especialmente con la utilización de atorvastatina a dosis de 80 mg/día22,23.
En relación con el tratamiento antihipertensivo, este debe ser iniciado en pacientes previamente hipertensos o en los que se constaten cifras de presión arterial (PA) > 140/90mmHg. El objetivo debe ser mantener las cifras de PA dentro de los límites normales (<140/90 mmHg), sin recomendaciones específicas sobre qué fármaco utilizar19.
El paciente con ictus aterotrombótico requerirá polimedicación de por vida para conseguir una disminución del riesgo de recurrencia asociado, lo que puede dificultar la adherencia. El uso de la polipíldora CV en pacientes que requerirían los 3fármacos por separado puede facilitar el cumplimiento, siempre que se alcancen de forma aceptable los objetivos terapéuticos.
Ictus lacunarLa hipertensión arterial es el principal factor de riesgo en el ictus lacunar (IL). Se ha demostrado que se puede reducir el riesgo de recurrencia de ictus en un 28% si se controla la PA de los pacientes con ictus isquémico24. En pacientes con IL, el estudio SPS3 identificó una tendencia de beneficio asociado a la reducción de la PA (aunque no estadísticamente significativa). Además, el uso de inhibidores de la enzima convertidora de la angiotensina evita la progresión de la microangiopatía cerebral por resonancia magnética25. En relación con el tratamiento antihipertensivo, este debe ser iniciado en pacientes previamente hipertensos o en los que se constaten cifras de PA > 140/90mmHg. El objetivo debe ser mantener las cifras de PA dentro de los límites normales (<140/90 mmHg); no hay recomendaciones específicas sobre qué fármaco utilizar19.
En relación con la dislipidemia, el estudio SPARCL mostró un beneficio del tratamiento con estatinas similar al de otros subtipos de ictus26, pese a que los pacientes con IL no suelen presentar ateromatosis en grandes vasos. Finalmente, en el IL está indicado el tratamiento antiagregante con un solo fármaco. El estudio SPS3 demostró que el tratamiento con 325 mg de AAS más 75 mg de clopidogrel no reduce significativamente el riesgo de ictus recurrente y aumenta el riesgo de hemorragia y mortalidad, en comparación con solo 325 mg27 de AAS. Así, el tratamiento antiagregante con AAS a dosis media (75-325 mg) sería de elección28. Por tanto, la polipíldora CV puede ser de utilidad en pacientes con IL y que requerirían los 3fármacos por separado.
Ictus criptogénico con factores de riesgo cardiovascularEn ocasiones, en el ictus de origen criptogénico se plantea la posibilidad de indicar el tratamiento anticoagulante, fundamentalmente en algunos pacientes que cumplen criterios de ictus tipo ESUS (embolic strokes of undetermined source, por sus siglas en inglés). Sin embargo, hasta la fecha, el tratamiento anticoagulante no ha demostrado ser más eficaz en la prevención secundaria del ictus criptogénico, por lo que el tratamiento de primera línea es la antiagregación con AAS.
Los FR vasculares clásicos, como la hipertensión arterial y la dislipidemia, deben ser controlados, ya que su presencia se asocia con un mayor riesgo de recurrencia, aunque esta sea menor que en otros subtipos de ictus. Por tanto, el uso de la polipíldora CV estaría indicado en pacientes con ictus criptogénico y que presentan hipertensión arterial e hipercolesterolemia.
Pacientes con indicación preferente de la polipíldora cardiovascular en la prevención de la enfermedad cerebrovascularAdemás de las situaciones clínicas descritas previamente, existen determinados perfiles de pacientes más adecuados para el uso de la polipíldora CV y en los que su indicación debería ser preferente. El caso más evidente es el de pacientes con sospecha de mala adherencia al tratamiento. Diferentes estudios han demostrado que la utilización de tratamientos en combinación fija mejora la adherencia respecto a los tratamientos en combinación libre12,29-34. No existe un perfil concreto de paciente no adherente al tratamiento, aunque se han identificado algunos predictores de no adherencia35-38: edad avanzada o joven, comorbilidades, polimedicación, desempleo o recursos económicos bajos, ámbito rural, antecedentes de ictus y atención sanitaria realizada en centros menos especializados. El aumento de adherencia, además, supone un ahorro económico, tal como muestran algunos estudios11,16.
El paciente polivascular o con alta carga aterotrombótica es un paciente complejo y con especial interés para el uso de la polipíldora CV. La coexistencia de ictus aterotrombótico con enfermedad arterial coronaria o arteriopatía periférica, sea o no sintomática, es habitual en la práctica clínica diaria y es determinante en el pronóstico de los pacientes, como se ha demostrado en varios estudios39-41. Además, la mortalidad por cardiopatía isquémica es mayor si el paciente tiene antecedentes de ictus y la recurrencia ictal es mayor en pacientes con antecedentes de cardiopatía isquémica. En este tipo de pacientes, por tanto, se hace especialmente necesario controlar los FR vasculares y asegurar un control de la toma de la medicación pues, además, son pacientes polimedicados. En la tabla 3 se indican otros perfiles de uso preferente.
Pacientes con indicación preferente de la polipíldora CV en la prevención de la enfermedad cerebrovascular
| Perfiles de pacientes |
|---|
| Pacientes con sospecha de pobre/mala adherencia al tratamiento |
| Pacientes polimedicados |
| Pacientes ancianos |
| Pacientes polivasculares o con alta carga aterotrombótica |
| Pacientes jóvenes activos laboralmente o con necesidad de desplazarse |
| Pacientes con preferencias en el uso de la polipíldora CV |
En las guías europeas sobre prevención de la ECV se incluye un apartado de la polipíldora CV, en el que la consideran dentro de una estrategia global de prevención de la enfermedad cerebrovascular42. Teniendo en cuenta las guías y lo considerado previamente, el grupo de expertos ha establecido recomendaciones de uso para el inicio y el seguimiento del tratamiento.
Para el inicio del tratamiento, se pueden considerar varias alternativas:
Paso de un tratamiento individualizado a la polipíldora CV: Aunque la dosis de AAS no varía a lo largo del seguimiento del paciente con ictus, sí pueden hacerlo las dosis de ramipril y atorvastatina en función de la evolución de la PA y del cLDL, la adherencia del paciente y las modificaciones en los hábitos de vida. Por eso, se deberán ajustar las dosis a los 3-6 meses para la consecución de los objetivos marcados de PA y cLDL y teniendo en cuenta la tolerabilidad. En el caso concreto de la atorvastatina en los ictus no cardioembólicos con cLDL > 100 mg/dl, la dosis recomendada inicialmente es de 80 mg/24 h, aunque a veces no se tolera o se consigue el objetivo de cLDL (<70 mg/dl) con dosis de 40 mg/24 h. La disponibilidad de la nueva presentación de la polipíldora CV con la dosis de 40 mg de atorvastatina facilitará el uso en estas situaciones.
Inicio de la polipíldora CV desde la fase aguda: Se podría valorar el inicio del tratamiento con la polipíldora CV durante la hospitalización si se prevén dificultades en la adherencia al tratamiento, el acceso al tratamiento o su cumplimiento durante el seguimiento.
Uso de la polipíldora CV en pacientes que están recibiendo una estatina diferente a atorvastatina o bien un ARAII35. En estos pacientes se puede sustituir la estatina por la de la polipíldora CV, siempre que esta mantenga la potencia reductora del cLDL43. También puede sustituirse el ARAII por ramipril, salvo en los casos en los que el paciente haya experimentado algún efecto secundario por la enzima convertidora de la angiotensina44-48. Sin embargo, es fundamental comprobar que la polipíldora CV siga consiguiendo los objetivos de PA y cLDL.
En pacientes de novo: Aquellos pacientes que no han requerido o no han seguido el tratamiento con los 3fármacos por separado y en los que se plantea administrarlos podrían ser candidatos a la polipíldora CV, sobre todo en los que se considere la posibilidad de un mal cumplimiento o la existencia de dificultades para el acceso al tratamiento, y en los pacientes que alcancen los objetivos terapéuticos con las dosis de la polipíldora CV.
En el seguimiento del tratamiento con la polipíldora CV se debe:
Asegurar el control de la PA y el cLDL, ajustando la dosis de ramipril o añadiendo/suspendiendo otros antihipertensivos, aumentando la dosis de atorvastatina o asociándola con ezetimiba, o volviendo a los monocomponentes si es necesario.
Vigilar su tolerabilidad: No hay estudios que indiquen que la polipíldora CV produce más efectos secundarios que la administración de los 3fármacos por separado, aunque sí hay algún estudio que compara varias polipíldoras contra placebo o alguno de los monocomponentes en el que se aprecia una ligera peor tolerabilidad de estas49. En caso de aparición, se deberán manejar con ajuste de dosis del fármaco implicado.
DiscusiónExiste una variedad de polipíldoras aprobadas con combinaciones de fármacos que incluyen el tratamiento de diversas enfermedades. Aunque su uso está extendido para el control de enfermedades infecciosas, en el ámbito de la prevención CV aún hay camino por recorrer, si bien numerosos estudios finalizados y en marcha en este campo muestran sus beneficios50,51. En este artículo se presentan las recomendaciones de empleo de la polipíldora CV con AAS, atorvastatina y ramipril en prevención secundaria cerebrovascular, elaboradas por expertos en neurología tras un proceso de consenso con una metodología participativa. En concreto, se realizan recomendaciones relacionadas con los perfiles de pacientes, las situaciones clínicas y las opciones de administración más adecuadas.
La aportación de la polipíldora CV se basa en el control de los FRCV y la mejora de la adherencia. Por esta razón, el uso preferencial de este medicamento incluye a pacientes con una posible afectación del cumplimiento y a aquellos en los que es importante mantener los objetivos terapéuticos, como son, entre otros, ancianos, polimedicados, polivasculares o con alta carga aterotrombótica. Asimismo, dentro del infarto cerebral hay situaciones clínicas en las que la combinación de la polipíldora CV es más adecuada que en otras y este documento realiza una primera aproximación a estas.
El interés por las combinaciones fijas de fármacos ha ido en aumento en los últimos años, probablemente por las ventajas que implica su empleo —algunas de ellas señaladas por los expertos en este documento— para los colectivos implicados: pacientes, profesionales sanitarios y el propio sistema de salud. Prueba de ese interés es la reciente aprobación de la guía actualizada sobre el desarrollo clínico de fármacos de combinación fija, realizada por el Comité de Medicamentos para Uso Humano de la Agencia Europea de Medicamentos, y que se espera que entre en vigor en octubre de 2017.
Algunos autores destacan el potencial de la polipíldora CV como herramienta para mejorar los resultados en prevención secundaria de ictus5,52,53. En la actualidad no existen recomendaciones que establezcan cuáles son los perfiles de pacientes o situaciones clínicas que más se podrían beneficiar de su uso en la enfermedad cerebrovascular aunque sí que en prevención secundaria de la enfermedad CV, González-Juanatey et al. han establecido unos criterios preferenciales para su uso. Ante esta situación, la opinión del experto cobra especial importancia, por lo que este trabajo sirve de punto de partida para definir y establecer los pacientes más idóneos para una estrategia de combinación fija para la prevención secundaria de eventos cerebrovasculares.
No obstante, este trabajo tiene limitaciones importantes, ya que precisamente se basa en la opinión de expertos y no en estudios clínicos bien diseñados, ni se ha realizado una revisión sistemática como base para la justificación de las evidencias. A pesar de ello, la opinión de los expertos fue consensuada por un panel de especialistas de reconocido prestigio y amplia experiencia clínica en el manejo de estos pacientes.
FinanciaciónEste trabajo ha contado con el soporte económico de Grupo Ferrer Internacional, S.A.
Conflicto de intereses•Jaime Masjuan declara haber recibido honorarios de laboratorios Ferrer para la realización de este trabajo.
•Jaime Gállego declara haber recibido honorarios de laboratorios Ferrer para la realización de este trabajo.
•José María Aguilera declara haber recibido honorarios de laboratorios Ferrer para la realización de este trabajo.
•Juan F. Arenillas declara haber recibido honorarios de laboratorios Ferrer para la realización de este trabajo.
•Mar Castellanos declara haber recibido honorarios de laboratorios Ferrer para la realización de este trabajo.
•Fernando Díaz declara haber recibido honorarios de laboratorios Ferrer para la realización de este trabajo.
•Juan Carlos Portilla declara haber recibido honorarios de laboratorios Ferrer para la realización de este trabajo.
•Francisco Purroy declara haber recibido honorarios de laboratorios Ferrer para la realización de este trabajo.
Los autores agradecen el soporte económico recibido por parte de Grupo Ferrer, que se ha mantenido al margen en todo el proceso, y a GOC Networking por el apoyo metodológico para la realización del trabajo.