Aida Lago et al.1 en su interesante trabajo nos envían un mensaje importante, no siempre los avances tecnológicos representan una mejora absoluta, la disminución de la mortalidad en el segundo periodo se ve contrarrestada por un aumento de la dependencia mRS>3, el 13,3% en la primera etapa frente a un 21,3% en la segunda etapa, para una gravedad y edad muy similares que son los 2 factores clave en el resultado2.
La mortalidad hospitalaria puede no ser el mejor indicador de la calidad asistencial, la mortalidad terapéutica distinguiendo embolización y cirugía, puede confundir y hacernos pensar que la cirugía tiene mayor mortalidad, aunque en la literatura hay ejemplos para todos los gustos, nosotros no encontramos diferencias entre 2 periodos, 1993-97 sin tratamiento endovascular y 2008-2012 con el tratamiento endovascular plenamente establecido3. Alfonso Lagares et al.4 han señalado la variabilidad que hay en nuestro país en cuanto a seguir las guías en relación con la elección del tipo de tratamiento endovascular o quirúrgico, aunque la elección del tipo de tratamiento no influyó en la evolución final. Por otra parte, Ángel Horcajadas et al.5 han observado que el tratamiento endovascular resulta más caro que el quirúrgico en aneurismas rotos fundamentalmente debido al precio de los materiales de embolización, la tasa de retratamientos y al seguimiento que precisan.
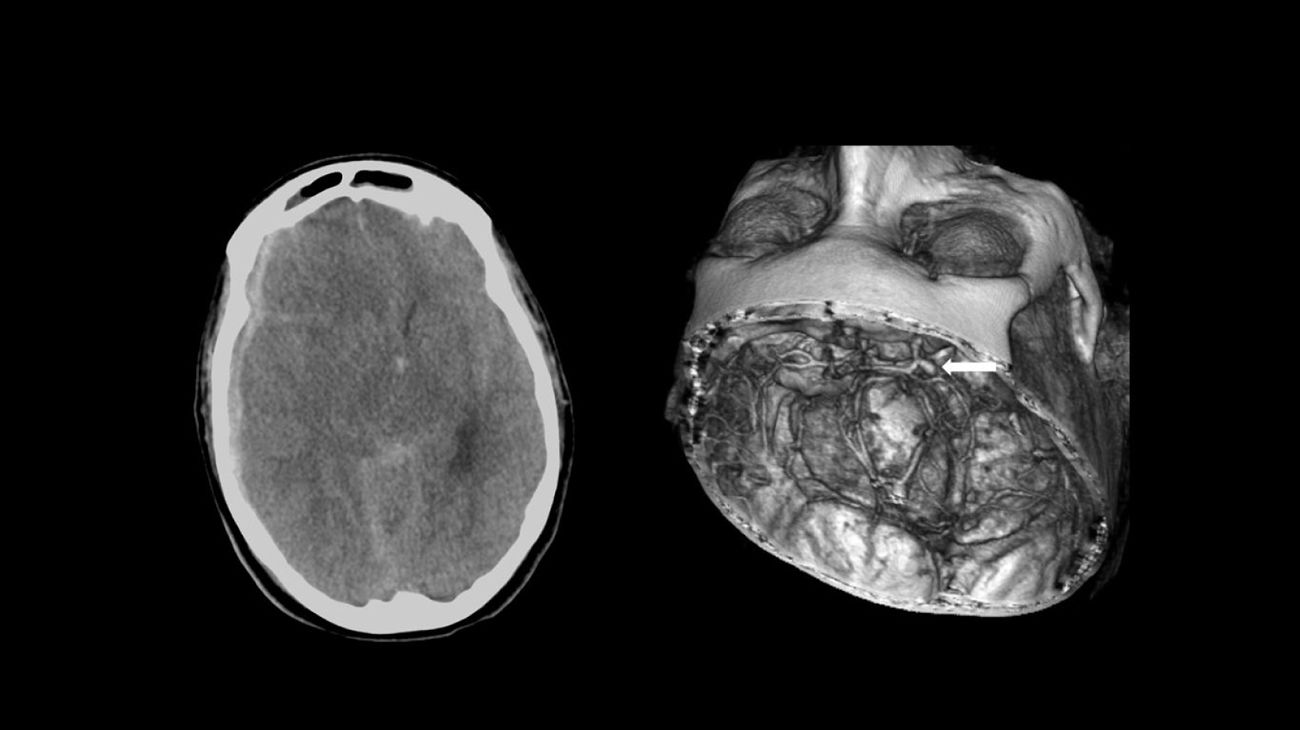
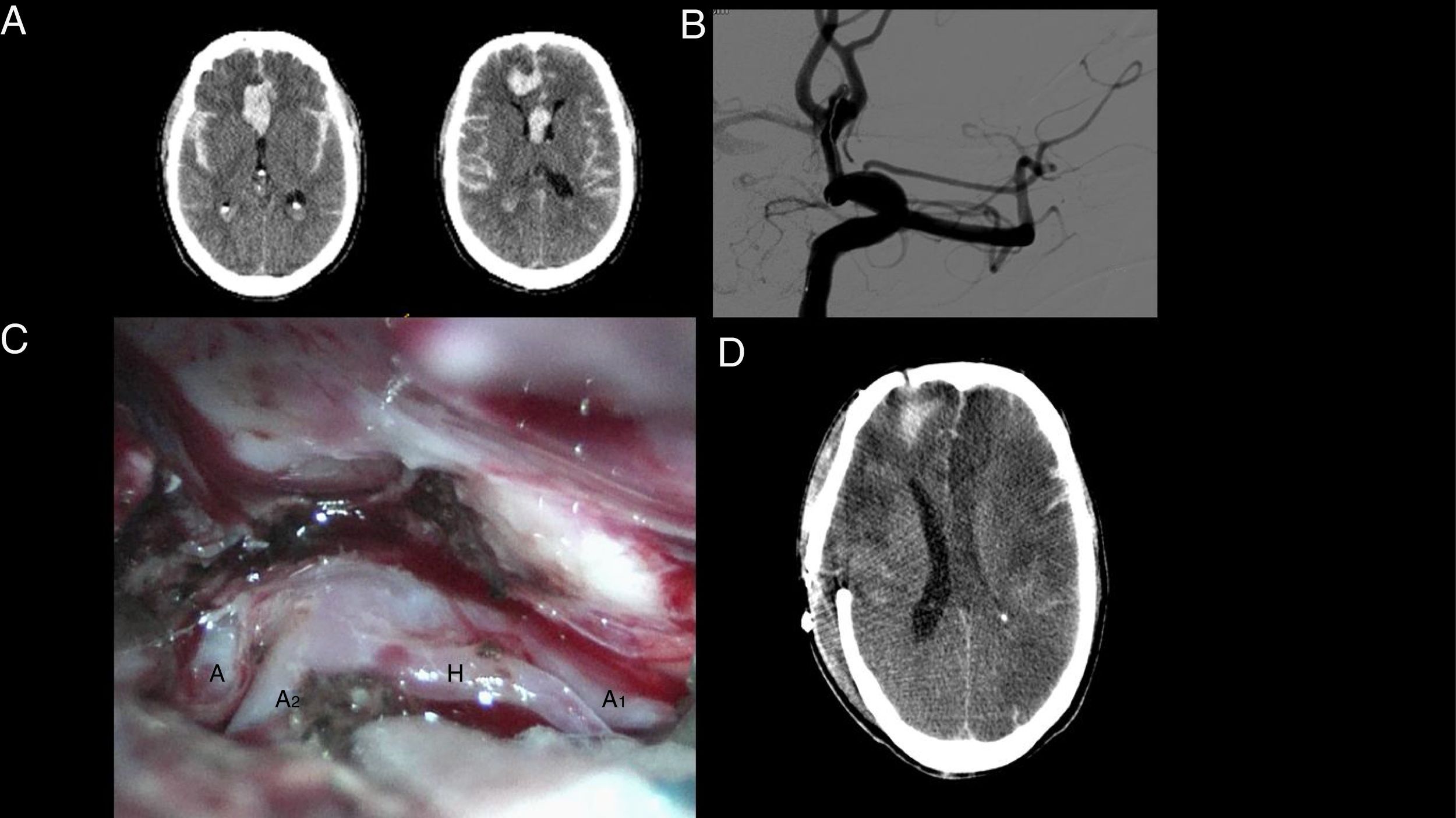
Los tratamientos combinados embolización y cirugía, en quirófanos híbridos para determinados casos (fig. 1) pueden ser una buena opción terapéutica, por eso los neurocirujanos que antes éramos los únicos especialistas dedicados a la HSAa podemos contribuir a mejorar los resultados. Por otra parte, si desde la residencia no se capacita a los diferentes especialistas interesados (neurocirujanos, neurólogos, neurorradiólogos) en el tratamiento endovascular, cada vez habrá menos neurocirujanos capacitados/interesados en esta enfermedad y solo se intervendrán quirúrgicamente casos muy difíciles-complejos que los especialistas en el tratamiento endovascular hayan considerado «malos» casos (fig. 2) a pesar de que la industria que avanza vertiginosamente y se ha afanado para encontrar algún/nos material/es para cada situación independientemente del índice cuello/cúpula, tamaño y localización. Aunque al igual que con la cirugía nos deberíamos preguntar más a menudo si determinado aneurisma se ha de tratar porque se puede o porque se debe.
Paciente de 53 años que sufrió cefalea súbita con pérdida de conciencia. El servicio de emergencias médicas procedió a la intubación orotraqueal y traslado al hospital H donde se hizo el diagnóstico de HSA con HSDA por rotura de aneurisma de ACoP (flecha). Se trasladó al hospital M que estaba de guardia de fin de semana para HSA donde se realizó craneotomía para evacuar el HSDA y después embolización del aneurisma. La paciente murió en el hospital M 13 días más tarde.
Paciente de 62 años que sufrió una HSA con cefalea y pérdida de conciencia. El servicio de emergencias médicas procedió a la intubación orotraqueal y ventilación mecánica trasladándolo a un hospital donde se realizó una TC. Desde el primer centro se remitió al hospital de guardia para HSA de fin de semana donde se repitió la TC (A) que mostró un aumento de sangre (resangrado). Se intentó un tratamiento endovascular y, aunque se consiguió introducir un microcatéter en el aneurisma (B), se desestimó el tratamiento endovascular y fue operado de urgencia clipándose el aneurisma (C). La TC practicada unos días más tarde mostraba infartos múltiples bilaterales (D) sugestivos de vasoespasmo. El paciente falleció 20 días después del ingreso.
Ya he expresado anteriormente mi opinión sobre algunos aspectos organizativos en el tratamiento de los ictus6 y obviamente, la conveniencia del abordaje multidisciplinario, pero nadie mejor que el especialista que ve al paciente en urgencias, estudia la TC y la TC multimodal, puede reconstruir las imágenes en una estación de trabajo y ver las características del aneurisma y su relación con otras estructuras anatómicas, podrá decidir que es mejor para el paciente, si un tratamiento endovascular, quirúrgico o combinado (fig. 1) especialmente si realiza las 2 técnicas. Algunos pacientes se pueden intervenir con solo las imágenes que aporta el angio-TC sin necesidad de estudio angiográfico con resultados aceptables7. En este sentido, me ha parecido interesante que el trabajo de Aida Lago et al.1 se refiere que desde 2014 se realiza angiografía urgente para la HSAa, pero parece deducirse que no se realiza el tratamiento en el mismo momento que se hace la angiografía diagnóstica urgente. Con la TC multimodal que se emplea para los ictus isquémicos se debería analizar algunos aspectos anatómicos y fisiológicos de la HSAa. Aún no consigo entender porqué en algunos hospitales con guardia para el ictus isquémico la información que puede dar la TC de perfusión no se utiliza en la HSAa y repitiendo lo dicho anteriormente, algunos aneurismas podrían ser tratados más eficientemente con cirugía.
El documento de consenso8 elaborado por las sociedades de neurología, neurocirugía, neurorradiología y el Grupo Español de Neurorradiología Intervencionista (GENI) para la capacitación y acreditación en neurorradiología intervencionista representa un hito en la historia de las neurociencias, quizás el siguiente paso será elaborar otro documento de consenso para que el neurocirujano vascular (NCV), especie en peligro de extinción, obtenga la capacitación en un centro acreditado para realizar un bypass, extirpar una malformación arteriovenosa y si llega el copago, clipar un aneurisma porque el material de embolización es muy costoso para una familia sin recursos económicos. Quizás el NCV primero se convierta en un especie ornamental, experto en clipatología y bypass que los grandes hospitales exhibirán en sus páginas web. Referente al documento de consenso8 yo añadiría que el especialista capacitado para el tratamiento endovascular, porque no, debería estar capacitado, también, para colocar un drenaje ventricular, un sensor para medir la presión intracraneal y realizar una hemicraniectomía descompresiva preventiva después de un tratamiento fútil con trombectomía mecánica. En mi opinión, en los hospitales que pueden hacer un tratamiento endovascular (acreditados) para determinados tipos de ictus deben tener un especialista de guardia de presencia física capacitado para poder realizar, también, un tratamiento endovascular de un aneurisma roto (es poco eficiente tener a un virtuoso en NRI atrapado en un atasco de tráfico). Es posible que en el futuro, estas actividades cruentas las realice cualquier especialista en neurociencias con la ayuda de un robot9. Parece que estamos encaminados a que un especialista en enfermedad cerebro-vascular desde un puesto de mando pueda analizar diferentes escalas, índices y formulas (NHISS, GCS, SPAN-100, RACE) y signo de Babinski que además de su aplicabilidad hayan demostrado su utilidad junto con parámetros que ofrezca la TC multimodal como el tipo de ictus, tiempo medio de tránsito, colaterales y en una telepantalla (telemedicina), cada vez más usamos la telepantalla para la actividad asistencial, desde el puesto de control del consorcio o con una aplicación en un teléfono inteligente diga lo que hay que hacer teniendo en el hospital donde esté el paciente a un especialista capacitado para estas actividades manuales, obviamente dirigidos por el experto en enfermedades cerebrovasculares (neurólogo). El microscopio quirúrgico, una reliquia del siglo pasado, imprescindible para el NCV, se irá sustituyendo por la medicina a través de pantallas y la ayuda de robots9 asistidos por intensivistas, anestesistas, y demás especialistas del equipo multidisciplinario, muy motivados para este tipo de enfermedad. Es muy saludable que en algunos centros como el Hospital La Fe, neurología tenga el liderazgo en este tipo de ictus como parece desprenderse de la naturaleza de los coautores con respecto a la serie antigua10, que como he expresado anteriormente hace años era en muchos hospitales competencia de neurocirugía, y ponga su empeño como se ha demostrado en los ictus isquémicos. Vivimos una época de transición en que el NCV acostumbrado a operar con el microscopio quirúrgico se deba acostumbrar a tratar a los pacientes a través de telepantallas con la ayuda de la abundante información obtenida por las pruebas de imagen. En esta época hay que huir de los arrebatos de entusiasmo terapéutico y no operar/embolizar a determinados pacientes (fig. 2), la técnica se aprende en 3 meses, 3 años se tarda en saber cuándo se puede aplicar, lo más difícil es saber/decidir cuando no se debe aplicar.
Me ha intrigado que en el trabajo de Aida Lago et al.1 no se comente porqué en el segundo periodo analizado (2007-2010) haya menos casos por año de HSAa, aproximadamente 23 por año, mientras que en el primer periodo (1997-2005), hay aproximadamente 31 casos por año, cuando la mayoría de autores reconoce que es el tipo de ictus cuya incidencia se mantiene más constante.
Referente al vasoespasmo, nos hemos acostumbrado a llamar así lo que más propiamente se debería llamar déficit isquémico tardío, es como una especie de «cajón de sastre» que a veces incluye otras complicaciones sistémicas como alteraciones metabólicas, infecciones, alteraciones cardiacas, etc.2, frecuentes en pacientes tan frágiles como los que padecen una HSAa y no han variado significativamente entre los 2 periodos analizados por Aida Lago et al.1, el 10,6% en la primera época y el 9,2% en la segunda época.
Los 2 factores clave la edad y el estado neurológico son los que determinan el resultado y me ha llamado la atención que Aida Lago et al.1 utilicen la escala de Glasgow y la de Hunt y Hess en lugar de la más empleada en neurología, el NHISS. En mi opinión, ahora que cada vez se implican más los neurólogos en liderar el manejo de este tipo de ictus, consensuar una escala para todos los ictus sería muy práctico. Para terminar, en mi modesta opinión, sería deseable elaborar unas guías entre todos los implicados para hacer posible un abordaje multidisciplinario de todos los ictus.