Las miopatías autoinmunes constituyen una entidad poco frecuente, con una prevalencia estimada entre 9-14 personas por cada 100.000 habitantes1. En concreto, la miopatía necrosante inmunomediada (MNI) se caracteriza por debilidad muscular proximal, elevación de CK y necrosis de fibras musculares con signos de regeneración, con mínima o ausente infiltración inflamatoria en la biopsia muscular2. Su desarrollo se ha relacionado con la toma de estatinas3, así como la presencia de determinadas enfermedades del tejido conectivo, infección por virus de la inmunodeficiencia humana2,4. De acuerdo con series de casos previamente publicados5, es posible encontrar positividad para anticuerpos anti-HMG-CR (33%) o anti-SRP (24%), si bien entre un 20-30% de las MNI son seronegativas6. Presentamos un caso de MNI tras tratamiento con adalimumab en un paciente con espondilitis anquilosante HLA-B27.
Varón de 55 años, con antecedentes de psoriasis cutánea y espondilitis anquilosante HLA-B27 de 20 años de evolución, en tratamiento con adalimumab desde hacía 2años. Consulta por cuadro de dolor muscular de predominio proximal en extremidades, que se inició a los 6meses de haber comenzado con dicho fármaco. El paciente refería desde entonces mayor dificultad para la marcha, para subir y bajar escaleras y pérdida de masa muscular, tanto en brazos como en piernas. En la exploración neurológica destacaba una paresia bilateral 4/5 según la escala Medical Research Council en músculos psoas y cuádriceps junto con atrofia muscular en ambos deltoides y cuádriceps. No se observaron fasciculaciones ni ninguna otra actividad muscular espontánea, así como tampoco escapula alada. Los reflejos musculares profundos se encontraban presentes y la marcha no mostraba alteraciones.
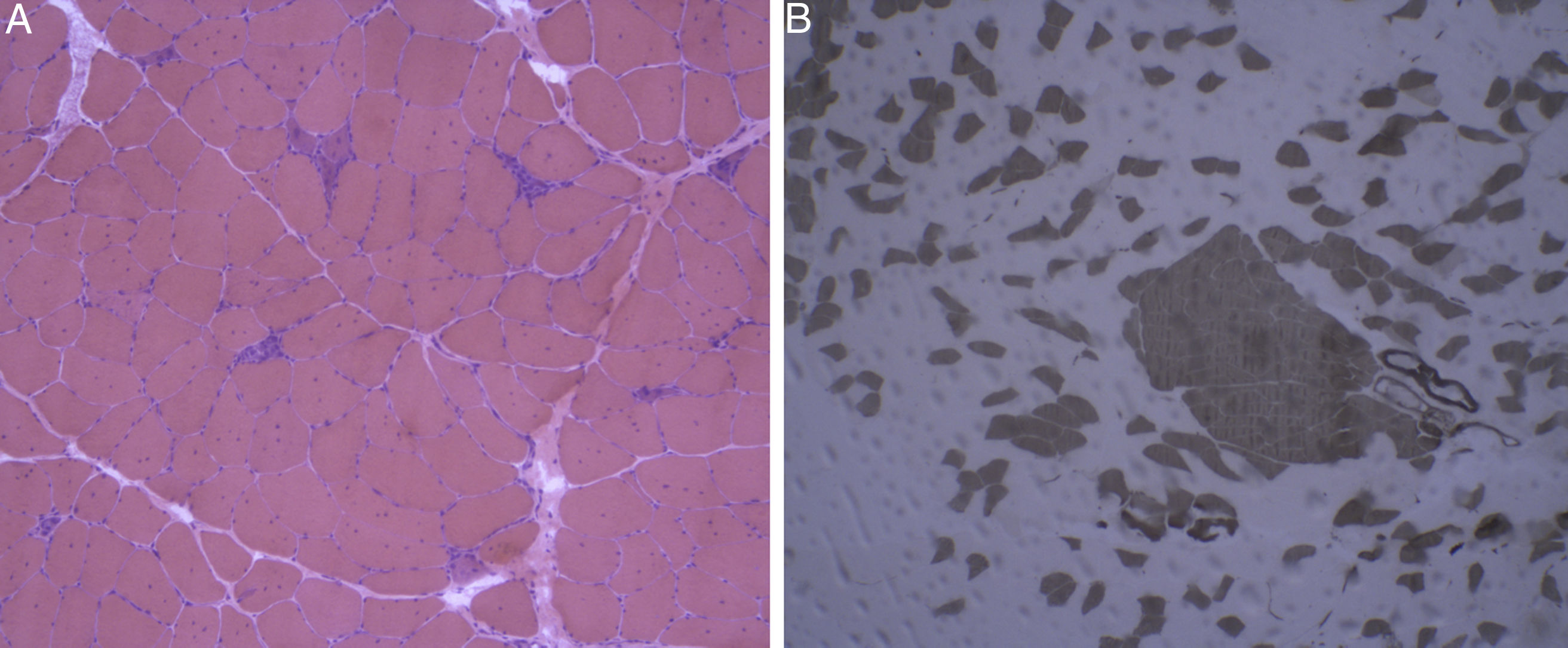
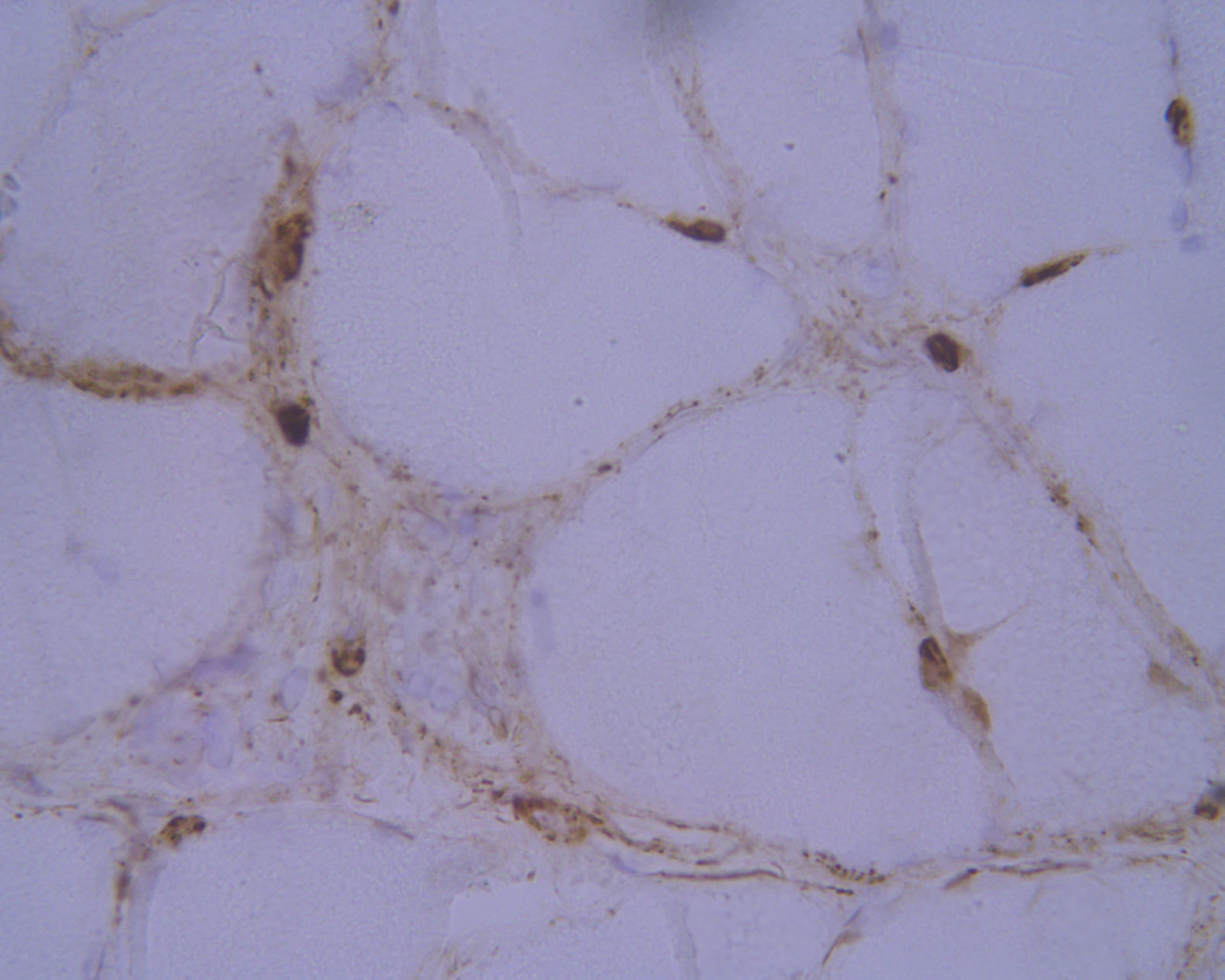
Los estudios analíticos mostraron elevación de cifras de CK de hasta 385 UI/l, determinada a los 7 meses del inicio del tratamiento, con hemograma, velocidad de sedimentación globular, aldolasa, perfil hepático, renal y serologías dentro de la normalidad. Ante la sospecha de cuadro miopático, se realizó resonancia magnética de extremidades inferiores que no mostró alteraciones y electromiograma sin datos indicativos de miopatía. Se realizaron también determinaciones periódicas de CK, siendo el valor máximo alcanzado de 598 UI/l. Se completó el estudio con la realización de una biopsia del músculo cuádriceps en la que se evidenciaron hallazgos compatibles con una MNI (figs. 1 [A y B] y 2). Ante este hallazgo, se completó el estudio de autoinmunidad con la determinación de anticuerpos antinucleares, ENA, anti-HMGCR, anti-SRP y panel de miositis, cuyo resultado fue negativo. Además, se realizó una tomografía axial computarizada toraco-abdomino-pélvica en la que se descartó existencia de neoplasia concomitante.
Tinción con hematoxilina eosina y técnicas inmunohistoquímicas de pieza de biopsia muscular. A) Tinción con hematoxilina-eosina: músculo esquelético con arquitectura conservada sin engrosamiento conectivo endomisial ni infiltración por tejido adiposo. Se identifican frecuentes fibras regenerativas, así como necróticas con fenómenos de miofagocitosis. B) ATPasa 9,4: muestra reagrupamiento por tipos de fibras, con presencia de grupos de fibras tipo 1 y tipo 2, compatible con reinervación.
Tras obtener resultado anatomopatológico, se decidió la suspensión de adalimumab y el inicio de corticoterapia, inicialmente mediante metilprednisolona 500mg por vía intravenosa durante 3 días, con posterior pauta descendente de prednisona por vía oral hasta dosis de mantenimiento de 20mg/día. A los 6meses, se observó descenso en las cifras de CK hasta 120-130 UI/l y discreta mejoría del déficit motor, aunque con persistencia de mialgias. Se decidió entonces asociar azatioprina 50mg cada 12 h, presentado una ligera mejoría de las mialgias.
Los fármacos inhibidores del factor de necrosis tumoral alfa (anti-TNF-α) son fármacos cada vez más usados en el tratamiento de enfermedades autoinmunes. Paradójicamente, debido a su efecto inmunomodulador, se han reportado casos de enfermedades de origen autoinmune asociadas a su uso: vasculitis, fenómenos lupus eritematoso-like o enfermedad intersticial pulmonar7. Se han descrito series de casos en las que los anti-TNF-α se han relacionado con la aparición de miopatías inmunomediadas, como miositis y dermatomiositis7,8. Pese a que se conoce esta posible relación, hasta la fecha no se han descrito cuadros de MNI asociada al uso de adalimumab como el paciente que presentamos. En nuestro caso, la estrecha relación temporal entre el inicio del fármaco y el comienzo de la sintomatología, así como la normalización de la CK y la mejoría de las mialgias tras la suspensión de adalimumab, sugerían la probable implicación de este en la aparición del cuadro de afectación miopática.
En cuanto al tratamiento de la MNI, se recomienda tratamiento de inducción con corticoides por vía oral o intravenosa, pudiendo asociar un agente inmunosupresor en ese mismo momento o en el siguiente mes, en función de la severidad y la respuesta terapéutica inicial. Se han descrito respuestas aceptables usando terapias inmunosupresoras tales como metotrexato, azatioprina, ciclosporina o micofenolato de mofetilo9. El uso combinado de varios inmunosupresores puede ser necesario en el 50% de los casos y el empleo de inmunoglobulinas por vía intravenosa o rituximab también puede ser una opción terapéutica en casos de refractariedad o incluso durante la terapia de inducción9. En conclusión, los fármacos inhibidores de TNF-α han sido asociados con el desarrollo de miopatías inmunomediadas, su identificación y retirada precoz es fundamental en el pronóstico final de la enfermedad.