En el tratamiento de la epilepsia existen una serie de comorbilidades y grupos poblacionales (mujeres en edad fértil y ancianos) para los cuales podemos encontrar limitaciones en el manejo y precisar ajustes del tratamiento.
DesarrolloBúsqueda de artículos en Pubmed y recomendaciones de las Guías de práctica clínica en epilepsia y sociedades científicas más relevantes referentes la epilepsia en situaciones especiales (comorbilidades, mujeres en edad fértil, ancianos). Se clasifican las evidencias y recomendaciones según los criterios pronósticos del Oxford Center of Evidence-Based Medicine (2001) y de la European Federation of Neurological Societies (2004) para las actuaciones terapéuticas.
ConclusionesEn las diversas comorbilidades, es necesaria una adecuada selección del tratamiento para mejorar la eficacia con el menor número de efectos secundarios. En la epilepsia catamenial es necesario un ajuste de la medicación antiepiléptica y/u hormonal, para poder controlar correctamente las crisis. La exposición a fármacos antiepilépticos durante la gestación aumenta el riesgo de malformaciones congénitas (MC) y puede afectar al crecimiento fetal y/o al desarrollo cognitivo. En el puerperio se aconseja la lactancia materna, vigilando los efectos adversos si se usan fármacos sedantes. Finalmente, los ancianos son una población muy susceptible de presentar epilepsia y que tiene unas características diferenciales con respecto a otros grupos de edad para el diagnóstico y el tratamiento. Estos pacientes pueden presentar con mayor frecuencia limitaciones terapéuticas por sus comorbilidades, pero suelen responder mejor al tratamiento y a dosis más bajas que en el resto de grupos de edad.
The characteristics of some population groups (patients with comorbidities, women of childbearing age, the elderly) may limit epilepsy management. Antiepileptic treatment in these patients may require adjustments.
DevelopmentWe searched articles in Pubmed, clinical practice guidelines for epilepsy, and recommendations by the most relevant medical societies regarding epilepsy in special situations (patients with comorbidities, women of childbearing age, the elderly). Evidence and recommendations are classified according to the prognostic criteria of Oxford Centre of Evidence-Based Medicine (2001) and the European Federation of Neurological Societies (2004) for therapeutic interventions.
ConclusionsEpilepsy treatment in special cases of comorbidities must be selected properly to improve efficacy with the fewest side effects. Adjusting antiepileptic medication and/or hormone therapy is necessary for proper seizure management in catamenial epilepsy. Exposure to antiepileptic drugs (AED) during pregnancy increases the risk of birth defects and may affect fetal growth and/or cognitive development. Postpartum breastfeeding is recommended, with monitoring for adverse effects if sedative AEDs are used. Finally, the elderly are prone to epilepsy, and diagnostic and treatment characteristics in this group differ from those of other age groups. Although therapeutic limitations may be more frequent in older patients due to comorbidities, they usually respond better to lower doses of AEDs than do other age groups.
Los estudios epidemiológicos detectan un mayor número de patologías concomitantes entre la población con epilepsia. El tipo de comorbilidad asociada es un factor importante para decidir el tratamiento más oportuno para el control de las crisis epilépticas (CE). En la tabla 1 se resumen las abreviaturas de los principales FAE.
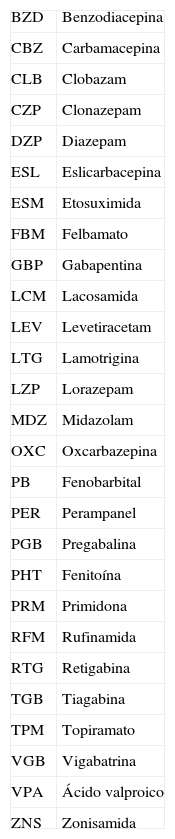
Abreviaturas de los fármacos antiepilépticos
| BZD | Benzodiacepina |
| CBZ | Carbamacepina |
| CLB | Clobazam |
| CZP | Clonazepam |
| DZP | Diazepam |
| ESL | Eslicarbacepina |
| ESM | Etosuximida |
| FBM | Felbamato |
| GBP | Gabapentina |
| LCM | Lacosamida |
| LEV | Levetiracetam |
| LTG | Lamotrigina |
| LZP | Lorazepam |
| MDZ | Midazolam |
| OXC | Oxcarbazepina |
| PB | Fenobarbital |
| PER | Perampanel |
| PGB | Pregabalina |
| PHT | Fenitoína |
| PRM | Primidona |
| RFM | Rufinamida |
| RTG | Retigabina |
| TGB | Tiagabina |
| TPM | Topiramato |
| VGB | Vigabatrina |
| VPA | Ácido valproico |
| ZNS | Zonisamida |
El tratamiento de las CE concurrentes con otras enfermedades sin relación causal con la epilepsia precisa algunas consideraciones1,2:
- 1.
La frecuencia de las crisis puede cambiar debido a las enfermedades concurrentes o a las medicaciones empleadas.
- 2.
El metabolismo de los FAE puede alterarse por las enfermedades o por las interacciones con las medicaciones utilizadas.
- 3.
Los FAE pueden exacerbar las enfermedades médicas debido a posibles efectos adversos.
- 4.
En pacientes con enfermedades médicas o quirúrgicas pueden verse limitadas las opciones del tratamiento antiepiléptico, según la posible vía de administración y la situación clínica.
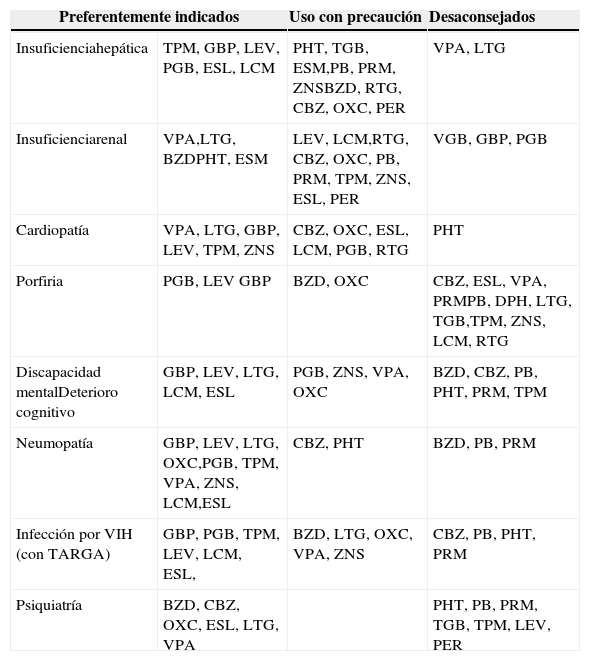
No se han realizado ensayos clínicos controlados y aleatorizados, diseñados específicamente para este tipo de situaciones clínicas. La mayor parte de la información disponible proviene de series de casos y análisis retrospectivos u opiniones de expertos o de recomendaciones en distintas GPC1-4 nivel de evidencia (NE) IV y se resumen en la tabla 2.
Antiepilépticos de elección en diversas enfermedades. Recomendaciones GE-SEN
| Preferentemente indicados | Uso con precaución | Desaconsejados | |
|---|---|---|---|
| Insuficienciahepática | TPM, GBP, LEV, PGB, ESL, LCM | PHT, TGB, ESM,PB, PRM, ZNSBZD, RTG, CBZ, OXC, PER | VPA, LTG |
| Insuficienciarenal | VPA,LTG, BZDPHT, ESM | LEV, LCM,RTG, CBZ, OXC, PB, PRM, TPM, ZNS, ESL, PER | VGB, GBP, PGB |
| Cardiopatía | VPA, LTG, GBP, LEV, TPM, ZNS | CBZ, OXC, ESL, LCM, PGB, RTG | PHT |
| Porfiria | PGB, LEV GBP | BZD, OXC | CBZ, ESL, VPA, PRMPB, DPH, LTG, TGB,TPM, ZNS, LCM, RTG |
| Discapacidad mentalDeterioro cognitivo | GBP, LEV, LTG, LCM, ESL | PGB, ZNS, VPA, OXC | BZD, CBZ, PB, PHT, PRM, TPM |
| Neumopatía | GBP, LEV, LTG, OXC,PGB, TPM, VPA, ZNS, LCM,ESL | CBZ, PHT | BZD, PB, PRM |
| Infección por VIH (con TARGA) | GBP, PGB, TPM, LEV, LCM, ESL, | BZD, LTG, OXC, VPA, ZNS | CBZ, PB, PHT, PRM |
| Psiquiatría | BZD, CBZ, OXC, ESL, LTG, VPA | PHT, PB, PRM, TGB, TPM, LEV, PER | |
La mujer con epilepsia (MCE) requiere consideraciones especiales y estrategias de tratamiento específicas que tengan en cuenta no solo el control de las CE, sino también los efectos secundarios a corto y largo plazo de los FAE, el efecto de las hormonas sexuales sobre las CE y el impacto de la epilepsia y los FAE sobre el bienestar reproductivo y la calidad de vida de estas pacientes. Estas consideraciones especiales alcanzan su máxima expresión durante el embarazo, en el que tanto las CE como el tratamiento con FAE pueden tener efectos nocivos sobre el feto.
Epilepsia, fertilidad y sexualidadLos principales problemas en este aspecto de la MCE, son5–8:
- –
Mayores cifras de infertilidad y disfunción sexual en la MCE.
- –
La prevalencia de síndrome de ovario poliquístico en MCE es mayor, aunque no tomen FAE. Aumenta si el tratamiento es con VPA, fundamentalmente si su instauración es por debajo de los 20 años.
- –
Se debe preguntar de forma rutinaria a la MCE acerca de ciclos menstruales, infertilidad, ganancia excesiva de peso, hirsutismo, galactorrea y alteraciones en las relaciones sexuales.
- –
En caso de detectar anomalías, debemos valorar la realización de determinaciones hormonales, ecografía pélvica y neuroimagen hipofisaria.
- –
Si la causa del problema se pone en relación con FAE, debe plantearse una alternativa terapéutica con otros FAE.
Existen 3 patrones de aumento de las CE: el perimenstrual, que es el más frecuente, durante la ovulación y en la fase luteínica inadecuada con ciclos anovulatorios, en la segunda parte del ciclo5. Aproximadamente un tercio de las MCE tienen el doble de crisis durante estos periodos del ciclo menstrual respecto al basal. Si se observa este patrón, se recogen en la bibliografía pautas de tratamiento elaboradas por expertos que aconsejan8, NE IV:
- 1.
Aumentar la dosis de FAE durante los periodos perimenstrual y ovulatorio.
- 2.
Emplear BZD, especialmente clobazam a dosis de 10-30mg/día perimenstrual.
- 3.
Acetazolamida 250mg/día en los periodos perimenstrual y ovulatorio.
- 4.
Terapia hormonal (progesterona) en los casos de ciclos anovulatorios y anticonceptivos hormonales, siempre bajo la supervisión del ginecólogo.
No hay evidencia que los anticonceptivos hormonales (ACO) combinados aumenten la frecuencia crítica8.
Embarazo y partoLa mayoría de las MCE tiene un embarazo, un parto y una descendencia normales. La frecuencia de las CE no cambia generalmente durante el embarazo, parto o puerperio en las MCE9, NE II. Los niveles plasmáticos de los FAE pueden cambiar en el trascurso del embarazo. Hay aumento del aclaramiento de PHT, CBZ y LTG con gran variabilidad interindividual, por lo que se aconseja la monitorización de dichos niveles (mínimo trimestral). También, si es posible, hay que controlar los niveles o adecuar las dosis del LEV y OXC.
La mayoría de las MCE tienen embarazo normal, pero pueden tener un riesgo mayor de complicaciones9, NE II. Las recomendaciones sobre el parto y puerperio serían10:
- –
Recomendación de parto vaginal.
- –
Se considerará cesárea si alto riesgo de CGTC (1-3%), si CPC prolongadas o frecuentes que dificulten la colaboración de la mujer.
- –
Se puede suministrar anestesia epidural.
- –
No contraindicado el uso de prostaglandinas.
- –
Niveles a las 2-3 semanas posparto, si se ha cambiado la dosis durante embarazo (si PRM, OXC y LTG monitorizar inmediatamente) para ajustar la dosis, sobre todo si se da lactancia materna.
- –
Consejos higiénicos sobre el sueño.
La exposición a los FAE durante el embarazo se asocia a un aumento del riesgo de MC y puede tener un efecto adverso sobre el crecimiento fetal y el desarrollo cognitivo13.
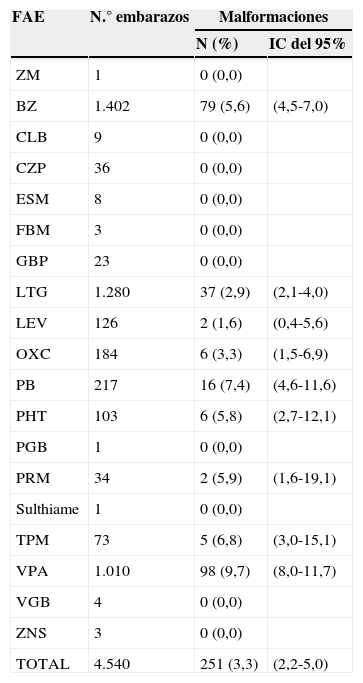
La tabla 3 muestra el porcentaje de malformaciones de los FAE en monoterapia, en el registro EURAP a junio del 201014. Si, a pesar de ello, la paciente precisa VPA, intentaremos que la dosis sea la mínima (< 800mg) y en varias tomas. VPA a dosis inferiores a 700mg tiene un riesgo similar al de CBZ a dosis de 400-1000mg, al de PB<150mg y al de LTG>300mg11, NE III.
Número de embarazos prospectivos con los diferentes FAE en monoterapia, porcentaje de malformaciones detectadas hasta el año del parto: intervalo de confianza del 95% (N=4.540). Registro EURAP 201014
| FAE | N.° embarazos | Malformaciones | |
|---|---|---|---|
| N (%) | IC del 95% | ||
| ZM | 1 | 0 (0,0) | |
| BZ | 1.402 | 79 (5,6) | (4,5-7,0) |
| CLB | 9 | 0 (0,0) | |
| CZP | 36 | 0 (0,0) | |
| ESM | 8 | 0 (0,0) | |
| FBM | 3 | 0 (0,0) | |
| GBP | 23 | 0 (0,0) | |
| LTG | 1.280 | 37 (2,9) | (2,1-4,0) |
| LEV | 126 | 2 (1,6) | (0,4-5,6) |
| OXC | 184 | 6 (3,3) | (1,5-6,9) |
| PB | 217 | 16 (7,4) | (4,6-11,6) |
| PHT | 103 | 6 (5,8) | (2,7-12,1) |
| PGB | 1 | 0 (0,0) | |
| PRM | 34 | 2 (5,9) | (1,6-19,1) |
| Sulthiame | 1 | 0 (0,0) | |
| TPM | 73 | 5 (6,8) | (3,0-15,1) |
| VPA | 1.010 | 98 (9,7) | (8,0-11,7) |
| VGB | 4 | 0 (0,0) | |
| ZNS | 3 | 0 (0,0) | |
| TOTAL | 4.540 | 251 (3,3) | (2,2-5,0) |
Tomado de Martínez Ferri et al.14.
El mayor riesgo de desarrollo de trastornos cognitivos en los hijos de MCE se ha ligado al tratamiento con VPA, PB, politerapia y/o haber presentado 5 o más CGTC durante el embarazo. Respecto al valproato existen estudios recientes que demuestran un efecto dosis-riesgo11; además, en los resultados a los 6 años influye de forma positiva el tratamiento con ácido fólico durante el embarazo y la lactancia materna.
Teratogenicidad de los nuevos fármacos antiepilépticosCon los FAE más recientes, incluso llevando algunos más de 10 años en el mercado, no existen por ahora datos fiables. Las publicaciones al respecto son escasas y el número de pacientes en monoterapia es bajo en su mayoría. Es necesario un mayor número de casos para determinar las diferencias en relación con malformaciones concretas, como son el paladar hendido, las comunicaciones interventriculares, o para aquellas aún menos comunes, como la anencefalia.
La Food and Drug Administration, en 2011, cambió la categoría del TPM del grupo C al D al encontrar el registro norteamericano un riesgo de MC del 4,2% (15/359 monoterapias), con una prevalencia de paladar hendido del 1,4%. Respecto al LEV, tenemos datos de 4 registros de MC: el de Reino Unido con 2 casos/304 monoterapias; EURAP 1,6%11 (2/126 monoterapias); el registro norteamericano 2,4% (11/450 monoterapias), y el registro de la propia compañía (UCB) con un 7,5% (26/297), aunque con inclusión y metodología diferente de la de otros registros12. Con OXC existen 248 casos publicados, de los cuales 6 con MC (2,4%)15. Con GBP, ZNS, PGB, LCM, ESL, RTG y PER, el número de pacientes es todavía es muy escaso.
Puerperio y lactanciaLos FAE de primera generación, PTH, PB, CBZ y VPA, no penetran en la leche materna en niveles clínicamente importantes y sí lo hacen GBP, LTG y TPM16, NE II-III. En el caso de PB, PRM o BZD, el recién nacido puede presentar somnolencia y tener dificultad para succionar o irritabilidad, por lo que hay que tener un control estricto de los efectos adversos. Es limitada la experiencia con los nuevos FAE.
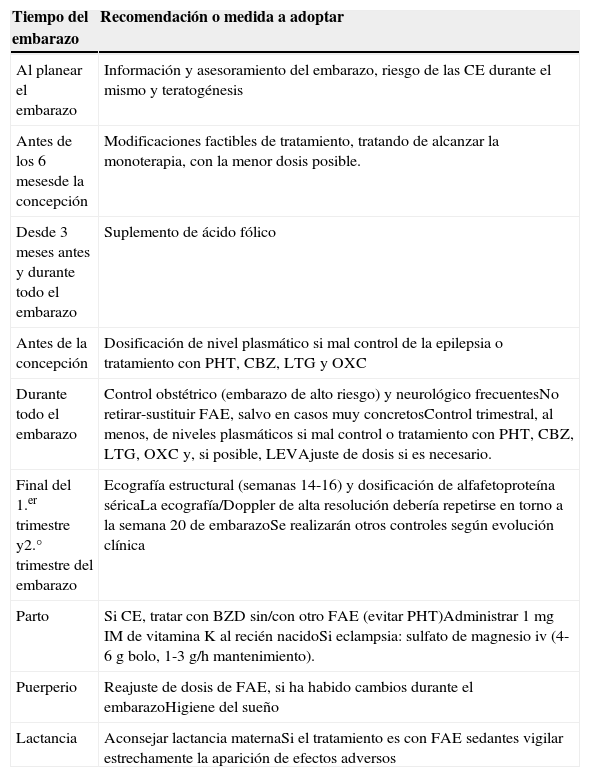
En la tabla 4 se recoge la información general para la MCE durante la preconcepción, el embarazo, el parto y el puerperio.
Consejos a la MCE en el embarazo, el parto y el puerperio
| Tiempo del embarazo | Recomendación o medida a adoptar |
|---|---|
| Al planear el embarazo | Información y asesoramiento del embarazo, riesgo de las CE durante el mismo y teratogénesis |
| Antes de los 6 mesesde la concepción | Modificaciones factibles de tratamiento, tratando de alcanzar la monoterapia, con la menor dosis posible. |
| Desde 3 meses antes y durante todo el embarazo | Suplemento de ácido fólico |
| Antes de la concepción | Dosificación de nivel plasmático si mal control de la epilepsia o tratamiento con PHT, CBZ, LTG y OXC |
| Durante todo el embarazo | Control obstétrico (embarazo de alto riesgo) y neurológico frecuentesNo retirar-sustituir FAE, salvo en casos muy concretosControl trimestral, al menos, de niveles plasmáticos si mal control o tratamiento con PHT, CBZ, LTG, OXC y, si posible, LEVAjuste de dosis si es necesario. |
| Final del 1.er trimestre y2.° trimestre del embarazo | Ecografía estructural (semanas 14-16) y dosificación de alfafetoproteína séricaLa ecografía/Doppler de alta resolución debería repetirse en torno a la semana 20 de embarazoSe realizarán otros controles según evolución clínica |
| Parto | Si CE, tratar con BZD sin/con otro FAE (evitar PHT)Administrar 1 mg IM de vitamina K al recién nacidoSi eclampsia: sulfato de magnesio iv (4-6 g bolo, 1-3 g/h mantenimiento). |
| Puerperio | Reajuste de dosis de FAE, si ha habido cambios durante el embarazoHigiene del sueño |
| Lactancia | Aconsejar lactancia maternaSi el tratamiento es con FAE sedantes vigilar estrechamente la aparición de efectos adversos |
Comparando con otras edades, las CE y la epilepsia en el anciano difieren en la forma de presentación, el diagnóstico y el pronóstico en los siguientes aspectos.
- 1.
Etiología. Lo más frecuente son las CE sintomáticas agudas y remotas, destacando la enfermedad cerebrovascular (40-50%), seguida de la patología degenerativa cerebral, tumores primarios y metástasis, traumatismos craneoencefálicos e infecciones del sistema nervioso central.
- 2.
Tipo de CE. Predominan las CP, especialmente las CPC (38%). La localización más frecuente del foco epiléptico es frontal, acorde con la localización predominante de los ictus. La semiología de la CE varía sobre todo en:
- –
Las auras y los automatismos son raros y, cuando ocurren, son poco específicos.
- –
Hay una mayor incidencia de síntomas motores y sensitivos que de síntomas psíquicos. A veces, las CE se manifiestan como episodios de confusión prolongados, enlentecimiento mental, lapsus de memoria, conducta extraña, periodos recurrentes de hiporreactividad y otros síntomas poco definidos que pueden ser la única expresión crítica.
- –
En ocasiones, pueden tener una semiología de características sincopales.
- –
Las CGTC secundarias son menos habituales que en adultos, pero pueden ocasionar importantes traumatismos.
- –
La duración de la poscrisis puede ser muy dilatada. La parálisis de Todd prolongada es muy prevalente en CE de origen vascular.
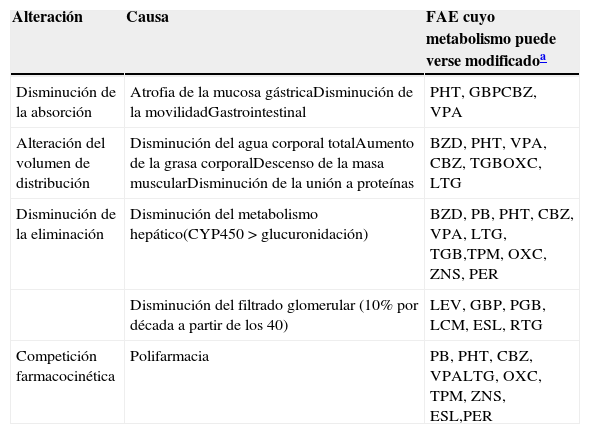
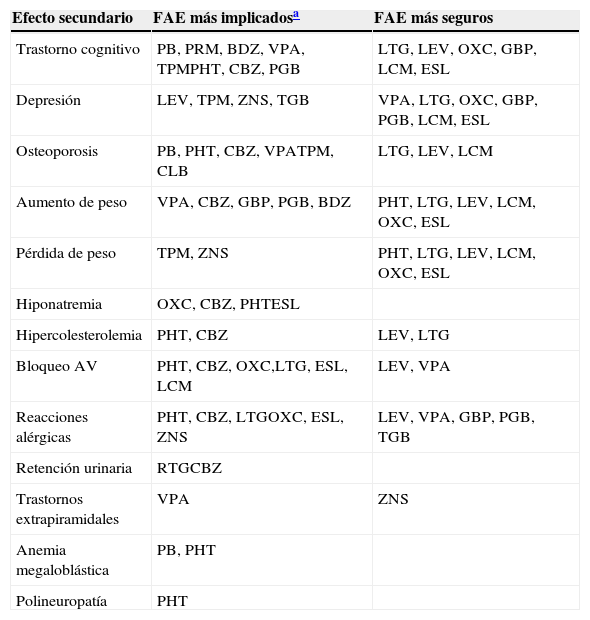
La tabla 5 recoge las principales modificaciones metabólicas y los FAE que se ven implicados. En la tabla 6 se recogen estos EA que consideramos de especial relevancia por las características de estos pacientes y los FAE más y menos implicados en su aparición
- –
Elección de FAE. Son escasos los estudios de FAE realizados en la población mayor de 65 años con evidencia alta. Se recogen en la literatura series de casos, opiniones y consensos de expertos en epilepsia21-26, NE IV. Los FAE recomendados por un perfil más favorable en el anciano serían el LEV, sin metabolismo hepático y posibilidad de interacciones, seguido de LTG, cuyo metabolismo hepático y su unión a proteínas aumentan ligeramente el riesgo de interacciones medicamentosas y de reacciones alérgicas graves, evitables con una titulación lenta27. La ZNS, tras demostrar su no inferioridad respecto a CBZ en el tratamiento de crisis parciales28, NE I, en una población amplia que incluyó a pacientes de hasta 75 años, ha obtenido la indicación en monoterapia en el tratamiento de la epilepsia.
Modificaciones farmacocinéticas en el anciano
| Alteración | Causa | FAE cuyo metabolismo puede verse modificadoa |
|---|---|---|
| Disminución de la absorción | Atrofia de la mucosa gástricaDisminución de la movilidadGastrointestinal | PHT, GBPCBZ, VPA |
| Alteración del volumen de distribución | Disminución del agua corporal totalAumento de la grasa corporalDescenso de la masa muscularDisminución de la unión a proteínas | BZD, PHT, VPA, CBZ, TGBOXC, LTG |
| Disminución de la eliminación | Disminución del metabolismo hepático(CYP450>glucuronidación) | BZD, PB, PHT, CBZ, VPA, LTG, TGB,TPM, OXC, ZNS, PER |
| Disminución del filtrado glomerular (10% por década a partir de los 40) | LEV, GBP, PGB, LCM, ESL, RTG | |
| Competición farmacocinética | Polifarmacia | PB, PHT, CBZ, VPALTG, OXC, TPM, ZNS, ESL,PER |
EA de especial relevancia en el anciano
| Efecto secundario | FAE más implicadosa | FAE más seguros |
|---|---|---|
| Trastorno cognitivo | PB, PRM, BDZ, VPA, TPMPHT, CBZ, PGB | LTG, LEV, OXC, GBP, LCM, ESL |
| Depresión | LEV, TPM, ZNS, TGB | VPA, LTG, OXC, GBP, PGB, LCM, ESL |
| Osteoporosis | PB, PHT, CBZ, VPATPM, CLB | LTG, LEV, LCM |
| Aumento de peso | VPA, CBZ, GBP, PGB, BDZ | PHT, LTG, LEV, LCM, OXC, ESL |
| Pérdida de peso | TPM, ZNS | PHT, LTG, LEV, LCM, OXC, ESL |
| Hiponatremia | OXC, CBZ, PHTESL | |
| Hipercolesterolemia | PHT, CBZ | LEV, LTG |
| Bloqueo AV | PHT, CBZ, OXC,LTG, ESL, LCM | LEV, VPA |
| Reacciones alérgicas | PHT, CBZ, LTGOXC, ESL, ZNS | LEV, VPA, GBP, PGB, TGB |
| Retención urinaria | RTGCBZ | |
| Trastornos extrapiramidales | VPA | ZNS |
| Anemia megaloblástica | PB, PHT | |
| Polineuropatía | PHT |
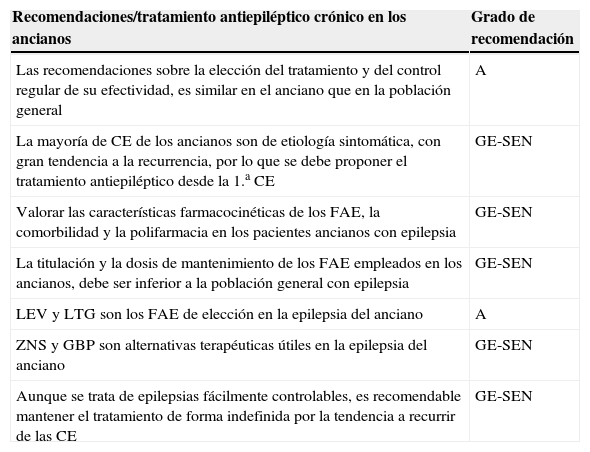
En la selección del tratamiento antiepiléptico, en especial en el anciano, va a ser muy importante la valoración de las comorbilidades asociadas, que nos orientarán en la elección de un determinado fármaco antiepiléptico (véase el grado de recomendaciones, posteriormente).
| Recomendaciones/tratamiento antiepiléptico crónico en los ancianos | Grado de recomendación |
|---|---|
| Las recomendaciones sobre la elección del tratamiento y del control regular de su efectividad, es similar en el anciano que en la población general | A |
| La mayoría de CE de los ancianos son de etiología sintomática, con gran tendencia a la recurrencia, por lo que se debe proponer el tratamiento antiepiléptico desde la 1.a CE | GE-SEN |
| Valorar las características farmacocinéticas de los FAE, la comorbilidad y la polifarmacia en los pacientes ancianos con epilepsia | GE-SEN |
| La titulación y la dosis de mantenimiento de los FAE empleados en los ancianos, debe ser inferior a la población general con epilepsia | GE-SEN |
| LEV y LTG son los FAE de elección en la epilepsia del anciano | A |
| ZNS y GBP son alternativas terapéuticas útiles en la epilepsia del anciano | GE-SEN |
| Aunque se trata de epilepsias fácilmente controlables, es recomendable mantener el tratamiento de forma indefinida por la tendencia a recurrir de las CE | GE-SEN |
| Recomendaciones/tratamiento de la epilepsia en pacientes ancianos con otras comorbilidades | Grado de recomendación |
|---|---|
| En pacientes con arritmias cardiacas, los FAE de elección por vía parenteral son: BZD, VPA y LEV, y deben evitarse PHT y LCM | GE-SEN |
| En pacientes con cardiopatía los FAE indicados son: GBP, LEV, LTG, TPM, VPA, ZNS | GE-SEN |
| En pacientes con insuficiencia respiratoria, deben evitarse por vía parenteral los FAE depresores respiratorios: barbitúricos y BZD. Su alternativa son: LEV, VPA y LCM | GE-SEN |
| En pacientes con osteopenia, hipercolesterolemia, e hipotiroidismo deben evitarse los FAE inductores enzimáticos | GE-SEN |
| En el tratamiento crónico de los pacientes con insuficiencia hepática los FAE más indicados son TPM, GBP, LEV, PGB, LCM. No se recomienda el uso de LTG, CBZ, VPA y PB | GE-SEN |
| Los FAE más recomendables en insuficiencia renal y en hemodiálisis son BZD, CBZ, PHT, VPA y LTG. No se recomienda el uso de VGB, GBP y PGB | GE-SEN |
| En pacientes con discapacidad mental y deterioro cognitivo son de elección: LTG, GBP, LEV, OXC, ESL, LCM | GE-SEN |
| Los FAE recomendados en los trastornos psiquiátricos son: BZD, CBZ, OXC, ESL, LCM, LTG y VPA | GE-SEN |
Los autores declaran no tener ningún conflicto de intereses.
Aparte de los autores de este capítulo, nuestro agradecimiento a todos los autores que colaboraron en la redacción de las Guías del Grupo de Epilepsia de la SEN: Maria Jose Aguilar-Amat Prior, Juan Alvarez-Linera Prado, Nuria Bargalló Alabart, Juan Luis Becerra Cuñat, Trinidad Blanco Hernández, Dulce Campos Blanco, Francisco Cañadillas Hidalgo, Mar Carreño Martínez, Carlos Casas Fernández, Antonio Donaire Pedraza, Irene Escudero Martínez, Merce Falip Centellas, Maria Isabel Forcadas Berdusan, Alberto Garcia Martínez, Irene Garcia Morales, Antonio Gil-Nagel Rein, José Luis Herranz Fernández, Vicente Ibañez Mora, Francisco Javier López González, Javier López-Trigo Pichó, Mercedes Martin Moro, Albert Molins Albanell, Maria Dolores Morales Martínez, Jaime Parra Gómez, Rodrigo Rocamora Zuñiga, Xiana Rodriguez Osorio, Juan Jesus Rodriguez Uranga, Miguel Rufo Campos, Rosa Ana Saiz Diaz, Xavier Salas-Puig, Juan Carlos Sánchez Alvarez, Jerónimo Sancho Rieger, Pedro Jesús Serrano Castro, Jose Serratosa Fernandez, Xabier Setoain Perego, Carlos Tejero Juste, Rafael Toledano Delgado, Manuel Toledo Argany, Francisco Villalobos Chaves, Vicente Villanueva Haba y César Viteri Torres.