Los síntomas de la esclerosis múltiple (EM) se asocian a un grado importante de discapacidad funcional progresiva y con un alto impacto en la calidad de vida (CV) de los pacientes. La CV y las actividades de la vida diaria son 2 áreas que presentan mayor modificación con el curso de la EM y, hasta hace poco, no se disponía de cuestionarios expresamente diseñados para cuantificarlos en pacientes con EM.
ObjetivoEvaluar la CV y la limitación de actividades del paciente con EM mediante cuestionario PRIMUS y discernir la posible relación entre CV, tiempo de evolución de la enfermedad y grado de discapacidad medida por EDSS.
Pacientes y métodosEstudio epidemiológico, transversal y multicéntrico, que incluyó a 261 pacientes con EM remitente recurrente (EMRR) o secundaria progresiva (EMSP) en tratamiento con interferón beta-1b durante al menos 6 meses. Se utilizó el cuestionario PRIMUS de calidad de vida validado para autoevaluar cambios en la CV y las actividades.
ResultadosLa edad media ± desviación estándar de los pacientes fue 41,7±10,3 años, siendo mujeres el 61,3%. La mayoría presentaba EMRR (83,9%) y el tiempo medio desde el diagnóstico fue de 7,6±5,8 años, resultando mayor en EMSP (6,9±5,2 vs. 11,2±7,4; p<0,0001). La discapacidad media según la EDSS fue 2,6±1,75 (EMSP 5,1±1,3 vs. EMRR 2,1±1,4; p<0,0001). El tiempo medio desde inicio del tratamiento fue 5,5±3,8 años. El componente de CV es superior en EMRR: 18,3±6,8 vs. 9,9±7,1 (p<0,0001), disminuyendo a medida que avanza el tiempo desde diagnóstico (p<0,01) y con la discapacidad del paciente (entre 18,8±6,6 en estadios iniciales [EDSS<3,5] hasta 8,4±6,3 en avanzados [EDSS>5], p<0,0001). El componente de actividades PRIMUS sigue el mismo patrón, aumentando la inactividad con el tiempo transcurrido desde diagnóstico p<0,0001) y con la discapacidad acumulada (p<0,0001).
ConclusionesLa CV del paciente con EM en tratamiento varía según tipología de la enfermedad y empeora progresivamente con la discapacidad y el tiempo. El cuestionario PRIMUS es una herramienta adecuada para la evaluación de la CV y la actividad en pacientes con EM.
Symptoms of multiple sclerosis (MS) are associated with significant and progressive functional disability and have a profound impact on patients’ quality of life (QoL). QoL and daily life activities are two areas that suffer major changes during the course of MS and there are currently no questionnaires specifically designed to evaluate these areas in MS patients.
PurposeTo evaluate QoL of MS patients using the PRIMUS questionnaire and determine the possible relationship between QoL, duration of disease, and disability measured on the EDSS.
Patients and methodsMulti-centre epidemiological and cross-sectional study including 261 patients with relapsing remitting MS (RRMS) or secondary progressive MS (SPMS) treated with interferon beta-1b for at least 6 months. The validated version of the PRIMUS questionnaire was used for patient reporting of changes in QoL and life activities.
ResultsMean age of patients was 41.7±10.3 years; 61.3% were women. Most had RRMS (83.9%). Mean time since MS diagnosis was 7.6±5.8 years, and longer in the SPMS group (11.2±7.4 vs 6.9±5.2, P<.0001). Mean EDSS score was 2.6±1.75 (5.1±1.3 in SPMS vs 2.1±1.4 in RRMS, P<.0001). Mean time since start of treatment was 5.5±3.8 years. The PRIMUS QoL component was higher in the RRMS group: 18.3±6.8 vs 9.9±7.1 (P<.0001); it also decreased with increases in both time since diagnosis (P<.01) and disability scores (from 18.8±6.6 in early stages [EDSS<3.5] to 8.4±6.3 in advanced stages [EDSS>5], P<.0001). The PRIMUS activity limitations component followed the same pattern: activity became more limited with increases in time since diagnosis (P<.0001) and overall disability (P<.0001).
ConclusionsQoL in MS patients varies according to the disease type, and it worsens progressively over time and with increasing disability. The PRIMUS questionnaire is a good tool for assessing QoL and activity in patients with MS.
La esclerosis múltiple (EM) es la causa más frecuente de discapacidad neurológica no traumática en adultos jóvenes, afectando a casi 400.000 personas en Europa y suponiendo un coste socioeconómico asociado de entre 8.800 y 12.500 millones de euros anuales en Europa1. La EM es una enfermedad inflamatoria y desmielinizante del sistema nervioso central de origen autoinmunitario y caracterizada por episodios repetidos de inflamación (recurrencias), seguidos por períodos de recuperación completa o incompleta (remisiones). Si la recuperación de las recurrencias es incompleta, la destrucción de la capa de mielina y el daño axonal provocan muchos de los síntomas progresivos e irreversibles de la EM.
Existen 3 formas principales de EM: remitente-recurrente (EMRR), secundaria progresiva (EMSP) y primaria progresiva (EMPP). El 85% de los pacientes presenta EMRR al inicio de la enfermedad y, en un plazo de unos 10 años, el 50% de ellos progresa hacia EMSP2. Los interferones beta, fármacos «modificadores de la enfermedad», constituyen en la actualidad el tratamiento estándar de la EM. Estos fármacos han demostrado su eficacia y seguridad, aunque presentan a medio plazo ciertos problemas de tolerabilidad y aceptación por parte de los pacientes debido, esencialmente, a su forma de administración. Además, estos esquemas de tratamiento suelen repercutir en la calidad de vida (CV) del paciente.
Los síntomas de la EM implican un grado importante de discapacidad progresiva e irreversible y, dado que habitualmente se diagnostica durante la juventud, determinan una repercusión física y psicológica considerable, afectando de forma importante a la CV tanto de los pacientes como de los familiares. La mayor parte de los pacientes vivirán más de la mitad de sus vidas con la enfermedad. Diversos estudios han evaluado la relación de la EM con la CV y, de hecho, existen varias escalas generales publicadas y validadas para medir la CV en estos pacientes3-7. La mayor parte de estas escalas, a pesar de estar validadas para su utilización en este grupo de pacientes, no han sido diseñadas específicamente para pacientes con EM. Una de las escalas más utilizadas y considerada de referencia en la EM es la Expanded Disability Status Scale (EDSS), especialmente diseñada para clasificar al paciente según su estado de discapacidad, pero que no evalúa la CV.
Cada vez son más utilizadas las escalas de valoración autoaplicada para el cuidado de los pacientes y la evaluación de condiciones de salud crónicas. Algunas de estas escalas, como la PRIMUS (Patient reported outcome indices for multiple sclerosis), se utilizan en la EM para evaluar aspectos de la CV relacionados con situaciones propias de la enfermedad, como las recaídas4,8, y tienen valor como predictores del curso de la enfermedad9, así como de la evolución del coste socioeconómico asociado10. La escala de autoevaluación PRIMUS ha sido especialmente diseñada para cubrir los aspectos de CV y nivel de actividad, 2 de los aspectos que experimentan mayor modificación con el curso de la EM, y ha sido validada en castellano en nuestro país11.
A pesar de la demanda generalizada de una escala específica que evalúe estos aspectos (CV y actividades) en población con EM, la escala PRIMUS es aún poco conocida entre los neurólogos españoles. El presente estudio pretende difundir las escalas de CV y actividades del PRIMUS entre los especialistas españoles que tratan esta afección, evaluando la CV en pacientes españoles con EM, y detectar si existe relación entre la CV, el tiempo de evolución y la discapacidad según la EDSS.
Pacientes y métodosEstudio epidemiológico, transversal, multicéntrico y de ámbito nacional, que incluyó a un total de 261 pacientes con EMRR o EMSP que acudieron a visita de rutina del neurólogo y que dieron su consentimiento informado por escrito para participar en el estudio. Los pacientes fueron incluidos en el estudio durante un período de 7 meses, según criterio de muestreo consecutivo, y para ser elegidos debían haber estado en tratamiento con interferón beta-1b durante un mínimo de 6 meses antes de la visita de inclusión. El protocolo del estudio fue sometido a evaluación independiente por parte de un comité ético de investigación clínica (CEIC del Hospital Universitario Nuestra Señora de Candelaria de Santa Cruz de Tenerife).
Se utilizaron los índices comunicados por el paciente en EM (cuestionario PRIMUS) validados para autoevaluar cambios en las subescalas de CV y de actividades. El componente de CV de PRIMUS se obtiene a partir de una medición basada en las necesidades del propio paciente, enfoque que mantiene que la CV personal es mayor en función de la capacidad individual para satisfacer las propias necesidades básicas. Esta subescala del cuestionario PRIMUS tiene una puntuación que oscila entre un mínimo de 0 y un máximo de 22 puntos. El componente de actividades del PRIMUS se obtuvo de las afirmaciones de los pacientes respecto de las maneras en que la EM afecta a sus actividades diarias básicas y se mide en una escala que va entre los 0 y los 38 puntos.
Complementariamente, se recogió el último valor disponible de la EDSS y su fecha, según condiciones asistenciales de práctica clínica habitual. También se detallaron los valores de la escala EuroQol que mide la CV en población general, clasificada según 5 dimensiones: movilidad, cuidado personal, actividades cotidianas, dolor/malestar y ansiedad/depresión. Cada dimensión puede tomar los valores 1 (indicando ausencia de problemas), 2 (indicando algunos problemas) y 3 (indicando muchos problemas). El rango de valores de la puntuación total EuroQol fue de 5 a 15, estando los valores más altos relacionados con un peor estado de salud. Además, se complementaron las variables recogidas con la autovaloración del estado de la salud, de 0 a 100, mediante escala visual analógica (EVA).
Con el objetivo de calcular la posible relación existente entre la subescala de CV del PRIMUS, la escala de CV del cuestionario EuroQol y la EVA sobre el estado de salud, se realizaron los correspondientes coeficientes de correlación de Spearman para su análisis posterior.
ResultadosCaracterísticas de la poblaciónSe reclutó a un total de 319 pacientes con EM, de los cuales 261 (81,8%) cumplieron todos los criterios de selección del estudio y cumplimentaron correctamente las subescalas estudiadas del cuestionario PRIMUS (actividades y CV). Los motivos principales de exclusión fueron: incumplimiento del diagnóstico de EMRR o EMSP en tratamiento con interferón beta-1b durante al menos los últimos 6 meses (13,8%) y no tener la escala de CV de vida del cuestionario PRIMUS contestada adecuadamente (19,0%).
La edad media ± desviación estándar de la población incluida fue de 41,7±10,3 años, siendo pacientes femeninos el 61,3% de los casos incluidos. La mayoría de los pacientes presentaban EMRR (83,9%) y el tiempo medio desde la primera manifestación detectada de la enfermedad se cuantificó en 9,7±7,7 años. El tiempo medio transcurrido desde el diagnóstico de la enfermedad fue de 7,6±5,8 años, siendo este período mayor en pacientes con EMSP que en los que presentaban EMRR (6,9±5,2 vs. 11,2±7,4, p<0,0001). La discapacidad media evaluada según la EDSS fue de 2,6±1,75, siendo esta casi 4 veces superior entre pacientes con EMSP frente a EMRR (5,1±1,3 vs. 2,1±1,4; p<0,0001).
Descriptiva del tratamiento para la esclerosis múltipleEl tiempo medio descrito desde el inicio oficial del tratamiento con fármacos modificadores de la enfermedad fue de 5,5±3,8 años. El interferón beta-1b fue el fármaco más frecuente entre los pacientes españoles con EM (87,9%), seguido del acetato de glatirámero (6,4%) y el natalizumab (3,0%). Además, el interferón beta-1b fue también el tratamiento más frecuente como primera opción terapéutica al iniciar tratamiento para la EM (en el 95,4% de los casos).
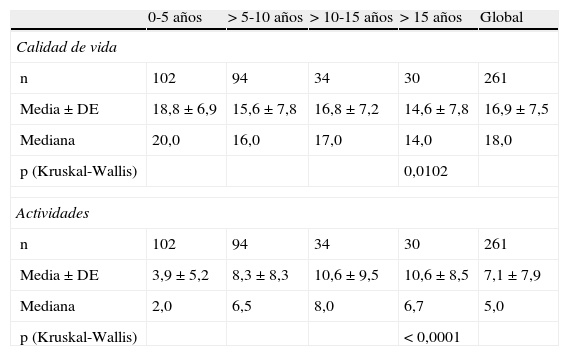
Evolución de la calidad de vidaLos componentes evaluados en el cuestionario PRIMUS fueron analizados según el tiempo transcurrido desde el diagnóstico inicial de la EM. En la tabla 1 se muestra el componente de CV medio (escala 0-22) para la población española con EM, que fue de 16,9±7,5, mientras que el componente de actividades alcanzó una media de 7,1±7,9. Tanto la CV del paciente como el nivel de actividades disminuyen a medida que aumenta el tiempo desde el diagnóstico de la enfermedad. Así, en el caso específico de la CV, que muestra puntuaciones mayores asociadas a un mejor nivel de calidad, esta puntuación oscila entre una media de 18,8±6,9 para los primeros años tras el diagnóstico hasta una puntuación media mínima de 14,6±7,8 cuando han transcurrido más de 15 años desde el diagnóstico inicial de EM (p<0,05).
Componentes del cuestionario PRIMUS según el tiempo transcurrido desde el diagnóstico de EM
| 0-5 años | >5-10 años | >10-15 años | >15 años | Global | |
| Calidad de vida | |||||
| n | 102 | 94 | 34 | 30 | 261 |
| Media±DE | 18,8±6,9 | 15,6±7,8 | 16,8±7,2 | 14,6±7,8 | 16,9±7,5 |
| Mediana | 20,0 | 16,0 | 17,0 | 14,0 | 18,0 |
| p (Kruskal-Wallis) | 0,0102 | ||||
| Actividades | |||||
| n | 102 | 94 | 34 | 30 | 261 |
| Media±DE | 3,9±5,2 | 8,3±8,3 | 10,6±9,5 | 10,6±8,5 | 7,1±7,9 |
| Mediana | 2,0 | 6,5 | 8,0 | 6,7 | 5,0 |
| p (Kruskal-Wallis) | < 0,0001 | ||||
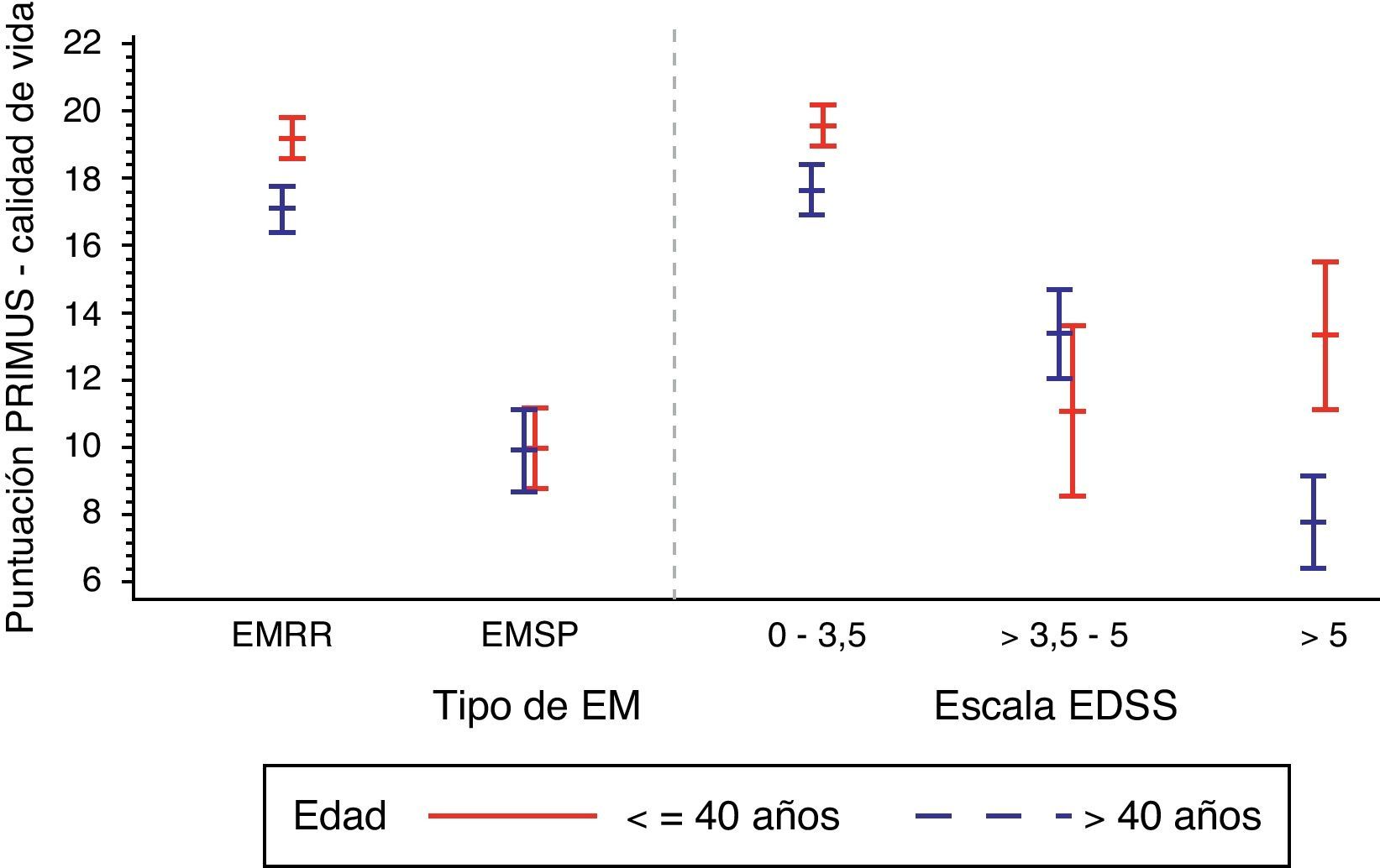
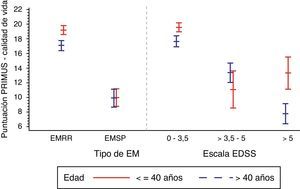
Se aprecia, además, una aparente influencia de la edad del paciente en el componente de CV del PRIMUS, que fue además superior en la EMRR respecto de la EMSP: 18,3±6,8 vs. 9,9±7,1 (p<0,0001), siendo este mayor en pacientes menores de 40 años con EMRR (fig. 1).
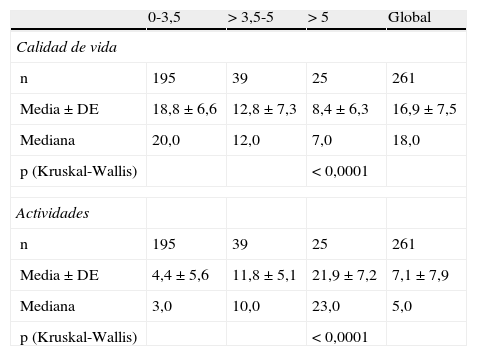
En la tabla 2 se observa que la CV medida con cuestionario PRIMUS disminuyó en relación con el avance del grado de discapacidad del paciente (entre 18,8±6,6 en los estadios iniciales de la enfermedad [EDSS<3,5] y 8,4±6,3 en los niveles más avanzados de discapacidad [EDSS>5], p<0,0001) (fig. 1).
Componentes del cuestionario PRIMUS según la EDSS de discapacidad
| 0-3,5 | >3,5-5 | >5 | Global | |
| Calidad de vida | ||||
| n | 195 | 39 | 25 | 261 |
| Media±DE | 18,8±6,6 | 12,8±7,3 | 8,4±6,3 | 16,9±7,5 |
| Mediana | 20,0 | 12,0 | 7,0 | 18,0 |
| p (Kruskal-Wallis) | < 0,0001 | |||
| Actividades | ||||
| n | 195 | 39 | 25 | 261 |
| Media±DE | 4,4±5,6 | 11,8±5,1 | 21,9±7,2 | 7,1±7,9 |
| Mediana | 3,0 | 10,0 | 23,0 | 5,0 |
| p (Kruskal-Wallis) | < 0,0001 | |||
Puntuaciones bajas en la subescala de actividades se muestran asociadas a menores niveles de limitación de actividades. En la tabla 1 se puede observar cómo la puntuación obtenida en la escala de actividades PRIMUS aumenta progresivamente con el tiempo transcurrido desde el diagnóstico de la EM (entre 3,9±5,2 para pacientes con menos de 5 años de diagnóstico hasta 10,6±8,5 en pacientes con más de 15 años transcurridos desde el diagnóstico; p<0,0001), indicando un deterioro progresivo y significativo de la funcionalidad del paciente relacionado la duración de la enfermedad.
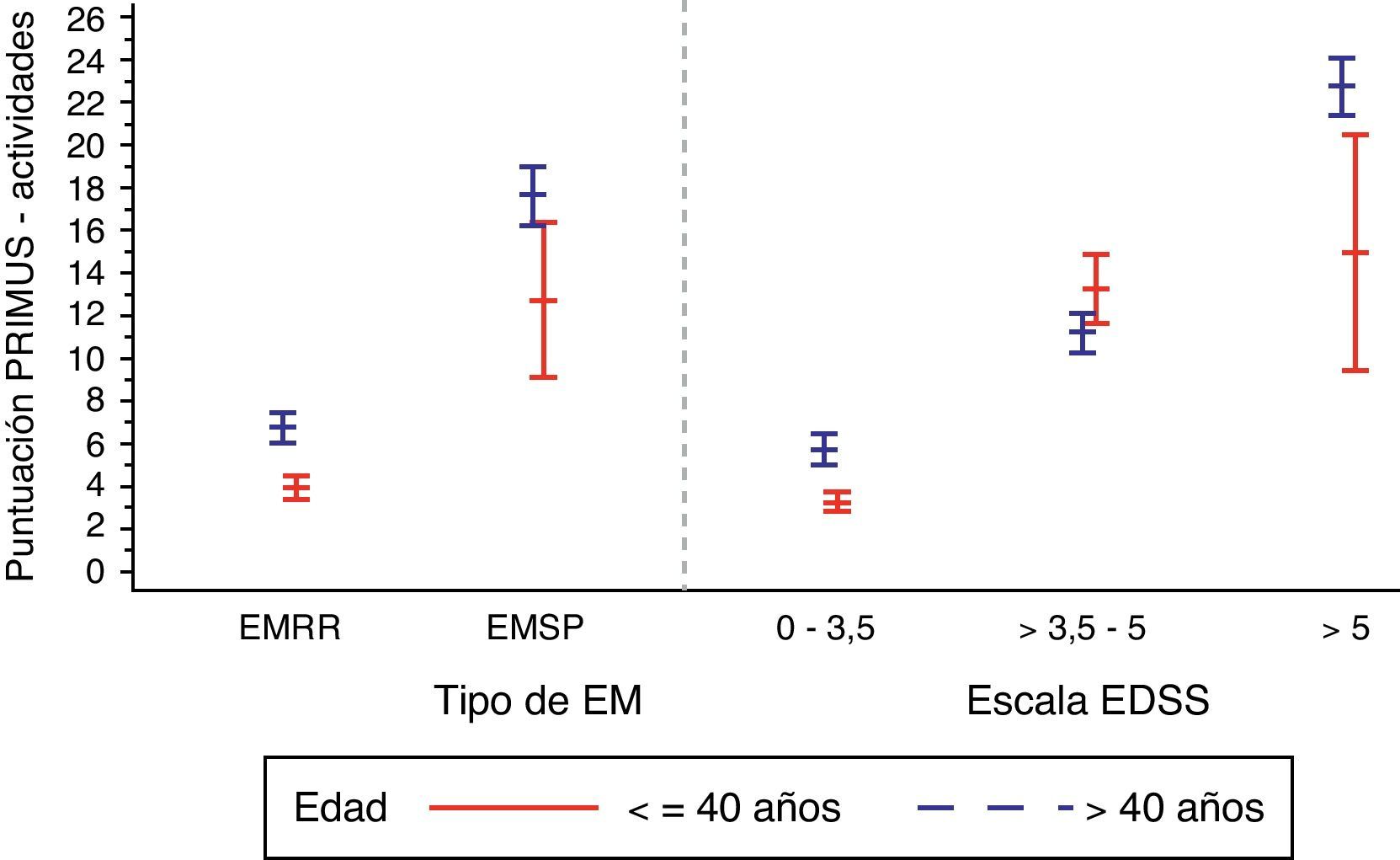
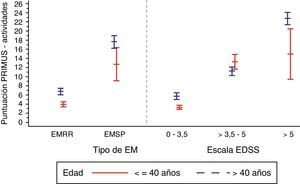
Cuando se analizó el efecto de la puntuación en la EDSS asociada al grado de discapacidad (tabla 2), se apreció una tendencia similar a la observada con la duración: valores de entre 4,4±5,6 en pacientes con < 3,5 puntos en la EDSS hasta 21,9±7,2 en pacientes con más de 5 puntos en la EDSS (p<0,0001). Además, en los pacientes mayores de 40 años, se observó un incremento en la puntuación de actividades del cuestionario PRIMUS a medida que la puntuación en la EDSS aumentaba, evidenciando una mayor dificultad para completar actividades diarias a medida que aumentan la discapacidad y la edad del paciente (fig. 2). En los pacientes menores de 40 años, dicho aumento se presenta solo para el rango de EDSS entre 0 y 5.
Los pacientes con EMRR tuvieron generalmente menores puntuaciones en la escala de actividades PRIMUS respecto de los pacientes con EMSP, evidenciando una menor limitación física en el primer estadio de la enfermedad (5,2±6,3 vs. 17,1±8,4; p<0,0001).
Escala EuroQol y escala autoevaluada de salud general (escala visual analógica)Dentro de las actividades diarias, la escala EuroQol permite detallar diferencias en la evolución de diferentes aspectos de estas actividades (tabla 3). Así, por ejemplo, en el ámbito de la «movilidad», se observó que el 51,0% de los pacientes referían algunos problemas para caminar, con un 90,5% entre los pacientes con EMSP y un 43,4% en los pacientes con EMRR (p<0,0001).
Componentes del cuestionario PRIMUS según la EDSS de discapacidad
| Puntuación EDSS | Tipo EM | Total (n=261) | |||||
| 0-3,5 (n=195) | >3,5-5 (n=39) | >5 (n=25) | ND (n=2) | Remitente recurrente (n=219) | Secundaria progresiva (n=42) | ||
| Puntuación EuroQol | |||||||
| n | 194 | 39 | 24 | 2 | 218 | 41 | 259 |
| Media±DE | 6,6±1,6 | 8,8±1,4 | 9,9±1,5 | 6,0±1,4 | 6,9±1,7 | 9,4±1,5 | 7,3±1,9 |
| p | < 0,0001 | < 0,0001 | |||||
| Autovaloración salud (EVA) | |||||||
| n | 189 | 38 | 24 | 2 | 213 | 40 | 253 |
| Media±DE | 74,0±15,0 | 51,7±14,6 | 47,3±14,0 | 70,0±28,3 | 71,7±16,7 | 48,8±12,5 | 68,1±18,1 |
| p | < 0,0001 | < 0,0001 | |||||
| Estado general de salud | |||||||
| Mejor | 22,05% | 15,38% | 20,00% | 0,00% | 21,92% | 14,29% | 20,69% |
| Igual | 64,10% | 41,03% | 44,00% | 100,00% | 62,10% | 42,86% | 59,00% |
| Peor | 13,33% | 43,59% | 28,00% | 0,00% | 15,07% | 40,48% | 19,16% |
Otro aspecto con diferencias destacadas fue el relativo a actividades de «cuidado personal», aspecto para el que el 73,2% de los pacientes no informaron de problema alguno. Sin embargo, se apreció una evidente diferencia en este ámbito respecto de la tipología de la enfermedad: los pacientes con EMSP reportaron problemas para la limpieza diaria en un 57,1% de los casos y el 28,6% no reportó problemas relacionados con el cuidado personal. Por el contrario, el 81,7% de los pacientes con EMRR respondieron no tener ningún problema con el cuidado personal y únicamente un 15,5% tenía problemas para la higiene diaria (p<0,0001).
Los pacientes con EMSP presentaron una mayor puntuación global de la escala EuroQol (equivalente a un menor grado de CV), en comparación con los pacientes con EMRR (9,4±1,5 vs. 6,9±1,7; p <0,0001). De modo similar, la escala de autoevaluación de la salud (EVA) reportó diferencias significativas entre tipologías de enfermedad (71,7±16,7 en EMRR vs. 48,8±12,5 en EMSP; p<0,0001).
Se puede apreciar que el tiempo transcurrido desde el diagnóstico ejerció una influencia significativa en las escalas medidas: aumentando progresivamente la puntuación del cuestionario EuroQol (p=0,0003) y disminuyendo el valor de la escala EVA (p=0,0002) a medida que aumentaba el tiempo desde el diagnóstico original de EM. El estadio EDSS es otro de los factores que determinan una alta influencia en las puntuaciones hacia peor nivel de actividad diaria y de estado de salud autoevaluado (EuroQol p<0,0001 y EVA p<0,0001).
Relación entre escalasLa asociación entre subescala de CV del PRIMUS y el cuestionario EuroQol fue alta pero de signo negativo (correlación de Spearman: –0,7869), indicando que las puntuaciones más altas en EuroQol implican un mayor deterioro del paciente, mientras que este deterioro está indicado por las puntuaciones bajas en la subescala de CV del PRIMUS. A su vez, la correlación entre la escala de CV del PRIMUS y la puntuación de la escala EVA fue fuerte y positiva (correlación de Spearman: 0,7272), un indicativo de que las puntuaciones altas en ambos indicadores muestran un empeoramiento general en la CV global.
En cuanto a la relación de la escala de actividades PRIMUS y el cuestionario EuroQol, se pudo evidenciar una buena correlación positiva entre ambos (correlación de Spearman: 0,8179), mientras que entre actividades del PRIMUS y la EVA la correlación fue alta pero de signo negativo (correlación de Spearman: –0,7571).
DiscusiónLas enfermedades crónicas como la EM presentan una serie de importantes dilemas a la hora de evaluar adecuadamente las medidas autorreportadas de evolución y progresión de la enfermedad, básicamente como consecuencia de la falta de escalas específicamente diseñadas para tal efecto10. Complementariamente, la rápida evolución de las terapias inmunomoduladoras para la EM en los últimos años hace de vital importancia un seguimiento efectivo del curso de los síntomas en una enfermedad que tradicionalmente implicaba un rápido deterioro de la calidad de vida de los pacientes y la consiguiente elevada carga social y familiar asociada12.
El desarrollo de escalas de autoevaluación específicamente diseñadas para valorar el curso de la EM en pacientes tratados con terapias modificadoras de la enfermedad debería permitir tutelar el curso efectivo de la enfermedad y las necesidades de control de la sintomatología en los nuevos pacientes. Entre estas herramientas de diseño reciente, cabe destacar el papel que pueden representar los índices PRIMUS a la hora de cuantificar adecuadamente la sintomatología, la CV del paciente y sus limitaciones de actividad10,13.
Este trabajo ha consistido en el desarrollo de un estudio observacional, transversal y multicéntrico, con el propósito de evaluar la CV y el nivel de actividad de los pacientes españoles con EM mediante el cuestionario PRIMUS. Como objetivo secundario, se ha pretendido evaluar la validez de la escala PRIMUS a la hora de monitorizar la evolución de la enfermedad en pacientes españoles con EM. Este propósito se ha alcanzado mediante el análisis de la relación exacta entre la subescala de CV del índice PRIMUS, el cuestionario EuroQol que valora CV y la escala visual aplicada sobre el estado de salud general percibido por el paciente.
Entre los principales resultados obtenidos, cabe destacar la elevada influencia que el tiempo transcurrido desde el diagnóstico de EM y la discapacidad asociada ejercen en el empeoramiento de la CV del paciente medida a partir de los índices PRIMUS. Este resultado estaría de acuerdo con resultados obtenidos en otros países del ámbito europeo14-16 y directamente relacionado con la evidencia acumulada recientemente a favor de la necesidad de un inicio temprano del tratamiento, que consiga bloquear primariamente el progreso de la enfermedad y contener los costes sociales y personales que se asocian a la creciente discapacidad y al peor estado de salud del paciente17-20.
En relación con la observación previa, la CV evaluada mediante el cuestionario PRIMUS también se ve afectada por la tipología de la enfermedad, siendo claramente peor en pacientes con EMSP que en pacientes con EMRR. Este hecho depende, en buena medida, de que el curso avanzado de la EM suele conducir a las tipologías EMSP que, en consecuencia, están asociadas a mayor tiempo transcurrido desde el diagnóstico y a un mayor nivel de discapacidad general21.
Junto con la escala de CV del índice PRIMUS, el presente trabajo también evaluó los cambios en la escala de actividades y su variación en relación con las principales variables clínicas de los pacientes españoles con EM. Como en el caso de la CV, las limitaciones en las actividades del paciente aumentan en relación directa con la gravedad de la discapacidad (puntuación EDSS), así como con el tiempo transcurrido desde el diagnóstico. Estos resultados están en concordancia con estudios previos que utilizaron la escala PRIMUS22, pero por primera vez han podido confirmarse específicamente para la población española con EM.
Del mismo modo, cabe resaltar que, por primera vez, se han correlacionado las características sociodemográficas de los pacientes españoles con EM —como la edad— con las subescalas PRIMUS de CV y de limitación de actividades. Estas evaluaciones únicamente se habían confirmado en estudios previos con escalas anteriormente utilizadas, como sería el caso de los cuestionarios Musi-QoL23,24, EuroQol25, FAMS26 y SF-366. Por lo tanto, el presente estudio ha conseguido cubrir ese vacío previo existente para una nueva escala de medida de la afectación de la CV y de las actividades que se ha diseñado expresamente para ser aplicada a pacientes con EM tratados con los nuevos fármacos modificadores de la enfermedad.
Nuestro estudio también ha permitido constatar que otras escalas utilizadas previamente, como el EuroQol o la escala visual autoevaluada de salud, se ven influidas por los mismos parámetros clínicos: el tiempo transcurrido desde el diagnóstico de EM, el estadio EDSS de discapacidad y la tipología de EM presentada por el paciente, 3 parámetros que, a su vez, están determinando el grado de deterioro de la salud del paciente.
Los nuevos tratamientos y el inicio temprano de los mismos hacen que el paciente tarde más en experimentar el progreso de la discapacidad. Así mismo, el hecho de disponer de herramientas de medida objetivas para evaluar adecuadamente la evolución de la discapacidad y la CV en estos pacientes son factores clave que permiten conocer mejor la fisiopatología de la EM27,28.
En trabajos publicados anteriormente, y en relación con la medición de la eficacia de los tratamientos, se han considerado tanto la CV como la funcionalidad del paciente con EM como variables de peso29. Hasta la actualidad, los cuestionarios de CV utilizados en EM solían ser escalas genéricas o adaptadas secundariamente a la enfermedad. El cuestionario PRIMUS desarrollado específicamente para la EM, y especialmente sus subescalas de discapacidad y CV, permite obtener la información clínica y funcional más útil para interpretar adecuadamente la evolución de la CV y su relación con los tratamientos prescritos13. La validez de los índices PRIMUS ha sido evidenciada en los estudios para su validación en EM y en sus diferentes versiones traducidas y adaptadas10,13. En el presente trabajo se ha demostrado su correlación en pacientes españoles con otro tipo de escalas utilizadas en EM, tanto de CV (EuroQol) y de sus componentes, como con la escala visual de autovaloración del estado de salud del paciente.
El presente trabajo presenta algunas limitaciones, como podría ser su diseño transversal, factor que no facilita la detección de variaciones estacionales o asociadas específicamente al curso de los tratamientos más recientes. Aun así, también cuenta con algunos puntos positivos que apoyan sus conclusiones, como podrían ser la homogeneidad geográfica de la muestra de pacientes utilizada y el considerable tamaño de la misma.
En conjunto, los resultados de nuestro estudio permiten asegurar que la CV de los pacientes españoles con EM en tratamiento actual con interferón beta-1b y evaluada mediante cuestionario PRIMUS varía según la tipología de la enfermedad y empeora progresivamente con la discapacidad acumulada y el tiempo transcurrido desde el diagnóstico. Finalmente, se han aportado argumentos clarificadores que evidencian la realidad de los índices PRIMUS como una buena herramienta para la evaluación de los componentes de la CV y de las actividades de la vida diaria en pacientes actuales con EM.
FinanciaciónEste estudio ha recibido financiación de Novartis Farmacéutica, S.A. para su realización.
Conflicto de interesesSheila Mora es empleada de Novartis Farmacéutica; y S.A. Miguel Ángel Hernández declara no tener ningún conflicto de intereses.
Agradecemos la participación activa de los investigadores del grupo de trabajo del Estudio SLIMS.
Agradecemos la colaboración en la elaboración del presente manuscrito de Emili González-Pérez, del Departamento Científico de Trial Form Support, España.
Lorena García (Hospital Clínico de Zaragoza); Gerard Soriano, Marina Bufanda, Francisco Lacruz y Teresa Ayuso (Hospital de Navarra); María José Sedano (Hospital Marqués de Valdecilla); Domingo Pérez (Hospital El Bierzo); Sergio Merino (C. Asistencial Palencia); Miguel Ángel Llaneza (C. Arquitecto Marcide); José Ramón Lorenzo (Hospital Povisa); Elvira Muntéis (Hospital del Mar); Miguel Marco (Hospital de Sabadell); Cristina Montero (F. Salut Empordà); Ana Belén Caminero (Hospital Nuestra Señora de Sonsoles); Inmaculada García (Hospital de Fuenlabrada); Inmaculada Pérez y María Rosa García (Hospital Virgen de la Salud); Octavio Sánchez (Hospital Nuestra Señora del Prado); Virginia Meca (Hospital de la Princesa); Antonio Yusta (Hospital Universitario Guadalajara); Josefina Martínez (Hospital Torrecárdenas); Francisco Padilla (Hospital Virgen de la Victoria); Francisco Barrero (Hospital San Cecilio); Esther Cancho (A. de Especialidades Don Benito); Laura Lacruz (Hospital Francesc de Borja); Antonio Belenguer (Hospital General de Castellón); José Meca y Rocío Hernández (Hospital Virgen de Arrixaca); José Antonio Pérez (Hospital Universitario Santa Maria del Rosell); Cristina Croissier (Hospital Universitario de Canarias); Claudia Villar (Hospital Virgen de la Candelaria); Laura Gubieras (Hospital Moisés Broggi); Antonio Cano (Hospital de Mataró).