En epilepsia farmacorresistente el incremento asociado de la morbimortalidad y el deterioro de calidad de vida hace necesario el ingreso en Unidades de Monitorización de Epilepsia (UME). En dichas Unidades se practican técnicas que facilitan la aparición de crisis epilépticas, implicando un riesgo de aparición de fenómenos adversos secundarios. El objetivo de nuestro estudio es caracterizar y cuantificar dichos fenómenos adversos en una UME en España.
Materiales y métodosEstudio descriptivo, longitudinal y retrospectivo de pacientes consecutivos ingresados en nuestra UME. Se excluyó a los pacientes que ingresaron por motivo de status epilepticus, serie de crisis o ensayo clínico.
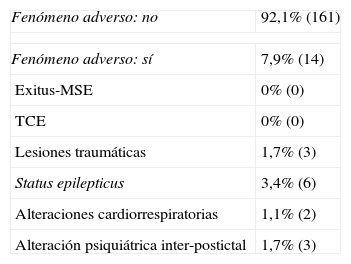
ResultadosSe incluyeron 175 pacientes. Un 92,1% (161) de los pacientes no presentó ningún fenómeno adverso. Un 3,4% (6) presentó status epilepticus, un 1,7% (3) presentó lesión traumática, un 1,7% (3) presentó alteración psiquiátrica inter-postictal, un 1,1% (2) presentó alteración cardiorrespiratoria de riesgo. No se detectaron factores de riesgo asociados a dichos fenómenos adversos.
ConclusionesLos fenómenos adversos detectados con mayor frecuencia fueron el status epilepticus, lesiones traumáticas, alteraciones psiquiátricas inter-postictales y alteraciones cardiorrespiratorias. La frecuencia de aparición de dichos fenómenos adversos fue similar al de series internacionales. Las complicaciones detectadas no contraindican la MVEEG.
The increased morbidity and mortality and poorer quality of life associated with drug-resistant epilepsy justify admitting patients to epilepsy monitoring units (EMU). These units employ methods that promote the occurrence of seizures, which involves a risk of secondary adverse events. The aim of our study is to characterise and quantify these adverse events in a Spanish EMU.
Materials and methodsA descriptive, longitudinal and retrospective study of patients admitted consecutively to our EMU. Patients admitted due to status epilepticus, clusters of seizures, or as participants in a clinical trial were excluded.
ResultsWe included 175 patients, of whom 92.1% (161) did not suffer any adverse events. Status epilepticus was present in 3.4% (6); 1.7% (3) had traumatic injury, 1.7% (3) had interictal or postictal psychosis, and 1.1% (2) had cardiorespiratory impairment. There were no risk factors associated with these adverse events.
ConclusionsThe most frequently-identified adverse events were status epilepticus, traumatic injury, interictal or postictal psychosis, and cardiorespiratory disorders. The frequency of these adverse events was similar to that seen in international literature. The complications detected do not contraindicate VEEGM.
En el diagnóstico y tratamiento de los pacientes epilépticos aproximadamente un tercio de los pacientes son resistentes al tratamiento farmacológico1. La mortalidad de estos pacientes es 2-3 veces superior a la de la población general2,3.
La reducción en la expectativa de vida4 y las complicaciones de estos pacientes: muerte súbita en epilepsia (MSE)5, status epilepticus, accidentes y suicidios justifican el ingreso en Unidad de Monitorización de Epilepsia (UME). El ingreso en una UME es fundamental en el diagnóstico prequirúrgico y diferencial de los pacientes con epilepsia farmacorresistente6,7. En dichas unidades se practican sistemáticamente técnicas orientadas a la facilitación de la aparición de crisis. Por tanto, se hace más probable la aparición de fenómenos adversos secundarios a crisis8–10.
En estudios recientes la frecuencia de aparición de fenómenos adversos fue del 11%, siendo los más frecuentemente observados las alteraciones psiquiátricas postictales (1,3-3,9%), las lesiones traumáticas (2,75-2,95%), el status epilepticus (0,67-1,97%) y las alteraciones vegetativas de riesgo (2%)11,12.
Los objetivos de nuestro estudio son: caracterizar los fenómenos adversos secundarios a crisis durante la monitorización por vídeo-electroencefalograma (MVEEG), determinar aquellos pacientes con mayor riesgo de presentar alguno de dichos fenómenos adversos y determinar qué procedimientos se asocian a un mayor riesgo. Hasta donde sabemos este es el primer estudio de seguridad en MVEEG en la literatura española y puede ser relevante para determinar estándares y modelos de actuación.
Materiales y métodosEstudio descriptivo, longitudinal y retrospectivo en el que se ha analizado la historia clínica y los registros en UME de todos los pacientes ingresados de manera consecutiva en nuestra UME entre diciembre de 2009 y julio de 2012 (31 meses). Los criterios de inclusión fueron: ingreso programado en UME para diagnóstico prequirúrgico o diagnóstico diferencial. Los criterios de exclusión fueron monitorizaciones por vídeo-EEG por causa de status, serie de crisis o estudios clínicos. Se documentaron los sucesos acontecidos durante el ingreso y se analizaron los fenómenos de interés secundarios a crisis con respecto a la integridad física durante la MVEEG. Los principales fenómenos a valorar fueron: exitus, MSE, lesiones traumáticas secundarias a crisis, status epilepticus (SE), alteraciones cardiorrespiratorias de riesgo y alteraciones psiquiátricas inter o postictales.La indicación de MVEEG fue realizada por un equipo especialista en epilepsia.
Los pacientes provenían de CCEE de nuestro centro o de otros centros de Cataluña o España. La MVEEG tuvo una duración de 5 días, la cual fue modificada en función de las necesidades de cada paciente.
Al ingreso se realizó entrevista clínica, exploración física y analítica sanguínea. En todos los pacientes se realizó RMN de 3T con protocolo de epilepsia, y en la mayoría también un estudio neuropsicológico. Se obtuvieron consentimientos informados. Posteriormente se colocaron los electrodos según el sistema internacional 10-20 o 10-10 según el caso. En algunos pacientes con sospecha de crisis del lóbulo temporal se utilizaron electrodos esfenoidales. La monitorización se realizó en camas protegidas, adaptadas y con registro continuo por video-EEG durante las 24h del día, los 5 días de la semana con personal técnico exclusivo durante las 24h.
Se indicó anticoagulación profiláctica en pacientes mayores de 50 años o con factores de riesgo vascular. Se registraron y analizaron todas las crisis y fenómenos adversos acontecidos. Durante la MVEEG se restringió la deambulación. Un equipo especializado de neurólogos, enfermeras y técnicos con formación específica en epilepsia siguieron durante las 24h del día los eventos de cada paciente.
Se tomaron individualizadamente las decisiones de retirada de la medicación con FAE, indicación de privación del sueño, indicación de test de flumazenilo y de inducción de pseudocrisis, así como también de realización de SPECT ictal y otras maniobras diagnósticas.
La metodología utilizada para la retirada del tratamiento con FAE se basó en la frecuencia previa de crisis de cada paciente, la vida media de los fármacos, la posibilidad de crisis por abstinencia y los antecedentes de SE o serie de crisis. El test de flumazenilo se aplicó únicamente en pacientes en los que las crisis epilépticas no aparecieron de manera espontánea tras suspender FAE13. El test de inducción de pseudocrisis se aplicó en los pacientes con sospecha de pseudocrisis en los que estas no aparecieron de manera espontánea en los primeros días de la MVEEG tras la retirada completa de FAE, en correspondencia con la metodología aplicada en la escuela de Bonn y aprobada por el comité de bioética de nuestro hospital.
En los casos en los que estaba indicado se llevó a cabo monitorización invasiva con implantación de electrodos subdurales. En estos casos se utilizaron protocolos de vendajes especiales en pacientes implantados. Se aplicaron protocolos de actuación ante serie de crisis y SE. Tales protocolos se resumen en la figura 1. Una vez concluida la MVEEG se reintrodujo el tratamiento con FAE, que fue modificado en función de las necesidades de cada paciente y la información obtenida durante la monitorización.
Por la normalidad de las variables edad y duración de la estancia en UME la «t» de Student fue usada en la comparación de grupos con respecto a estas variables. Dada la no normalidad de las variables el coeficiente de Spearman se utilizó para hallar la correlación entre las variables cuantitativas crisis por mes previo al ingreso y crisis presentadas durante ingreso, y el test de U de Mann-Whitney para la comparación de grupos con respecto a las variables continuas (duración de la epilepsia previa al ingreso y número de crisis presentadas durante el ingreso). El test de Chi cuadrado fue usado para la comparación de grupos con respecto a las variables cualitativas (sexo, antecedente de SE, antecedente psiquiátrico, retirada de FAE, privación de sueño y realización de SPECT ictal). El T-sample test para datos apareados se utilizó para comparar la frecuencia de crisis por mes previo y tras el ingreso.
Los análisis de regresión univariados y multivariados se utilizaron para detectar factores independientes de riesgo para la aparición de fenómenos adversos, incluyendo datos demográficos (edad, sexo) y clínicos (duración de la epilepsia, motivo de ingreso, historia de SE, reducción de FAE, privación de sueño, realización de SPECT ictal, test de inducción, test de provocación). Por el bajo número de fenómenos adversos detectados se construyó la variable conjunta fenómeno adverso, que englobó las variables SE, lesiones traumáticas, alteraciones cardiorrespiratorias de riesgo y alteraciones psiquiátricas secundarias a crisis.
Finalmente, se llevaron a cabo análisis de regresión logística con los potenciales factores de riesgo para la aparición de fenómenos adversos, que mostraron una relación significativa o próxima a la significación estadística en el análisis univariado.
ResultadosSe analizaron 301 monitorizaciones cursadas por 236 pacientes. El número de pacientes y monitorizaciones admitidas a estudio, por cumplir criterios de inclusión y ninguno de exclusión, fue de 175 pacientes y 220 monitorizaciones. Se excluyeron 61 pacientes y 81 monitorizaciones por cumplir criterio de exclusión.
Un 77,1% (135) de los pacientes admitidos cursó una única monitorización, un 20% (35) precisó 2 monitorizaciones y un 2,9% (5) precisó 3 monitorizaciones. Ningún paciente precisó más de 3 monitorizaciones. Un 32% (56) de los pacientes ingresó para realizar diagnóstico diferencial, y un 68% (119) ingresó para realizar diagnóstico prequirúrgico. El número de días de ingreso total fue de 1.013días.
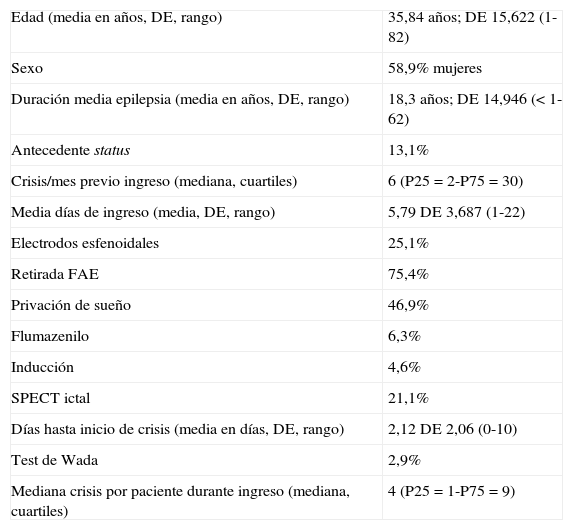
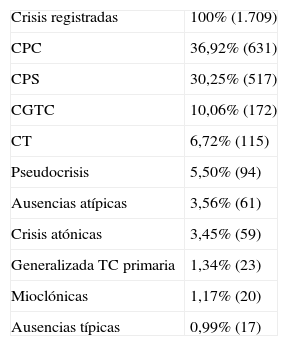
Se encontró una relación significativa entre el número de crisis que los pacientes presentaban previo al ingreso y el número de crisis que los pacientes presentaron durante el ingreso, con un CC de 0,442 (p<0,001). Las características de la muestra, los eventos de cada monitorización y los fenómenos adversos acontecidos se recogen en las tablas 1–3.
Datos demográficos
| Edad (media en años, DE, rango) | 35,84 años; DE 15,622 (1-82) |
| Sexo | 58,9% mujeres |
| Duración media epilepsia (media en años, DE, rango) | 18,3 años; DE 14,946 (<1-62) |
| Antecedente status | 13,1% |
| Crisis/mes previo ingreso (mediana, cuartiles) | 6 (P25=2-P75=30) |
| Media días de ingreso (media, DE, rango) | 5,79 DE 3,687 (1-22) |
| Electrodos esfenoidales | 25,1% |
| Retirada FAE | 75,4% |
| Privación de sueño | 46,9% |
| Flumazenilo | 6,3% |
| Inducción | 4,6% |
| SPECT ictal | 21,1% |
| Días hasta inicio de crisis (media en días, DE, rango) | 2,12 DE 2,06 (0-10) |
| Test de Wada | 2,9% |
| Mediana crisis por paciente durante ingreso (mediana, cuartiles) | 4 (P25=1-P75=9) |
DE: desviación estándar FAE: fármaco antiepiléptico.
Crisis registradas
| Crisis registradas | 100% (1.709) |
| CPC | 36,92% (631) |
| CPS | 30,25% (517) |
| CGTC | 10,06% (172) |
| CT | 6,72% (115) |
| Pseudocrisis | 5,50% (94) |
| Ausencias atípicas | 3,56% (61) |
| Crisis atónicas | 3,45% (59) |
| Generalizada TC primaria | 1,34% (23) |
| Mioclónicas | 1,17% (20) |
| Ausencias típicas | 0,99% (17) |
CGTC: crisis generalizada tónico-clónica secundariamente; CPC: crisis parcial compleja; CPS: crisis parcial simple; CT: crisis tónica; TC: tónico-clónica.
Complicaciones durante la MVEEG
| Fenómeno adverso: no | 92,1% (161) |
| Fenómeno adverso: sí | 7,9% (14) |
| Exitus-MSE | 0% (0) |
| TCE | 0% (0) |
| Lesiones traumáticas | 1,7% (3) |
| Status epilepticus | 3,4% (6) |
| Alteraciones cardiorrespiratorias | 1,1% (2) |
| Alteración psiquiátrica inter-postictal | 1,7% (3) |
MSE: muerte súbita en epilepsia; TCE: traumatismo craneoencefálico.
Todos los casos de SE respondieron correctamente al tratamiento en UME, salvo en un caso que precisó manejo por UCI por cumplir criterios de SE refractario, sin complicaciones, para luego continuar la monitorización.
Todas las lesiones traumáticas fueron menores, a excepción de una doble fractura vertebral compresiva, una hernia discal y una luxación glenohumeral crónica recidivada. Se produjo un caso de taquicardia de riesgo (Fc> 200) y un caso de hipopnea severa postictal con aplanamiento EEG prolongado tras la crisis. Únicamente se registraron 3 casos de alteración psiquiátrica postictal (2 psicosis postictal, una depresión postictal).
Se contactó con los pacientes, que a su vez también podían contactar con el equipo de epilepsia, para constatar la ausencia, entre otras, de este tipo de complicaciones tras el ingreso. En su conjunto un 7,9% de los pacientes presentó algún fenómeno adverso secundario a crisis durante la monitorización, de los cuales fueron de gravedad un 5,1% (SE, fractura vertebral, hernia discal, hipopnea). Solo 2 eventos (1,14%) (fractura vertebral y hernia discal) conllevaron consecuencias tras el alta.
En referencia a los factores de riesgo o protección de fenómenos adversos secundarios a crisis se estudiaron las siguientes variables: sexo, edad, duración de la epilepsia, antecedente de SE, antecedentes psiquiátricos, retirada de FAE, privación de sueño, duración de la estancia en la UME, número de crisis durante el ingreso, tipo predominante de crisis, realización de SPECT ictal y test de flumazenilo o test de provocación de pseudocrisis. En nuestra serie no se identificaron factores de riesgo o de protección con respecto a la probabilidad de fenómenos adversos secundarios a crisis. Las variables retirada de FAE y privación del sueño mostraron una relación inversa con respecto a los días hasta la primera crisis (p=0,035 y p=0,001 respectivamente). La retirada de fármacos mostró una relación significativa con respecto al número de crisis presentadas durante el ingreso (p=0,004).
En 17 pacientes se llegó al diagnóstico de pseudocrisis sin crisis epilépticas, y 5 más fueron diagnosticados de enfermedades diferentes de la epilepsia, descartándose epilepsia concomitante. Se indicó electrocorticografía con electrodos subdurales o SEEG en un total de 13 pacientes (10,92% del total de estudios prequirúrgicos), de las cuales 3 se habían realizado ya al término del período de este estudio. De los 119 pacientes que ingresaron para diagnóstico prequirúrgico se realizaron un total de 51 indicaciones de cirugía de la epilepsia (42,8%), de las cuales 27 se han realizado ya y 24 están pendientes de intervención quirúrgica. De estos casos la cirugía se indicó para implantación de VNS en 14 pacientes, de los cuales 6 se habían colocado ya al final del período de estudio.
DiscusiónEn referencia a la mortalidad no se produjo en nuestra casuística, así como tampoco en los resultados obtenidos en otras series11,12. No obstante, la MSE se ha reportado como complicación durante la MVEEG14.
En relación con la morbilidad, en nuestra casuística el porcentaje de fenómenos adversos fue del 7,9%, mientras que en el estudio publicado por Trinka et al. se obtiene un porcentaje total de pacientes del 9% (44 de 507 pacientes), pero algunos presentaron más de un fenómeno adverso, siendo la cifra total de 53 en 507 pacientes (10,4%); así, las diferencias porcentuales entre sus resultados y los nuestros podrían justificarse por la diferencia de n (175<507), y por las diferencias con respecto a los fenómenos adversos que se reportan (éxitus, lesiones traumáticas, SE, alteraciones psiquiátricas secundarias a crisis y efectos adversos de la medicación, no se reportan alteraciones vegetativas de riesgo).
En la serie publicada por Noe y Drazkowski se reporta un porcentaje total de fenómenos adversos del 14%, pero aquí los criterios de inclusión son mas restrictivos, ya que solo se tuvieron en cuenta para el análisis aquellos pacientes que presentaban crisis tónico-clónicas, excluyéndose a los que presentaban ausencias, pseudocrisis, etc.
En lesiones traumáticas el grupo de Trinka et al. reporta 15 pacientes (2,9%) que presentaron 19 lesiones (14 caídas con lesiones, 2 caídas con fracturas, 2 fracturas sin caída y un TCE con sangrado intracraneal epidural). En nuestra serie como fenómeno traumático severo únicamente se ha producido una fractura vertebral y una hernia discal, por lo que nuestra proporción de lesiones traumáticas severas es inferior (1,14%), lo cual podría deberse a que en nuestra UME se restringe la deambulación durante la MVEEG. En la misma línea Noe y Drazkowski reportan un porcentaje de pacientes con lesiones traumáticas del 2,75%, con 4 casos de fractura vertebral compresiva tras crisis secundariamente generalizadas, por un 1,14% producido en nuestra serie. En ninguna serie se reporta ningún caso de fallecimiento secundario a lesión traumática.
Con respecto a la aparición de SE en nuestra serie se produjo en el 3,4% de los pacientes en comparación con el 2,5% reportado por Trinka et al., que reportan una total de 13 episodios acontecidos en 507 pacientes. En ambos estudios se utilizó la misma definición de SE (crisis con duración> 5-10min). Noe y Drazkowski reportan un 0,67% de pacientes con SE (1 caso), pero su definición de SE utiliza un criterio temporal de 30min, por lo que las cifras no son comparables y debería definirse lo que comunican como crisis prolongadas (reportan 2 casos) para poder comparar las cifras. En ninguna de las 2 series, como tampoco en la nuestra, se reporta necesidad de IOT e inducción anestésica para tratar el SE.
En relación con las alteraciones cardiorrespiratorias de riesgo, en nuestra serie se detectaron 2 casos (1,1%). Estas no se estudiaron en la serie de Trinka et al., mientras que en la serie de Noe y Drazkowski se documentan 3 casos en 149 pacientes (2%). Referente a las alteraciones psiquiátricas inter-postictales en nuestra serie solo se han producido 3 casos (1,7%), en comparación con un 3,9% del trabajo de Trinka et al. (20 de 507 pacientes) (psicosis postictal, psicosis interictal y ataque de pánico), y un 1,34% (2 de 149 pacientes) de psicosis postictal como única alteración psiquiátrica documentada en el grupo de Noe y Drazkowski. A diferencia de lo observado en estas series, en la nuestra las alteraciones psiquiátricas inter-postictales son un fenómeno adverso raro, lo que probablemente está relacionado con criterios de exclusión psiquiátricos más restrictivos usados en nuestro grupo a la hora de seleccionar candidatos a MVEEG. Dado que en nuestra UME se restringe la deambulación por motivos de seguridad, es necesario seleccionar pacientes que por sus características conductuales puedan tolerar tal restricción. En nuestra serie se ha detectado una reducción significativa de la mediana de la frecuencia de crisis que los pacientes presentaban por mes previo al ingreso y tras el ingreso en UME, lo que constata la eficacia de la MVEEG como herramienta en su conjunto para la reducción de la frecuencia de crisis de la población con epilepsia farmacorresistente. Dicha reducción ha sido mucho más llamativa, como es de esperar, en los pacientes que fueron intervenidos quirúrgicamente. Así mismo se ha modificado el diagnóstico del tipo de epilepsia en una parte de la muestra estudiada, pudiendo mejorar el enfoque terapéutico tras el ingreso, y retirar la medicación con FAE a los pacientes diagnosticados de pseudocrisis sin crisis epilépticas o diagnosticados de otras enfermedades diferentes de la epilepsia. Teniendo en cuenta tales beneficios los fenómenos adversos acontecidos en nuestra serie no contraindican el ingreso en UME.
En conclusión, el índice de aparición global de fenómenos adversos secundarios a crisis durante la MVEEG en nuestra serie es equivalente al de grandes series internacionales. Los fenómenos adversos registrados no contraindican la realización de la MVEEG en relación con el riesgo de la epilepsia. Solo un 1,14% de los pacientes presenta complicaciones con consecuencias tras el ingreso. Si bien en nuestro estudio no se encontraron casos de MSE, esta es un riesgo potencial en pacientes ya de por sí con un riesgo de esta complicación, que ha sido reportada en la literatura internacional durante la MVEEG14. A la vista de estos resultados, el estudio en UME, realizado con los protocolos adecuados, constituye una herramienta segura en el diagnóstico diferencial y prequirúrgico de los pacientes con epilepsia farmacorresistente.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Trabajo presentado en la Reunión Anual de la SEN y de la SCN.