Revisar la evidencia científica sobre la efectividad de la aplicación de estímulos auditivos en la fase de iniciación de la marcha y giro en pacientes con enfermedad de Parkinson.
MétodosSe realizó la búsqueda en las bases de datos Brain, PubMed, Medline, Cinahl, Scopus, Science Direct, Web of Science, Cochrane Database of Systematic Reviews, Biblioteca Cochrane Plus, CENTRAL, Trip Database, PEDro, DARE, OTSeeker y Google Académico. Se incluyeron estudios que analizasen la influencia de estímulos auditivos sobre el inicio y el giro de la marcha independiente en pacientes con enfermedad de Parkinson, publicados entre 2007 y 2016. Su calidad metodológica fue valorada mediante la escala Jadad.
ResultadosSe seleccionaron 13 artículos, todos ellos de baja calidad (Jadad≤2) que mostraron resultados positivos en relación con el uso de estímulos auditivos a alta frecuencia e intensidad sobre el inicio de la marcha y la ejecución de giros. En concreto, 1) mejoraron los parámetros espaciotemporales y cinemáticos, 2) disminuyeron la congelación, el tiempo de giro y las caídas y 3) aumentaron la velocidad de iniciación de la marcha, la activación muscular y la velocidad y cadencia de la marcha en los pacientes con EP.
ConclusionesSe requiere un mayor número de estudios y de mayor calidad metodológica para justificar y comprender en qué estadio los pacientes se beneficiarían más de esta señal sensorial, así como el tipo de guía auditiva y la frecuencia de estimulación más eficaz en la fase de iniciación de la marcha y de giro en pacientes con Parkinson.
To review the available scientific evidence about the effectiveness of auditory cues during gait initiation and turning in patients with Parkinson's disease.
MethodsWe conducted a literature search in the following databases: Brain, PubMed, Medline, CINAHL, Scopus, Science Direct, Web of Science, Cochrane Database of Systematic Reviews, Cochrane Library Plus, CENTRAL, Trip Database, PEDro, DARE, OTseeker, and Google Scholar. We included all studies published between 2007 and 2016 and evaluating the influence of auditory cues on independent gait initiation and turning in patients with Parkinson's disease. The methodological quality of the studies was assessed with the Jadad scale.
ResultsWe included 13 studies, all of which had a low methodological quality (Jadad scale score≤2). In these studies, high-intensity, high-frequency auditory cues had a positive impact on gait initiation and turning. More specifically, they 1) improved spatiotemporal and kinematic parameters; 2) decreased freezing, turning duration, and falls; and 3) increased gait initiation speed, muscle activation, and gait speed and cadence in patients with Parkinson's disease.
ConclusionsWe need studies of better methodological quality to establish the Parkinson's disease stage in which auditory cues are most beneficial, as well as to determine the most effective type and frequency of the auditory cue during gait initiation and turning in patients with Parkinson's disease.
La enfermedad de Parkinson (EP) es un proceso neurodegenerativo idiopático de evolución progresiva e insidiosa, cuyo principal hallazgo histológico es la muerte de las neuronas dopaminérgicas de la pars compacta de la sustancia negra y del núcleo estriado y la presencia de cuerpos de Lewy en diferentes regiones del cerebro1–3. Es la enfermedad neurodegenerativa más frecuente después de la enfermedad de Alzheimer y se inicia generalmente entre los 50 y 60 años. Su prevalencia aumenta en edades avanzadas, en torno al 1-2% en sujetos mayores de 65 años y 3-5% en sujetos de 85 años o más1,4,5.
Los síntomas cardinales de la EP incluyen la rigidez, la acinesia, el temblor en reposo y alteraciones de los reflejos de enderezamiento6. Los déficits motores no se traducen únicamente en alteraciones de aspectos cinemáticos del movimiento (velocidad o tiempo), sino también en aspectos relacionados con su variabilidad6–8.
Con la progresión de la enfermedad aparece la típica marcha del paciente con EP, conocida como «marcha festinante», con pasos cortos y acelerados arrastrando los pies, con una tendencia a girar en bloque, y con un incremento del riesgo de caídas6. El frecuente fenómeno de bloqueo o congelación (freezing) o la dificultad para iniciar o continuar un ritmo normal de pasos, parecen estar relacionados con los problemas para generar voluntariamente un ritmo endógeno, adecuado y necesario para ejecutar cualquier movimiento repetitivo, como la marcha7,9,10. De hecho, la dificultad a la hora de iniciar la marcha es uno de los problemas más comunes en las personas con EP. Además, más de la mitad de los pacientes presentan dificultad a la hora de realizar giros, lo cual se asocia a caídas, con sus implicaciones sobre la calidad de vida11–14. Por ello, la iniciación de la marcha y los giros son dos fases críticas en los pacientes con EP.
En el proceso de rehabilitación en la EP se propone como tratamiento de elección la aplicación de estímulos externos de retroalimentación para la mejora de los trastornos de la marcha. Puesto que los ganglios basales desempeñan una función fundamental en el control de las secuencias motoras complejas, en su mayoría automáticas, se ha planteado el uso de dichos estímulos externos auditivos (a modo de metrónomos o golpes rítmicos en el suelo) o visuales (huellas o líneas perpendiculares marcadas en el suelo), en aras de activar otras vías implicadas y eludir los circuidos dañados en la generación de movimientos rítmicos en la EP8,15–17.
El objetivo de esta revisión sistemática es estudiar la evidencia científica sobre la efectividad de la aplicación de los estímulos auditivos sobre la fase de iniciación de la marcha y giro en pacientes con EP.
Material y métodosMetodología de búsquedaSe realizó una búsqueda bibliográfica para identificar todos los posibles estudios originales que pudieran dar respuesta a la pregunta de investigación planteada. Las bases de datos empleadas fueron: Brain, PubMed, Medline, Cinahl, Scopus, Science Direct, Web of Science, Cochrane Database of Systematic Reviews, La Biblioteca Cochrane Plus, CENTRAL, Trip Database, PEDro, DARE, OT Seeker y Google Académico. Se consideraron los años de publicación comprendidos entre enero del 2007 y el 2016 para poder recopilar un mayor número de artículos científicos, al tratarse de dos fases muy específicas de la marcha.
Los términos Medical Subject Headings (MESH) y palabras clave utilizadas en la estrategia de la búsqueda fueron: «Parkinson's disesase», «auditory cues», «cueing», «audio biofeedback», «externally cued», «sensory stimuli», «sensory guides», «freezing», «gait», «turning», «turn», «gait initiation». Cuando las bases de datos permitían detallar límites de búsqueda, esta se restringió a estudios controlados aleatorizados, estudios clínicos originales con pacientes y actas de congresos. También fueron identificados estudios a través de las listas de referencias bibliográficas empleadas en los artículos identificados en las diferentes bases de datos y que cumplían con los requisitos de la búsqueda. El idioma de los estudios debía ser español o inglés.
Criterios de inclusiónLos pacientes incluidos en los estudios debían poseer 1) diagnóstico clínico de EP de acuerdo con los criterios del United Kingdom Parkinson's Disease Society Data Bank18, 2) capacidad de deambulación de forma independiente, 3) episodios de congelación (opcional). Los criterios de exclusión fueron 1) no ingreso previo, ni haber estado sometido a intervención quirúrgica que pudieran modificar el patón de marcha, 2) presencia de otras alteraciones neurológicas, vestibulares o del equilibrio. La intervención debía estar basada en la aplicación de estímulos auditivos, comparando esta intervención con otras modalidades de estímulos sensoriales, otras medidas de tratamiento neurorrehabilitador en la EP o la falta de aplicación de tratamiento. Los resultados debían estar relacionados específicamente con las fases de giro e iniciación de la marcha.
Selección de los artículos y evaluación de la calidad metodológicaSe realizó un cribado de los títulos y resúmenes de las búsquedas electrónicas como medida de selección de los artículos a incluir en la presente revisión sistemática. En función de su contenido, se decidió qué estudios podían cumplir potencialmente los criterios de inclusión. Posteriormente, se procedió a determinar la relevancia de los artículos mediante la lectura de los trabajos a texto completo.
Se realizó una extracción de la información de manera estandarizada de acuerdo con la Consolidated Standards of Reportings Trials Statement19,20. De cada trabajo se extrajo la siguiente información: criterios de inclusión y exclusión, diseño metodológico, aleatorización (si era aplicable), descripción del estudio, enmascaramiento (si era aplicable), medidas de resultado, descripción de la intervención terapéutica y resultados. Para garantizar una evaluación crítica y objetiva de los estudios incluidos, se empleó la escala de calidad metodológica Jadad. Esta escala considera aspectos relacionados con los sesgos, utilizando una serie de ítems referidos a la aleatorización, el enmascaramiento de los pacientes y del investigador al tratamiento, y la descripción de las pérdidas de seguimiento. Puntuaciones mayores indican una mayor calidad metodológica, con una máxima puntuación posible de 5 puntos21.
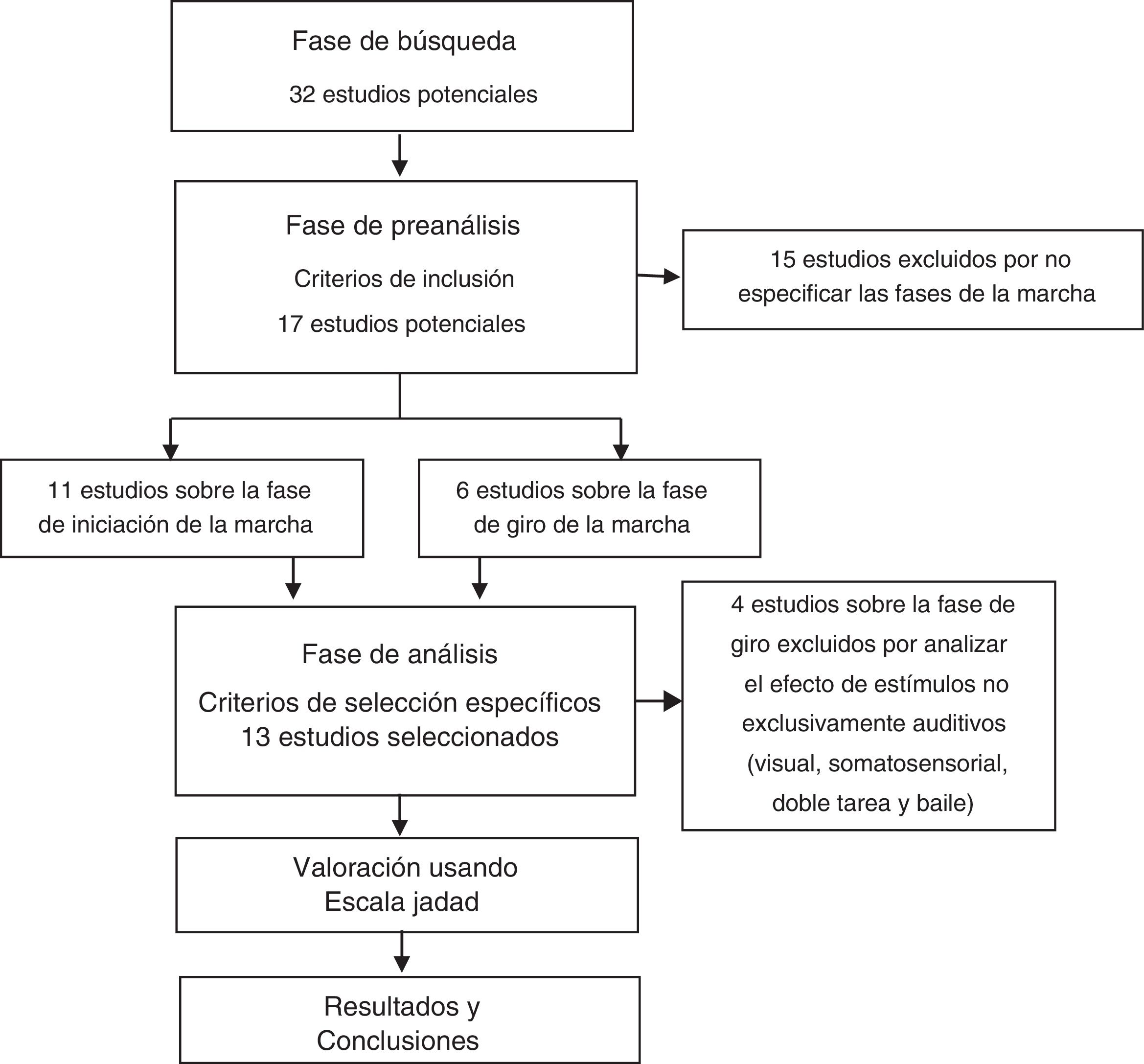
ResultadosResultados de la búsquedaSe localizaron un total de 32 artículos relacionados con la materia de estudio. Se descartaron 15 estudios en los que se aplicaban estímulos sensoriales pero no se relacionaban con ninguna de las dos fases investigadas (fases de giro e iniciación de la marcha)22–36. De los 17 artículos seleccionados, tras aplicar los criterios de selección específicos, se excluyeron 4 trabajos37–40. Finalmente, 13 artículos fueron incluidos41–53 (fig. 1).
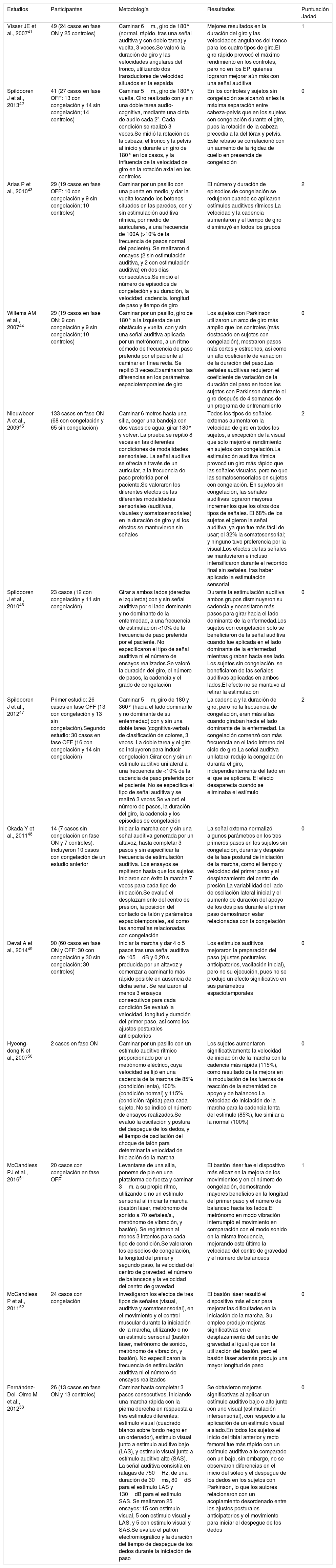
En la tabla 1 se encuentra una descripción detallada de las características de los artículos incluidos en la presente revisión sistemática (con un total de 546 participantes), especificando los autores, el número de participantes y la fase en la que se encontraban con respecto a la medicación, en el caso de los pacientes con EP, la metodología empleada, resultados más destacables y su puntuación según la escala Jadad.
Descripción de los artículos incluidos
| Estudios | Participantes | Metodología | Resultados | Puntuación Jadad |
|---|---|---|---|---|
| Visser JE et al., 200741 | 49 (24 casos en fase ON y 25 controles) | Caminar 6m., giro de 180° (normal, rápido, tras una señal auditiva y con doble tarea) y vuelta, 3 veces.Se valoró la duración de giro y las velocidades angulares del tronco, utilizando dos transductores de velocidad situados en la espalda | Mejores resultados en la duración del giro y las velocidades angulares del tronco para los cuatro tipos de giro.El giro rápido provocó el máximo rendimiento en los controles, pero no en los EP, quienes lograron mejorar aún más con una señal auditiva | 1 |
| Spildooren J et al., 201342 | 41 (27 casos en fase OFF: 13 con congelación y 14 sin congelación; 14 controles) | Caminar 5m., giro de 180° y vuelta. Giro realizado con y sin una doble tarea audio-cognitiva, mediante una cinta de audio cada 2”. Cada condición se realizó 3 veces.Se midió la rotación de la cabeza, el tronco y la pelvis al inicio y durante un giro de 180° en los casos, y la influencia de la velocidad de giro en la rotación axial en los controles | En los controles y sujetos sin congelación se alcanzó antes la máxima separación entre cabeza-pelvis que en los sujetos con congelación durante el giro, pues la rotación de la cabeza precedía a la del tórax y pelvis. Este retraso se correlacionó con un aumento de la rigidez de cuello en presencia de congelación | 0 |
| Arias P et al., 201043 | 29 (19 casos en fase OFF: 10 con congelación y 9 sin congelación; 10 controles) | Caminar por un pasillo con una puerta en medio, y dar la vuelta tocando los botones situados en las paredes, con y sin estimulación auditiva rítmica, por medio de auriculares, a una frecuencia de 100A (>10% de la frecuencia de pasos normal del paciente). Se realizaron 4 ensayos (2 sin estimulación auditiva, y 2 con estimulación auditiva) en dos días consecutivos.Se midió el número de episodios de congelación y su duración, la velocidad, cadencia, longitud de paso y tiempo de giro | El número y duración de episodios de congelación se redujeron cuando se aplicaron estímulos auditivos rítmicos.La velocidad y la cadencia aumentaron y el tiempo de giro disminuyó en todos los grupos | 2 |
| Willems AM et al., 200744 | 29 (19 casos en fase ON: 9 con congelación y 9 sin congelación; 10 controles) | Caminar por un pasillo, giro de 180° a la izquierda de un obstáculo y vuelta, con y sin una señal auditiva aplicada por un metrónomo, a un ritmo cómodo de frecuencia de paso preferida por el paciente al caminar en línea recta. Se repitió 3 veces.Examinaron las diferencias en los parámetros espaciotemporales de giro | Los sujetos con Parkinson utilizaron un arco de giro más amplio que los controles (más destacado en sujetos con congelación), mostraron pasos más cortos y estrechos, así como un alto coeficiente de variación de la duración del paso.Las señales auditivas redujeron el coeficiente de variación de la duración del paso en todos los sujetos con Parkinson durante el giro después de 4 semanas de un programa de entrenamiento | 0 |
| Nieuwboer A et al., 200945 | 133 casos en fase ON (68 con congelación y 65 sin congelación) | Caminar 6 metros hasta una silla, coger una bandeja con dos vasos de agua, girar 180° y volver. La prueba se repitió 8 veces en las diferentes condiciones de modalidades sensoriales. La señal auditiva se ofrecía a través de un auricular, a la frecuencia de paso preferida por el paciente.Se valoraron los diferentes efectos de las diferentes modalidades sensoriales (auditivas, visuales y somatosensoriales) en la duración de giro y si los efectos se mantuvieron sin señales | Todos los tipos de señales externas aumentaron la velocidad de giro en todos los sujetos, a excepción de la visual que solo mejoró el rendimiento en sujetos con congelación.La estimulación auditiva rítmica provocó un giro más rápido que las señales visuales, pero no que las somatosensoriales en sujetos con congelación. En sujetos sin congelación, las señales auditivas lograron mayores incrementos que los otros dos tipos de señales. El 68% de los sujetos eligieron la señal auditiva, ya que fue más fácil de usar; el 32% la somatosensorial; y ninguno tuvo preferencia por la visual.Los efectos de las señales se mantuvieron e incluso intensificaron durante el recorrido final sin señales, tras haber aplicado la estimulación sensorial | 2 |
| Spildooren J et al., 201046 | 23 casos (12 con congelación y 11 sin congelación) | Girar a ambos lados (derecha e izquierda) con y sin señal auditiva por el lado dominante y no dominante de la enfermedad, a una frecuencia de estimulación <10% de la frecuencia de paso preferida por el paciente. No especificaron el tipo de señal auditiva ni el número de ensayos realizados.Se valoró la duración del giro, el número de pasos, la cadencia y el grado de congelación | Durante la estimulación auditiva ambos grupos disminuyeron su cadencia y necesitaron más pasos para girar hacia el lado dominante de la enfermedad.Los sujetos con congelación solo se beneficiaron de la señal auditiva cuando fue aplicada en el lado dominante de la enfermedad mientras giraban hacia ese lado. Los sujetos sin congelación, se beneficiaron de las señales auditivas aplicadas en ambos lados.El efecto no se mantuvo al retirar la estimulación | 0 |
| Spildooren J et al., 201247 | Primer estudio: 26 casos en fase OFF (13 con congelación y 13 sin congelación).Segundo estudio: 30 casos en fase OFF (16 con congelación y 14 sin congelación) | Caminar 5m, giro de 180 y 360° (hacia el lado dominante y no dominante de su enfermedad) con y sin una doble tarea (cognitiva-verbal) de clasificación de colores, 3 veces. La doble tarea y el giro se incluyeron para inducir congelación.Girar con y sin un estímulo auditivo unilateral a una frecuencia de <10% de la cadencia de paso preferida por el paciente. No se especifica el tipo de señal auditiva y se realizó 3 veces.Se valoró el número de pasos, la duración del giro, la cadencia y los episodios de congelación | La cadencia y la duración de giro, pero no la frecuencia de congelación, eran más altas cuando giraban hacia el lado dominante de la enfermedad. La congelación comenzó con más frecuencia en el lado interno del ciclo de giro.La señal auditiva unilateral redujo la congelación durante el giro, independientemente del lado en el que se aplicara. El efecto desaparecía cuando se eliminaba el estímulo | 2 |
| Okada Y et al., 201148 | 14 (7 casos sin congelación en fase ON y 7 controles). Incluyeron 10 casos con congelación de un estudio anterior | Iniciar la marcha con y sin una señal auditiva generada por un altavoz, hasta completar 3 pasos y sin especificar la frecuencia de estimulación auditiva. Los ensayos se repitieron hasta que los sujetos iniciaron con éxito la marcha 7 veces para cada tipo de iniciación.Se evaluó el desplazamiento del centro de presión, la posición del contacto de talón y parámetros espaciotemporales, así como las anomalías relacionadas con congelación | La señal externa normalizó algunos parámetros en los tres primeros pasos en los sujetos sin congelación, durante y después de la fase postural de iniciación de la marcha, como el tiempo y velocidad del primer paso y el desplazamiento del centro de presión.La variabilidad del lado de oscilación lateral inicial y el aumento de duración del apoyo de los dos pies durante el primer paso demostraron estar relacionadas con la congelación | 0 |
| Deval A et al., 201449 | 90 (60 casos en fase ON y OFF: 30 con congelación y 30 sin congelación; 30 controles) | Iniciar la marcha y dar 4 o 5 pasos tras una señal auditiva de 105dB y 0,20 s. producida por un altavoz y comenzar a caminar lo más rápido posible en ausencia de dicha señal. Se realizaron al menos 3 ensayos consecutivos para cada condición.Se evaluó la velocidad, longitud y duración del primer paso, así como los ajustes posturales anticipatorios | Los estímulos auditivos mejoraron la preparación del paso (ajustes posturales anticipatorios, vacilación inicial), pero no su ejecución, pues no se produjo un efecto significativo en sus parámetros espaciotemporales | 0 |
| Hyeong-dong K et al., 200750 | 2 casos en fase ON | Caminar por un pasillo con un estímulo auditivo rítmico proporcionado por un metrónomo eléctrico, cuya velocidad se fijó en una cadencia de la marcha de 85% (condición lenta), 100% (condición normal) y 115% (condición rápida) para cada sujeto. No se indicó el número de ensayos realizados.Se evaluó la oscilación y postura del despegue de los dedos, y el tiempo de oscilación del choque de talón para determinar la velocidad de iniciación de la marcha | Los sujetos aumentaron significativamente la velocidad de iniciación de la marcha con la cadencia más rápida (115%), como resultado de la mejora en la modulación de las fuerzas de reacción de la extremidad de apoyo y de balanceo.La velocidad de iniciación de la marcha para la cadencia lenta del estímulo (85%), fue similar a la normal (100%) | 0 |
| McCandless PJ et al., 201651 | 20 casos con congelación en fase OFF | Levantarse de una silla, ponerse de pie en una plataforma de fuerza y caminar 3m. a su propio ritmo, utilizando o no un estímulo sensorial al iniciar la marcha (bastón láser, metrónomo de sonido a 70 señales/s., metrónomo de vibración, y bastón). Se registraron al menos 3 intentos para cada tipo de condición.Se valoraron los episodios de congelación, la longitud del primer y segundo paso, la velocidad del centro de gravedad, el número de balanceos y la velocidad del centro de gravedad | El bastón láser fue el dispositivo más eficaz en la mejora de los movimientos y en el número de congelación, demostrando mayores beneficios en la longitud del primer paso y el número de balanceo hacia los lados.El metrónomo en modo vibración interrumpió el movimiento en comparación con el modo sonido en la misma frecuencia, mejorando este último la velocidad del centro de gravedad y el número de balanceos | 1 |
| McCandless P et al., 201152 | 24 casos con congelación | Investigaron los efectos de tres tipos de señales (visual, auditiva y somatosensorial), en el movimiento y el control muscular durante la iniciación de la marcha, utilizando o no un estímulo sensorial (bastón láser, metrónomo de sonido, metrónomo de vibración, y bastón). No especificaron la frecuencia de estimulación auditiva ni el número de ensayos realizados | El bastón láser resultó el dispositivo más eficaz para mejorar las dificultades en la iniciación de la marcha. Su empleo produjo mejoras significativas en el desplazamiento del centro de gravedad al igual que con la utilización del bastón, pero el bastón láser además produjo una mayor longitud de paso | 0 |
| Fernández-Del- Olmo M et al., 201253 | 26 (13 casos en fase ON y 13 controles) | Caminar hasta completar 3 pasos consecutivos, iniciando una marcha rápida con la pierna derecha en respuesta a tres estímulos diferentes: estímulo visual (cuadrado blanco sobre fondo negro en un ordenador), estímulo visual junto a estímulo auditivo bajo (LAS), y estímulo visual junto a estímulo auditivo alto (SAS). La señal auditiva consistía en ráfagas de 750Hz, de una duración de 30ms, 80dB para el estímulo LAS y 130dB para el estímulo SAS. Se realizaron 25 ensayos: 15 con estímulo visual, 5 con estímulo visual y LAS, y 5 con estímulo visual y SAS.Se evaluó el patrón electromiográfico y la duración del tiempo de despegue de los dedos durante la iniciación de paso | Se obtuvieron mejoras significativas al aplicar un estímulo auditivo bajo o alto junto con uno visual (estimulación intersensorial), con respecto a la aplicación de un estímulo visual aislado.En todos los sujetos el inicio del tibial anterior y recto femoral fue más rápido con un estímulo auditivo alto comparado con un bajo, sin embargo, no se observaron diferencias en el inicio del sóleo y el despegue de los dedos en los sujetos con Parkinson, lo que los autores relacionaron con un acoplamiento desordenado entre los ajustes posturales anticipatorios y el movimiento para iniciar el despegue de los dedos | 0 |
En relación a las características generales de los trabajos incluidos, todos los pacientes presentaban EP idiopática, siendo capaces de caminar 10 metros sin ayuda y los pacientes sin congelación, presentaban una puntuación de 0 en el ítem 3 del Freezing of Gait Guestionnaire. Solamente en tres estudios se indicó el tiempo medio del inicio de la enfermedad. Además, los pacientes presentaban entre 1-16 años de evolución desde el diagnóstico de la enfermedad. Los pacientes se encontraban en fase ON u OFF de la medicación.
El material empleado con mayor frecuencia para proporcionar estimulación auditiva rítmica era un metrónomo, aunque también se utilizaron otros como grabación de audio, auriculares y altavoces. Se realizaron un total de 3 ensayos previos a cada tarea o condición en la mayoría de los trabajos, tanto en la fase de iniciación de la marcha, como en la fase de giro, con el fin de obtener valores objetivos de las diferentes variables cinemáticas. El orden de los ensayos fue al azar y se proporcionaron periodos de descanso para evitar la fatiga entre repeticiones. Cabe destacar que en la mayoría de los casos no se indicaba el tiempo, número de semanas o meses de tratamiento.
Las escalas más empleadas para la valoración y/o clasificación de los pacientes fueron la Unified Parkinson's Disease Rating Scale, especialmente la sección III; la clasificación en estadios de Hoehn y Yahr, encontrándose los pacientes principalmente en estadio II (afectación bilateral sin alteración del equilibrio) y III (afectación leve a moderada; cierta inestabilidad postural pero físicamente independiente; necesita ayuda para recuperarse en la «prueba del empujón»); Mini-Mental State Exploration>24 puntos y el Freezing of Gait Guestionnaire.
Las frecuencias de los materiales empleados para producir estimulación auditiva rítmica más utilizadas fueron: frecuencia de 100Hz (> 10% de la frecuencia normal de pasos del paciente);<10% de la frecuencia o cadencia de paso preferida del paciente; o bien a un ritmo cómodo de frecuencia de paso preferida del paciente, mientras camina en línea recta.
La valoración instrumental de los resultados se realizó mediante sistemas de análisis de movimiento con cámaras de VICON 3D; marcadores retrorreflectantes; plataformas de fuerza; electromiografía de superficie; y programas de software específicos para la visualización de los episodios de FOG y para definir los primeros contactos del pie.
Los resultados principales sobre la eficacia del uso de las guías acústicas en la fase de iniciación de la marcha y giro en pacientes con EP se indican a continuación: 1) cuando se aplican estímulos auditivos rítmicos a una alta frecuencia, se obtienen mejores resultados, tanto en la fase de iniciación de la marcha: aumento significativo de la velocidad de iniciación de la marcha con la cadencia más rápida (115%)50 e inicio más rápido de la actividad del tibial anterior y recto femoral con un estímulo auditivo de sobresalto53, como en la fase de giro: reducción del número y duración de episodios de congelación, aumento de la velocidad y la cadencia y disminución del tiempo de giro a >10% de la frecuencia de paso normal del paciente43. 2) A una frecuencia de paso cómoda y preferida por el paciente, las señales auditivas solo redujeron el coeficiente de variación de la duración de paso durante el giro, pero no otros parámetros de la marcha44. 3) A<10% de la frecuencia de paso preferida por el paciente, los pacientes con EP disminuyeron su cadencia, y por tanto, aumentó la duración del giro46. La velocidad de iniciación de la marcha para la cadencia lenta (85%), fue similar a la normal (100%)50.
Los estímulos auditivos parecen mejorar la preparación de los primeros pasos (ajustes posturales anticipatorios y grado de vacilación inicial). En relación al fenómeno de congelación, la estimulación auditiva unilateral parece reducir la aparición de congelación durante la fase de giro, siendo el lado a estimular el hemicuerpo más afecto por la EP46. Sin embargo, otro estudio señaló que la señal auditiva unilateral reducía la congelación durante el giro, independientemente del lado en el que se aplicara dicha señal47. Los efectos conseguidos no parecen mantenerse al retirar la estimulación46,47.
Calidad metodológica de los estudios incluidosSegún la escala Jadad, la puntuación de los estudios incluidos en la presente revisión sistemática indicó una calidad metodológica baja. Solo tres trabajos obtuvieron una puntuación de 2, dos una puntuación de 1 y 8 trabajos una puntuación de 0, por lo que todos los estudios evaluados se consideran de baja calidad metodológica21 (tabla 1).
DiscusiónEn nuestro conocimiento, esta es la primera revisión sistemática que estudia la evidencia científica en relación con el uso de estímulos auditivos de manera específica en el inicio de la marcha y la ejecución de giros en la EP. El limitado número de artículos encontrados, así como su baja calidad, no permiten realizar recomendaciones terapéuticas con elevado nivel de evidencia. Sin embargo, los estudios analizados sugieren que con el uso de estímulos sensoriales de tipo auditivo a una alta frecuencia se obtienen los mejores resultados en ambas fases, disminuyendo la aparición de congelación y caídas en los pacientes con EP.
Primeras aplicaciones, tipos de estímulos auditivos y justificación neurofisiológicaLas primeras aplicaciones terapéuticas realizadas para demostrar el efecto positivo de las señales auditivas sobre la marcha en la EP se deben a Thaut et al., en 199654. Sometieron a pacientes con EP a un entrenamiento que consistía en caminar en sincronía con un estímulo auditivo rítmico. Varios estudios posteriores parecían corroborar la mejora en la velocidad, amplitud y cadencia de la marcha en la EP7,55. La forma de señalización auditiva más utilizada y que ha demostrado mayores mejorías en los parámetros de marcha de los pacientes con Parkinson, es el metrónomo con una frecuencia>10% de la cadencia habitual del paciente56–60.
La hipótesis más aceptada de cómo las guías sensoriales mejoran el patrón de marcha en la EP, postula que estos estímulos alcanzarían el córtex premotor y el área motora suplementaria por una vía alternativa a los ganglios basales, compensando así los mecanismos deficitarios61–64. Además, los estímulos auditivos podrían tener un efecto sobre los mecanismos atencionales del paciente y la ejecución de movimientos que requieren una mayor planificación45,63.
Estímulos auditivos en la iniciación de la marcha y girosLa iniciación de la marcha se acompaña de ajustes posturales anticipatorios y la EP se caracteriza por la falta de preparación y ejecución de paso durante la iniciación de la misma, lo que podría explicar la pobre ejecución del primer paso (menor velocidad y longitud de paso)48,49. En este sentido, las señales externas mejoran las anomalías y disminuyen la duración de la fase postural de iniciación de la marcha en EP y aumentan la producción de fuerza y el desplazamiento del centro de presión durante esta fase48.
El giro es el acto motor que más frecuentemente desencadena el bloqueo de la marcha (63%), especialmente durante giros rápidos y completos (360°)42, pero el bloqueo o la congelación también aparece al inicio de la marcha (23%), al caminar a través de espacios estrechos (12%) y al llegar a destinos (9%)14. Los episodios de congelación también ocurren más frecuentemente a mitad de un giro de 180° cuando el paciente se dispone a dar la vuelta, es decir, ante un giro de 90° cuando la separación entre cabeza y pelvis es mayor y, posiblemente, el giro más inestable42. La evidencia parece indicar que, al girar hacia el lado más afectado, la cadencia y duración de giro son más altas; sin embargo, los pacientes sufren el mismo número de episodios de congelación independientemente del lado al que giren47. Los estímulos auditivos han demostrado mejorar los movimientos en bloque durante el giro, así como los parámetros de la marcha42,48.
Estímulos auditivos y comparación con otras modalidades sensorialesCuando se comparan diferentes tipos de condiciones de giro (giro normal, rápido, tras una señal auditiva y con doble tarea), los pacientes con EP consiguen el máximo rendimiento al aplicar una señal auditiva41. Y al valorar los efectos de las diferentes modalidades sensoriales, la estimulación auditiva rítmica provoca un giro más rápido que las señales visuales45. Cuando los pacientes inician la marcha utilizando diferentes estímulos sensoriales, el uso de un bastón láser resultó el dispositivo más eficaz, disminuyendo el número de episodios de congelación y aumentando principalmente la longitud del primer paso51,52. Además, un ensayo53 mostró mejoras más significativas en la iniciación de la marcha al aplicar una estimulación intersensorial (visual junto con auditiva), que un estímulo visual solo.
Por tanto, la presente revisión sugiere que los estímulos auditivos (principalmente a>10% de la frecuencia de paso) resultan más eficaces para la mejora de la cadencia de la marcha, implicando un aumento de la velocidad al hacer un giro, mientras que los estímulos visuales presentan mayor eficacia sobre el aumento de la longitud de paso, imprescindible para la iniciación de la marcha64–68. Los hallazgos sobre las dificultades para el mantenimiento del efecto en el tiempo podrían relacionare con que el uso de señales externas puede redirigir la atención hacia los procesos de la marcha y mejorar su realización, pero este efecto se debilita a medida que pasa el tiempo49, como han expuesto diversos trabajos69–72.
Los resultados de la presente revisión sistemática sugieren que un programa de entrenamiento de la marcha a través de estímulos propioceptivos y exteroceptivos, con una frecuencia de tres sesiones por semana, de aproximadamente media hora de duración, provocaría una mejoría en la longitud de paso, la cadencia y velocidad de la marcha, así como en el número de episodios de congelación durante las fases de iniciación del paso y la realización de giros, limitando el riesgo de caídas y mejorando así la calidad de vida en la EP64. No obstante, la presente revisión sistemática adolece de una serie de limitaciones metodológicas, como el incluir únicamente trabajos publicados en inglés y español. Asimismo, el diseño y la metodología de la mayoría de los trabajos incluidos son heterogéneos y no permiten otorgar un grado de recomendación en función de su nivel de evidencia superior a razonable o aceptable.
ConclusionesLa iniciación de la marcha y la realización de giros son desencadenantes importantes para sufrir episodios de congelación en pacientes con Parkinson. El uso de guías auditivas ha demostrado producir mejorías en los parámetros espaciotemporales y cinemáticos en ambas fases. Los mayores beneficios se obtienen con la aplicación de un metrónomo a una frecuencia de>10% de la cadencia habitual del paciente, aumentando la velocidad de iniciación de la marcha, la activación muscular, la velocidad y cadencia de marcha en la EP, así como disminuyendo la duración de la congelación de la marcha y el tiempo de giro, especialmente ante una alta intensidad del estímulo. No obstante, los estímulos visuales han demostrado una mayor eficacia sobre el aumento de la longitud de paso, imprescindible para la iniciación de la marcha.
La aplicación de estrategias terapéuticas como el uso de señales auditivas externas en combinación con el tratamiento rehabilitador convencional en EP, puede incrementar la calidad de vida de estos pacientes mejorando aspectos motores y minimizando el riesgo de caídas. Sin embargo, se requiere un mayor número de estudios y de mayor calidad metodológica para justificar y comprender qué pacientes se benefician más de esta señal sensorial, así como el tipo de guía auditiva y la frecuencia de estimulación más eficaz en la fase de iniciación de la marcha y de giro en pacientes con EP.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.