En este estudio se compararon los resultados de la radioterapia holocraneal (RTHC) con el tratamiento farmacológico exclusivo (TFE) respecto del control de síntomas y la mejoría en la función neurológica en pacientes con metástasis cerebrales y con un mal pronóstico según el índice RPA.
MétodosEntre diciembre de 2012 y diciembre de 2014, 100 pacientes con diagnóstico de cáncer ingresados a raíz de metástasis cerebrales sintomáticas fueron valorados por nuestro servicio. Treinta y siete pacientes fueron clasificados como RPA3. En este grupo se compararon los resultados clínicos del TFE (n=11) con los de la RTHC (n=26).
ResultadosLa mediana de supervivencia fue de 1,2 meses, sin diferencias estadísticamente significativas entre los pacientes que recibieron TFE (0,83 meses) y aquellos tratados con RTHC (1,4 meses) (p=0,18). No se observaron diferencias en el alivio sintomático ni en la mejoría de la función neurológica entre ambos grupos de tratamiento. En los pacientes tratados con RTHC, el alivio sintomático y la mejoría de la función neurológica no mostraron diferencias estadísticamente significativas cuando se compararon distintas dosis y fraccionamiento de radioterapia ni el tiempo transcurrido entre el diagnóstico de metástasis cerebrales y el inicio del tratamiento.
ConclusionesLa RTHC no produjo ningún beneficio clínico en cuanto al control sintomático ni en la mejoría de la función neurológica. No se observaron diferencias en la supervivencia entre ambos grupos de tratamiento. En los pacientes RPA3, el TFE puede ser una opción terapéutica razonable.
In this study we analysed the results of whole brain radiotherapy (WBRT) compared to exclusive pharmacologic treatment (EPT) regarding symptom control and improvement of neurological function in patients with brain mestastases and a poor prognosis (RPA3).
MethodsFrom December 2012 to December 2014, 100 consecutive cancer inpatients with symptomatic brain mestastases were assessed in our department. We identified patients classified as RPA3 (n=37) and compared the results of patients receiving EPT (n=11) and those undergoing WBRT (n=26).
ResultsThe median survival of the entire group was 1.2 months, with no statistically significant differences between EPT (0.83 months) and WBRT (1.4 months) (P=.18). Neither were differences in symptom relief observed between the 2 groups at the last follow up. Improvement of neurological signs was poor in both treatment groups. Symptom relief and improvement of neurological function in patients undergoing WBRT showed no differences compared to radiation doses, schedules or the time from brain mestastases diagnosis to the first radiotherapy session.
ConclusionsWBRT did not provide clinical benefits in control of symptoms, improvement of neurological function or survival compared with EPT. In RPA3 inpatients EPT may be a reasonable option of treatment.
Aproximadamente un 40% de los pacientes con cáncer presentarán metástasis craneales (MC) durante el curso de la enfermedad1. La radioterapia holocraneal (RTHC) es una alternativa terapéutica en muchos de ellos, especialmente si existe también enfermedad metastásica extracraneal.
En los pacientes con cáncer, la estimación de la supervivencia mediante índices pronósticos permite la elección de tratamientos más ajustados a las necesidades de cada individuo, contribuyendo a evitar la indicación de terapias fútiles2.
El recursive partitioning analysis (RPA)3 es una escala pronóstica ampliamente utilizada que considera la edad, el índice de Karnofsky (IK), la presencia de metástasis extracraneales y el estatus del tumor primario (controlado o no controlado) para clasificar a los pacientes en 3 grupos pronósticos. Los pacientes RPA1 (<65 años, IK≥70, tumor primario controlado y ausencia de enfermedad metastásica extracraneal) tienen una supervivencia mediana de 7,1 meses; aquellos pacientes clasificados como RPA3 (IK<70) tienen una supervivencia mediana de 2,3 meses, mientras que los pacientes no clasificables en las categorías anteriores forman el grupo RPA2, cuya mediana de supervivencia es de 4,2 meses.
En aquellos pacientes con buen pronóstico se han hecho considerables esfuerzos para establecer el mejor tratamiento y analizar sus resultados, mientras que el grupo RPA3 ha recibido escasa atención. En estos pacientes con un mal estado funcional, una importante carga sintomática y escasa supervivencia, la indicación de RTHC implica mantenerlos ligados al hospital, con un beneficio clínico no del todo claro4.
En este estudio se revisaron y compararon los resultados del tratamiento farmacológico exclusivo (TFE) versus la RTHC en cuanto al alivio sintomático y la recuperación neurológica en pacientes RPA3 valorados por nuestro servicio.
Pacientes y métodoEntre diciembre de 2012 y diciembre de 2014, 100 pacientes consecutivos, con diagnóstico de cáncer e ingresados por MC sintomáticas fueron valorados por nuestro servicio. Todos ellos fueron clasificados de acuerdo con la escala RPA. Mediante la revisión de las historias clínicas se identificó a aquellos pacientes RPA3 (n=37). En 11 pacientes se indicó TFE (dexametasona 12mg/día [n=11], anticomiciales [n=3] y antipsicóticos [n=2]). En 26 pacientes se realizó RTHC y en todos ellos se administró también dexametasona 12mg/día en el momento del diagnóstico por tomografía computarizada.
Los resultados del tratamiento se revisaron considerando variables clínicas y hallazgos radiológicos. Como variables clínicas se incluyeron: síntoma de presentación, signos neurológicos, IK (>o≤60%), control del tumor primario (controlado o no controlado en los 3 meses previos), enfermedad metastásica extracraneal y deterioro neurológico durante el tratamiento. Como variable radiológica se consideró el número de MC (única o múltiples) visualizadas mediante tomografía computarizada.
Se valoró el control de los síntomas (mejoría/no mejoría) según la impresión del paciente o del cuidador (en caso de alteración de la conciencia), mientras que la evolución de los signos neurológicos fue valorada clínicamente. Para la valoración de la evolución de los síntomas y los signos neurológicos se consideró la medición en la fecha del último seguimiento, que fue definido como la fecha del exitus.
Para el tratamiento con RTHC se prescribieron 2 esquemas: 30Gy en 10 fracciones (n=14) y 20Gy en 5 fracciones (n=12). Se registró el tiempo transcurrido entre el diagnóstico de MC y el inicio del tratamiento radioterápico. Se definió como inicio precoz del tratamiento un lapso≤2 días entre el diagnóstico de MC y la primera sesión de radioterapia.
Las características basales de los pacientes incluidos se reportaron como números absolutos y porcentajes. La comparación de las variables categóricas de ambos grupos de tratamiento se realizó utilizando el test de Chi-cuadrado o el test exacto de Fisher, según fuese más apropiado. El tiempo de supervivencia se calculó desde el momento del diagnóstico de MC hasta la fecha de exitus. Para el cálculo de la supervivencia se utilizó el test de Kaplan-Meier y las comparaciones entre los 2 grupos se realizó mediante el log-rank test. Todos los test estadísticos fueron bilaterales y la significación estadística fue definida como p<0,05. El análisis estadístico se realizó mediante el programa SPSS versión 20.
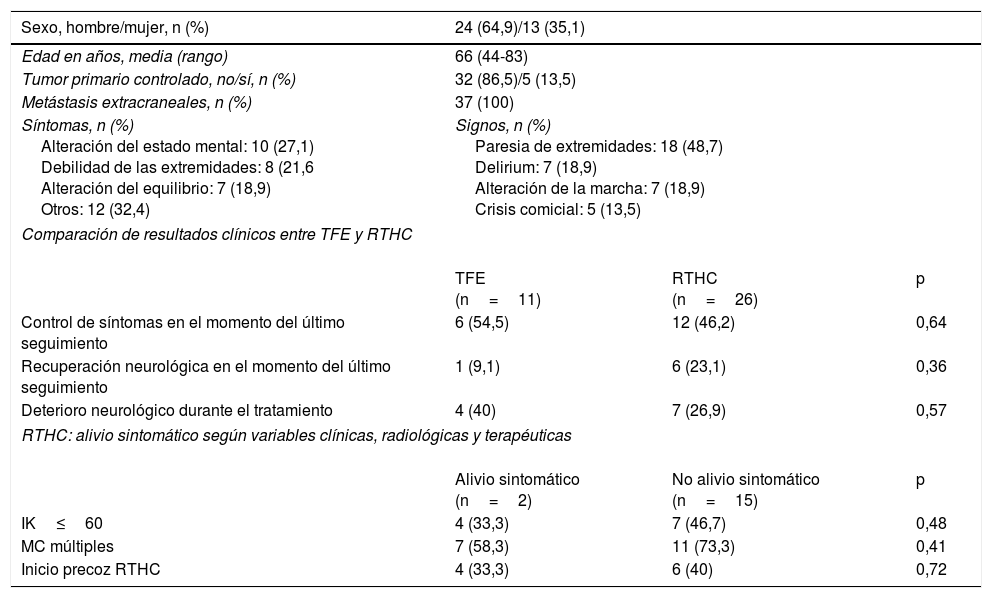
ResultadosLos datos demográficos, las características clínicas y los resultados del tratamiento en ambos grupos se muestran en la tabla 1.
Características demográficas, clínicas y resultados del tratamiento farmacológico exclusivo y la radioterapia holocraneal
| Sexo, hombre/mujer, n (%) | 24 (64,9)/13 (35,1) | ||
|---|---|---|---|
| Edad en años, media (rango) | 66 (44-83) | ||
| Tumor primario controlado, no/sí, n (%) | 32 (86,5)/5 (13,5) | ||
| Metástasis extracraneales, n (%) | 37 (100) | ||
| Síntomas, n (%) Alteración del estado mental: 10 (27,1) Debilidad de las extremidades: 8 (21,6 Alteración del equilibrio: 7 (18,9) Otros: 12 (32,4) | Signos, n (%) Paresia de extremidades: 18 (48,7) Delirium: 7 (18,9) Alteración de la marcha: 7 (18,9) Crisis comicial: 5 (13,5) | ||
| Comparación de resultados clínicos entre TFE y RTHC | |||
TFE (n=11) | RTHC (n=26) | p | |
| Control de síntomas en el momento del último seguimiento | 6 (54,5) | 12 (46,2) | 0,64 |
| Recuperación neurológica en el momento del último seguimiento | 1 (9,1) | 6 (23,1) | 0,36 |
| Deterioro neurológico durante el tratamiento | 4 (40) | 7 (26,9) | 0,57 |
| RTHC: alivio sintomático según variables clínicas, radiológicas y terapéuticas | |||
Alivio sintomático (n=2) | No alivio sintomático (n=15) | p | |
| IK≤60 | 4 (33,3) | 7 (46,7) | 0,48 |
| MC múltiples | 7 (58,3) | 11 (73,3) | 0,41 |
| Inicio precoz RTHC | 4 (33,3) | 6 (40) | 0,72 |
IK: índice de Karnofsky; MC: metástasis cerebrales; RTHC: radioterapia holocraneal; TFE: tratamiento farmacológico exclusivo.
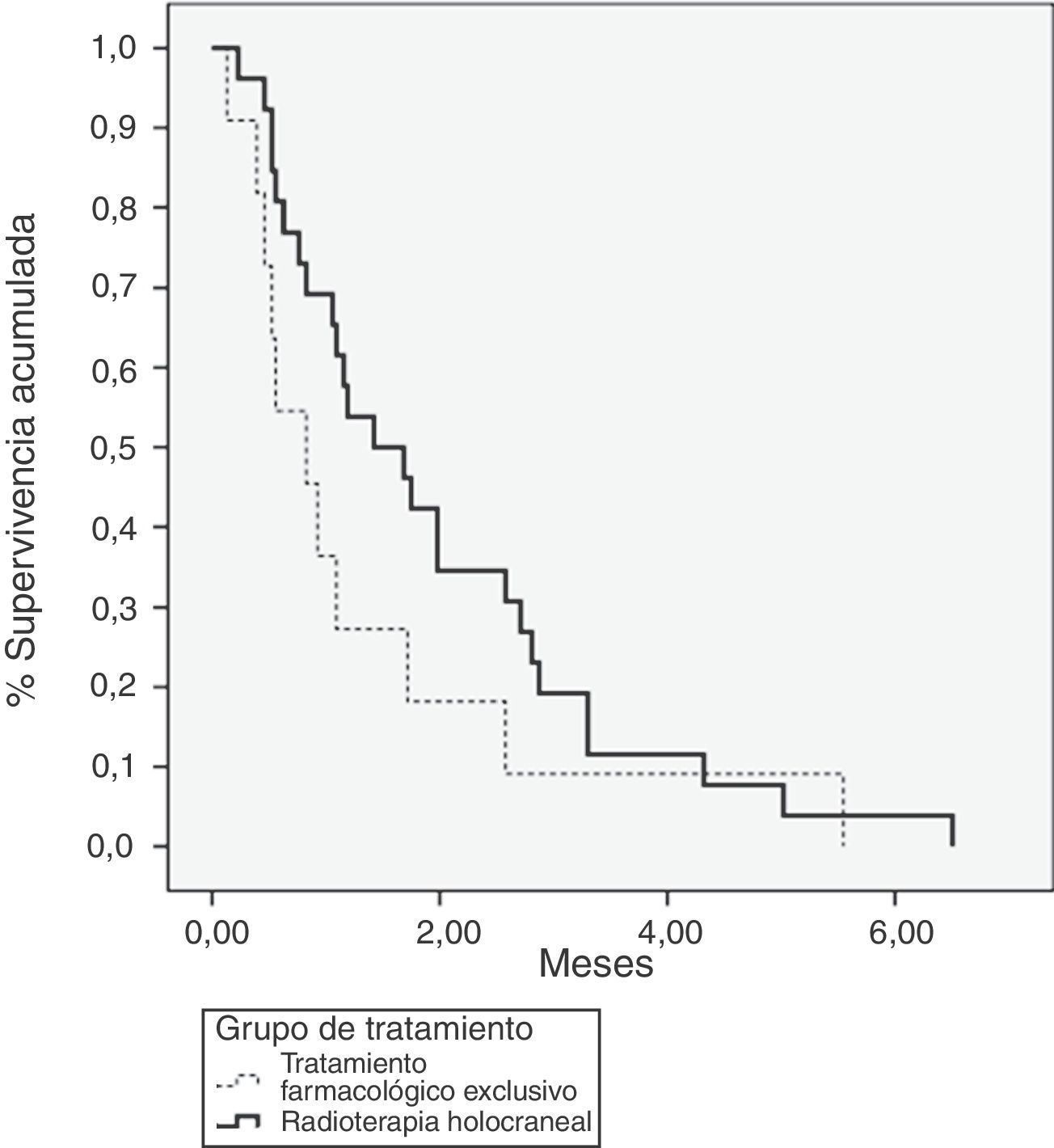
La mediana de supervivencia del grupo de pacientes tratados con TFE fue de 0,83 meses (IC 95% 0,39-1,25) y de 1,4 meses (IC 95% 0,67-2,16) en el grupo de RTHC (p=0,18) (fig. 1).
El inicio precoz o tardío de la RTHC no influyó en el control de los síntomas. Un 48,6% de los pacientes con una supervivencia mayor de 4 semanas presentaron alivio sintomático, sin observarse diferencias respecto del grupo con una supervivencia menor (51,4%) (p=0,14).
No se observaron diferencias estadísticamente significativas en el alivio sintomático entre aquellos pacientes tratados con una dosis de 30Gy/10 sesiones y aquellos tratados con 20Gy/5 sesiones (p=0,78). Tampoco se encontraron diferencias en la mejoría de la función neurológica (p=0,52).
En 7/26 pacientes que recibieron RTHC, el deterioro neurológico condicionó la interrupción del tratamiento.
Solo 2 pacientes tratados con TFE y 7 de los tratados con RTHC regresaron a su domicilio tras el alta hospitalaria. A causa del deterioro funcional, la mayoría de los pacientes (n=28) murió en centros de cuidados paliativos (n=14) o en el hospital (n=14). Entre los pacientes tratados con RTHC, un 30% murió en el hospital.
DiscusiónLos pacientes RPA3 tienen una escasa supervivencia3,4, aunque en aquellos muy seleccionados (tumor primario controlado y ausencia de enfermedad metastásica extracraneal) se han reportado beneficios en términos de supervivencia en los tratados con cirugía, radiocirugía y/o RTHC4,5.
En el presente estudio, la escasa mediana de supervivencia observada (1,2 meses) posiblemente esté influida por el tipo de pacientes incluidos, todos estaban ingresados debido a la severidad de la sintomatología y/o de los signos neurológicos. Además, una gran parte de ellos presentaba un tumor primario no controlado y todos tenían enfermedad metastásica extracraneal.
En el presente estudio, un 51,4% de los pacientes tratados con RTHC no mostró ningún alivio sintomático y la función neurológica mejoró solo en el 18%, sin que se observaran diferencias entre los 2 esquemas de RTHC utilizados. Estos datos son similares a los reportados en el estudio de Bezjak et al.6, que incluyó 75 pacientes con MC. Solo un 19% evidenció mejoría o resolución de los síntomas de presentación a un mes del tratamiento con RTHC, mientras que un 23% se mantuvo estable y un 55% progresó o murió. Los autores concluyeron que muchos pacientes tenían una corta expectativa de supervivencia y no se beneficiaban de la RTHC, incluso si esta era administrada en esquemas cortos.
En el estudio de Henriquez et al.7, un 30% de los pacientes tratados con RTHC no presentó alivio sintomático, independientemente del tiempo transcurrido entre el diagnóstico de MC y el inicio de la RTHC. En el presente estudio, tampoco se observó un beneficio en la recuperación neurológica con el inicio precoz del tratamiento.
A pesar de que algunos autores han demostrado que el máximo beneficio clínico de la RTHC se alcanzaría a las 3-4 semanas de iniciado el tratamiento, en este estudio no se observaron diferencias estadísticamente significativas entre los pacientes que vivieron más de 4 semanas respecto de los que vivieron menos.
Según Conill et al.8, el IK puede ser considerado como una medida global válida y confiable de la calidad de vida. Aun cuando en el presente estudio no se registró específicamente este último ítem, se observó una escasa recuperación funcional y por consiguiente de la calidad de vida en los pacientes RPA3, pues la mayor parte de estos no presentó mejoría del IK, a pesar del tratamiento radioterápico.
A día de hoy, carecemos de evidencia acerca del mejor tratamiento en el grupo de pacientes RPA3 debido a la falta de estudios aleatorizados. De momento, la experiencia acumulada apunta a que muchos pacientes no se benefician del tratamiento radioterápico y que los cuidados paliativos sin RTHC pueden ser una alternativa apropiada en muchos pacientes de mal pronóstico9.
Aunque las principales limitaciones del presente estudio son su diseño retrospectivo y el pequeño tamaño muestral, creemos que su principal aporte es compartir la experiencia de nuestro centro, dada la actual falta de estudios aleatorizados en este ámbito. Los resultados obtenidos en este estudio, junto con aquellos aquí referenciados, enfatizan la importancia de la selección cuidadosa de los pacientes RPA3 a la hora de ofrecer opciones terapéuticas, evitando el sobretratamiento y maximizando los recursos del sistema sanitario10.
Sin lugar a dudas, el estudio QUARTZ aportará la evidencia necesaria para contestar las cuestiones no resueltas. En él se comparan la RTHC a dosis de 20Gy en 5 fracciones más cuidados de soporte versus corticoides más cuidados de soporte en pacientes con cáncer de pulmón. En el análisis interino, recientemente publicado, no se ha evidenciado un detrimento en la calidad de vida ni en la supervivencia global en aquellos pacientes que han recibido cuidados paliativos respecto de los tratados con RTHC11.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Este trabajo fue presentado como comunicación oral en las XI jornadas nacionales de la SECPAL. Valencia 5-6 de noviembre de 2015.