Cuantificar, describir el origen y estimar el coste de las solicitudes de antígeno prostático específico (PSA) con fines de cribado a varones de 70 años o más realizadas en una zona de salud urbana.
MétodosEstudio transversal. Se obtuvieron todas las determinaciones de PSA a pacientes adscritos a una zona de salud entre los años 2018 y 2020. Se clasificaron retrospectivamente como cribado (PSAc) o no, de acuerdo a criterios preestablecidos revisando historiales clínicos. Se comparó la edad de los pacientes sometidos a cribado con aquellos que no lo fueron. Se calcularon tasas de solicitud por centros y solicitantes de acuerdo a la población de referencia provista por el padrón municipal (VM70). Se estimó el coste consultando las tarifas de facturación.
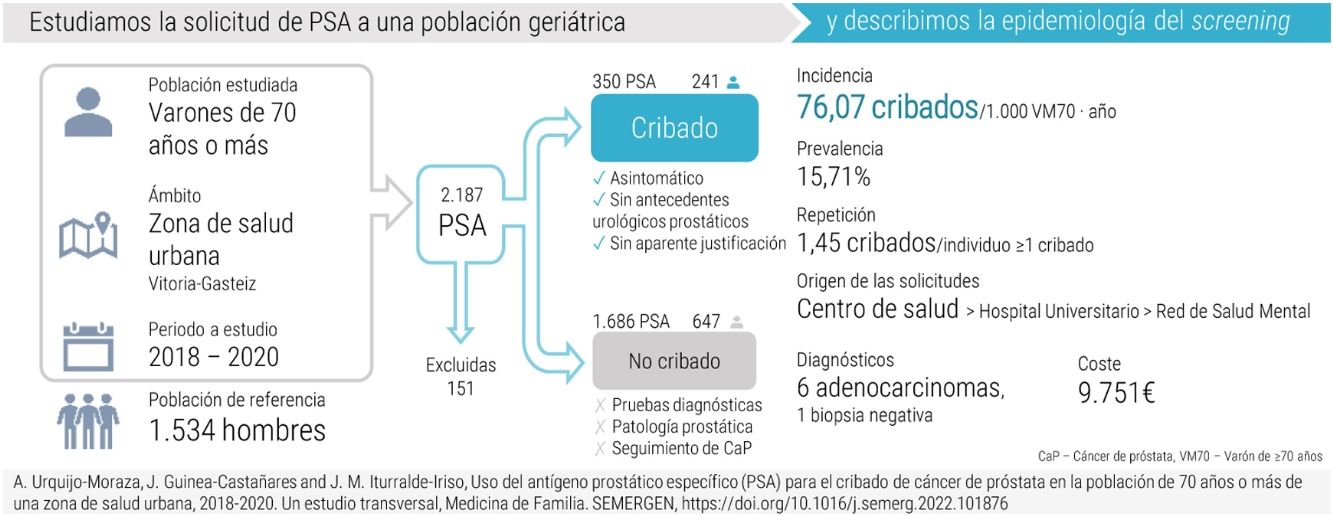
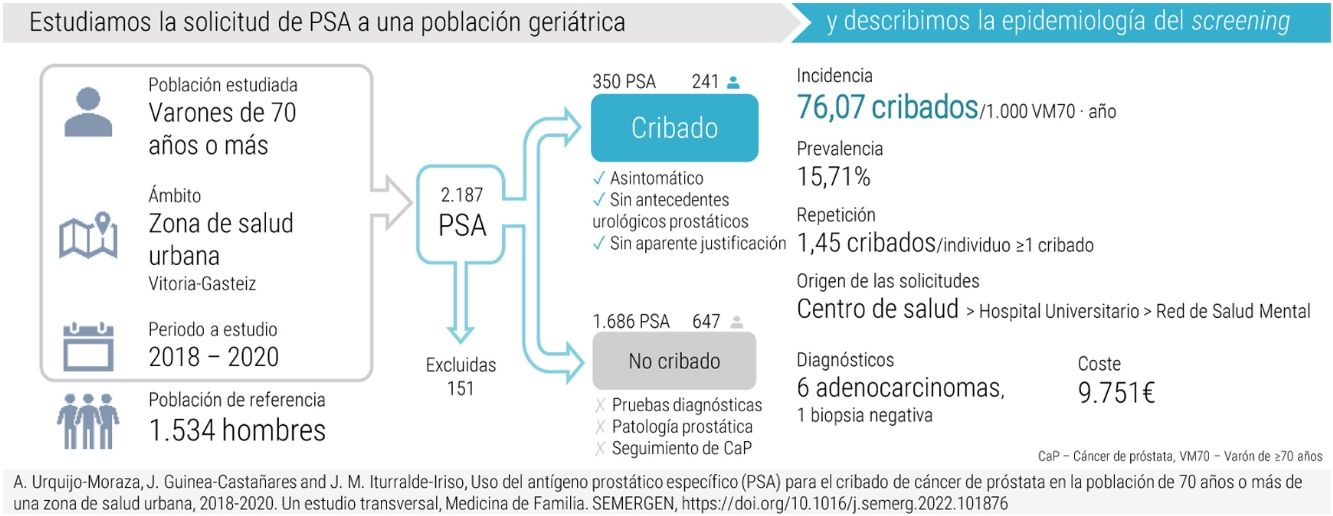
ResultadosFueron estudiadas 2.036 PSA, de 888 hombres ≥ 70 años, y 350 clasificadas como cribado. Se diagnosticaron seis adenocarcinomas. Se estimaron 76,07 PSAc/1.000 VM70-año con origen en cualquier centro, 1,45 solicitudes por individuo cribado, y una prevalencia de 15,71%; población media de referencia de 1.534 hombres (DE 45,37). Los pacientes sometidos a cribado (edad media 75 años, DE 4,04) fueron más jóvenes que aquellos no cribados (media 76,5, DE 4,81). Se estimó un coste del cribado de 9.751 €.
ConclusionesSe describe la epidemiología y estima el coste de los cribados con PSA a varones ≥ 70 años sin cáncer prostático en nuestra zona, en atención primaria y hospitalaria. Se trata de una práctica habitual, predominantemente en atención primaria, y en magnitud similar a la reportada en la bibliografía estatal.
To describe the epidemiology and estimate the cost of Prostate-Specific Antigen (PSA) screening tests to men ≥ 70 years old in an urban health zone.
MethodsA cross-sectional study was performed. We obtained every PSA test made in the health zone from 2018 to 2020, and classified them retrospectively as screening (PSAc) or not according to pre-established criteria, reviewing electronic health records. Testing rates were calculated by centres and clinical specialities. The standard population was provided by the city register of inhabitants (VM70). Cost estimation was made using our health system's price list.
ResultsTwo thousand and thirty six PSA, of 888 men ≥ 70 years old were obtained, and 350 met screening classification criteria. Six adenocarcinomas were diagnosed from those tests. We estimated 76.07 PSAc/1000 VM70-year from any centre, 1.45 tests for each screened individual, and 15.71% prevalence. The standard population was 1534 men (mean 2018-2020, SD 45.37). Patients who were screened (median age 75, SD 4.04) were younger than those not screened. We estimated a total screening test cost of 9,751 €.
ConclusionsThe epidemiology and cost of PSA screening tests to men ≥ 70 years old are reported, both in primary health care and in the hospital. PSA screening tests are common practice amongst professionals attending elderly men in our health zone, mostly in primary care. The screening testing rate of men without prostate cancer is similar to that reported in the literature.
El adenocarcinoma de próstata es la neoplasia urogenital más frecuente, la segunda en frecuencia en el varón, y el cáncer con mayor prevalencia en países con bajo y alto índice de desarrollo humano1. En España, en 2015, se estimó una incidencia de 146,4 casos/100.000 habitantes2. En Euskadi, la próstata es la principal localización de cáncer, y la tercera causa de muerte por patología oncológica del varón3.
El uso del PSA total para cribado ocasional del cáncer de próstata (CaP) es controvertido en la actualidad4, debido a que no se ha demostrado que disminuya la mortalidad específica por la enfermedad, y se ha asociado a sobrediagnóstico y sobretratamiento5,6. A fin de evitar biopsias o tratamientos innecesarios están emergiendo nuevos biomarcadores que pretenden mejorar la especificidad del PSA total y predecir mejor qué cánceres serán relevantes o agresivos7.
Tanto la United States Preventive Services Task Force (USPSTF)6 como la Sociedad Española de Medicina de Familia y Comunitaria, en su Programa de Actividades de Prevención y Promoción de la Salud (PAPPS)8 recomiendan en contra de la realización de determinaciones de PSA con fines de cribado del CaP en hombres asintomáticos cuyo riesgo de padecer dicho cáncer no sea elevado. La Asociación Europea de Urología (EAU) desaconseja el cribado del CaP con PSA a varones cuya expectativa de vida sea menor de 15 años9.
No obstante, la solicitud de PSA a varones ancianos sin CaP parece una práctica habitual en atención primaria10–12. En Valencia, la prevalencia de ≥ 1 PSA se estimó de 45,73% en hombres de 70-79 años sin CaP, y de 35,7% en aquellos de ≥ 80 años10. Aquellos médicos de familia que refirieron seguir guías de buena práctica clínica (PAPPS, EAU y USPSTF principalmente) finalizarían el cribado entre los 75-80 años, y los que no, en torno a los 80 años, siendo la periodicidad preferida anual o bianual11.
Páez et al.13 (en Getafe 1997-1999) reportaron 152,6 PSA/1.000 VM70-año y una razón promedio de 1,44 PSA/individuo. No determinaron la indicación de la prueba, ni los criterios de exclusión. Concluyeron que la incidencia de cribado en su medio era alta.
Oller Colom et al.14 observaron 838 determinaciones de PSA total ≥ 4 ng/mL realizadas en 1998 en un centro de atención primaria urbano de Barcelona que atendía a 4.422 hombres de 50 años o más, y reportaron 42 cribados, de los cuales, 13 pruebas (1,5% del total de analíticas que observaron) fueron realizadas a hombres de 70 años o más.
Cepeda-Piorno et al.15 (en Gijón 2000-2001) reportaron 27,43 solicitudes de PSA/100 varones ≥ 50 años-año, con origen en cualquier servicio. Un estudio ecológico con datos de atención primaria (en Ourense 2012) determinó una tasa de 36,6 solicitudes de PSA/100 varones ≥ 50 años, por año y cupo de atención primaria16.
Panach-Navarrete et al.10 estudiaron las solicitudes de PSA en centros de atención primaria en un área de salud de Valencia en 2011 y 2012, y reportaron una prevalencia de ≥ 1 PSA a pacientes de entre 70 y 79 años sin CaP conocido de 45,73%, y de 35,7% entre los de 80 años o más.
Hasta donde alcanza nuestro conocimiento, no existe literatura reciente acerca de la incidencia específica de PSA con fines de cribado en población geriátrica en España.
El cribado con PSA a pacientes mayores es práctica frecuente en otros países como Francia17, Suiza18, o Australia19. En EE. UU., la prevalencia del screening es alta en ≥ 70 años y no ha variado sustancialmente con las nuevas recomendaciones del USPSTF20.
Nuestra zona de salud contaba en 2018 con una población de más de 10.100 personas, de la cual, 14,7% eran varones de ≥ 70 años. Dicha población es atendida por un centro de salud con ocho cupos (CS), el Hospital Universitario de Álava (HUA) y la Red de Salud Mental de Álava (RSMA). Todos forman parte de la red asistencial de Osakidetza/Servicio Vasco de Salud. Osakidetza cuenta con un único sistema de información de historiales clínicos compartido por todos sus centros asistenciales. Médicos y enfermeras solicitan analíticas que pueden incluir PSA.
ObjetivosHipótesis: la solicitud de PSA como cribado oportunista de CaP a hombres de 70 años o más (VM70) sería una práctica clínica habitual en nuestro entorno.
Los objetivos son: determinar la incidencia de determinaciones de PSA a hombres de 70 años o más, con fines de cribado de CaP, en una zona de salud de Vitoria-Gasteiz; describir los diagnósticos realizados a partir del cribado oportunista, y estimar su coste.
Materiales y métodosSe realizó un estudio descriptivo transversal. Este informe sigue la declaración STROBE21.
ParticipantesA fin de estudiar la población masculina ≥ 70 años de la zona de salud, se observó a todos aquellos que pertenecieran a algún cupo de atención primaria del único centro de salud de la zona, y a los que se les hubiera solicitado al menos un PSA.
Criterios de inclusiónFueron incluidos en el estudio los pacientes que cumplieron todos los siguientes criterios: cuyo sexo fuera masculino, edad igual o mayor a 70 años en el momento de solicitud, cuyo médico de referencia perteneciera al centro de salud, y al cual se le hubiera solicitado al menos una determinación de PSA en el periodo del estudio.
Criterios de exclusiónFueron excluidos de este estudio: los pacientes desplazados de, o a otro centro de salud; los pacientes fallecidos en los dos años anteriores al inicio del periodo del estudio; y cualquier paciente que no cumpliera los criterios de inclusión.
Obtención de datosSe volcaron de forma agregada de las bases de datos del sistema de información sanitaria de la red pública todas las determinaciones de PSA solicitadas entre el 1 de enero del 2018 y el 31 de diciembre del 2020, ambos inclusive, a los varones nacidos antes del 1 de enero de 1951, y adscritos a la zona de salud en el momento de la solicitud.
Dado que todos los diagnósticos son codificados con un código CIE, se obtuvo la lista de los diagnósticos urológicos (suplemento) hasta la fecha de fin del estudio, sin límite de antigüedad; y la lista de prescripciones retiradas en farmacia de medicamentos urológicos (suplemento), del 2016 hasta la fecha de fin del estudio, de los pacientes representados en la base de datos anterior. El sistema pseudonimizó los datos con identificadores individuales aleatorios, únicos y comunes a todos los conjuntos.
Se calculó la edad del paciente en el momento de la solicitud restando la fecha de nacimiento a la fecha de la solicitud.
Una vez por cada analítica, se asignó al paciente una categoría (grupo previo a la solicitud) en función de los diagnósticos urológicos presentes en el momento de la solicitud, con arreglo a los criterios del suplemento: CaP, hiperplasia benigna de próstata (HBP), prostatitis, traumatismo perineal/prostático, síndrome de tracto urinario inferior (STUI), o sano. Los grupos previos CaP y HBP pudieron ser asignados por coincidencia con los códigos CIE, mientras que el resto fueron asignados manualmente.
Se accedió a las historias clínicas de los pacientes cuyos datos eran incompletos, dudosos, o sin antecedentes urológicos, y se verificaron los criterios de inclusión/exclusión, los antecedentes, las prescripciones farmacológicas en activo en dichas fechas, y la indicación de la prueba y la presencia de clínica. Solo en aquellas pruebas clasificadas como cribado, se estudió la derivación a urología, la realización de biopsia y el diagnóstico final.
Se calculó el grupo de riesgo de D’Amico22 a los pacientes diagnosticados de adenocarcinoma por medio de un cribado y estadiaje T2c o menor.
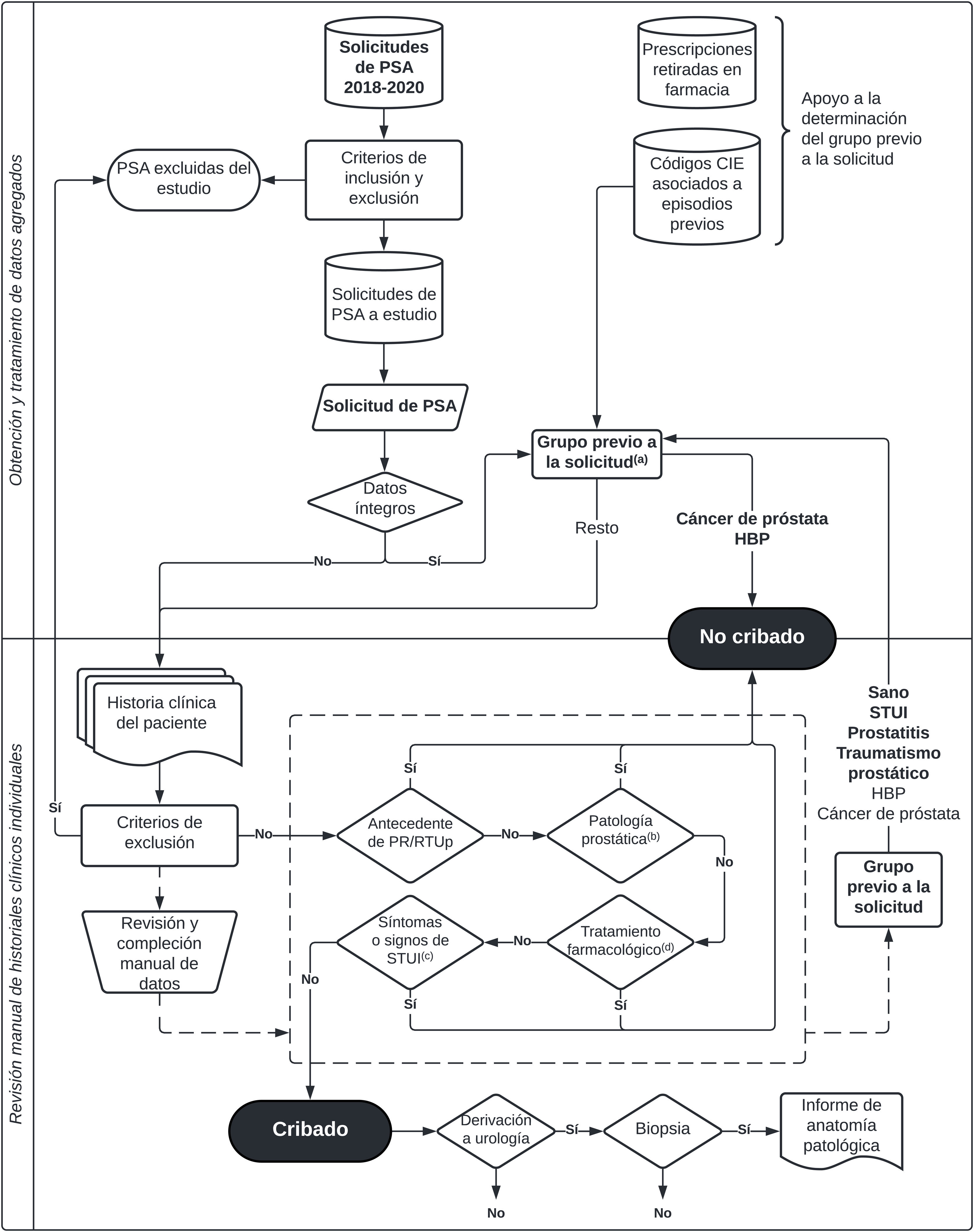
La figura 1 sintetiza esta metodología.
Obtención de los datos y sistemática de clasificación de solicitudes de PSA como «cribado» o «no cribado», y de los pacientes en grupos previos a la solicitud.
Se obtuvieron tres bases de datos pseudonimizados con un número identificador del individuo común de los sistemas de información del sistema público vasco de salud: las solicitudes de analíticas que contuvieron PSA (2018-2020), las prescripciones de medicamentos retiradas por el paciente en oficina farmacia (2016-2020) y los códigos CIE-9-MC y CIE-10 diagnóstico asociados a los historiales clínicos del paciente (hasta el 31/12/2020, inclusive). Tras la retirada de las entradas cuyos individuos no cumplían criterios de inclusión, se verificó la integridad de los datos; las entradas con campos faltantes fueron revisadas manualmente. Buscando coincidencias entre las tres bases citadas, en base a los criterios del Suplemento, se establecen los grupos previos «cáncer de próstata» e «hiperplasia benigna de la próstata». Tras la comprobación de los criterios definitorios de cribado, y del contexto clínico del paciente, se clasificó cada solicitud como «cribado» o «no cribado» y se completaron los grupos previos a la solicitud faltantes (ibidem). Finalmente, se estudió el resultado diagnóstico de los cribados.
(a) Véase el suplemento para la definición de los grupos previos a la solicitud. (b) Patología prostática, de acuerdo al Suplemento. (c) Se consideró STUI a la presencia de al menos un signo o síntoma de los descritos por Abrams et al., 200212, en el historial del acto clínico que dio lugar a la solicitud de la analítica, o el inmediatamente anterior. (d) Consulte en suplemento los grupos farmacológicos considerados para la asignación a cada grupo previo.
HBP: hiperplasia benigna de la próstata; PR: prostatectomía radical; RTU: presección transuretral de próstata; STUI: síndrome del tracto urinario inferior.
Se consideraron «con fines de cribado» (cribado, PSAc) aquellas solicitudes de PSA realizadas a pacientes asintomáticos, sin patología urológica aguda o crónica conocida, ni tratamiento activo con medicamentos empleados en terapéutica urológica, y que en la historia clínica del acto que diera lugar a la solicitud o el inmediatamente anterior no constara sintomatología urinaria (suplemento). Se consideró sintomatología urinaria la presencia de ≥1 síntoma o signo de STUI23, hematuria y/o hemospermia.
Solo las solicitudes de pacientes del grupo previo sano pudieron ser clasificadas como cribado. El resto de solicitudes, incluyendo las de pacientes con CaP, fueron consideradas como «sin fines de cribado» (no cribado).
Demografía de la población de referenciaSe consultó a la Oficina del Padrón Municipal el número de hombres de 70 años o más empadronados en las secciones municipales que componen la zona básica de salud, a fecha de 1 de enero de los años 2018, 2019 y 2020, desglosado por grupos etarios de 10 años.
Métodos estadísticosPara el análisis estadístico se usó R 4.1.124.
Se calcularon la media (M), la mediana (Me) y las desviaciones estándar (DE) para las variables numéricas. Se reportan frecuencias y porcentajes para las variables categóricas.
La edad de los pacientes de las solicitudes de cribado se comparó con las de no cribado por medio del test de suma de rangos de Wilcoxon (ajuste de Bonferroni). Se reporta r (Cohen25) como medida de tamaño de efecto (TE).
Para el estudio de la incidencia de cribados oportunistas, se calculó la tasa de solicitudes por 1.000 habitantes-año [(1.000 x número de cribados):(población de referencia x años)].
El promedio de la población de la zona al 1 de enero de cada año constituyó la población de referencia.
Se calcularon, además, la proporción de individuos con ≥ 1 petición de PSA sobre la población de referencia, como medida de prevalencia; y la razón de cribados por individuo al que se le hubiera realizado al menos un cribado, como indicador de repetición.
Elaboramos tablas de frecuencia ajustando por centro de origen, servicio del solicitante, categoría profesional, y clasificación de la prueba.
Estimación del coste del cribadoConsultamos las «tarifas para facturación de servicios sanitarios y docentes de Osakidetza» de los ejercicios 201726, 201827, 201928 y 202029.
Se calculó el coste por analítica de acuerdo a la tarifa en vigor en el momento de cada solicitud, sumando al coste unitario de PSA total y/o libre, el de gestión de muestra y el de extracción. Se asumió una determinación de PSA libre por cada cociente. Se calculó el coste por diagnóstico, sobre el total del cribado.
Limitación de sesgosLa realización de este estudio se ciñó a criterios prestablecidos. Los datos dudosos o incompletos fueron revisados manualmente y retirados si procedía. Se excluyeron las entradas duplicadas. No se aplicó enmascaramiento de los datos, debido a limitaciones técnicas y temporales. A fin de limitar el error subjetivo, se predefinieron criterios de inclusión y exclusión, y de definición de cada categoría y variable relevante.
Ética en la investigaciónEl Comité de Ética en la Investigación Clínica de la Organización Sanitaria Integrada Álava aprobó este trabajo (expediente sin código 2021-088 TFG), concediendo una exención del consentimiento informado.
ResultadosParticipantes y solicitudes de PSAEntre el 1 de enero del 2018 y el 31 de diciembre del 2020, se solicitaron 2.187 PSA a 935 hombres nacidos antes del 1 de enero de 1951 adscritos a la zona de salud; 151 PSA (89 individuos) fueron excluidos.
Dos mil treinta y seis (2.036) solicitudes de PSA, correspondientes a 888 varones de ≥ 70 años fueron incluidas en el análisis. La población de referencia la compusieron 1.534 personas (DE = 45,37); 350 (17,2%) analíticas fueron clasificadas con fines de cribado, y 1.686 (82,8%) como no de cribado.
La media de edad en el momento de la solicitud fue de 76,2 años (Me = 75, DE = 4,72). Para el grupo de solicitudes de cribado la edad promedio fue 75 años (Me = 74, DE = 4,04); en el grupo no cribado la edad promedio fue 76,5 años (Me = 75, DE = 4,81). La diferencia entre la mediana de edad de ambos grupos fue estadísticamente significativa (W = 242.597,5, p < 0,001, IC -2,00 – -1,00; TE pequeño r = 0,12, IC 0,07-0,16).
Epidemiología del cribado oportunista de CaP con PSASe ha calculado una tasa de cribado de 76,07 solicitudes de PSA por cada 1.000 varones ≥ 70 años (VM70)-año, en tres años y todos los centros, para la población de referencia en la zona básica de salud.
En todo el periodo 2018-2020 se solicitó al menos un cribado con PSA a 241 hombres (M anual = 110,67, DE = 8,33), 15,71% del promedio la población de referencia de los tres años (tabla 1). Se realizaron 1,45 cribados con PSA por cada individuo ≥ 1 cribado (M anual = 1,08, DE = 0,01).
Demografía de la muestra e incidencia y prevalencia de cribado oportunista de cáncer de próstata con PSA en la zona básica de salud (solicitudes con cualquier centro de origen)
| P. Ref. | Muestra | Cribados oportunistas con PSA | Incidencia de cribado | ||||||
|---|---|---|---|---|---|---|---|---|---|
| Año, y rango de edad | Edad | Individuos≥ 1 cribado | PSAc | PSAc/1.000 VM70 | PSAc/ind. ≥ 1 cribado | Ind. ≥ 1 cribado(% P. Ref.) | |||
| N | n | M | DE | ||||||
| Incidencia de PSAc/1.000 varones ≥ 70 años-año (3 años): | |||||||||
| 2018-2020 | 1.534* | 888 | 75,0 | 4,04 | 241 | 350 | 76,07** | 1,45 | 15,71 |
| Incidencia de PSAc/1.000 varones ≥ 70 años (anual): | |||||||||
| 2018 | 1.482 | 525 | 74,6 | 3,66 | 120 | 131 | 88,39‡ | 1,09 | 8,10% |
| 70-79 | 1.104 | 103 | 103 | 114 | 103,26 | 1,11 | 9,33% | ||
| 80-89 | 332 | 17 | 17 | 17 | 51,20 | 1,00 | 5,12% | ||
| 90-99 | 45 | 0 | 0 | 0 | – | – | – | ||
| 100 + | 1 | 0 | 0 | 0 | – | – | – | ||
| 2019 | 1.552 | 440 | 74,4 | 3,33 | 104 | 111 | 71,52‡ | 1,07 | 6,70% |
| 70-79 | 1.149 | 97 | 97 | 104 | 90,51 | 1,07 | 8,44% | ||
| 80-89 | 352 | 7 | 7 | 7 | 19,89 | 1,00 | 1,99% | ||
| 90-99 | 51 | 15 | 0 | 0 | – | – | – | ||
| 100 + | 0 | 0 | 0 | 0 | – | – | – | ||
| 2020 | 1.567 | 497 | 76,1 | 4,89 | 101 | 108 | 68,92‡ | 1,07 | 6,45% |
| 70-79 | 1.146 | 83 | 83 | 90 | 78,53 | 1,08 | 7,24% | ||
| 80-89 | 367 | 15 | 15 | 15 | 40,87 | 1,00 | 4,09% | ||
| 90-99 | 53 | 3 | 3 | 3 | 56,60 | 1,00 | 5,66% | ||
| 100 + | 1 | 0 | 0 | 0 | – | – | – | ||
Población de referencia para el cálculo de la tasa de cribado/1.000 VM70-año: redondeo a la unidad de la media aritmética 2018-2020 (DE = 45,37).
Incidencias de PSAc/1.000 varones ≥70 años, 2018-2020: M = 76,28 PSAc/1.000 varones ≥ 70 años (DE = 10,57).
Fuente de la población de referencia: Oficina del Padrón Municipal de Vitoria-Gasteiz, a 1 de enero de cada año.
P. Ref. población de referencia; N/n: número de individuos en P. Ref. (N) o Muestra (n); ind.: individuos; M: media aritmética; DE: desviación estándar; PSAc: solicitudes de PSA clasificadas como cribado; VM70: varones de edad igual o mayor a 70 años; %P. Ref.: porcentaje de la población de referencia.
Excluidos los varones con CaP, indistinta la finalidad, y en todo el periodo, se solicitaron 154,4 PSA/1.000 VM70-año desde cualquier centro (0,85 PSA/individuo ≥ 1 PSA); 243,4 PSA/1.000 VM70-año solicitados en el centro de salud (0,61 PSA/individuo ≥ 1 PSA). Se realizaron 442,51 PSA/VM70-año, cualquiera que fuese el centro de origen o la patología del paciente. La prevalencia global de solicitud de ≥ 1 PSA sobre la población de referencia fue de 57,9%, sin ajuste en función de los antecedentes del paciente.
Trescientos dos (86,3%) solicitudes de PSA de cribado provinieron del centro de salud, 47 (13,4%) del HUA, y 1 (0,3%) de la RSMA (tabla 2).
Solicitudes de PSA a pacientes de la zona de salud en 2018-2020, por categoría y origen de la solicitud
| Origen de la solicitud (centro, grupo del profesional y servicio) | Cribado | No cribado | Total | |||
|---|---|---|---|---|---|---|
| Cant. | % (col.) | Cant. | % (col.) | Cant. | % (col.) | |
| Centro de salud | 302 | 86,29% | 818 | 48,52% | 1.120 | 55,01% |
| Medicina, adjunto de | 290 | 82,86% | 782 | 46,38% | 1.072 | 52,65% |
| Medicina de familia y comunitaria | 290 | 82,86% | 782 | 46,38% | 1.072 | 52,65% |
| Medicina, interno residente de | 2 | 0,57% | 8 | 0,47% | 10 | 0,49% |
| Medicina de familia y comunitaria | 2 | 0,57% | 8 | 0,47% | 10 | 0,49% |
| Enfermería* | 10 | 2,86% | 28 | 1,66% | 38 | 1,87% |
| Hospital Universitario de Álava‡ | 47 | 13,43% | 868 | 51,48% | 915 | 44,94% |
| Medicina, servicio de | 47 | 13,43% | 868 | 51,48% | 915 | 44,94% |
| Urología | 4 | 1,14% | 601 | 35,65% | 605 | 29,72% |
| Oncología médica | 3 | 0,86% | 94 | 5,58% | 97 | 4,76% |
| Oncología radioterápica | 0 | 0,00% | 91 | 5,40% | 91 | 4,47% |
| Otros servicios | 39 | 11,14% | 80 | 4,73% | 119 | 5,99% |
| No codificado/desconocido | 1 | 0,29% | 2 | 0,12% | 3 | 0,15% |
| Enfermería* | 0 | 0,00% | 0 | 0,00% | 0 | 0,00% |
| Red de Salud Mental de Álava‡ | 1 | 0,29% | 0 | 0,00% | 1 | 0,05% |
| Medicina, servicio de | 1 | 0,29% | 0 | 0,00% | 1 | 0,05% |
| Psiquiatría | 1 | 0,29% | 0 | 0,00% | 1 | 0,05% |
| Enfermería* | 0 | 0,00% | 0 | 0,00% | 0 | 0,00% |
| Total | 350 | 100% | 1.686 | 100% | 2.036 | 100% |
La incidencia fue de 65,64 PSAc/1.000 VM70-año en el CS; 10,22 PSAc/1.000 VM70-año en el HUA, y 0,22 solicitudes de PSAc/1.000 VM70-año en la RSMA, con la población de referencia de la zona básica de salud.
Resultado diagnóstico de las solicitudes de PSA de cribadoDe 241 individuos sometidos a cribado oportunista con PSA, seis fueron diagnosticados de CaP (tabla 3).
Descripción del curso de las derivaciones por cribado positivo y diagnóstico final
| Pacientes sometidos a cribado oportunista con PSA | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Derivación a urología | Pacientes derivados a urología | Anatomía patológica de la biopsia | |||||||
| Solicitudes | Derivados4 | No derivados5 | Biopsiados6 | No biopsiados | Cáncer de próstata9 | Benigna10 | |||
| [PSAt]p1 | PSAc2 | Individuos3 | No enviados7 | Decisión especia-lista8 | |||||
| < 4* | 313 | 214 | 3 | 211 | 0 | 211 | 3 | 0 | 0 |
| 4-10 | 37 | 29 | 12 | 17 | 7 | 17 | 5 | 6 | 1 |
| > 10 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
| Total | 350 | 241‡ | 15 | 228 | 7 | 228 | 8 | 6 | 1 |
1 [PSAt]p representa la concentración sérica de PSA total (ng/mL). 2 Cantidad de solicitudes de PSA con fines de cribado. 3 Individuos que han sido sometidos a un cribado oportunista con PSA en el C. S. 4 Individuos derivados a un Servicio de Urología tras realizarse dicho cribado. 5 Individuos que no fueron derivados a un Servicio de Urología tras realizarse dicho cribado. 6 Individuos derivados a un Servicio de Urología que fueron sometidos a biopsia de la próstata por cualquier método. 7 Individuos que no fueron biopsiados por no haber sido enviados a un Servicio de Urología. 8 Individuos derivados a un Servicio de Urología que no fueron biopsiados por decisión del especialista. 9 Individuos sometidos a biopsia de la próstata por cualquier método, cuyo diagnóstico anatomopatológico final fuera de adenocarcinoma prostático, indistintamente del subtipo histológico, grados de Gleason y/o clasificación de riesgo de D’Amico; inclusive el adenocarcinoma in situ de próstata. 10 Individuos sometidos a biopsia de la próstata por cualquier método, cuyo diagnóstico anatomopatológico final fuera de hiperplasia benigna de la próstata (HBP) u otra patología no neoplásica.
La edad media de los pacientes diagnosticados fue 75,3 años (DE = 4,97), y la concentración sérica de PSA total 6,70 ng/mL (DE = 1,36).
Los grados de Gleason más frecuentes fueron 3 + 3 (n = 2) y 3 + 4 (n = 2), seguidos de 4 + 3 (n = 1), y 4 + 4 (n = 1). Todos fueron ≤ T2c, localizados. Según la clasificación D’Amico para CaP localizado, cuatro sujetos fueron de riesgo intermedio (3 + 3, n = 1; 3 + 4, n = 2; 4 + 3, n = 1), uno bajo (3 + 3, n = 1), y uno alto (4 + 4, n = 1).
Estimación del coste del cribadoEl coste total estimado del cribado fue 9.751,00 € por 350 determinaciones de PSA total, y 27 de PSA libre (cociente de PSA), tomando en consideración los costes de extracción y gestión. Cada diagnóstico de cáncer con cribado oportunista en la zona de salud supuso un coste de 1.625,17 €.
DiscusiónLa incidencia de cribados fue de 76,07 PSAc/1.000 VM70-año, la prevalencia de ≥ 1 cribado, del 15,71%, y se realizaron 1,45 cribados por individuo. La mayor parte de las solicitudes provino del centro de salud. Los resultados indican que la solicitud de PSA para cribado oportunista de CaP es una práctica habitual sobre la población de la zona de salud estudiada, en todos los ámbitos asistenciales.
Estimamos una tasa de solicitud de PSA, excluidos los pacientes con cáncer, muy similar al dato informado en Getafe (1997-1999)13. Ha de tenerse en cuenta que el citado se elaboró hace más de 20 años, cuando la evidencia acerca de los beneficios del cribado era insuficiente, y las recomendaciones contradictorias30.
La proporción de cribados solicitados a varones ≥70 años con un resultado ≥ 4 ng/mL obtenida en nuestro centro de salud fue similar a la reportada en otro CS en 199814: 1,8% (37 cribados PSAt ≥4 ng/mL).
Debido a la diferencia de composición etaria de la población de referencia, nuestros resultados no son comparables con aquellos de Cepeda-Piorno et al.15 ni Díaz Grávalos et al.16
En nuestra zona de salud, la prevalencia de varones ≥ 70 años con al menos una PSA con cualquier fin solicitados en el centro de salud, en pacientes sin CaP, es de 39,12%; cifra similar a la calculada en Valencia10. Ello orienta a pensar que la práctica clínica en relación a la solicitud de PSA sería similar en ambos territorios.
Los resultados obtenidos son coherentes con Juliá Romero et al.11 y Panach-Navarrete et al.10,12 cuando concluyen que el cribado con PSA es una práctica arraigada entre los profesionales de atención primaria. No obstante, ignoramos los factores que condicionan la solicitud de cribados por parte de los profesionales sanitarios a los pacientes estudiados.
Limitaciones del estudioDebido al método de muestreo, la inferencia está limitada a la población estudiada. Se podría haber incurrido en clasificación incorrecta o sesgo de memoria debido a errores de codificación informática o de las historias clínicas, riesgo inherente al diseño retrospectivo.
Las determinaciones de PSA solicitadas fuera de la red asistencial pública vasca no fueron estudiadas.
No se han podido obtener los valores de PSA libre, y han debido ser calculados a partir del cociente, aunque no se han empleado en ningún análisis.
La metodología de este estudio no es adecuada para valorar la eficacia del cribado oportunista de CaP; dicho dato se ofrece con fines descriptivos.
ConclusionesLa solicitud de determinaciones de PSA con fines de cribado del CaP es una práctica frecuente, principalmente en atención primaria de salud, en la zona de salud estudiada.
La persistencia de esta controvertida práctica, si bien actualmente está desaconsejada en este grupo de edad, amerita que se estudien los motivos de solicitud de las pruebas, así como el sustento racional del cribado por parte de sus practicantes.
Se ha cuantificado el coste al sistema público que supone la práctica de cribados desaconsejados.
Resultaría de interés investigar la percepción y el nivel de formación acerca del cribado del CaP entre los profesionales sanitarios de los centros estudiados, ya que ayudarían a contextualizar nuestros resultados. Asimismo, se muestra necesario estudiar la incidencia de cribado en otros territorios en el grupo específico de población de hombres de 70 años o mayores, en el cual la recomendación en contra del cribado por parte de diferentes sociedades es generalizada.
FinanciaciónLa presente investigación no ha recibido ayudas específicas provenientes de agencias del sector público, sector comercial o entidades sin ánimo de lucro.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.