Actualmente disponemos de 3 familias de fármacos que son los que se utilizan habitualmente en la práctica clínica y que ayudan a los fumadores a dejar de serlo: la terapia sustitutiva con nicotina, bupropión y vareniclina. El conocimiento resumido de las particularidades, eficacia y contraindicaciones de cada uno de ellos nos puede resultar útil para realizar una prescripción adecuada a nuestros pacientes.
There are currently three families of drugs that are commonly used in the clinic to help smokers to stop; nicotine replacement therapy, bupropion and varenicline. Summary knowledge of the specific efficacy and contraindications of each of them can be useful before prescribing them to our patients.
Todos los médicos de atención primaria debemos tener muy en cuenta 2 importantes características del tabaquismo. Por un lado, que es la primera causa de muerte prematura en los países desarrollados, y, por otro, que es una adicción que comporta vulnerabilidad a la recidiva durante largo tiempo, lo cual avala su reconocimiento como enfermedad crónica. Por ello, los médicos están obligados a intervenir siempre sobre el tabaquismo de sus pacientes proporcionándoles el asesoramiento, el apoyo y el tratamiento farmacológico idóneo que les ayuden a abandonar definitivamente el consumo del tabaco. Los médicos de familia, como profesionales sanitarios que atienden en primer lugar las enfermedades directamente relacionadas con el consumo del tabaco, tienen incluso una mayor responsabilidad en este aspecto.
El tratamiento farmacológico del tabaquismo tiene por objetivo fundamental combatir la dependencia física que el fumador presenta de la nicotina. A continuación vamos a describir resumidamente las principales características de los fármacos más utilizados1,2, lo que nos ayudará a decidir cuál es el más adecuado ante cada paciente concreto al que tengamos que prescribir este tratamiento3–8.
Los tratamientos farmacológicos de primera línea son: los sustitutivos de nicotina (TSN) en todas sus formas, el hidrocloruro de bupropión y la vareniclina (aprobados por la FDA para esta indicación). También se pueden utilizar como fármacos de segunda línea el clorhidrato de nortriptilina y el clorhidrato de clonidina (no aprobados por la FDA para esta indicación), por lo que en la práctica no se suelen utilizar para la deshabituación tabáquica.
Terapia sustitutiva con nicotinaLa nicotina es la sustancia del cigarrillo que provoca la adicción del tabaco. Cuando un fumador inhala el humo de su cigarrillo, en tan solo 8 s la nicotina hace su efecto en los receptores nicotínicos del cerebro. La nicotina que se libera del cigarrillo y que pasa a la corriente sanguínea, tiene la particularidad de producir concentraciones plasmáticas de 25 a 30ng/ml. El grupo de Hughes et al.9 demostró que los fumadores mantienen unas concentraciones de nicotina en plasma de 20 a 40ng/ml, y que son necesarios unos niveles de 10 a 15ng/ml, para que el fumador no desarrolle los síntomas del síndrome de abstinencia9.
Pues bien, había que buscar un tratamiento para mitigar el síndrome de abstinencia que se produce cuando un fumador deja de administrarse la nicotina, y es cuando surge la TSN. Se define la TSN como la administración de nicotina por una vía diferente a la del consumo del cigarrillo, y en una cantidad suficiente para disminuir los síntomas del síndrome de abstinencia, pero insuficiente para crear dependencia. La administración se hace por vía oral, si se trata de chicles de nicotina, inhalador bucal, caramelos de nicotina, tabletas sublinguales, por vía transdérmica si se utilizan los parches de nicotina, y por vía nasal si se utiliza el inhalador nasal.
En cualquiera de las formas de TSN, la concentración plasmática de nicotina nunca alcanza los niveles que se obtienen cuando se fuma un cigarrillo. Con la TSN se obtienen valores que superan los 10ng/ml.
El tratamiento del tabaquismo con TSN4,10–13 debe durar entre 2 y 3 meses. Es muy importante que se indique al fumador la necesidad de que cumpla el tratamiento en su totalidad, pues muchas recaídas se producen por el incumplimiento o por la mala aplicación y dosificación del mismo. Los parches de nicotina producen una liberación transdérmica media de 0,9mg de nicotina/hora en un periodo de 16 h. En los parches con dosis más bajas dicha liberación desciende a 0,5mg/h. Se pueden utilizar hasta 16 piezas de chicle de nicotina de 4mg en un periodo de 24 h. El inhalador nasal de nicotina libera 0,5mg de nicotina por nebulización. Se recomienda una nebulización en cada fosa nasal, que corresponde a 1mg de nicotina en total. Se recomienda 2 o un máximo de 3 dosis por hora. Es muy importante la correcta utilización de la TSN por el paciente fumador. En este sentido el parche de nicotina se aplicará en la piel sin pelo, fundamentalmente en brazos, hombro y espalda, cambiando cada día el lugar de aplicación.
Hay que airear el parche antes de su colocación, una vez retirado el protector. Es necesario indicar al fumador que no debe fumar mientras utilice la TSN.
En cuanto al chicle de nicotina, hay que indicar al fumador que tenga paciencia para percibir sus efectos, pues no es tan rápido como la nicotina del cigarrillo. Debe masticar despacio el chicle de nicotina hasta que note su sabor o picor, en este momento dejará de masticar, y lo guardará entre su mejilla y la encía hasta que desaparezca el sabor, y cuando esto ocurra volverá a masticar el chicle. Como ejemplo de dosis necesaria y tiempo recomendado de uso de la TSN vamos a exponer el de los chicles. Existen chicles con un contenido de nicotina de 2mg o bien de 4mg, recomendándose uno u otro en función del nivel de dependencia del fumador: En fumadores de 10 a 19 cigarrillos al día, puntuación en el test de Fagerström menor o igual a 3 y con niveles de monóxido de carbono en el aire espirado menores a 15ppm, se pueden utilizar de 8 a 10 chicles de 2mg de nicotina al día, durante un periodo de 8 a 10 semanas, reduciéndose progresivamente la dosis a partir de la cuarta semana. En fumadores de 20 a 30 cigarrillos al día, con 4 a 6 puntos en el test de Fagerström y con niveles de monóxido de carbono entre 15 y 30ppm se recomienda utilizar un chicle de 4mg cada 90 min mientras el sujeto esté despierto, durante un periodo de 12 semanas; se recomendará reducir la dosis de forma progresiva a partir de la sexta semana. En fumadores de más de 30 cigarrillos al día, con 7 o más puntos en el test de Fagerström y con más de 30ppm de monóxido de carbono se recomienda utilizar un chicle de 4mg cada 60 min mientras el sujeto esté despierto, durante 12 semanas, reduciéndose progresivamente la dosis a partir de la octava semana.
La utilización del comprimido de nicotina es similar a la del chicle, en lugar de masticar la pieza de chicle, chupará lentamente el comprimido.
Por último el inhalador de nicotina, que es el que produce mayor concentración plasmática de nicotina de todas las formas de TSN, debe aplicarse una instilación en cada fosa nasal, y no es necesario hacer una inspiración al tiempo que se instila.
Las contraindicaciones comunes de la TSN son: infarto agudo de miocardio reciente, arritmias cardíacas, ictus reciente y angina inestable. Las contraindicaciones relativas son: hipertensión grave, insuficiencia cardíaca grave, enfermedad vascular cerebral, hipertiroidismo, diabetes insulinodependiente, úlcera gastroduodenal y deterioro renal o hepático grave. No se han detectado interacciones clínicamente significativas.
Los efectos secundarios comunes en la aplicación de la TSN son: cefalea, mareos, náuseas, vómitos, palpitaciones y fibrilación auricular.
BupropiónEl bupropión de liberación retardada (sustained-release bupropion, SR) es un polvo blanco y amargo que se expende en forma de comprimidos de liberación sostenida que contienen 150mg de sustancia activa. No se conoce con exactitud el mecanismo de acción de este fármaco, aunque se sabe que actúa en el núcleo accumbens inhibiendo la recaptación neuronal de dopamina; este efecto explicaría la reducción del craving (deseo o ansia por el consumo de droga, en este caso tabaco) que experimentan los fumadores cuando lo utilizan14.
También inhibe la recaptación neuronal de noradrenalina en el locus caeruleus, consiguiendo con ello una reducción significativa de la intensidad de los síntomas del síndrome de abstinencia de nicotina (ansiedad, irritabilidad, nerviosismo, trastornos del sueño, etc.14. El bupropión es un inhibidor funcional no competitivo de los receptores nicotínicos de acetilcolina. Esta actividad antinicotínica puede contribuir a su eficacia en el tratamiento de la dependencia nicotínica. El bupropión en dosis de 300mg/día durante un periodo de 7 semanas se asocia con un incremento significativo de la abstinencia continua a las 7 semanas de tratamiento (OR=2,71; IC del 95%: 1,88-4,07) y a los 12 meses de seguimiento (OR=2,10; IC del 95%: 1,62-2,73)15. Además se ha determinado que la eficacia de esta medicación está relacionada con la dosis, con su concentración plasmática media y con la concentración sanguínea de sus metabolitos16. Los fumadores que utilizan bupropión en dosis de 100, 150 o 300mg diarios tienen 1,42; 1,69 y 2,84 veces más probabilidades de dejar de fumar que los que reciben placebo, respectivamente. Finalmente, el National Institute for Clinical Excellence (NICE) ha realizado un metanálisis con 10 ensayos clínicos aleatorizados que incluyen más de 3.800 fumadores y ha demostrado que la OR para el éxito en la abstinencia, comparando bupropión con placebo, es de 2,16 (IC del 95%: 1,51-3,10)17. Es decir, el 19% de los fumadores que recibieron bupropión permanecieron completamente abstinentes al cabo de un año de seguimiento, frente a solo el 9% de los que recibieron placebo.
El bupropión debe ser utilizado durante un periodo de 7 a 9 semanas en dosis de 300mg/día en 2 tomas de 150mg. El tratamiento se iniciará de 7 a 15 días antes de abandonar definitivamente el consumo del tabaco. Durante la primera semana el sujeto consumirá solo un comprimido de 150mg cada día, y después de este período la dosis se incrementará a 2 comprimidos de 150mg. No debe superarse esa dosis de 300mg/día. Conviene tomar un comprimido a primera hora de la mañana, en el momento de levantarse, y el segundo 8 h después1,18–21. No existe contraindicación para prolongar más el tratamiento si se considerase necesario.
El bupropión está contraindicado en aquellos fumadores con: convulsiones, historia previa de bulimia o anorexia nerviosa, cirrosis hepática grave, historia de trastorno bipolar. También está contraindicado el uso concomitante de bupropión e inhibidores de la monoaminooxidasa. Respecto a sus interacciones, bupropión es metabolizado primariamente a hidroxibupropión por la isoenzima CYP2B6, por lo tanto el uso concurrente con fármacos que afecten a su metabolismo, como orfenadrina y ciclofosfamida, puede aumentar sus efectos farmacológicos. Las combinaciones conteniendo cualquiera de las siguientes medicaciones (alcohol, inductores e inhibidores de enzimas hepáticas, ritonavir, levodopa), dependiendo de la cantidad presente, también pueden interactuar con esta medicación. Los efectos secundarios más comúnmente hallados son náuseas, cefalea, rinitis, boca seca e insomnio19.
VareniclinaVareniclina es un agonista parcial de los receptores α4β2 de la nicotina que está siendo utilizado como tratamiento farmacológico del tabaquismo.
Las principales novedades de vareniclina hacen referencia a su descubrimiento y a sus especiales características bioquímicas y de biodisponibilidad. Vareniclina es un fármaco específicamente desarrollado para ayudar a los fumadores a dejar de fumar. Por ello, se buscó un medicamento que estimulara de forma selectiva los receptores nicotínicos de las neuronas del área tegmental ventral del meséncefalo. Vareniclina se desarrolló como un agonista parcial de estos receptores. Al ser agonista parcial cumpliría características comunes a los agonistas y a los antagonistas. Por ser un agonista tiene la capacidad de estimular el receptor nicotínico y por ello es capaz de controlar el craving y el síndrome de abstinencia de la nicotina que los fumadores presentan cuando están dejando de serlo. Pero, por ser un antagonista, es capaz de bloquear los efectos que la nicotina produce sobre el receptor, por ello, la utilización de vareniclina en un fumador que está dejando de fumar facilita que las recaídas no se acompañen de sensación placentera y recompensa, y con esto, vareniclina está impidiendo que una recaída se convierta en fracaso22.
Pero otra de las características definitorias de este fármaco es su biodisponibilidad. Vareniclina es un fármaco que se elimina casi en su totalidad a través de la orina sin metabolización hepática. Es esta característica la que hace que vareniclina no tenga problemas de interacción con otros medicamentos22.
Si destacamos los principales ensayos clínicos con esta molécula23–26, los primeros se llevaron a cabo con el objetivo fundamental de encontrar la dosis óptima de vareniclina, es decir, la dosis a la cual este fármaco es más eficaz y produce menos efectos adversos. Posteriormente se evaluó la eficacia y seguridad de uso de vareniclina frente a bupropión y a placebo26. Otros han servido para analizar la eficacia de la utilización de este fármaco a largo plazo. Todos han sido estudios aleatorizados doble ciego y controlados con placebo. Han incluido a un elevado número de fumadores en cada uno de los grupos y han obtenido resultados valorables.
Ha quedado establecido que vareniclina en dosis de 1mg dos veces al día durante 12 semanas es eficaz y seguro como tratamiento de la dependencia del tabaco. Durante la primera semana los sujetos podrán fumar y deberán utilizar el fármaco en dosis de 0,5mg una vez al día durante los 3 primeros días y después a dosis de 0,5mg dos veces al día hasta completar la primera semana. Pasado este tiempo, el sujeto deberá abandonar el consumo de tabaco y comenzar a utilizar el fármaco en dosis de 1mg dos veces al día, a partir del día 8 de tratamiento con vareniclina23,24.
Los resultados y conclusiones de los estudios que evaluaron la eficacia y seguridad de uso de esta medicación frente a placebo y frente a bupropión encontraron los siguientes datos25,26. Las cifras de abstinencia completa entre la 9 y 52 semanas de seguimiento fueron de 22,1 y 23%, para cada uno de los estudios con diferencias significativas con respecto a placebo (p < 0,001 y p < 0,001, respectivamente; OR 3,13 y OR 2,66, respectivamente)25,26. Igualmente en estos estudios se comparó la eficacia de vareniclina con respecto a bupropión 150mg dos veces al día durante 12 semanas. Los resultados muestran que vareniclina es significativamente más eficaz que bupropión en uno de los estudios, 23 frente a 15%, p < 0,01, OR 1,7226, y en el otro las cifras son ligeramente más marginales, 22,1 frente a 16,4%, p<0,07, OR 1,4525. Una constante que se observa en los resultados de los 4 estudios es que las cifras de abstinencia en las primeras semanas de tratamiento son más bajas que las obtenidas en las semanas posteriores27. Probablemente sea ésta una de las características diferenciales del tratamiento con vareniclina. Las propiedades de agonista parcial que tiene esta molécula explican estos resultados27,28.
El estudio de mantenimiento de la abstinencia mostró que la prolongación de tratamiento con vareniclina hasta completar 24 semanas producía un incremento significativo de los índices de abstinencia completa con respecto a placebo tanto a los 6 como a los 12 meses de seguimiento (70,6 frente a 49,6%, p<0,0001, OR 2,47. a los seis meses y 44,0% frente a 37,1%, p=0.0126, OR 1,35, a los 12 meses de seguimiento)29. Estos resultados abogarían por una prolongación del tratamiento con este fármaco en algunos pacientes. Un dato importante es que el incremento del tiempo de tratamiento no aumentó los efectos adversos29.
Sus contraindicaciones son hipersensibilidad al principio activo o a cualquiera de los excipientes. Respecto a sus interacciones, basándose en las características de vareniclina y en la experiencia clínica hasta la fecha, no tiene ninguna interacción con otros medicamentos que sea clínicamente significativa. Sus efectos secundarios son: náuseas (2,7 frente a 0,6% para placebo), dolor de cabeza (0,6 frente a 1,0% para placebo), insomnio (1,3 frente a 1,2% para placebo) y sueños anormales (0,2 frente a 0,2% para placebo)30,31.
Factores que influyen en la elección del fármacoEn el momento de decidir si se inicia o no tratamiento farmacológico es fundamental valorar el grado de motivación para dejar de fumar y el grado de dependencia de la nicotina (test de Fagerström, anexo 1). Como directrices generales si la puntuación del test de Fagerström es superior a 7 puntos la adicción al tabaco es muy elevada y sería conveniente utilizar algún tratamiento farmacológico para abandonar el hábito tabáquico. Si la puntuación es de 6 a 7 puntos la adicción es moderada y el tratamiento indicado no debería ir más allá de la TSN. Si la puntuación es de 0 a 5 puntos la dependencia es baja y no sería necesario en principio el empleo de tratamiento farmacológico.
Si se decide emplear tratamiento farmacológico la elección del fármaco de primera línea debe hacerse en función de factores como la experiencia del profesional en su manejo, las contraindicaciones del fármaco, las preferencias del paciente, su experiencia previa y ciertas características del paciente (antecedentes depresivos, preocupación por el peso, posibilidades económicas, etc.). Realmente no existe un fármaco que como norma general se pueda considerar de primera elección. Como normas generales si el paciente tiene una mala tolerancia previa a los antidepresivos o fármacos psicoactivos debemos utilizar la TSN. En caso contrario podemos valorar el uso de bupropión o vareniclina según nuestra experiencia previa. En la tabla 1 aparece una evaluación de los métodos de tratamiento para dejar de fumar32. A modo de ejemplo en la tabla 2 se muestran algunos datos y observaciones para el uso de bupropión.
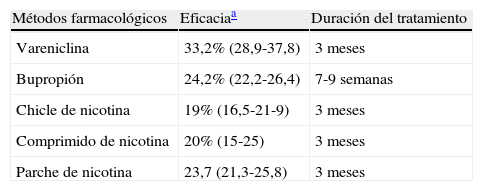
Evaluación comparativa de los métodos para dejar de fumar
| Métodos farmacológicos | Eficaciaa | Duración del tratamiento |
| Vareniclina | 33,2% (28,9-37,8) | 3 meses |
| Bupropión | 24,2% (22,2-26,4) | 7-9 semanas |
| Chicle de nicotina | 19% (16,5-21-9) | 3 meses |
| Comprimido de nicotina | 20% (15-25) | 3 meses |
| Parche de nicotina | 23,7 (21,3-25,8) | 3 meses |
Tomada de Fiore et al.32.
Empleo y precauciones con bupropión SR
| - En fumadores con baja y moderada dependencia, 150mg dos veces al día durante 7-9 semanas |
| - En fumadores con dependencia alta, 150mg dos veces al día durante 9 a 12 semanas |
| - En ancianos (más de 65 años) y en pacientes con insuficiencia hepática o renal conviene reducir la dosis a 150mg diarios o en días alternos |
| - En caso de aparición de efectos adversos, recordar que el insomnio y la sequedad de boca son dependientes de las dosis |
| - Evitar su uso en caso de antecedentes convulsivos, tumor del SNC, situaciones clínicas o toma de medicaciones que disminuyan el umbral convulsivante, bulimia, anorexia nerviosa, trastorno psiquiátrico bipolar y alergia conocida a esta medicación |
Se define unidad especializada en tabaquismo como un servicio sanitario integrado en el contexto de un área de salud que propugna, coordina y realiza acciones en pro de la prevención y el tratamiento del tabaquismo en dicha área, en colaboración directa con otros servicios sanitarios de la misma. Los principales objetivos de un centro de estas características son tres: asistencial, docente y de investigación33. Los programas de asistencia sanitaria a los fumadores que sean ofertados por una unidad especializada en tabaquismo deben cumplir con una serie de requisitos sobre cuya eficacia existe probada evidencia científica34–38. Así, es importante que en estos centros la ayuda sea impartida por profesionales sanitarios de diferentes ámbitos (facultativos, diplomados en enfermería, licenciados en psicología, nutricionistas, etc.), que todos ellos acrediten excelentes conocimientos y amplia experiencia en el diagnóstico y tratamiento del tabaquismo y que los programas de tratamiento que se apliquen sean intensivos (más de 4 sesiones, de más de 10 min de duración cada una, con un año de seguimiento) e impartidos en diferentes formatos (individual, grupal y telefónico).
La experiencia acumulada por los diferentes centros sanitarios que en distintas partes del mundo funcionan como unidades especializadas en tabaquismo muestran que este tipo de asistencia es eficaz, segura y cumple con una excelente relación coste/efectividad. En Reino Unido, los «servicios para dejar de fumar» (smoking cessation services) que se implantaron de forma generalizada en todo el país después de una fuerte inversión por parte del Ejecutivo rindieron magníficos resultados. Los estudios mostraron que el coste medio por año de vida ganado fue de 684 libras esterlinas, que se redujo a 438 cuando se tuvo en cuenta el ahorro en futuros gastos sanitarios. En el peor de los casos el coste ascendería hasta 2.293 libras por año de vida ganado, y en el mejor de los casos el coste sería de tan solo 102 libras. En ambas asunciones el precio se mantendría por debajo de la cifra de 20.000 libras de coste por año de vida ganado ajustado a calidad, que es el tope normalmente usado por el Nacional Institute for Clinical Excellence de Reino Unido39. En nuestro país la experiencia no es tan amplia. No obstante, recientemente se han publicado los datos de una unidad especializada en tabaquismo que funciona de forma muy similar a como lo hacen los servicios ingleses, y se ha encontrado que el coste en fármacos por paciente atendido fue de 118 euros, y el coste por fumador atendido que consiguió mantenerse abstinente a los 6, 12, 36 y 57 meses fue de 202, 215, 281 y 338 euros, respectivamente36,40.
En España, en estas unidades se realiza un tratamiento multicomponente del tabaquismo, afrontado como una dependencia, empleando técnicas cognitivo-conductuales, tratamiento farmacológico (terapia sustitutiva con nicotina, bupropión u otros fármacos con evidencia científica de eficacia), educación para la salud y monitorización de parámetros biológicos. Los programas de tratamiento se desarrollan en sesiones en grupo y posteriormente se hace un seguimiento hasta cumplidos los 2 años de abstinencia.
Suelen contar con una consulta de enfermería para valoración del fumador, lo que permite atender a un mayor número de fumadores, reduciéndose la cuantiosa lista de espera. También suelen contar con un teléfono de ayuda al fumador, a través del cual se combina la terapia psicológica y consejos de ayuda a través de conversaciones telefónicas programadas con el envío de material por correo convencional.
Responsabilidades éticasProtección de personas y animales. Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datos. Los autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informado. Los autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
- 1.
Tiempo transcurrido desde que te levantas hasta que fumas el primer cigarrillo:
- •
Menos de 5 min (3 puntos)
- •
Más de 5-30 min (2 puntos)
- •
De 31 a 60 min (1 puntos)
- •
Más de una hora (0)
- •
- 2.
¿Fumas por las mañanas?
- •
Sí (1 punto)
- •
No (0 puntos)
- •
- 3.
¿Fumas cuando estás enfermo?
- •
Sí (1 punto)
- •
No (0 puntos)
- •
- 4.
¿Fumas en lugares prohibidos?
- •
Sí (1 punto)
- •
No (0 puntos)
- •
- 5.
¿Qué cigarrillo te gusta más?
- •
El primero del día (1 punto)
- •
Otros (0 puntos)
- •
- 6.
¿Te tragas el humo?
- •
Siempre (2 puntos)
- •
A veces (1 punto)
- •
Nunca (0 puntos)
- •
- 7.
¿Qué cantidad de nicotina tienen tus cigarrillos? (la información viene en el paquete de tabaco)
- •
0,8mg (0 puntos)
- •
0,9 a 1,2mg (1 punto)
- •
Más de 1,3mg (2 puntos)
- •
- 8.
¿Cuántos cigarrillos fumas al día?
- •
1 a 15 (0 puntos)
- •
16 a 25 (1 punto)
- •
26 o más (2 puntos)
- •