La gota es una enfermedad provocada por el depósito de cristales de urato monosódico. Su presentación clínica como una artritis aguda autolimitada y la creencia de que es una enfermedad banal y autoinfligida han provocado que su manejo sea deficitario. A pesar de los avances en el conocimiento de la enfermedad y la sencillez del manejo, no más del 30% de los enfermos están bien tratados. En España la gota afecta al 2,5% de la población y su incidencia está en aumento.
En el siguiente artículo repasaremos la patogenia de la gota y la hiperuricemia, destacando el mayor peso de la genética y la función renal sobre la dieta. Analizaremos las consecuencias del depósito de los cristales. La gota, además de su presentación articular y de su afectación renal, ha demostrado ser un factor de riesgo cardiovascular independiente.
El tratamiento hipouricemiante es el más importante, ya que es el que permite la disolución de los cristales y la curación de la enfermedad. Para ello es necesario conseguir de forma sostenida niveles de uricemia inferiores a 6mg/dl. Revisaremos también el tratamiento preventivo y de los ataques, así como el papel de la educación de los enfermos tanto a nivel de hábitos higienicodietéticos como de adherencia al tratamiento farmacológico.
Gout is a disease caused by the chronic deposition of monosodium urate crystals. Its clinical presentation as an acute, self-limiting arthritis and the belief that it is a banal, self-inflicted disease have led to its poor management. Despite advances in the knowledge of the disease and the simplicity of its management, no more than 30% of patients are well treated. In Spain, the prevalence of gout is 2.5% and its incidence is increasing.
In the following article we will review the pathogenesis of gout and hyperuricaemia, highlighting the greater weight of genetics and renal function over diet. We will look at the consequences of crystal deposition. Gout, in addition to its joint presentation and renal involvement, has been shown to be an independent cardiovascular risk factor.
Hypouricemic therapy is the most important treatment, as it is the one that dissolves the crystals and cures the disease. This requires the sustained achievement of uricemia levels below 6mg/dl. We will also review preventive and flares treatment, as well as the role of patient education in terms of both lifestyle and dietary habits and adherence to pharmacological treatment.
La gota es la artropatía inflamatoria crónica más frecuente. En España se calcula que afecta a casi un 2,5% de la población mayor de 20 años, un 4,55% en hombres y un 0,38% en mujeres1. Su prevalencia, incidencia y años de vida con discapacidad están aumentando en todo el mundo debido a los cambios en el estilo de vida y la mejoría de la esperanza de vida2. La gota es producida por el depósito crónico de cristales de urato monosódico (UMS) en las articulaciones y otros tejidos y actualmente conocemos que sus consecuencias van más allá de los característicos ataques agudos de artritis. Se ha demostrado que los enfermos con gota presentan más comorbilidades, empeoramiento de su calidad de vida y mayor morbimortalidad3. El aumento de la mortalidad, en los enfermos con gota, es sobre todo debido a eventos cardiovasculares. Este aumento no se explica solamente por las comorbilidades; la gota, hoy en día, debe ser considerada un factor de riesgo cardiovascular independiente4.
De la gota se conoce su patogenia, su historia natural y su evolución, y tiene un tratamiento asequible y sencillo en la mayor parte de los enfermos. A pesar de ello, su manejo habitual no es el adecuado. Esto se ha demostrado dentro y fuera de nuestro país. Hay múltiples estudios europeos o del resto del mundo donde se describen resultados deficientes en el manejo de la gota5. En nuestro entorno tenemos evidencia del mal control de estos pacientes, tanto en atención primaria (AP)6 como en las consultas hospitalarias de reumatología7. Por ejemplo, en un estudio reciente en 7 centros de AP de Barcelona, solo el 37% de los enfermos estaban bien tratados6. Las causas de este déficit son varias, y han sido objeto de estudio, aunque las principales son el desconocimiento de la enfermedad por parte de profesionales sanitarios y pacientes y la creencia de que es una patología poco importante y en cierta manera autoinfligida por excesos en la dieta y la toma de alcohol8,9. Hay múltiples publicaciones que de forma indirecta demuestran el mal manejo de la gota. Por ejemplo, si comparamos los ingresos hospitalarios en las últimas décadas por artritis reumatoide y por gota, podemos observar una disminución del primero de más del 60% mientras que los ingresos por gota se han doblado. En la actualidad, hay más ingresos por gota que por artritis reumatoide10. También se ha demostrado que mientras en otras artropatías, como la artritis reumatoide, la brecha de mortalidad ha disminuido en las últimas décadas, en el caso de la gota esta brecha no se ha modificado11.
El conocimiento sobre la patogenia y manejo de la gota ha mejorado mucho en las dos últimas décadas. Quizás los avances terapéuticos no han sido tan importantes, comparados con otras enfermedades crónicas prevalentes, pero los fármacos disponibles actualmente son útiles, y su manejo en la mayoría de enfermos sigue siendo sencillo. No obstante, no se ha conseguido una traslación generalizada de este conocimiento a la AP, que es la responsable del manejo de la mayoría de los enfermos.
¿En qué se diferencian uricemia, hiperuricemia y gota o por qué la gota es una enfermedad crónica?Es importante diferenciar uricemia, hiperuricemia y gota. El ácido úrico soluble es el antioxidante más importante que existe en el organismo, e incluso se ha propuesto como tratamiento en enfermedades en las que predomina el estrés oxidativo12, por tanto, a priori, la hiperuricemia no debería ser perjudicial para nuestro organismo. Pero cuando el ácido úrico en sangre supera su nivel de solubilidad de manera sostenida, empiezan a formarse los cristales de urato monosódico por nucleación13 y se desarrolla la gota. Este nivel se sitúa en 6,8mg/dl, y niveles superiores deben considerarse hiperuricemia14. Debemos hacer caso omiso a los rangos de referencia informados en las hojas de resultados de los distintos laboratorios de análisis clínicos (que se basan en datos estadísticos poblacionales y que diferencian entre ambos sexos). Se trata de un fenómeno físico-químico que se da en condiciones fisiológicas y viene definido por la solubilidad de esta molécula. Es a este depósito de cristales de ácido úrico, y a sus consecuencias clínicas, a lo que debemos llamar gota.
Las causas de la hiperuricemia son múltiples. La predisposición genética es el factor más importante, y en contra de lo que está generalmente establecido, la dieta no tiene un papel relevante. La hiperuricemia se produce básicamente por alteraciones del transporte de ácido úrico a nivel renal o intestinal. La insuficiencia renal crónica o el uso de diuréticos también es un factor determinante en las hiperuricemias secundarias15.
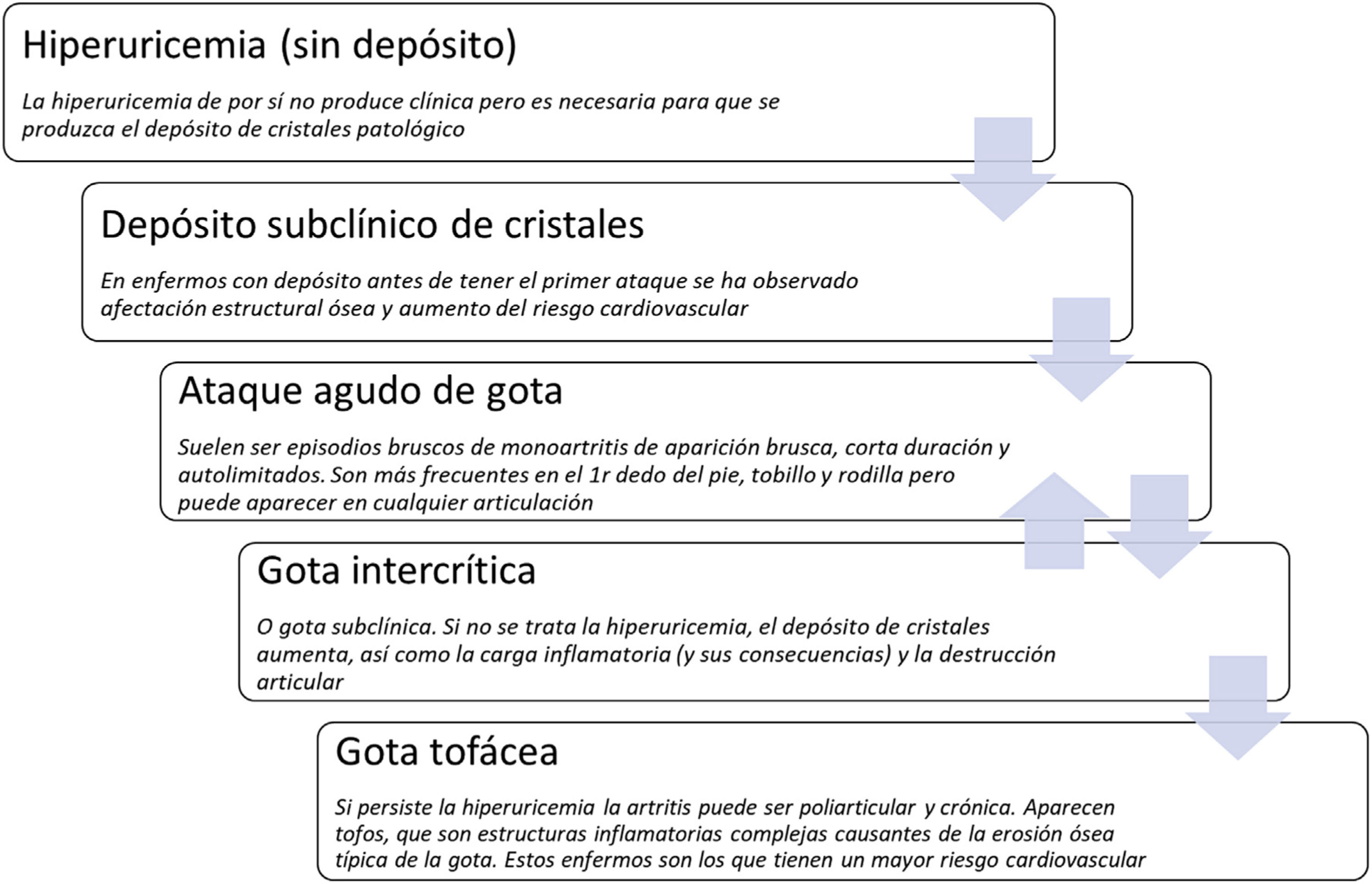
Los cristales de ácido úrico se forman en la superficie del cartílago hialino en presencia de hiperuricemia sostenida. Si no se trata la hiperuricemia, se van agregando nuevos cristales, y el depósito va creciendo. La presencia de estos depósitos se ha demostrado antes del primer episodio con manifestaciones clínicas de gota aguda mediante ecografía16. Los cristales inician la cascada inflamatoria a través de un complejo multiproteico llamado inflamasoma, que permite la liberación de IL-1 y otras citoquinas proinflamatorias provocando el ataque de gota17. Si no disolvemos los cristales, y estos siguen presentes, a pesar de la mejora del episodio de inflamación aguda, persiste la inflamación subclínica18. Por tanto, no podemos considerar la gota como una enfermedad aguda, sino como una entidad crónica que clínicamente suele presentarse con ataques y que consta de diferentes estadios (fig. 1).
Clínica¿Cómo se presenta la gota en nuestro día a día?Suele sospecharse gota ante un paciente con una artritis de aparición rápida (muchas veces de inicio nocturno) con dolor, eritema y tumefacción en la articulación metatarsofalángica del primer dedo (podagra). La gota suele afectar también a tarso, tobillo y rodilla y menos frecuentemente a mano o codo19. La dificultad en la movilización de la articulación afectada y un dolor intenso al roce, además del derrame articular, es característico de la artritis gotosa.
Si no se tratan estos episodios, se autolimitan en menos de 2 semanas y el paciente queda clínicamente asintomático. Estos episodios son los que llamamos ataques de gota. Esta forma de presentación ha favorecido la creencia de que la gota es una enfermedad aguda y leve. Por este motivo, en parte, no se trata de manera adecuada. Al no hacerlo, persistirá la hiperuricemia, aumentará el depósito de cristales y aparecerán nuevos brotes, tofos y destrucción articular17.
Por otro lado, la presencia de inflamación subclínica secundaria al depósito crónico podría tener consecuencias más allá de la articulación afectando el sistema cardiovascular. Estas consecuencias del depósito de cristales podrían aparecer precozmente, incluso antes del primer ataque clínico de gota. En un estudio de enfermos ingresados por cardiopatía isquémica que nunca habían padecido un ataque de gota se observó que los enfermos con hiperuricemia y depósito de cristales (demostrados por ecografía) tenían más calcificación coronaria que los enfermos normouricémicos o los enfermos hiperuricémicos sin depósito de cristales20. Otro estudio demostró también que, en enfermos con gota, el riesgo de evento y mortalidad cardiovascular se asocia al tamaño del depósito de cristales de urato monosódico21. Es más, un reciente metaanálisis que incluye más de 11 estudios, y el seguimiento de 786.250 enfermos con gota, demostró un aumento de la mortalidad debido a enfermedad cardiovascular, gastrointestinal e infecciosa22.
Otra de las consecuencias del aumento del depósito de los cristales de ácido úrico es la formación de tofos. El tofo va más allá de un simple depósito de cristales. Es una estructura inflamatoria compleja. Tiene una parte central donde se encuentran los cristales rodeados de una zona coronal donde predominan macrófagos, mastocitos y células plasmáticas. Además, el tofo es el responsable de la formación de erosiones óseas en los enfermos con gota23.
Tanto la gota como la hiperuricemia se asocian a una mayor prevalencia y a un mayor riesgo de enfermedad renal crónica (ERC). Aunque hay cierta controversia en los motivos de esta asociación, está claro que es multifactorial y recíproca. Las personas con ERC tienen más hiperuricemia y más gota. Además, cada vez queda más claro que el tratamiento reductor de la uricemia es efectivo en los enfermos con gota o con hiperuricemia e insuficiencia renal crónica24.
Es importante destacar que hay diferencias en la presentación de síntomas de la gota entre hombres y mujeres. En las mujeres la gota aparece más tarde, se asocia más al uso de diuréticos y menos al consumo del alcohol y se acompaña de más comorbilidades25. En varones la uricemia se incrementa de forma progresiva desde edades tempranas, mientras que en las mujeres se mantiene estable hasta los 50 años y con la menopausia se incrementa de forma abrupta26.
DiagnósticoAunque en AP su uso es bastante limitado, el patrón oro en el diagnóstico de la gota sigue siendo la demostración de cristales de urato monosódico en el líquido sinovial. Estos cristales se caracterizan por tener una intensa birrefringencia negativa en el microscopio óptico con luz polarizada. En los últimos años, se han desarrollado pruebas de imagen que pueden ayudar al diagnóstico de gota. A nivel de AP, el uso de la ecografía de forma cada vez más generalizada podrá ser muy útil para mejorar el diagnóstico de esta enfermedad. La imagen del doble contorno y de tofos no son complicadas de obtener y tienen una alta especificidad para demostrar la presencia del depósito de cristales27.
En AP, la mayoría de diagnósticos de gota suelen hacerse por impresión clínica acompañada o no de la presencia de hiperuricemia. Hay múltiples criterios de clasificación o de diagnóstico para la gota. Dos son especialmente útiles en este ámbito: los criterios holandeses, diseñados especialmente para población atendida en AP28. y los criterios de clasificación de gota 2016 ACR/EULAR29. Para estos últimos existe una útil calculadora online que puede encontrarse en https://goutclassificationcalculator.auckland.ac.nz/.
Al no tratarse la hiperuricemia asintomática, deberá medirse la uricemia en los casos en que se sospeche gota en todas sus formas clínicas (afectación monoarticular, poliarticular y nefrolitiasis).
TratamientoEl tratamiento de la gota tiene que abordar tres dimensiones: el tratamiento reductor de la uricemia, el tratamiento de los episodios de artritis aguda (ataques de gota) y el tratamiento profiláctico de los ataques al iniciar el tratamiento hipouricemiante. Es importante darle un papel central al tratamiento reductor de la uricemia, ya que es este el que elimina al elemento patógeno de la enfermedad.
Tratamiento reductor de la uricemiaEl objetivo del tratamiento hipouricemiante es la disolución de los cristales y, por tanto, la desaparición del depósito. Para ello es necesario conseguir niveles de ácido úrico en sangre por debajo del nivel de solubilidad (6,8mg/dl) de forma sostenida. Se sabe que la velocidad de disolución de los cristales es mayor cuanto más bajo es el nivel de uricemia alcanzado30. Las principales guías recomiendan niveles de uricemia por debajo de 6mg/dl o de 5mg/dl en casos de gota grave31.
No existe evidencia científica para determinar cuándo es el momento ideal para empezar el tratamiento reductor de la uricemia. Pero teniendo en cuenta que se trata de una enfermedad crónica, con consecuencias extraarticulares, fácilmente tratable y que puede curarse, parece lógico pensar que es mejor no esperar a que aumente el depósito de cristales en el organismo. Las últimas recomendaciones EULAR indican iniciar el tratamiento hipouricemiante en enfermos con ataques recurrentes (≥2/año), tofos, erosiones óseas o litiasis renal. También sugieren un tratamiento precoz (tras el primer ataque) en enfermos con gota y con uratos >8mg/dl, inicio de la enfermedad antes de los 40 años y/o presencia de comorbilidades31. Estudios recientes demuestran que no es necesario esperar a que el ataque de gota finalice para iniciar el tratamiento hipouricemiante. Distintos estudios coinciden en demostrar que el ataque no es más intenso ni más largo si iniciamos el tratamiento reductor de la uricemia durante el ataque de gota32.
A nivel de AP, solo existen 2 fármacos con indicación hipouricemiante para el tratamiento de la gota, el alopurinol y el febuxostat. Ambos son inhibidores de la xantin-oxidasa y el uso de uno u otro fármaco vendrá determinado por criterios de eficiencia, características del paciente y perfil de comorbilidades.
El tratamiento debe iniciarse con dosis bajas y aumentar de forma progresiva hasta alcanzar el objetivo terapéutico (<6mg/dl). En el caso de alopurinol se recomienda iniciar con una dosis cercana al filtrado glomerular estimado multiplicado por 1,533. Así evitaremos la aparición del síndrome de hipersensibilidad al alopurinol, un síndrome extremadamente infrecuente, pero potencialmente fatal.
Otra de las ventajas del inicio lento con escalada progresiva del tratamiento con alopurinol o febuxostat es la disminución de la frecuencia de los ataques que aparecen al iniciar el tratamiento hipouricemiante. La aparición de estos ataques muchas veces provoca el abandono del mismo, al hacer pensar al enfermo que la terapia no es efectiva34. La educación sanitaria, con explicaciones precisas del tratamiento hipouricemiante, es fundamental para conseguir una adherencia terapéutica adecuada en el tratamiento de esta patología35.
Una vez iniciado el tratamiento, la dosis deberá aumentarse progresivamente hasta alcanzar el objetivo terapéutico (≤5 o 6mg/dl). Es importante no caer en la inercia terapéutica y subir la dosis hasta conseguir las uricemias recomendadas. Se ha demostrado que, en AP, 2 de cada 3 enfermos que están siendo tratados no alcanzan estos niveles6. Las dosis máximas permitidas en España son: 900mg/día de alopurinol y 120mg/día de febuxostat.
Los estudios pivotales de febuxostat han demostrado que febuxostat 80mg/día tiene una mayor capacidad hipouricemiante que alopurinol 300mg/día36, aunque una correcta escalada en la dosificación de los fármacos es la clave de un tratamiento eficaz. Febuxostat puede ser útil en enfermos con ERC, incluso en estadios 4-5 que no están en diálisis37, si bien en estos casos recomendamos remitir al paciente a reumatología.
Actualmente no existe evidencia que nos permita contestar a la pregunta de si el tratamiento reductor de la uricemia debe mantenerse toda la vida. Lo que parece claro es que el objetivo terapéutico puede relajarse una vez el depósito de cristales haya desaparecido38.
El estudio CARES alarmó sobre el posible aumento de riesgo cardiovascular con febuxostat en comparación con alopurinol39. Pero si se analizan detenidamente los resultados de este estudio, se detectan severas limitaciones metodológicas: los participantes presentan una alta tasa de discontinuación del tratamiento (>50%), y se pierde mucha información en el seguimiento debido a que el 45% de los pacientes no acuden a las citas de seguimiento. Los eventos cardiovasculares reportados, además, suceden mayormente cuando los enfermos ya no están tomando el fármaco40. Finalmente, la publicación del estudio FAST, 2 años más tarde41, con tamaños y diseño parecidos, pero sin sus limitaciones, provocó que se eliminara la advertencia en ficha técnica al uso de este fármaco en enfermos con alto riesgo cardiovascular.
El único estudio que existe de coste-efectividad realizado en nuestro país demostró que febuxostat 80 y 120mg/día son más eficientes que alopurinol 300mg/día42. Las recomendaciones clínicas de uso de alopurinol indican subir la dosis de forma progresiva hasta alcanzar el objetivo terapéutico, pudiendo utilizarse dosis superiores a los 300mg/día y esta situación clínica no ha sido valorada.
El único uricosúrico actualmente disponible en España es la benzbromarona. Se trata de un fármaco de prescripción hospitalaria que solo puede ser iniciado por reumatólogos y nefrólogos. Por tanto, en caso de que el tratamiento con alopurinol y febuxostat fracase deberá remitirse el enfermo al especialista.
Hay diversos estudios sobre los efectos de distintas dietas en los niveles de uricemia. En general, se ha visto que el efecto de la dieta o el ejercicio sobre estos niveles es escaso43. Sin embargo, no debemos pasar por alto que la mayoría de estos enfermos van a tener un riesgo cardiovascular elevado y múltiples comorbilidades. Actualmente las recomendaciones para estos enfermos son el seguimiento de una dieta de estilo mediterráneo, la pérdida de peso en el caso de que exista sobrepeso, y la realización de ejercicio físico de manera habitual. Estas recomendaciones son similares a las de los enfermos con riesgo cardiovascular elevado. Deben evitarse también las bebidas azucaradas ya que aumentan el riesgo de padecer hiperuricemia y gota44.
No existen ensayos clínicos que demuestren que el tratamiento correcto de la uricemia disminuya la mortalidad o mejore la función renal en enfermos con gota. En un estudio observacional en Auckland con más de 30.000 gotosos, se observó un aumento de muerte cardiovascular en los gotosos. Entre los hombres, el riesgo aumentaba en aquellos a los que no se les había dispensado alopurinol y en aquellos en los que no se consiguió el objetivo terapéutico45. En una cohorte prospectiva de más de 1000 enfermos con gota del País Vasco se observó que, en aquellos en los que no se consiguió el objetivo terapéutico (<6mg/dl), la mortalidad cardiovascular era 2,05 veces mayor3.
Un resumen con los principales conceptos del tratamiento hipouricemiante se muestra en la tabla 1.
Puntos clave en el tratamiento reductor de la uricemia en enfermos con gota
| ¿Se trata la hiperuricemia asintomática? | No, solo se tratarán los enfermos con gota |
| ¿Cuál es el objetivo principal en el tratamiento de la gota? | La disolución de los cristales de urato monosódico |
| ¿Cuándo debemos empezar el tratamiento reductor de la uricemia en enfermos con gota? | En enfermos con gota tofácea, ataques recurrentes, litiasis úrica, <40 años, ácido úrico >8mg/dl o múltiples comorbilidades |
| ¿Cómo empezar el tratamiento reductor de la uricemia? | Todos los TRU se empezarán a dosis bajas. Las dosis se incrementarán cada 2-4 semanas, hasta conseguir el objetivo terapéutico |
| ¿Qué dosis de tratamiento hipouricemiante es la adecuada? | La que sea necesaria para conseguir niveles de uricemia <6mg/dl (o <5mg/dl en enfermos con tofos, artritis crónica o ataques frecuentes) |
| ¿Cómo prevenir los ataques asociados al inicio de la terapia hipouricemiante? | Se utilizará colchicina a dosis de 0,5-1mg/día durante los primeros 6 meses. Si la colchicina está contraindicada o no es tolerada, pueden usarse AINE (si no están contraindicados) a dosis bajas |
El tratamiento de elección en los ataques de gota depende sobre todo del perfil de comorbilidades del paciente. Los AINE y los corticoides son los tratamientos de elección de estos episodios de artritis aguda.
En la actualidad la colchicina ha perdido peso en el tratamiento de estos episodios, debido en parte a los cambios que ha introducido la AEMPS en la ficha técnica de este fármaco. Actualmente, la dosis máxima recomendada es de 2mg/día, hasta un máximo de 6mg acumulados en 4 días. Este cambio se debe a la publicación del primer ensayo clínico de tratamiento de gota con colchicina46. Este estudio demostró igual eficacia del fármaco con dosis bajas que con dosis altas, con muchos menos efectos secundarios. Además, demostró una eficacia limitada del fármaco ya que ni a dosis altas ni bajas redujo el dolor a menos de la mitad, a 3 días de tratamiento.
Respecto a los AINE, todos son efectivos, pero es importante para su uso tener en cuenta las comorbilidades de los enfermos, especialmente la insuficiencia renal y el riesgo cardiovascular. Hay datos a favor de que etoricoxib 120mg/día e indometacina 150mg/día serían algo más efectivos que el resto. En los estudios, etoricoxib presenta menos efectos secundarios que la indometacina, pero al tratarse de tratamientos cortos, en general, hay pocos efectos secundarios47.
Los corticoides han demostrado también ser eficaces y seguros y pueden utilizarse en enfermos en los que los AINE están contraindicados. Este grupo terapéutico puede ser especialmente útil en AP, donde el perfil de los pacientes es la avanzada edad y las comorbilidades48.
Tratamiento preventivo de los ataques al inicio del tratamiento reductor de la uricemiaEs ampliamente conocido que, al inicio del tratamiento hipouricemiante, hay un aumento de los ataques de gota. El buen manejo de este efecto colateral del tratamiento reductor de la hiperuricemia será un factor importante a tener en cuenta, para que los enfermos no malinterpreten estos síntomas como una falta de eficacia del mismo. Por este motivo, la mayoría de guías recomiendan la profilaxis con colchicina al inicio del tratamiento hipouricemiante. La profilaxis se realizará con colchicina a dosis de 0,5-1mg/día y se mantendrá 6 meses o como mínimo hasta que se consiga el objetivo terapéutico19,31.
Cada vez hay más evidencia del papel protector cardiovascular de la colchicina a dosis bajas. Estos datos podrían hacernos replantear alargar el tratamiento con colchicina en enfermos seleccionados49.
En caso de que la colchicina esté contraindicada, podrán valorarse dosis bajas de AINE o de corticoesteroides. También se ha demostrado que los enfermos que aumentan la dosis del tratamiento hipouricemiante de forma progresiva hasta conseguir el objetivo terapéutico presentan menos brotes que aquellos en los que se inicia con dosis más altas34. Estas dos estrategias no son incompatibles entre ellas y pueden implementarse conjuntamente. De todas formas, la mejor manera de evitar los ataques de gota es haciendo desaparecer el depósito de cristales con un tratamiento reductor de la uricemia eficaz durante el suficiente tiempo.
Educación al pacienteInformar al paciente de manera sencilla pero completa acerca de la naturaleza de la enfermedad, sus consecuencias y las diferentes dimensiones del tratamiento es clave e imprescindible para el buen manejo y control de esta.
También es importante conocer y abordar las creencias del paciente sobre la enfermedad. En muchos casos, la visión que la sociedad y los mismos enfermos tienen de esta es estigmatizante y culpabilizante. No abordarlas puede suponer una barrera para un control óptimo.
Las consultas de AP, tanto del médico como de la enfermera, son lugares idóneos para llevar a cabo esta educación al paciente y el seguimiento de esta patología.
Se ha demostrado que las enfermeras son mejores que los médicos en trabajar la educación sanitaria de esta enfermedad en sus consultas.
FinanciaciónLa presente investigación no ha recibido ayudas específicas provenientes de agencias del sector público, sector comercial o entidades sin ánimo de lucro.
Conflicto de interesesCDT ha recibido subvenciones de Asacpharma y Menarini por participar en cursos y asistir a congresos. MAP ha recibido subvenciones de Asacpharma por participar en cursos. DML no tiene conflictos de interés.