Los glucómetros demuestran habitualmente una gran exactitud, y en la práctica, la glucemia capilar y la glucemia plasmática (GP) son utilizadas indistintamente. Sin embargo, numerosas variables pueden afectar la validez de estos aparatos. El objetivo de este estudio fue conocer la exactitud y la concordancia de 3 glucómetros utilizados en las consultas de un EAP.
Material y métodosDe 59 participantes se obtuvieron una muestra de sangre venosa y una gota de sangre capilar, que fue analizada en 3 glucómetros: 2 FreeStyle® Optium (OP1 y OP2) y un Accu-Chek® Aviva. El valor de referencia fue la GP y fueron analizados asimismo el hematocrito y los niveles plasmáticos de urea, bilirrubina, ácido úrico y triglicéridos. Se utilizaron la regresión de Passing-Bablok para la exactitud, y el coeficiente de correlación intraclase y el método Bland-Altman para la concordancia. Se ha considerado el estándar actual (American Diabetes Association) de un error tolerado de±5%.
ResultadosLa diferencia de medias±desviación estándar (mg/dL) y el error sistemático fueron: 5,8±7 y 5,8% (OP1); 6,2±8 y 5,9% (OP2); 8,3±8 y 6,3% (Accu-Chek®). El par más concordante fue OP1/OP2, con un coeficiente de correlación intraclase=0,97, sesgo=−0,4mg/dL y una amplitud de los límites de acuerdo con el 95%=28,6mg/dL. Se observaron los mayores grados de exactitud y de concordancia en rangos glucémicos elevados (GP≥126mg/dL).
ConclusionesAunque mostraron una diferencia de medias clínicamente aceptable respecto a la GP, los 3 glucómetros incumplieron el estándar actual de la American Diabetes Association. Es recomendable la realización periódica de controles de calidad de estos dispositivos.
The glucose meters usually show a high accuracy, and in clinical practice, capillary and plasma glucose (PG) are used interchangeably. However, many variables can affect the validity of these devices. The aim of this study was to determine the accuracy and reliability of 3 glucose meters that are currently used in a primary care centre.
Material and methodsA sample of venous blood and a drop of capillary blood were obtained from 59 participants. The drop was analysed in 3 glucose meters: 2 FreeStyle® Optium (OP1 and OP2), and one Accu-Chek® Aviva. The PG acted as the reference value, and the haematocrit and plasma levels of urea, bilirubin, uric acid and triglycerides were also analysed. We used the Passing-Bablok regression for accuracy and the intraclass correlation coefficient and the Bland-Altman method for reliability. The current American Diabetes Association standard of a total error of±5% was applied.
ResultsDifferences in mean±standard deviation (mg/dL) and the systematic error were 5.8±7 and 5.8% (OP1); 6.2±8 and 5.9% (OP2); 8.3±8 and 6.3% (Accu-Chek®). The OP1/OP2 pair showed the highest level of reliability, with an intraclass correlation coefficient=0.97, bias=−0.4mg/dL, and a width of the 95% limits of agreement of 28.6mg/dL. The highest levels of accuracy and reliability were observed in high glucose ranges (PG≥126mg/dL).
ConclusionsDespite their clinically acceptable mean difference compared to the PG, the 3 glucose meters did not fulfill the current American Diabetes Association standard. The regular performance of quality control tests of these devices is recommended.
El desarrollo de sistemas de autoanálisis de glucemia mediante los dispositivos conocidos como glucómetros portátiles ha sido uno de los avances más significativos en la tecnología dirigida a la diabetes mellitus1. Una elevada proporción de profesionales sanitarios y un número creciente de pacientes diabéticos utilizan actualmente estos dispositivos de forma rutinaria.
Los glucómetros han demostrado un alto grado de exactitud2,3, y en la práctica clínica, los valores basales de glucemia en sangre capilar (GC) y de glucemia plasmática en sangre venosa (GP) son a menudo intercambiables y utilizados de forma indistinta, aun asumiendo un cierto riesgo de error4. Las ventajas de la rapidez en el resultado y la cercanía al paciente contribuyen, asimismo, a facilitar el manejo de la enfermedad.
Sin embargo, tienen una serie de limitaciones que pueden afectar de forma importante a su validez. Así, se han descrito numerosos factores que potencialmente pueden interferir en el resultado, como son las condiciones clínicas del paciente, el uso de ciertas medicaciones, parámetros bioquímicos, factores ambientales y errores en el procedimiento de la toma de la muestra capilar5–7. En consecuencia, tanto por parte de las sociedades de diabetes8 como por grupos de investigadores9, se recomienda realizar controles de calidad de los glucómetros de forma periódica, con objeto de comprobar la exactitud de las mediciones de GC.
En referencia al diseño de estos estudios, junto con evaluaciones en entornos muy controlados, como los laboratorios10, se ha recomendado asimismo su realización en condiciones habituales de práctica clínica o «rutina diaria»11,12, que aportan la posibilidad de incluir variables no estrictamente dependientes del glucómetro.
En esta línea, aprovechando la organización asistencial del centro de salud, este estudio se ha realizado con el objetivo de conocer la exactitud (validez de criterio) de 3 glucómetros utilizados habitualmente en nuestras consultas. Un objetivo adicional ha sido conocer el grado de concordancia que presentan los glucómetros en la medición de la GC.
Material y métodosDiseño generalEstudio observacional analítico dirigido a evaluar la exactitud de 3 glucómetros portátiles, así como la concordancia entre ellos.
Población y muestraLos participantes, de 18 y más años y de ambos sexos, pertenecían a la población general adscrita al Centro de Salud Camargo Interior, municipio de la bahía de Santander. El criterio de inclusión era haber sido citado para una analítica sanguínea solicitada desde la consulta de medicina de familia por cualquier motivo. Fue criterio de exclusión no haber realizado un ayuno nocturno mínimo de 10h. El cálculo del tamaño muestral se realizó siguiendo los criterios siguientes: para el análisis de validez, con una potencia deseada del 80% para detectar un tamaño de efecto de 0,5 eran necesarios 51 sujetos. Para el análisis de concordancia, con dicha muestra la potencia del estudio era del 100% para detectar un coeficiente de correlación intraclase (CCI) de 0,95. En previsión de pérdidas de información, la muestra calculada se amplió en un 10%, quedando finalmente compuesta por 59 sujetos.
A partir de la agenda diaria de extracciones se realizó un muestreo aleatorio sistemático hasta completar el tamaño muestral. Se cumplieron los principios éticos de la Declaración de Helsinki para la investigación sobre personas, y cada participante seleccionado fue informado del objetivo del estudio mediante la entrega de una hoja informativa. No hubo ninguna renuncia a participar, dando todos ellos el consentimiento verbal. La recogida de datos tuvo lugar en el mes de marzo de 2015.
Variables analizadasLas variables principales del estudio han sido las determinaciones de GC obtenidas en 3 glucómetros portátiles, tras un ayuno nocturno de 10h. Han sido evaluados 3 aparatos de uso actual en las consultas del centro de salud: 2 glucómetros idénticos de la marca FreeStyle® Optium (Abbott Diabetes Care), y un tercer glucómetro, Accu-Chek® Aviva (Roche Diagnostics), basados todos ellos en la reacción de la glucosa-deshidrogenasa. Las series han sido denominadas OP1, OP2 y AC. El valor de referencia ha sido la GP venosa basal obtenida en los Laboratorios Centrales del Hospital Universitario Marqués de Valdecilla con el analizador ADVIA® 2400 Chemistry System (Siemens Healthcare) mediante el método de hexoquinasa/glucosa-oxidasa. En la misma muestra de sangre venosa se analizaron otros parámetros que pueden interferir con la determinación de GC, como son el hematocrito y los valores plasmáticos de urea, ácido úrico, triglicéridos y bilirrubina total7.
Técnica de estudioSe comprobó el estado correcto de las tiras reactivas respecto a su caducidad, y los 3 dispositivos fueron calibrados según las instrucciones del fabricante. La extracción de la muestra de sangre venosa fue realizada por un profesional de enfermería mediante venopunción del antebrazo con la técnica convencional. Posteriormente, el paciente realizaba un lavado de manos con agua y jabón, con secado posterior, y uno de los investigadores (KDM, OGD) le practicaba una punción digital en el pulpejo del dedo con una lanceta estéril. Siguiendo las recomendaciones actuales13, la primera gota de sangre capilar era analizada en los 3 glucómetros, en un orden que era cambiado aleatoriamente al principio de cada jornada. La obtención de ambas muestras en cada paciente se realizó en un tiempo inferior a un minuto, en unas condiciones ambientales adecuadas (temperatura 20°C, humedad<80%).
Análisis estadísticoEn el análisis de la exactitud se han seguido procedimientos de la Guía de Consenso EP09-A3 (Clinical and Laboratory Standards Institute), dirigida a estudios de comparación de métodos utilizando muestras de pacientes14. Los valores de GC han sido caracterizados mediante la mediana con el rango intercuartílico, y la media con la desviación estándar (DE). Se comprobó el supuesto de normalidad mediante el test de Kolmogorov-Smirnov. Se analizó, en global y en subgrupos, la diferencia de medias de cada GC con respecto a la GP, con su intervalo de confianza (IC) al 95%. Los valores de GP de 110 y 126mg/dL fueron utilizados como puntos de corte para el análisis, y corresponden a los valores diagnósticos de glucemia basal alterada y diabetes mellitus, respectivamente, establecidos por la OMS15. Una vez comprobada la relación lineal entre las series, se calculó la regresión lineal no paramétrica de Passing-Bablok, que ha permitido conocer el error sistemático asociado a cada glucómetro. Se ha considerado el estándar de la American Diabetes Association, que establece actualmente un error total tolerado de±5% en estos dispositivos6.
Para evaluar la concordancia entre los datos de GP fueron analizadas 3 series, correspondientes a los pares de mediciones OP1/OP2, OP1/AC y OP2/AC. Se utilizaron de forma complementaria 2 estadísticos: el CCI en su variante 2,1, como estadístico global de concordancia, y el método gráfico de Bland-Altman, ampliamente utilizado en la comparación de métodos diagnósticos16, que informa sobre la distribución de las diferencias. Mediante este último método se presentó gráficamente la diferencia entre cada par de mediciones frente a su media, y se obtuvieron el sesgo sistemático, los límites de acuerdo con el 95% para la diferencia de medias, y el coeficiente de repetibilidad.
Los cálculos se realizaron con MedCalc® 8 (MedCalc Software, Ostende, Bélgica) y con SPSS® 15 (SPSS Inc., Chicago, Illinois, EE. UU.). Se ha considerado significativo un valor de p<0,05.
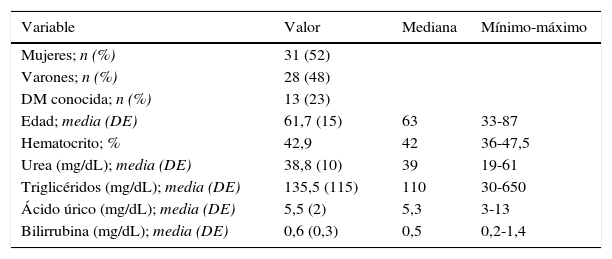
ResultadosSe han analizado 59 personas de ambos sexos, pertenecientes a la población general adscrita al centro de salud, con unas características clínicas que se muestran en la tabla 1. En la muestra había una representación similar de ambos sexos, los participantes eran predominantemente no diabéticos, y tenían una media de edad de 61,7 años.
Características clínicas y bioquímicas de la población de estudio
| Variable | Valor | Mediana | Mínimo-máximo |
|---|---|---|---|
| Mujeres; n (%) | 31 (52) | ||
| Varones; n (%) | 28 (48) | ||
| DM conocida; n (%) | 13 (23) | ||
| Edad; media (DE) | 61,7 (15) | 63 | 33-87 |
| Hematocrito; % | 42,9 | 42 | 36-47,5 |
| Urea (mg/dL); media (DE) | 38,8 (10) | 39 | 19-61 |
| Triglicéridos (mg/dL); media (DE) | 135,5 (115) | 110 | 30-650 |
| Ácido úrico (mg/dL); media (DE) | 5,5 (2) | 5,3 | 3-13 |
| Bilirrubina (mg/dL); media (DE) | 0,6 (0,3) | 0,5 | 0,2-1,4 |
DE: desviación estándar; DM: diabetes mellitus.
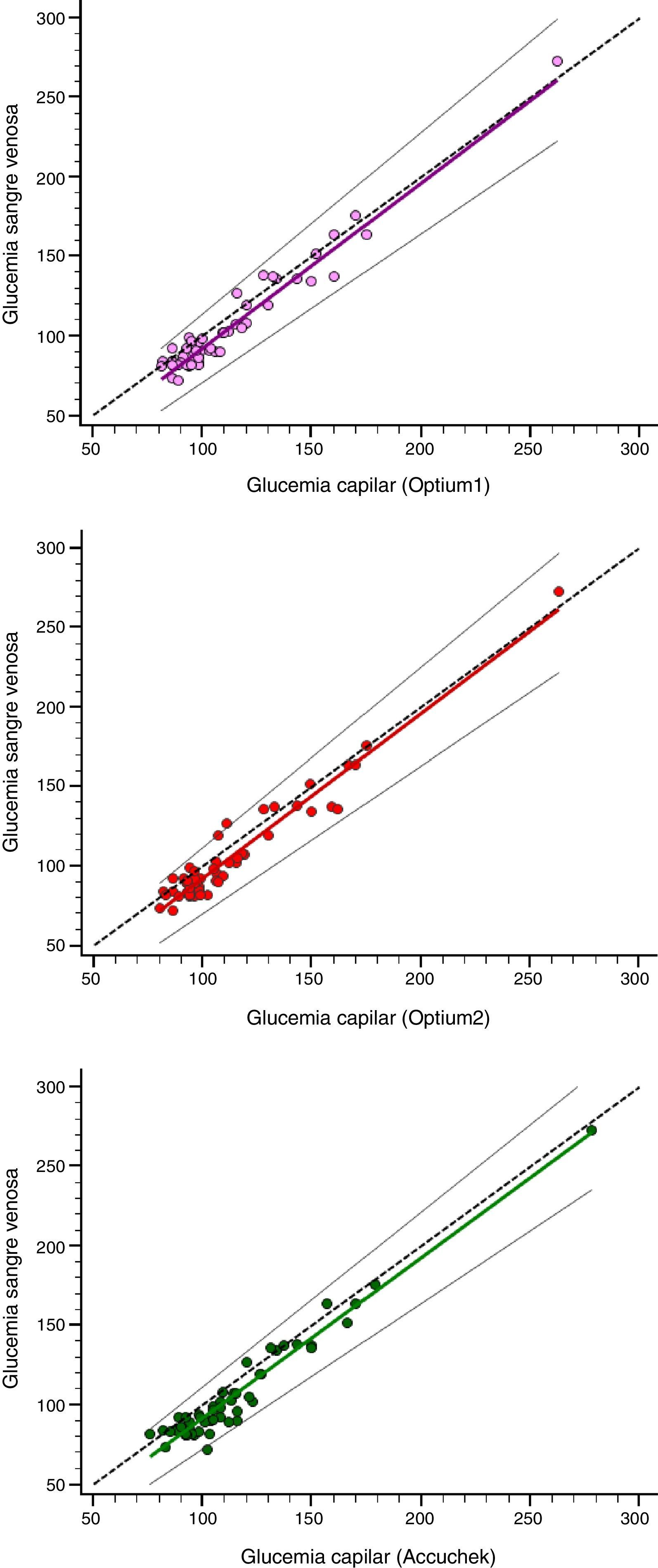
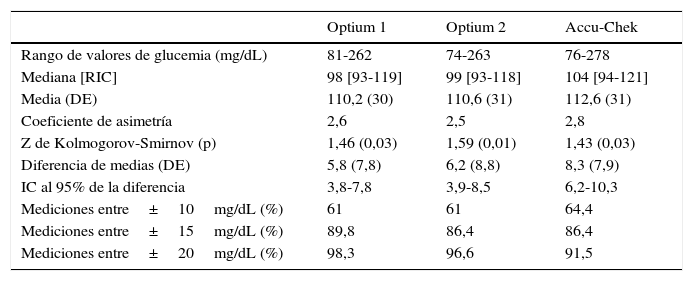
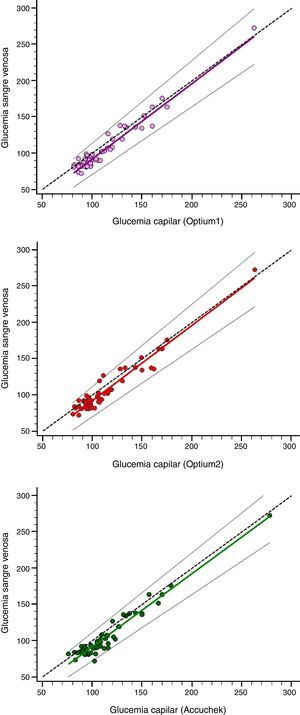
El rango de valores de GP osciló entre 72 y 273mg/dL, con una mediana (rango intercuartílico) de 92 (84-108) y una media (DE) de 104,3 (32) mg/dL. Las series OP1, OP2 y AC eran asimétricas, no seguían una distribución normal, y mostraban un fuerte predominio de valores en torno a 100mg/dL (tabla 2). Las GC presentaron unos valores superiores a los de la GP, que se mantuvieron en el análisis de subgrupos (tabla 3). Se observó una reducción gradual de las diferencias a medida que se incrementaba el valor de la GP. Así, mientras que en sujetos con GP<110mg/dL las desviaciones medias fueron de 8, 8,2 y 10,6% (para OP1, OP2 y AC, respectivamente), en los sujetos con GP≥126mg/dL fueron de 0,4, 1,9 y 2,2%. Las ecuaciones de la regresión de Passing-Bablok, siendo «x» el valor de la GC e «y» el valor de la GP (fig. 1), fueron y=−11,4+1,03x (OP1); y=−11,5+1,03x (OP2); y=−9,3+1,01x (AC). Al sustituir el parámetro «y» por el nivel de decisión crítica GP=126mg/dL se obtuvieron unos valores de GC de 133,4, 133,5 y 134mg/dL, lo que suponía unos errores sistemáticos de 5,8, 5,9 y 6,3% para OP1, OP2 y AC, respectivamente.
Descripción de las series de glucemia capilar y diferencias respecto a la glucemia plasmática en sangre venosa
| Optium 1 | Optium 2 | Accu-Chek | |
|---|---|---|---|
| Rango de valores de glucemia (mg/dL) | 81-262 | 74-263 | 76-278 |
| Mediana [RIC] | 98 [93-119] | 99 [93-118] | 104 [94-121] |
| Media (DE) | 110,2 (30) | 110,6 (31) | 112,6 (31) |
| Coeficiente de asimetría | 2,6 | 2,5 | 2,8 |
| Z de Kolmogorov-Smirnov (p) | 1,46 (0,03) | 1,59 (0,01) | 1,43 (0,03) |
| Diferencia de medias (DE) | 5,8 (7,8) | 6,2 (8,8) | 8,3 (7,9) |
| IC al 95% de la diferencia | 3,8-7,8 | 3,9-8,5 | 6,2-10,3 |
| Mediciones entre±10mg/dL (%) | 61 | 61 | 64,4 |
| Mediciones entre±15mg/dL (%) | 89,8 | 86,4 | 86,4 |
| Mediciones entre±20mg/dL (%) | 98,3 | 96,6 | 91,5 |
DE: desviación estándar; IC: intervalo de confianza; RIC: rango intercuartílico.
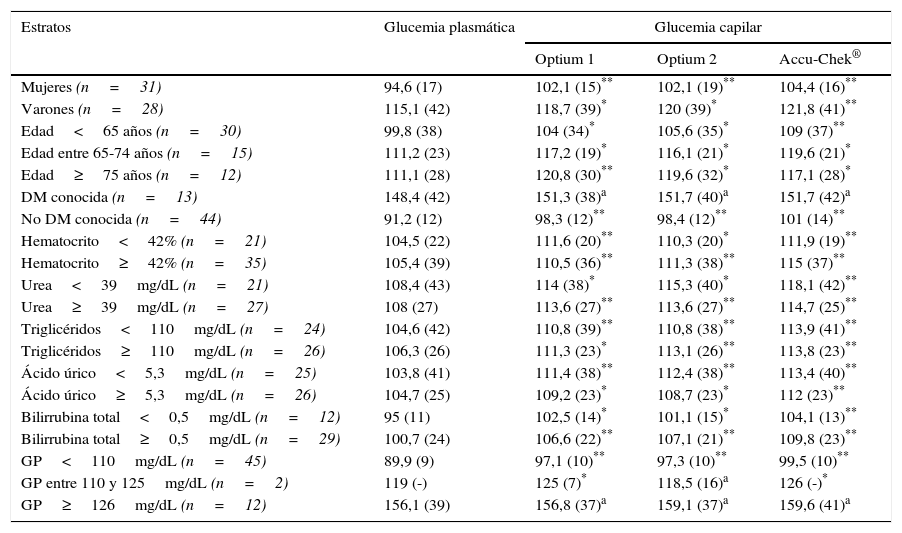
Diferencias por subgrupos entre la glucemia plasmática y la glucemia capilar para los glucómetros analizados
| Estratos | Glucemia plasmática | Glucemia capilar | ||
|---|---|---|---|---|
| Optium 1 | Optium 2 | Accu-Chek® | ||
| Mujeres (n=31) | 94,6 (17) | 102,1 (15)** | 102,1 (19)** | 104,4 (16)** |
| Varones (n=28) | 115,1 (42) | 118,7 (39)* | 120 (39)* | 121,8 (41)** |
| Edad<65 años (n=30) | 99,8 (38) | 104 (34)* | 105,6 (35)* | 109 (37)** |
| Edad entre 65-74 años (n=15) | 111,2 (23) | 117,2 (19)* | 116,1 (21)* | 119,6 (21)* |
| Edad≥75 años (n=12) | 111,1 (28) | 120,8 (30)** | 119,6 (32)* | 117,1 (28)* |
| DM conocida (n=13) | 148,4 (42) | 151,3 (38)a | 151,7 (40)a | 151,7 (42)a |
| No DM conocida (n=44) | 91,2 (12) | 98,3 (12)** | 98,4 (12)** | 101 (14)** |
| Hematocrito<42% (n=21) | 104,5 (22) | 111,6 (20)** | 110,3 (20)* | 111,9 (19)** |
| Hematocrito≥42% (n=35) | 105,4 (39) | 110,5 (36)** | 111,3 (38)** | 115 (37)** |
| Urea<39mg/dL (n=21) | 108,4 (43) | 114 (38)* | 115,3 (40)* | 118,1 (42)** |
| Urea≥39mg/dL (n=27) | 108 (27) | 113,6 (27)** | 113,6 (27)** | 114,7 (25)** |
| Triglicéridos<110mg/dL (n=24) | 104,6 (42) | 110,8 (39)** | 110,8 (38)** | 113,9 (41)** |
| Triglicéridos≥110mg/dL (n=26) | 106,3 (26) | 111,3 (23)* | 113,1 (26)** | 113,8 (23)** |
| Ácido úrico<5,3mg/dL (n=25) | 103,8 (41) | 111,4 (38)** | 112,4 (38)** | 113,4 (40)** |
| Ácido úrico≥5,3mg/dL (n=26) | 104,7 (25) | 109,2 (23)* | 108,7 (23)* | 112 (23)** |
| Bilirrubina total<0,5mg/dL (n=12) | 95 (11) | 102,5 (14)* | 101,1 (15)* | 104,1 (13)** |
| Bilirrubina total≥0,5mg/dL (n=29) | 100,7 (24) | 106,6 (22)** | 107,1 (21)** | 109,8 (23)** |
| GP<110mg/dL (n=45) | 89,9 (9) | 97,1 (10)** | 97,3 (10)** | 99,5 (10)** |
| GP entre 110 y 125mg/dL (n=2) | 119 (-) | 125 (7)* | 118,5 (16)a | 126 (-)* |
| GP≥126mg/dL (n=12) | 156,1 (39) | 156,8 (37)a | 159,1 (37)a | 159,6 (41)a |
GP: glucemia plasmática.
Valores de glucemia expresados en mg/dL y media (desviación estándar). El punto de corte para las variables cuantitativas –excepto para la edad y la glucemia plasmática– es la mediana de la distribución.
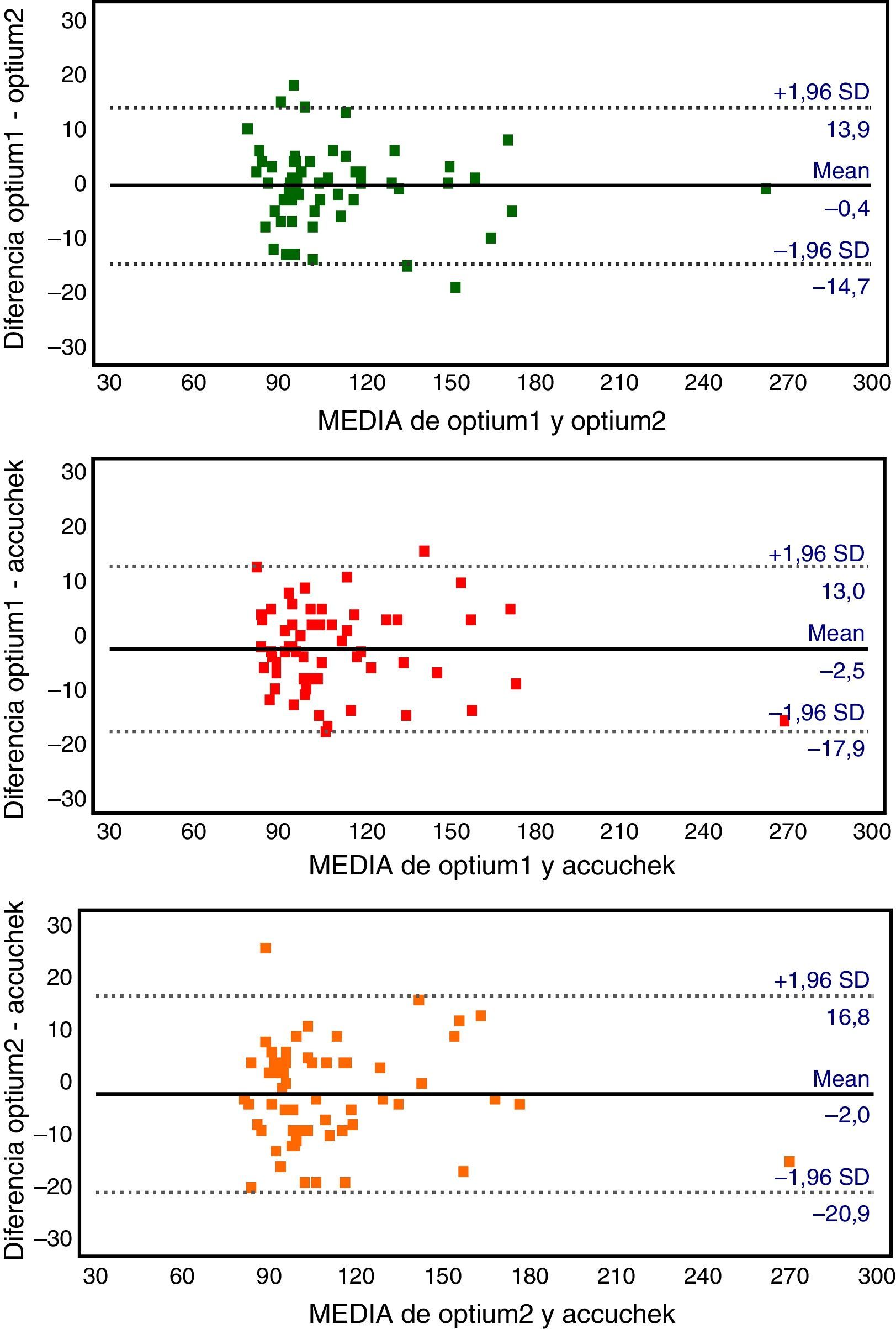
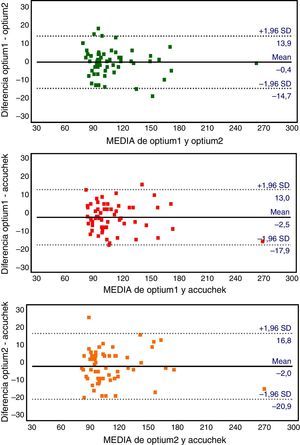
En la evaluación de la concordancia entre los glucómetros, los valores del CCI (IC 95%) fueron 0,97 (0,95-0,98) para la serie OP1/OP2, 0,96 (0,94-0,98) para OP1/AC y 0,95 (0,92-0,97) para OP2/AC. Al analizar el CCI en cada uno de los rangos de glucemia, se observaron los valores más elevados en el rango de GP≥126mg/dL (CCI de 0,97, 0,96 y 0,96 para OP1/OP2, OP1/AC y OP2/AC, respectivamente), mientras que en el rango de GP<110mg/dL fueron de 0,78, 0,73 y 0,62. El método Bland-Altman (fig. 2) mostró que el par OP1/OP2 presentó la menor variabilidad tanto por el menor sesgo sistemático (−0,4mg/dL) como por la menor amplitud de los límites de acuerdo con el 95% (28,6mg/dL frente a 30,9 en OP1/AC y 37,7 en el caso de OP1/AC). El coeficiente de repetibilidad fue de 14,3, 15,5 y 18,8mg/dL para OP1/OP2, OP1/AC y OP2/AC, respectivamente.
DiscusiónExactitud de los glucómetros: glucemia capilar vs. glucemia plasmáticaContrariamente a nuestros resultados, tradicionalmente se ha considerado que la GC era menor que su equivalente en plasma venoso6. Sin embargo, en estudios recientes se han observado unos valores basales muy similares de GC y GP17 o, en concordancia con nuestros resultados, unos valores de GC más elevados que los de la GP: Casas-Oñate y Montoya-Martínez3, en un estudio dirigido a la validez de glucómetros sobre 50 pacientes diabéticos, observaron unas GC basales superiores a la GP en 6 de los 7 aparatos evaluados, con unas diferencias de medias que oscilaban entre 10,2 (DE=12,7; p<0,0001) y 13,6mg/dL (DE=11,4; p<0,0001). Yang et al.18 analizaron 12 voluntarios sanos y evaluaron la GC y la GP tanto en condiciones basales como tras una sobrecarga de glucosa; en las mediciones basales encontraron que las GC eran ligeramente superiores, con una diferencia de medias, no significativa, de 4,2mg/dL. Por su parte, Finkielman et al.19 realizaron un estudio sobre pacientes ingresados en UCI y obtuvieron mediciones simultáneas de GC y GP; tras ajustar el efecto confusor de la hipotensión, observaron que en 767 casos, la media de GC fue de 159, frente a 151mg/dL para la GP (diferencia de medias=7,9, DE=17,6; p<0,001). Este aparente incremento en los valores de GC puede estar en relación con los esfuerzos de los fabricantes para convertir las GC a valores correlativos sobre plasma6, en línea con las recomendaciones de la International Federation of Clinical Chemistry and Laboratory Medicine. Esta organización propuso en 2005 que los glucómetros reportaran la concentración de GP, independientemente del tipo de muestra o la tecnología, aplicando un factor constante de calibración (1,11) al dato obtenido con la sangre capilar20. La concurrencia en la práctica clínica de glucómetros calibrados y no calibrados para reportar valores de GP ha originado a la larga una cierta confusión6, y por ello, se sigue asumiendo que el valor de glucemia obtenido por un glucómetro es algo inferior al obtenido por el laboratorio.
En el análisis por subgrupos de sexo y edad, las diferencias entre la GC y la GP se han mantenido uniformes. Sin embargo, otros autores han encontrado un aumento de la discrepancia entre ambas mediciones en el estrato de las mujeres4 y en el de las personas>75 años4, posiblemente relacionado en este último caso con un flujo distal disminuido. Como resultado de interés, la exactitud de los glucómetros fue mayor a medida que aumentaba el nivel de GP. De hecho, en sujetos con GP<110mg/dL la diferencia media fue de 8,9mg/dL, reduciéndose a 1,5mg/dL en los sujetos con GP≥126mg/dL. Este efecto de reducción de las diferencias se ha observado asimismo en el estrato de los pacientes diabéticos, aunque hay que señalar que en dicho estrato la GP media fue de 148,4mg/dL. Es probable que dicha reducción de diferencias se deba simplemente al elevado valor de las GP en este subgrupo.
En concordancia con este hallazgo, otros autores han observado asimismo un mejor rendimiento de ciertos dispositivos en rangos de hiperglucemia4,21, aunque también se ha reportado una mayor exactitud en situaciones de normoglucemia3 o, por el contrario, un incremento en la diferencia entre GC y GP al aumentar los niveles de glucemia22. En la actualidad, se acepta que la exactitud de un glucómetro presenta variaciones a lo largo del rango de valores glucémicos2, y en este sentido, se ha planteado el establecimiento de unos estándares de calidad diferenciados para valores clínicamente relevantes (como pudieran ser los rangos de hipoglucemia, de normoglucemia y de hiperglucemia) que faciliten una correcta toma de decisiones clínicas23.
Aunque la exactitud global de los aparatos ha sido elevada, con un error sistemático entre el 5,8 y el 6,3%, hay que considerar las variaciones que puede presentar una GC aislada. A modo de ejemplo, OP1, que ha sido el dispositivo más exacto, ha presentado GC con una discrepancia superior a 15mg/dL respecto a la GP hasta en un 10% de las mediciones (tabla 2). Los pacientes que realizan autoanálisis de glucemia deben ser conocedores de dicha variabilidad. En este sentido, en un estudio de Zueger et al.24, en el que se evaluaron 3 glucómetros de uso habitual sobre una muestra de pacientes diabéticos, los autores argumentaban que aunque los pacientes podían confiar en los glucómetros evaluados, debían esperar con cualquiera de ellos una desviación media de hasta un 7-10%. Esta desviación media es similar a la observada en nuestro estudio, que osciló entre el 5,6 (OP1) y el 7,9% (AC).
Son numerosos los factores que pueden interferir la medición de la GC, y entre ellos está bien documentada la alteración en el valor del hematocrito6,7: al aumentar el hematocrito se ofrece una GC inferior a la real, y en el caso opuesto, un hematocrito bajo hace que la GC aparente esté aumentada. Como límites de seguridad inferior y superior suelen considerarse unos valores de hematocrito del 30 y del 55%, respectivamente2. Otras posibles causas de alteración de la GC son las elevaciones plasmáticas de la urea, la bilirrubina total, los triglicéridos y el ácido úrico6,7, que pueden ocasionar una falsa lectura de hipoglucemia. Por el contrario, la presencia de azúcares25 o povidona iodada7 sobre la zona de punción puede incrementar falsamente la GC. En los sujetos de la muestra tanto el hematocrito como el resto de los parámetros se encontraban en el rango de normalidad. Cabe señalar que en el estudio se han tomado medidas dirigidas tanto a las variaciones preanalíticas (lavado de manos con agua y jabón, sin antisépticos, utilización de la primera gota de sangre capilar, aleatorización del orden de los glucómetros, profesionales sanitarios entrenados para la obtención de las muestras) como analíticas (inclusión del hematocrito y la bioquímica sanguínea como variables, realización de un análisis estratificado).
Concordancia entre los glucómetros: glucemia capilar vs. glucemia capilarEl CCI mostró unos valores≥0,95, que apuntaban a una concordancia casi perfecta entre los 3 dispositivos. Sin embargo, hay que recordar que una de las limitaciones de este coeficiente es su fuerte dependencia de la variabilidad de las series; es decir, hay un incremento artificial del CCI ante distribuciones heterogéneas, independientemente del grado de concordancia obtenido. La asimetría de las 3 series, el alejamiento de la normalidad, y la existencia de un valor extremo de GP (273mg/dL) evidencian que se ha podido producir dicho efecto.
En el nivel de GP≥126mg/dL, el CCI de los pares OP1/OP2, OP1/AC y OP2/AC presentó unos valores muy cercanos a 1, la concordancia perfecta. Según nuestros resultados, en las glucemias más elevadas han coincidido la mayor exactitud de los glucómetros y la mayor concordancia entre ellos.
Por otro lado, OP1/OP2 fue el par que mostró el mayor grado de concordancia, mostrando simultáneamente la menor diferencia de medias y la menor amplitud de los límites de acuerdo. Sin embargo, es difícil poder precisar el grado de concordancia alcanzado. Frente a los estándares disponibles para comparar la exactitud de los resultados de un glucómetro en referencia a su correlato en sangre venosa2,6, la situación es diferente respecto al grado de concordancia. En la revisión efectuada no se han encontrado unos estándares de conformidad aceptados mayoritariamente, y de acuerdo con otros autores26, es necesario estandarizar los diferentes niveles de concordancia entre los dispositivos.
Se ha dicho que con la misma gota de sangre, entre 2 glucómetros iguales puede haber una diferencia de±15mg/dL en las lecturas de GC27. Según nuestros resultados, en el par OP1/OP2 el valor del coeficiente de repetibilidad fue de 14,3, lo que indica que con una probabilidad del 95%, la diferencia entre ambos glucómetros era inferior a esa cifra. Si se considera±15mg/dL como punto de corte, los dispositivos OP1 y OP2 presentarían un grado de concordancia aceptable.
Debilidades y fortalezas del estudioLa principal debilidad es no haber incluido pacientes con concentraciones extremas de glucemia, dada la importancia clínica que tiene valorar la exactitud de los glucómetros en estas situaciones. Sin embargo, fuera del ámbito hospitalario es muy difícil seleccionar pacientes con niveles críticos de hiperglucemia o hipoglucemia. Asimismo, hay que considerar la pérdida de potencia estadística al dividir la muestra en el análisis por subgrupos; una solución a ello hubiera sido seleccionar más participantes, para asegurar un mayor número de elementos en los diferentes estratos. Un 77% de los participantes en el estudio no eran diabéticos, lo cual pudiera limitar la extrapolación de los resultados a la población diabética. Por último, se decidió asumir un posible sesgo de selección al extraer la muestra de los sujetos citados para extracciones, en vez de extraerla de entre los que acudían a consulta por cualquier motivo. Como punto de interés, cabe señalar el propio diseño del estudio, que ha permitido evaluar la exactitud y la concordancia entre glucómetros en condiciones habituales de práctica clínica, aprovechando la organización asistencial existente, en un tiempo breve y, en nuestra opinión, con una razonable ausencia de sesgos significativos.
En conclusión, las GC de los 3 dispositivos se aproximaron razonablemente a las cifras de GP, presentando una diferencia de medias clínicamente aceptable; sin embargo, con unos errores sistemáticos de 5,8, 5,9 y 6,3%, los 3 glucómetros incumplían el estándar actual de la American Diabetes Association de un error tolerado de±5%.
Se han observado los mayores niveles de exactitud y de concordancia en el rango glucémico más elevado (≥126mg/dL). Los 2 aparatos Optium fueron los más concordantes, si bien la ausencia de un estándar en este aspecto dificulta concretar el nivel alcanzado.
El resultado permite un alto grado de confianza en los aparatos evaluados. Sin embargo, coincidimos con la recomendación de realizar periódicamente controles de calidad de los glucómetros mediante estudios en condiciones habituales de uso.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.